Biopsia del tubo digestivo bajo
Texto completo
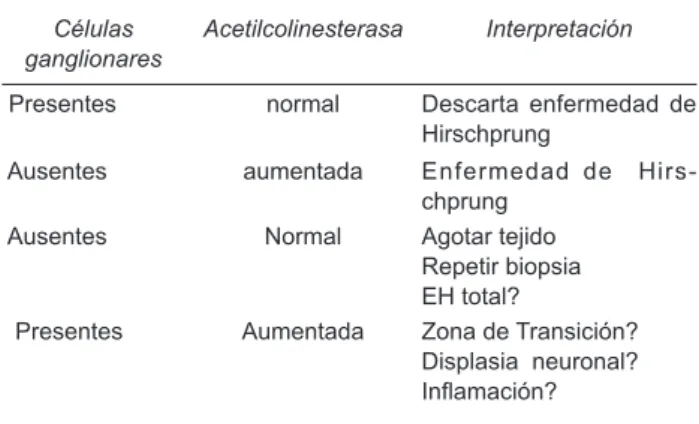
Figure


Documento similar
[r]
SVP, EXECUTIVE CREATIVE DIRECTOR JACK MORTON
De este modo se constituye un espacio ontológico y epistemológico a la vez, en el que cada elemento (cada principio) ocupa un lugar determinado en la totalidad, y desde ahí está
La combinación, de acuerdo con el SEG, de ambos estudios, validez y fiabilidad (esto es, el estudio de los criterios de realidad en la declaración), verificada la
Con el cometido de evaluar la credibilidad del testimonio en casos de violencia de gé- nero, a la vez que la huella psíquica con- trolando una potencial simulación, hemos
El Programa de Mecenazgo organiza un concurso para "Amigos del IAC" en el cual podrán realizar una propuesta de observación para un telescopio robótico 1. Aquellas que
En total se prepararon 30 muestras, 10 por cada pareja de primers: muestras de cDNA procedentes de las tres líneas celulares por 3 veces cada muestra (triplicado técnico)
Pero antes hay que responder a una encuesta (puedes intentar saltarte este paso, a veces funciona). ¡Haz clic aquí!.. En el segundo punto, hay que seleccionar “Sección de titulaciones