Primer Consenso Mexicano de Cáncer de Endometrio
Grupo de Investigación en Cáncer de Ovario y
Tumores Ginecológicos de México “GICOM”
Eva Ruvalcaba-Limón,
1David Cantú-de-León,
2Eucario León-Rodríguez,
3Patricia Cortés-Esteban,
4Alberto Serrano-Olvera,
2Flavia Morales-Vásquez,
2Ricardo Sosa-Sánchez,
5Andrés Poveda-Velasco,
6Alejandro Crismatt-Zapata,
2Antonio Santillán-Gómez,
7Carmen Aguilar-Jiménez,
8Patricia Alanís-López,
9Paulino Alfaro-Ramírez,
10Miguel Ángel Álvarez-Avitia,
2Carlos Eduardo Aranda-Flores,
11José Héctor Reynaldo
Arias-Ceballos,
12Oscar Arrieta-Rodríguez,
2Eduardo Barragán-Curiel,
13Daniel Botello-Hernández,
14Rocío Brom-Valladares,
15Paula Anel Cabrera-Galeana,
16Juan Carlos Cantón-Romero,
17Daniel Capdeville-García,
18Jesús Cárdenas-Sánchez,
19Gerardo Castorena-Roji,
20Friedman Rafael Cepeda-López,
19Guadalupe Cervantes-Sánchez,
4Lucely del Carmen Cetina-Pérez,
2Jaime Alberto Coronel-Martínez,
2Seir Alfonso
Cortés-Cárdenas,
4Juan Carlos Cruz-López,
21Jaime G. de la Garza-Salazar,
2Consuelo Díaz-Romero,
2Alfonso
Dueñas-González,
2Aura Erazo Valle-Solís,
4Pedro Escudero-de los Ríos,
12Efrén Flores-Álvarez,
22Rolando García-Matus,
23Raquel Gerson-Cwilich,
20Aarón González-Enciso,
2César González-de-León,
24Alfonso Genaro Guevara-Torres,
25Guillermo Sidney Herbert-Núñez,
26Carlos Hernández-Hernández,
23Dulce María Hernández-Hernández,
12David Isla-Ortiz,
2Ramiro Jesús-Sandoval,
27Carlos Jiménez-Cervantes,
28Roberto Kuri-Exsome,
29José Luis López-Obispo,
9Antonio Maffuz-Aziz,
1Luis Manuel Martínez-Barrera,
30Juan Manuel Medina-Castro,
16Gonzalo Montalvo-Esquivel,
2Víctor Hugo Mora-Aguilar,
31Miguel Ángel Morales-Palomares,
32Andrés Morán-Mendoza,
17Gilberto Morgan-Villela,
33Aída Mota-García,
2David Eduardo Muñoz-González,
2Dino Alberto Murillo-Cruz,
4Arturo Novoa-Vargas,
34Francisco J. Ochoa-Carrillo,
2Luis Fernando Oñate-Ocaña,
2Andrea Ortega-Rojo,
35Alma Georgina Palacios-Martínez,
36Antonio Palomeque-López,
37María Delia Pérez-Montiel,
2Félix Quijano-Castro,
12Samuel Rivera-Rivera,
12Lesbia María Rivera-Rubí,
2Juan Ubaldo Robles-Flores,
2Amelia Rodríguez-Trejo,
38Efraín Salas-Gonzáles,
17Juan Alejandro Silva,
12Gilberto Solorza-Luna,
2Rosalía Souto-del-Bosque,
39Laura Leticia Tirado-Gómez,
40Salvador Torrescano-González,
41Alfonso Torres-Lobatón,
32Elizabeth Trejo-Durán,
2Verónica Villavicencio-Valencia,
2Dolores Gallardo-Rincón
21Instituto de Enfermedades de la Mama FUCAM. 2Instituto Nacional de Cancerología. 3Instituto Nacional de Nutrición y Ciencias Médicas
Salvador Zubirán. 4Centro Médico Nacional 20 de Noviembre del ISSSTE. 5Centro Oncológico Médica Sur
6Instituto Valenciano de Oncología. 7The Johns Hopkins Medical Institutions, Baltymore USA. 8Práctica Privada, Puebla. 9Centro Médico
La Raza, IMSS. 10Hospital General de Veracruz. 11Hospital Ángeles del Pedregal. 12Centro Médico Nacional Siglo XXI, IMSS. 13
Hospi-tal Civil Juan I. Menchaca Guadalajara Jal. 14Fundación Rodolfo Padilla, León Guanajuato. 15Radiología e Imagen, Fundación Clínica
MédicaSur. 16Centro Oncológico Estatal ISSEMYM. 17Centro Médico de Occidente, IMSS, Guadalajara. 18Hospital Aranda de la Parra. 19Centro Estatal de Cancerología de Colima. 20Centro Médico ABC. 21Unidad de Oncología, Servicios de Salud de Puebla. 22Centro
Hospitalario Miguel Hidalgo, Aguascalientes. 23Hospital Regional de Alta Especialidad, Oaxaca. 24Organización Para el Cuidado
Integral en Oncología. 25Hospital Oncológico del Estado de Sonora. 26Hospital Ángeles de Querétaro. 27Servicios a la Comunidad
Universitaria, UNAM. 28Hospital Presidente Juárez, ISSSTE, Oaxaca. 29Hospital Regional de Alta Especialidad del Bajío. 30Instituto
Nacional de Enfermedades Respiratorias. 31Hospital ISSSTEcali, Mexicali. 32Hospital General de México. 33Hospital de Especialidades,
IMSS, Guadalajara. 34Centro Médico Dalinde. 35Instituto Tecnológico de Estudios Superiores de Monterrey. 36ISSSTE Torreón, Coahuila. 37Hospital Regional de Alta Especialidad de Tapachula, Chiapas. 38Centro Estatal de Cancerología de Nayarit. 39 Unidad Médica de Alta
RESUMEN
Introducción. El cáncer de endometrio (CE) es la segunda neoplasia ginecológica más frecuente a nivel mundial, más co-mún en la peri y postmenopausia. Mayor frecuencia para la variedad endometrioide. Supervivencia a largo plazo en la pa clínica temprana es mayor a 80%, mientras que en las eta-pas avanzadas es menor a 50%. En nuestro país no existe un manejo totalmente estandarizado entre instituciones. Grupo GICOM, en colaboración y bajo el auspicio de las diferentes instituciones, ha realizado el siguiente consenso con la finali-dad de dar recomendaciones para el manejo de las pacientes con este tipo de neoplasia. Material y métodos. Este con-senso se realizó mediante paneles independientes de profesio-nales de la salud en el campo de la ginecología oncológica, las preguntas y declaraciones realizadas fueron con base a una revisión exhaustiva y sistemática de la literatura, hechas en el marco de una reunión de cuatro días en donde se llevó a cabo un debate abierto. Estas declaraciones corresponden a las con-clusiones alcanzadas por acuerdo de sus integrantes. Resul-tados. El escrutinio se debe hacer sólo a mujeres con alto riesgo (diabéticas, historia familiar de cáncer de colon heredi-tario no polipósico, S. Lynch tipo II). El grosor endometrial en pacientes es mejor evaluado mediante US transvaginal, un grosor mayor o igual a 5 mm debe ser biopsiado. Las mujeres que toman tamoxifeno deben ser monitoreadas con este méto-do. Sangrado transvaginal es la manifestación inicial, todas las mujeres que posterior a la menopausia presenten sangrado vaginal deben ser estudiadas. El Diagnóstico se hace mediante biopsia guiada por histerescopia. La RMN es el mejor estudio radiológico de estadificación preoperatoria. El estudio transo-peratorio evalúa grado histológico, profundidad de infiltración miometrial, extensión de la enfermedad a cérvix y afectación de los anexos. Se realiza panhisterectomía con linfadenectomía pélvica y para-aórtica excepto en variedad endometrioide Gra-do 1 y 2, afectación menor de 50% del miometrio, sin evidencia de enfermedad fuera del útero. Omentectomía se recomienda variedad no endometrioide. La cirugía debe ser realizada por parte de un ginecólogo oncólogo o un cirujano oncólogo, se puede hacer por laparoscopía, especialmente en pacientes dia-béticas e hipertensas por ser menos mórbida. El tratamiento adyuvante posterior a la cirugía incluye a la radioterapia diri-gida a la pelvis, braquiterapia y quimioterapia. A las pacientes con EC III y IV se les debe practicar cirugía con intención de lograr citorreducción óptima, ya que tiene impacto en la su-pervivencia (51 m vs. 14 m). El tratamiento de la recurrencia puede ser de nuevo con cirugía dependiendo del patrón de la recaída, tratamiento sistémico hormonal o de quimioterapia. El seguimiento es principalmente clínico de manera seriada. Conclusiones. Existe un programa de escrutinio sólo para pacientes de alto riesgo, el tratamiento multidisciplinario im-pacta en mejor supervivencia y control local de la enfermedad, incluye cirugía, radioterapia y quimioterapia, el tratamiento hormonal se reserva para casos seleccionados de recurrencia. Este es el primer producto de un Grupo Colaborativo Mexica-no en Ginecología Oncológica en dar recomendaciones para un manejo estandarizado en una neoplasia específica.
Palabras clave. Cáncer de endometrio. Cirugía. Radiotera-pia. QuimioteraRadiotera-pia. Tratamiento hormonal.
The first Mexican
consensus of endometrial cancer
ABSTRACT
Introduction. Endometrial cancer (EC) is the second most common gynecologic malignancy worldwide in the peri and postmenopausal period. Most often for the endometrioid vari-ety. In early clinical stages long-term survival is greater than 80%, while in advanced stages it is less than 50%. In our coun-try there is not a standard management between institutions. GICOM collaborative group under the auspice of different in-stitutions have made the following consensus in order to make recommendations for the management of patients with this type of neoplasm. Material and methods. The follow-ing recommendations were made by independent profession-als in the field of Gynecologic Oncology, questions and statements were based on a comprehensive and systematic re-view of literature. It took place in the context of a meeting of four days in which a debate was held. These statements are the conclusions reached by agreement of the participant mem-bers. Results. Screening should be performed women at high risk (diabetics, family history of inherited colon cancer, Lynch S. type II). Endometrial thickness in postmenopausal patients is best evaluated by transvaginal US, a thickness greater than or equal to 5 mm must be evaluated. Women taking tamox-ifen should be monitored using this method. Abnormal bleed-ing in the usual main symptom, all post menopausal women with vaginal bleeding should be evaluated. Diagnosis is made by histerescopy-guided biopsy. Magnetic resonance is the best image method as preoperative evaluation. Frozen section eval-uates histologic grade, myometrial invasion, cervical and adn-exal involvement. Total abdominal hysterectomy, bilateral salpingo oophorectomy, pelvic and para-aortic lymphadenec-tomy should be performed except in endometrial histology grades 1 and 2, less than 50% invasion of the myometrium without evidence of disease out of the uterus. Omentectomy should be done in histologies other than endometriod. Sur-gery should be always performed by a Gynecologic Oncologist or Surgical Oncologist, laparoscopy is an alternative, especial-ly in patients with hypertension and diabetes for being less morbid. Adjuvant treatment after surgery includes radiation therapy to the pelvis, brachytherapy, and chemotherapy. Pa-tients with Stages III and IV should have surgery with inten-tion to achieve optimal cytoreducinten-tion because of the impact on survival (51 m vs. 14 m), the treatment of recurrence can be with surgery depending on the pattern of relapse, systemic chemotherapy or hormonal therapy. Follow-up of patients is basically clinical in a regular basis. Conclusions. Screening programme is only for high risk patients. Multidisciplinary treatment impacts on survival and local control of the disease, including surgery, radiation therapy and chemotherapy, hormonal treatment is reserved to selected cases of recur-rence. This is the first attempt of a Mexican Collaborative Group in Gynecology to give recommendations is a special type of neoplasm.
INTRODUCCIÓN
El carcinoma de endometrio (CE) es la segunda neoplasia ginecológica más frecuente a nivel mun-dial. Su mayor frecuencia está condicionada al in-cremento en la expectativa de vida en la población femenina, al uso de tamoxifeno y al surgimiento de la obesidad como problema de salud.
La incidencia del CE es casi seis veces mayor en países desarrollados que en los menos desarrollados, aunque su mortalidad es menor que en aquellos paí-ses con menos desarrollo.2
De los tumores del cuerpo uterino el CE es el más frecuente, predominando la variedad endometrioide y desarrollándose generalmente en la perimenopau-sia, atribuyéndose a una asociación con la exposi-ción excesiva a estrógenos.
Aunque el pronóstico del CE en etapas tempranas es favorable con tasas de supervivencia de 80%, las pacientes con enfermedades de alto riesgo y enferme-dad avanzada tienen una supervivencia a largo pla-zo menor a 50%. Desafortunadamente, en los últimos 30 años el avance en el tratamiento de esta neoplasia ha sido muy limitado, por un lado debido al escaso número de estudios clínicos realizados y por otro, al poco conocimiento de su patología mole-cular.
Actualmente se conoce que el CE tipo I (relacio-nado a estrógenos) y el tipo II (no relacio(relacio-nado a estrógenos) tienen diferentes perfiles genéticos.3,4
El tipo I se origina de una lesión precursora: la
hiperplasia atípica o neoplasia intraepitelial endo-metrial. En el desarrollo de ésta, está implicada la mutación con inactivación de PTEN, un gen su-presor de tumores. También se han encontrado mutaciones de genes reparadores de mismatch, de K-ras y de catenina A. En el CE tipo II se han de-mostrado mutaciones de p53 y diferentes patrones de aneuploidía.
Un mayor conocimiento de los genes involucra-dos en la carcinogénesis endometrial permitirá en un futuro conocer en detalle los mecanismos de ini-cio, progresión y desarrollo de metástasis, así como el desarrollo de biomarcadores pronósticos y blancos terapéuticos. A este respecto hay que señalar que ac-tualmente inhibidores de m-TOR se encuentran en valoración en estudios clínicos combinados con qui-mioterapia en enfermedad avanzada, dado que en el CE tipo I se encuentran sobreexpresados el m-TOR y la S6 cinasa.4 Por otro lado, debido a que el receptor
del factor de crecimiento epidérmico y el HER-2 se encuentran también sobreexpresados en esta neopla-sia en 50 y 60%, respectivamente, se han iniciado estudios fase II con trastuzumab, cetuximab y lapatinib.5
Con base en lo anterior y con el objeto de anali-zar el conocimiento actual del CE y establecer crite-rios diagnósticos y terapéuticos, en octubre de 2008 se llevó a cabo el primer consenso nacional que invo-lucró a 87 expertos de 41 instituciones, bajo el aus-picio de la Sociedad Mexicana de Oncología. El grupo de oncólogos médicos, radioterapeutas, gine-ANTECEDENTES
El Grupo de Investigación en Cáncer de Ovario y Tumores Ginecológicos de México (GICOM) ha prepara-do esta declaración por consenso al respecto del escrutinio, diagnóstico y manejo del carcinoma enprepara-dometrial en México. Este documento ha sido realizado por profesionales de la salud cuidadosamente seleccionados por ser líderes de opinión en el área de la Oncología Ginecológica o en áreas afines a nivel nacional. Las pregun-tas y las declaraciones fueron elaboradas con base en una revisión exhaustiva y sistemática de la literatura científica al respecto del CE. Los investigadores de GICOM se reunieron por primera vez en el mes de octubre de 2008 y realizaron presentaciones orales referentes a las áreas de cuestionamiento específicas y en sesiones de dos, tres y cuatro días en donde se debatieron abiertamente tanto las preguntas como las declaraciones, así en paneles independientes de especialistas como en sesiones plenarias.
Estas declaraciones corresponden a las conclusiones alcanzadas por acuerdo y representan la información científica disponible hasta el momento en que fue hecho este documento.
cólogos oncólogos, cirujanos oncólogos, radiólogos y patólogos convocados, con base en un análisis críti-co de la información actual y de su experiencia insti-tucional, se dieron a la tarea de elaborar criterios de diagnóstico, estadificación y tratamiento en las dife-rentes etapas del CE, con el propósito de elaborar un documento de referencia a los diferentes especialis-tas involucrados en el manejo cotidiano de las pa-cientes con esta patología.
El esfuerzo conjunto de los integrantes de este grupo de trabajo dio como resultado este documento final, el cual se espera pueda contribuir a abatir la morbilidad y mortalidad de esta neoplasia en las mu-jeres de nuestro país.
¿CÓMO DEBE SER EL
ESCRUTINIO DEL CÁNCER ENDOMETRIAL?
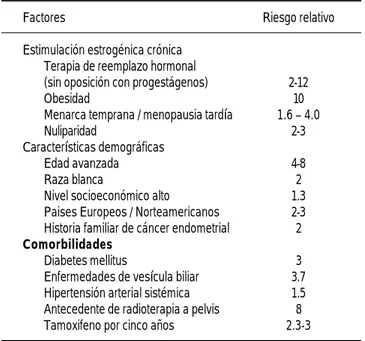
Se reconocen como factores de riesgo para el de-sarrollo de CE los relacionados con la exposición crónica a estrógenos, y a trastornos que se derivan y asocian a la obesidad6 (Cuadro 1).
No se acepta un programa de escrutinio para esta neoplasia, ya que en más de 75% de las pacien-tes con CE el diagnóstico se realiza en etapa I, debido a que el sangrado transvaginal es la manifestación inicial excepto para las mujeres con riesgo para desarrollar estas enfermedades. A partir de la me-nopausia, en caso de existir cualquier tipo de sangrado transvaginal (abundante o goteo no espe-rado), al igual que pacientes diabéticas
asintomáti-cas mayores de 45 años y cualquier mujer mayor a 40 años con presencia de sangrado transvaginal anormal, mujeres con citología cervical en donde se encuentre la presencia de células glandulares atípi-cas, se recomienda la realización de biopsia endo-metrial, reconociendo a la hiperplasia endometrial como la lesión precursora.7
Mujeres consideradas de alto riesgo para el de-sarrollo de CE que son las que poseen historia fami-liar de cáncer de colon hereditario no polipósico y las pacientes con síndrome de Lynch tipo II.8 En
es-tas mujeres se recomienda el escrutinio para CE a partir de los 35 años.
¿QUÉ FACTORES DEBEN
CONSIDERARSE PARA UTILIZAR PROGRAMAS DE DETECCIÓN PRECOZ EN CE?
El uso de estrógenos orales sin oposición está asociado a un alto riesgo para el desarrollo de CE, siendo aún mayor con el empleo a dosis altas. El riesgo se ha considerado a partir de dos años de uso y al igual que otros tumores hormonodepen-dientes, éstos generalmente son detectados en eta-pas tempranas siendo tumores de bajo grado histológico.7
En pacientes con cáncer de mama que utilizan ta-moxifeno, el riesgo relativo de desarrollar CE es de 2.5 veces más que la población de pacientes que no lo usan.9
Se recomienda realizar un ultrasonido transvagi-nal basal previo al tratamiento con tamoxifeno.10 En
el transcurso de su uso, ante la presencia de un en-dometrio con espesor ≥ a 5 mm se deberá practicar histeroscopia con toma de biopsia, independiente-mente de la presencia o ausencia de sangrado trans-vaginal.11,12
Debido a que es variable el tiempo en que se puede desarrollar CE posterior al empleo de ta-moxifeno, la vigilancia endometrial debe conti-nuar después de suspenderlo por un periodo de 12 años.13(Evidencia C, recomendación 1). El uso
de raloxifeno, antagonista selectivo de estrógenos representa menor riesgo para el desarrollo de CE que con el uso de tamoxifeno. Aquellas pacientes que cambian de tamoxifeno a un inhibidor de aroma-tasa como el anastrozol, letrozol o exemestano, presentan disminución del espesor endometrial y menor necesidad de histeroscopias y biopsias en-dometriales.14-16 (Evidencia B, recomendación 1).
No es claro y aún existe controversia si el CE relacionado con el empleo de tamoxifeno es de ma-yor agresividad. Hay autores que reportan
estir-Cuadro 1. Factores de riesgo para cáncer de endometrio.
Factores Riesgo relativo
Estimulación estrogénica crónica Terapia de reemplazo hormonal
(sin oposición con progestágenos) 2-12
Obesidad 10
Menarca temprana / menopausia tardía 1.6 – 4.0
Nuliparidad 2-3
Características demográficas
Edad avanzada 4-8
Raza blanca 2
Nivel socioeconómico alto 1.3 Paises Europeos / Norteamericanos 2-3 Historia familiar de cáncer endometrial 2
Comorbilidades
Diabetes mellitus 3
pes histológicas desfavorables y tumores indiferen-ciados en pacientes con CE secundario al uso de este fármaco.17,18
¿CÓMO SE HACE EL DIAGNÓSTICO DE CE?
El diagnóstico se realiza mediante estudio de biopsia, mismo que se decide realizar con base en factores de riesgo y espesor endometrial evaluado mediante ultrasonido transvaginal. La biopsia pue-de realizarse en el consultorio empleando una cánu-la de Novak o Pipelle, puede ser tomada bajo visión directa mediante histeroscopia, dilatación-curetaje o realizando legrado fraccionado, cuya sensibilidad para realizar el diagnóstico es de 78% (IC 95% 76.3-79.6%) y especificidad de 95.8% (IC 95-96.1%)19
(Evidencia A, recomendación 1).
¿QUÉ GROSOR
ENDOMETRIAL DEBE CONSIDERARSE SOSPECHOSO DE CÁNCER?
Si bien no hay un acuerdo sobre cuál es el espesor endometrial considerado como sospechoso de maligni-dad, se acepta que a partir de un grosor de 5 mm, se recomienda realizar una biopsia.20 Los estudios de
Langer y Gull reportan un valor predictivo negativo de 99 y 100%, respectivamente, con un espesor del en-dometrio < 5 mm y 4 mm en mujeres posmenopáusi-cas21,22(Evidencia C, recomendación 1).
¿CUÁLES SON LOS ESTUDIOS PREOPERATORIOS Y DE DETECCIÓN
DE ENFERMEDAD EXTRAUTERINA?
Debe realizarse una historia clínica detallada y exploración física completa con especial énfasis en búsqueda de hallazagos que sugieran afección ex-trauterina del tipo del involucro parametrial, afec-ción vesical y/o rectal. Los estudios de laboratorio deben incluir: biometría hemática, química sanguí-nea, perfil de coagulación, tele-radiografía de tórax, citología cervicovaginal y biopsia endometrial23
(Evi-dencia C, recomendación 1).
Debido a que el CE se desarrolla con mayor prevalencia en mujeres con otras comorbilidades, se deberán solicitar los estudios necesarios acor-de a la patología acor-de la paciente y realizar una evaluación integral previa a la estadificación qui-rúrgica.
Por otro lado, la realización preoperatoria de estudio radiológico tiene como objetivo detectar enfermedad extrauterina como es la afección
gan-glionar pélvica y/o para-aórtica, extensión a los anexos u otros órganos intraabdominales, así como para la identificación de involucro del estro-ma cervical y estro-magnitud de la invasión miome-trial.24
Se ha encontrado que pacientes con CE conside-radas en etapa temprana poseen enfermedad extrau-terina en 10 a 22% de los casos.25
¿CUÁL ES LA UTILIDAD
DEL ULTRASONIDO TRANSVAGINAL?
Si bien es un método útil para identificar el espe-sor endometrial, es controversial su utilidad para la identificación preoperatoria de afección cervical, de-pendiendo mucho de la experiencia del radiólogo que lo practique, y pudiera no ser el mejor método.26
(Evidencia B, recomendación 1).
¿CUÁL ES LA UTILIDAD DE LA TOMOGRAFÍA COMPUTADA?
La sensibilidad de la tomografía computada para la identificación de involucro al estroma cervical e invasión miometrial es menor a 20%, mientras que la sensibilidad para determinar afección ganglionar pélvica, para-aórtica y enfermedad anexial es de 60% con una especificidad de 92%27(Evidencia B,
reco-mendación 1).
¿CUÁL ES LA UTILIDAD DE LA RESONANCIA MAGNÉTICA?
Es el estudio que posee mayor eficacia para identi-ficar invasión miometrial, enfermedad ganglionar, ya que posee una sensibilidad y especificidad de 87 y 100%, respectivamente, muy superior a otros méto-dos radiológicos.28
Aún practicándose este estudio, la linfadenecto-mía no debe obviarse ante el riesgo de una posible subestadificación.29 Para detección de afección
cervi-cal, la resonancia magnética posee sensibilidad de 72% y especificidad de 93.2%29,30(Evidencia B,
reco-mendación 1).
¿QUÉ DEBE
INCLUIR EL REPORTE DEL ESTUDIO HISTOPATOLÓGICO?
endometria-les.31 La clasificación de grado de diferenciación
considera dos factores: el porcentaje de áreas sóli-das y el grado nuclear; así tenemos que el grado 1 tiene menos de 5% de áreas sólidas, el grado 2 tiene de cinco a 50% y el grado 3 tiene más de 50%. En presencia de atipia citológica marcada el grado au-menta, por ejemplo: un tumor con menos de 5% de áreas sólidas, pero con atipia citológica marcada se clasifica como grado 232(Evidencia B,
recomenda-ción 1).
Aproximadamente 10% de los CE corresponden a carcinomas serosos papilares, de células claras, indi-ferenciados, mixtos, epidermoides y neuroendócri-nos. Todas estas variantes se consideran de alto grado, considerándose histologías de riesgo para recurrencia.33 El patólogo realiza estudio
transope-ratorio y estudio definitivo del espécimen para con-tribuir a la mejor decisión terapéutica.
Habitualmente el diagnóstico de CE se realiza me-diante biopsia o legrado previo a la cirugía, siendo esto el panorama ideal, ya que al realizar un estudio transoperatorio para diagnóstico puede entorpecerse por la presencia de artificios que dificultan la inter-pretación, aunado a que la cantidad de tejido anali-zado generalmente es pequeña y conlleva a errores de muestreo. Sólo en ocasiones muy particulares como cuando existe una alta sospecha de carcinoma con biopsias previas insuficientes, el estudio transo-peratorio para diagnóstico de malignidad es de ma-yor utilidad.34
Tomando en cuenta que los factores de alto ries-go en carcinoma de endometrio son el grado histoló-gico, la profundidad de infiltración miometrial, la presencia de extensión al cérvix y la afectación de los anexos, son los elementos que se evalúan duran-te el estudio transoperatorio, facilitando identificar al grupo de pacientes que pueden tener beneficio con la disección ganglionar pélvica y para-aórtica. Las pacientes con CE que tienen mayor riesgo de metás-tasis ganglionares son las que poseen invasión mio-metrial mayor a 50%, invasión al cérvix y/o enfermedad anexial.35
El útero debe ser abierto cortando las paredes la-terales siguiendo el radio de las tres a las nueve; se revisa cuidadosamente la cavidad endometrial y el canal endocervical en búsqueda de tumor. Posterior-mente se realizan cortes transversales de la pared miometrial en forma completa cada 5 mm buscando las áreas de mayor infiltración macroscópica; se rea-lizan cortes para congelación de dichas áreas y se analizan en el microscopio para evaluar la infiltra-ción microscópica.36
El estudio transoperatorio debe informar:
1. Corroboración histológica del tumor (en caso de no contar con diagnóstico previo o en presencia de duda diagnóstica en biopsia previa). 2. Presencia o no de infiltración miometrial,
en caso de estar infiltrado el miometrio se debe es-pecificar si ésta es mayor o menor de 50% del espesor miometrial.
3. Extensión o no al cérvix, en caso de estar in-filtrado el cérvix se debe especificar si existe o no infiltración al estroma cervical.
4. Grado histológico del tumor (si no se cuenta con biopsia previa).
5. Presencia de tumor en los anexos.
La precisión del estudio transoperatorio para de-terminar la infiltración miometrial es de 70% cuan-do se utiliza sólo la observación macroscópica, elevándose a 95% cuando se utiliza además cortes por congelación. Los factores que dificultan el deter-minar la infiltración al miometrio son la presencia de miomas, adenomiosis y errores en el muestreo.
El grado histológico en el estudio transoperatorio y en el estudio definitivo puede variar hasta en 30% de los casos, siendo más frecuente sub-gradificar el tumor.37La causa más frecuente de la
sub-gradifica-ción es por errores en el muestreo, tomando en cuen-ta que en el estudio transoperatorio solo se congela una pequeña parte del tumor y en el estudio definiti-vo el muestreo es mucho más amplio. La correlación entre el estudio transoperatorio y el estudio definiti-vo es del 75%38(Evidencia C, recomendación 1).
¿CÓMO DEBE
REALIZARSE LA CLASIFICACIÓN TNM?
La clasificación por etapas TNM es quirúrgica-his-tológica. La cirugía para clasificar la etapa clínica debe realizarse por un cirujano oncólogo o por un gi-necólogo oncólogo, esto permite un mejor criterio en el momento de la cirugía, además de reducir tiempos qui-rúrgicos y costos39(Evidencia C, recomendación 1).
En caso de que la paciente no sea tratada inicial-mente por un oncólogo, el Colegio Americano de Gi-necología y Obstetricia,40 recomienda la valoración
de la paciente por parte de un oncólogo en las si-guientes situaciones:
• Necesidad de reintervención quirúrgica por dificul-tad técnica en la primera intervención quirúrgica. • Reporte histopatológico preoperatorio con alto
con diferenciación grado 3 o variedades seroso pa-pilar, de células claras y en el carcinosarcoma). • Estudio histopatológico definitivo de CE no
espe-rado posterior a histerectomía realizada por otras indicaciones.
• Evidencia de enfermedad cervical o enfermedad extrauterina.
• Citología de lavado peritoneal positivo a células malignas.
• Sospecha o diagnóstico de enfermedad recurren-te.
• Cuando se ha considerado paciente no candida-ta a manejo quirúrgico (Evidencia C, recomenda-ción 1).
¿CÓMO DEBE SER LA HISTERECTOMÍA?
Dado que los factores de pronóstico más impor-tantes en esta neoplasia son la invasión del miome-trio y la afección ganglionar, se requiere de una cirugía adecuada para poder definirlos.41
Se recomienda que todas las pacientes con CE de-ben obtener el de-beneficio de una cirugía etapificadora completa, que comprende:
• Citología peritoneal.
• Histerectomía total abdominal con salpingo-oofo-rectomía bilateral.
• Linfadenectomía pélvica y para-aórtica bilateral en pacientes con tumores G3, invasión miome-trial > 50%, o tumor fuera del cuerpo uterino. Obviamente la evaluación de toda la cavidad ab-dominal debe ser realizada y los tejidos removi-dos deben estudiarse por separado por parte del patólogo.42
En el caso de la EC II (afectación del estroma cer-vical) en el abordaje quirúrgico inicial debe realizar-se histerectomía radical tipo III de Rutledge, que consiste en una histerectomía total más salpingo-ooforectomía bilateral, removiendo tejido parame-trial adicional hasta la pared pélvica con sección de la arteria uterina en su emergencia y preservación de la arteria vesical superior, con disección ganglio-nar de ganglios pélvicos y para-aórticos en forma sistemática (Evidencia C, recomendación 1).
La vía de abordaje por la cual se realice la cirugía depende de las características propias de la paciente, de la institución donde se hace el procedimiento así como del entrenamiento y preferencia del cirujano tratante ya que pueda ser por vía abdominal, vaginal o laparos-cópica. La cirugía sólo debe obviarse en casos muy se-leccionados de pacientes con un estado funcional muy
deteriorado o en caso de comorbilidades que no lo per-mitan43(Evidencia C, recomendación 1).
No se recomienda realizar en forma rutinaria la omentectomía en pacientes con histología endome-trioide, independientemente del grado histológico o de la invasión miometrial. Puede ayudar en la toma de decisión, la palpación previa del omento. La frecuen-cia de metástasis a este nivel es sólo de tres a 8.3%44,45 (Evidencia B, recomendación 1).
¿EN QUÉ PACIENTES SE
DEBE REALIZAR MUESTREO GANGLIONAR O LINFADENECTOMÍA?
Ha sido un punto de discusión la realización de la linfadenectomía pélvica y para-aórtica así como el número óptimo de ganglios que deben extirparse, mismo que ha variado de un número de 14 a 20 gan-glios.46-48
La realización de la linfadenectomía conlleva un mayor tiempo quirúrgico y de hospitalización, aun-que no existe un incremento en el número y severidad de complicaciones.47 Es recomendada por diferentes
guías de diagnóstico y tratamiento para CE, tales como FIGO, SGO, NCCN y ACOG excepto en pacien-tes con histología endometrioide, grado 1, 2; invasión miometrial <50%; sin evidencia de enfermedad fuera del útero (Evidencia C, recomendación 1).
¿EN QUÉ PACIENTES
SE PUEDE REALIZAR LAPAROSCOPÍA?
Tomando en cuenta que las pacientes con CE sue-len tener comorbilidades como obesidad, hiper-tensión arterial, diabetes, endometriosis severa, enfermedades cardiovasculares, entre otras, la mayoría de los autores coinciden, que estas pacien-tes son de alto riesgo quirúrgico. La laparoscopía es la mejor opción para estas pacientes, ya que existe menor sangrado transoperatorio, se disminuye el tiempo de estancia hospitalaria y se obtiene una re-cuperación más rápida.49-51
Las complicaciones postquirúrgicas en la cirugía laparoscópica son iguales o menores comparadas con la laparotomía, con un rango entre 0 y 17.5%.52
El porcentaje de conversión varía, con reportes hasta de 12%, generalmente por la presencia de ad-herencias, obesidad, dificultad para hemostasia, in-tolerancia al incremento de la presión abdominal y enfermedad avanzada entre otras53(Evidencia B,
re-comendación 1).
simi-lares al realizarla por esta vía comparada con la téc-nica abierta, existiendo menor frecuencia de compli-caciones53,54(Evidencia B, recomendación 1).
El equipo quirúrgico requiere de una curva de aprendizaje, recomendándose de 25 a 30 procedi-mientos laparascópicos para adquirir la experiencia necesaria para este tipo de cirugías.
¿CUÁL ES LA CLASIFICACIÓN POR ETAPAS CLÍNICAS MÁS ADECUADA?
La estadificación según la Federación Internacio-nal de Ginecología y Obstetricia (FIGO), actualizada en 2009 es la siguiente:55
• ETAPA I. Tumor confinado al cuerpo ute-rino.
° ETAPA IA. G1, G2, G3. Afectación menor de 50% del miometrio.
° ETAPA IB. G1, G2, G3. Invasión igual o ma-yor de 50% del miometrio con o sin afectación de glándulas endocervicales.
• ETAPA II. Tumor confinado al cuerpo y cuello uterino.
° ETAPA IIA. Tumor que invade estroma cer-vical, pero no se extiende más allá del útero.
• ETAPA III. Tumor que involucra serosa, anexos, ganglios retroperitoneales, vagina y/o citología peritoneal positiva.
° ETAPA IIIA. G1, G2, G3. Tumor que invade la serosa del cuerpo uterino y/o los anexos. ° ETAPA IIIB. G1, G2, G3. Afectación vaginal
y parametrial.
° ETAPA IIIC. G1, G2, G3. Metástasis a gan-glios pélvicos y/o para-aórticos.
° III. C1. Ganglios pélvicos positivos.
° III. C2. Ganglios para-aórticos positivos con o sin ganglios pélvicos positivos.
• ETAPA IV. Metástasis intraabdominales, metástasis extraabdominales, y/o involucro a ganglios linfáticos inguinales, mucosa vesical o mucosa rectal.
° ETAPA IVA. G1, G2, G3. Invasión tumoral de vejiga y/o mucosa de intestino.
° ETAPA IVB. Metástasis a distancia incluyen-do metástasis intra-abincluyen-dominales e inguinales.
La citología positiva se debe reportar de manera separada sin que cambie la etapa clínica.
Además se le debe asignar el grado de diferencia-ción:
• G1 = 5% o menos de un patrón de crecimiento sólido no escamoso o no morular.
• G2 = Seis a 50% de un patrón de crecimiento só-lido no escamoso o no morular.
• G3 = Más de 50% de un patrón de crecimiento no escamoso o no morular.
Cabe señalar que la selección de pacientes para estudios clínicos en cáncer de endometrio han sido diseñados y reportados con la antigua estadificación, la cual se señala a continuación:56
• ETAPA I. Tumor confinado al cuerpo uterino.
° ETAPA IA. G1, G2, G3. Tumor limitado al endometrio.
° ETAPA IB. G1, G2, G3. Invasión de menos de la mitad del miometrio.
° ETAPA IC. G1, G2, G3. Invasión de la mitad o más de la mitad del miometrio.
• ETAPA II. Tumor confinado al cuerpo y cuello uterino.
° ETAPA IIA. G1, G2, G3. Sólo compromiso glandular endocervical.
° ETAPA IIB. G1, G2, G3. Invasión del estro-ma cervicouterino.
• ETAPA III. Tumor que involucra serosa, anexos, gangliosretroperitoneales, vagina y/o citología peritoneal positiva.
° ETAPA IIIA. G1, G2, G3. Tumor que invade la serosa y/o los anexos y/o citología perito-neal positiva.
° ETAPA IIIB. G1, G2, G3. Metástasis a vagina.
° ETAPA IIIC. G1, G2, G3. Metástasis a gan-glios pélvicos y/o para-aórticos.
• ETAPA IV. Metástasis intraabdominales, metástasis extraabdominales, y/o involucro a ganglios linfáticos inguinales, mucosa vesical o mucosa rectal.
° ETAPA IVB. Metástasis a distancia inclu-yendo ganglios intraabdominales y/o in-guinales.
Además se le debe asignar el grado de diferenciación:
• G1 = 5% o menos de un patrón de crecimiento sólido no escamoso o no morular.
• G2 = Seis a 50% de un patrón de crecimiento só-lido no escamoso o no morular.
• G3 = Más de 50% de un patrón de crecimiento no escamoso o no morular.
¿CUÁL ES EL PAPEL DEL TRATAMIENTO ADYUVANTE POSTOPERATORIO?
Para poder proponer un tratamiento adyuvante es fundamental la realización de una cirugía comple-ta con clasificación adecuada por ecomple-tapas, indepen-dientemente de la vía de abordaje.
MANEJO DE LA EC I, II
Corresponde a 80% de los casos, se asocia a una supervivencia de 85 a 90% para la EC I, mientras que para la EC II cuyo tumor se ha ex-tendido al estroma del cérvix es de 70%, con posi-bilidad de recaída local de 13%. La histología endometrioide es la más común en 75% de los ca-sos; los factores que confieren pronóstico desfa-vorable y mayor posibilidad de recurrencia son: variedad histológica no endometrioide, tumores G3, afección al miometrio mayor a 50%, presen-cia de invasión linfovascular y edad mayor a 60 años.
Radioterapia postoperatoria
Estudios aleatorizados han demostrado que la ra-dioterapia (RT) externa disminuye el riesgo de recu-rrencia local en CE, sin que exista mejoría en la supervivencia.57,58
La administración de RT adyuvante en CE tempra-no (etapas I y II), ha sido analizada en dos diferentes periodos para comparar el valor de la RT externa contra la braquiterapia; los períodos analizados abar-caron de 1988 a 1996 y de 1997 a 2005. En el primer periodo se incluyeron 44 pacientes tratados con RT externa y en el segundo, 82 casos tratados con bra-quiterapia. Estos dos grupos estuvieron bien balan-ceados en cuanto a edad, raza, profundidad de invasión del miometrio, grado histológico y afección al estroma cervical. El porcentaje de control pélvico
para el primer grupo fue de 93% comparado con 97% en el segundo grupo, sin existir impacto significativo en el tipo de tratamiento en cuanto al porcentaje de re-currencia en la cúpula vaginal así como en la super-vivencia libre de enfermedad o la supersuper-vivencia global entre los dos grupos.59,60
Quimioterapia adyuvante
En los tumores del cuerpo uterino diversos agentes citotóxicos han sido explorados cisplatino, doxorru-bicina, paclitaxel, topotecan, carboplatino, do-cetaxel, epirubicina, ifosfamida, ciclofosfamida, doxorrubicina liposomal. Cuando se han utilizado como modalidad de tratamiento de agente único, el cisplatino y la doxorrubicina han generado los índices de respuesta más altos (25 y 28%, respecti-vamente), en tanto que con la combinación de dos o tres de estos fármacos incrementa la proporción de respuestas objetivas entre 40 y 60%.
Las combinaciones más estudiadas son:
• Doxorrubicina/cisplatino (AP).
• Cisplatino/doxorrubicina/ciclofosfamida (CAP). • Cisplatino/epirubicina/ciclofosfamida (CEP). • Cisplatino/doxorrubicina/paclitaxel (TAC) y
paclitaxel/carboplatino (PC).61
En la población con CE en etapas tempranas I, II y factores de alto riesgo para recurrencia, se ha ex-plorado –en estudios retrospectivos– la quimiotera-pia adyuvante con el uso del esquema CAP; en pacientes en estadio I-IIB y IC-IIA (afectación menor o mayor de 50% del miometrio, glándulas endocervi-cales), se observó una supervivencia de 93 y 87% a cinco años, respectivamente.62,63
Otro estudio fase III, realizado en Italia, incluyó pacientes etapas IC-IIIC, 166 pacientes recibieron RT pélvica externa y 174 quimioterapia combinada (CAP); los resultados del análisis no mostraron dife-rencias en supervivencia libre de progresión ni so-brevida a tres, cinco o siete años.58
Ante esta evidencia se puede concluir que la qui-mioterapia adyuvante es una alternativa a la RT pélvica externa adyuvante ya que ha mostrado simi-lares resultados en supervivencia libre de progresión y supervivencia global; en enfermedad de alto riesgo se demostró una supervivencia superior con quimio-terapia que con RT.
Radioquimioterapia adyuvante
Greven, et al., reportaron los resultados finales del estudio fase II-RTOG 9708 en 46 pacientes con EC IC-IIIC en quienes se analizaron los efectos de la RT externa adyuvante (4,500 cGy en 25 fracciones) asociada a cisplatino 50 mg/m2 día uno y 28, seguida
de braquiterapia vaginal y cuatro ciclos de cisplati-no y paclitaxel cada 28 días. Con una mediana de se-guimiento de 4.3 años, la supervivencia libre de progresión fue de 85% y la supervivencia global de 81% a cuatro años, mientras que en las pacientes con etapa III fue 77 y 72%, respectivamente; en las pacientes con CE etapas IC, IIA y IIB no se observa-ron casos con recurrencia.64
En 2007, el grupo Nórdico de gineco-oncología, en colaboración con la EORTC presentaron los resulta-dos preliminares del estudio fase III que asignó 196 mujeres a recibir RT adyuvante y 186 a radioquimiote-rapia, las etapas incluidas fueron IC-IIIC. El grupo en estudio recibió quimioterapia después de la RT pélvica externa con o sin braquiterapia. Las combinaciones de fármacos fueron diversas (AP, paclitaxel/epirubicina/ carboplatino o paclitaxel/carboplatino). La mayoría de las pacientes completó la RT en el brazo control (90%), mientras que en el brazo en estudio, 25% no completó la quimioterapia principalmente por toxicidad. La su-pervivencia libre de progresión fue mayor en aquéllos tratados con radioquimioterapia (p=0.046) con dife-rencia absoluta a cinco años de 7% (75 vs. 82%) así como la supervivencia global (74 vs. 82%), sin signifi-cancia estadística en esta última diferencia (p = 0.08). Además, se observó progresión en 22% de las tratadas sólo con RT en comparación con 12% en el grupo de tratamiento combinado. Los autores concluyeron que la radioquimioterapia es mejor opción para aquellos casos con enfermedad de alto riesgo.65
Con la información previa, el Consenso considera que las mujeres con CE en etapas tempranas que
tengan factores de mal pronóstico, deben recibir RT y quimioterapia adyuvante secuencial, ya que mejo-ra la sobrevida libre de progresión y sobrevida glo-bal. Permanece por definirse la secuencia óptima de tratamiento (primero RT o primero quimioterapia) así como el esquema de quimioterapia, puntos que deben ser investigados en ensayos clínicos.
Para los casos en quienes esté contraindicada la RT adyuvante o no sea factible administrarla, la quimioterapia adyuvante debe ser considerada el tratamiento adyuvante de elección, sobre todo en los casos con alto riesgo de recurrencia. En el momento actual, los esquemas recomendados de quimioterapia son ciclofosfamida/doxorubicina/cisplatino o la com-binación de carboplatino/paclitaxel, tomando en cuenta su alta toxicidad hematológica por lo que debe ser planeada, administrada y vigilada por mé-dicos expertos en el manejo de fármacos citotóxi-cos.65,66
MANEJO DE LAS ETAPAS III Y IV
Aproximadamente 20% de las pacientes poseen en-fermedad extrauterina en el momento de la cirugía, la mayor parte de ellas se encontrarán en etapa III, mientras que la etapa IV se muestra en sólo 5%.
La EC III representa un grupo heterogéneo en términos de pronóstico, la supervivencia a cinco años varía de 30 a 70, existiendo una amplia varie-dad de manejos para esta etapa, que incluyen RT dirigida al sitio afectado, RT abdominal total, qui-mioterapia sola y radioquiqui-mioterapia.
En un estudio de 70 pacientes, 12 de ellas con EC IIIC y 58 con EC IV, se logró citorreducción óptima en 60% (42 pacientes), de las cuales, en 26 se logró dejar sin enfermedad residual visible, teniendo mejor supervivencia en comparación con el grupo en el que no se logró extirpar toda la enfermedad visible (51 meses vs. 14 meses, respectivamente). En este estu-dio, 45 pacientes recibieron quimioterapia post-ciru-gía. La supervivencia media para las que recibieron quimioterapia y no tenían enfermedad residual fue 52 meses, mientras que las que recibieron quimiote-rapia y tenían enfermedad residual fue de 16 meses. No se observó disminución en la supervivencia cuan-do fue necesario realizar procedimientos más radica-les que incluyeron esplenectomía, resección de algún segmento de intestino delgado, resección hepática o diafragmática.67
en los resultados del estudio fase II de Bruzzone donde 45 mujeres con EC III-IVB, después de ciru-gía radical fueron tratadas con 50 Gy de RT pélvica externa durante cinco semanas y posteriormente cuatro ciclos de quimioterapia con CEP cada 21 días. La supervivencia libre de progresión a cinco años fue 30% y la sobrevida global 53%; la princi-pal toxicidad de la RT fue diarrea grado 2 (38.2%) y de la quimioterapia fueron anemia, leucopenia, nausea y vómito. La sobrevida libre de progresión y sobrevida global a nueve años por etapa fueron:
IIIA/B 73 y 64%, IIIC 44 y 47%, IVA/B 44 y 22%, respectivamente.68
El estudio del GOG-122 aleatorizó 165 pacientes con EC III y IV posterior a cirugía óptima, a recibir RT abdominal total vs. quimioterapia adyuvante ba-sada en doxorubicina/cisplatino. Con seguimiento de 52 meses hubo mejor sobrevida libre de progresión y global en el brazo de quimioterapia en comparación con el de RT. El 55% de las pacientes desarrollaron recurrencia, la mayoría fuera de la pelvis. La recaí-da en pelvis fue de 21% para las pacientes tratarecaí-das
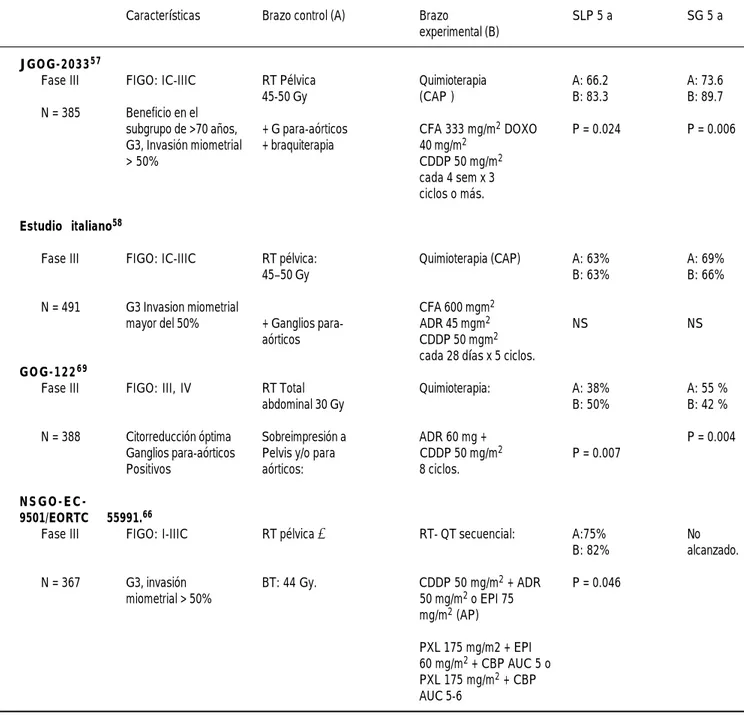
Cuadro 2. Estudios comparativos de tratamiento en cáncer de endometrio.
Características Brazo control (A) Brazo SLP 5 a SG 5 a experimental (B)
JGOG-203357
Fase III FIGO: IC-IIIC RT Pélvica Quimioterapia A: 66.2 A: 73.6
45-50 Gy (CAP ) B: 83.3 B: 89.7
N = 385 Beneficio en el
subgrupo de >70 años, + G para-aórticos CFA 333 mg/m2 DOXO P = 0.024 P = 0.006 G3, Invasión miometrial + braquiterapia 40 mg/m2
> 50% CDDP 50 mg/m2
cada 4 sem x 3 ciclos o más.
Estudio italiano58
Fase III FIGO: IC-IIIC RT pélvica: Quimioterapia (CAP) A: 63% A: 69%
45–50 Gy B: 63% B: 66%
N = 491 G3 Invasion miometrial CFA 600 mgm2
mayor del 50% + Ganglios para- ADR 45 mgm2 NS NS aórticos CDDP 50 mgm2
cada 28 días x 5 ciclos.
GOG-12269
Fase III FIGO: III, IV RT Total Quimioterapia: A: 38% A: 55 %
abdominal 30 Gy B: 50% B: 42 %
N = 388 Citorreducción óptima Sobreimpresión a ADR 60 mg + P = 0.004 Ganglios para-aórticos Pelvis y/o para CDDP 50 mg/m2 P = 0.007
Positivos aórticos: 8 ciclos.
N S G O E C
-9501/EORTC 55991.66
Fase III FIGO: I-IIIC RT pélvica ± RT- QT secuencial: A:75% No B: 82% alcanzado.
N = 367 G3, invasión BT: 44 Gy. CDDP 50 mg/m2 + ADR P = 0.046 miometrial > 50% 50 mg/m2 o EPI 75
mg/m2 (AP)
con RT abdominal total y de 26% en el brazo de qui-mioterapia, el mayor beneficio de la quimioterapia fue reducir la recaída a distancia siendo de 18% en el bra-zo de RT y de 10% en el brabra-zo del tratamiento sistémi-co, aunque el brazo de quimioterapia se asoció con mayor toxicidad hematológica y gastrointestinal.69
De acuerdo a los resultados de este estudio las pa-cientes con EC III y IV, deben ser candidatas para tratamiento sistémico con o sin RT dirigida al sitio del volumen tumoral. El esquema de doxorubicina y cisplatino fue considerado por muchos años el esque-ma estándar para enfermedad avanzada. El estudio GOG 177 en CE avanzado o recurrente que comparó un esquema triple paclitaxel + doxorubicina + cispla-tino (TAP) con factor estimulante de colonias, vs. el uso de doxorubicina + cisplatino (AP), mostró que el esquema triple es superior, pero también resultó ser un esquema mucho más tóxico teniendo que sus-pender el tratamiento en 24% de los pacientes en el grupo con TAP contra 10% en el grupo de AP.70
El esquema de paclitaxel + carboplatino, por su perfil de eficacia y buena tolerabilidad a pesar de que no ha sido evaluado en un estudio aleatorizado es un esquema que se prefiere utilizar.71
En el cuadro 2, se muestran los diferentes estu-dios aleatorizados que han comparado distintos es-quemas de tratamiento por etapas clínicas así como sus resultados.
MANEJO DE LA
ENFERMEDAD RECURRENTE
Aproximadamente 33% de las recaídas son localiza-das a la pelvis y 66% se han diseminado a otros sitios. En presencia de recaída pélvica se puede intentar ciru-gía, con la posibilidad de realizar excenteración pélvica de salvamento cuando esto es factible, así como la op-ción de utilizar la RT.72 Pacientes con recaída local no
susceptible de tratamiento con cirugía o RT y aquéllas
con enfermedad extensa y patrón diseminado, son con-sideradas para tratamiento sistémico paliativo que puede ser hormonal a base de progesterona o con qui-mioterapia, debiéndose tomar en cuenta para ello el ni-vel de actividad de las pacientes teniendo como objetivo retrasar la progresión de la enfermedad y mejorar la supervivencia, se debe atender el manejo de síntomas y mejorar la calidad de vida.
La quimioterapia para enfermedad recurrente ha sido basada en doxorubicina, epirubicina, cisplatino, carboplatino y paclitaxel, debiéndose tomar en cuen-ta para la decisión terapéutica la quimioterapia previa recibida. Se puede optar por administrar mo-nodroga o quimioterapia combinada con base en la edad de la paciente y el nivel de actividad. Con la quimioterapia combinada, se obtienen respuestas en un rango de 30 a 69%, mientras que con monodroga son de 17 a 34%. Comparando doxorubicina + cis-platino (AC) contra doxorubicina sola se obtuvieron respuestas de 42 vs. 25%,73 respectivamente. El
es-quema TAP, ya comentado previamente, aunque se asocia a mejor supervivencia no es aconsejable su uso por conllevar la posibilidad de alta toxicidad.
El tratamiento hormonal con un agente progesta-cional, habitualmente acetato de medroxiprogestero-na es umedroxiprogestero-na opción terapéutica, especialmente en pacientes con tumores de bajo grado, con receptores progestacionales positivos y con intervalo libre de enfermedad largo, pudiéndose esperar respuestas en pacientes con estas características hasta de 37%.74
Seguimiento
Se aconseja una evaluación cada tres o cuatro me-ses durante los tres primeros años, basado en histo-ria clínica, examen físico que incluya las áreas linfoportadoras y exploración ginecológica completa que incluya tacto recto-vaginal. A partir del tercer año las evaluaciones deben ser cada seis meses.
RECOMENDACIONES DEL
PRIMER CONSENSO MEXICANO DEL CÁNCER DE ENDOMETRIO
No existe evidencia suficiente para realizar escrutinio en mujeres con riesgo promedio. Si la mujer tiene dos o más factores de riesgo (diabetes mellitus, obesidad, ex-posición crónica a estrógenos, uso de tamoxifeno), de-ben entrar a un programa de escrutinio a partir de los 45 años, así como las mujeres posmenopáusicas que presenten sangrado transvaginal (abundante o goteo no
esperado) se les debe realizar biopsia endometrial me-diante histerescopia (Evidencia C, recomendación 1).
I.
PACIENTES CON
TERAPIA DE REEMPLAZO HORMONAL
Aplicable a pacientes posmenopáusicas que reci-ben estrógenos solos sin oposición o con progestáge-nos en su presentación oral, parenteral o tópica.
Vigilancia anual con ultrasonido de alta resolu-ción para medir espesor endometrial, preferentemen-te ultrasonido transvaginal:
• 1. Endometrio ≤ 5 mm.
° 1.1. Paciente asintomática.
∅ ∅ ∅ ∅
∅ 1.1.1. Continuar con vigilancia anual.
° 1.2. Paciente sintomática (sangrado transva-ginal).
∅ ∅ ∅ ∅
∅ 1.2.1. Se abordará como paciente con
endo-metrio ≥ 5 mm.
• 2. Endometrio ≥ 5 mm.
° 2.1. Paciente asintomática, optar por una de las siguientes:
∅ ∅ ∅ ∅
∅ 2.1.1. Histeroscopia con biopsia dirigida
(Evidencia A, recomendación 2).
∅ ∅ ∅ ∅
∅ 2.1.2. Biopsia fraccionada* en consultorio.
Utilizar cánula Pipelle o Novak.
∅ ∅ ∅ ∅
∅ 2.1.3. Legrado uterino instrumentado bajo
anestesia (en caso de no lograr realizar la biopsia endometrial en consultorio por do-lor, estenosis cervical o atrofia).
∅ ∅ ∅ ∅
∅ 2.1.4. Histerectomía total abdominal (tipo I)
con estudio transoperatorio (HTA+ETO) en caso de no lograr realizar alguno de los procedimientos previos (Evidencia C, reco-mendación 1).
° 2.2. Paciente sintomática (sangrado transvaginal).
∅ ∅ ∅ ∅
∅ 2.2.1. Suspender terapia de reemplazo
hor-monal.
∅ ∅ ∅ ∅
∅ 2.2.2. Ultrasonido de alta resolución con
Doppler, preferentemente transvaginal (en caso de no contar con ultrasonido previo) (Evidencia B, recomendación1).
∅ ∅ ∅ ∅
∅ 2.2.3. Histeroscopia con biopsia dirigida
(Evidencia A recomendación 1).
∅ ∅ ∅ ∅
∅ 2.2.4. Biopsia fraccionada en consultorio.
Utilizar cánula Pipelle o Novak.
∅ ∅ ∅ ∅
∅ 2.2.5. Legrado uterino instrumentado bajo
anestesia (en caso de no lograr realizar la biopsia endometrial en consultorio por do-lor, estenosis cervical o atrofia) (Evidencia C, recomendación 1).
∅ ∅ ∅ ∅
∅ 2.2.6. Histerectomía total abdominal (tipo I)
con estudio transoperatorio (HTA+ETO) en caso de no lograr realizar alguno de los procedimientos previos (Evidencia C, reco-mendación 1).
Resultado de la biopsia:
a) Positiva a cáncer endometrial:
• Suspender terapia de reemplazo hormonal. • Tratamiento específico para cáncer de
endo-metrio.
b) Negativa a malignidad:
• Evaluar la necesidad de continuar con terapia de reemplazo hormonal (tomar en cuenta otros factores de riesgo para cáncer de endo-metrio).
II.
PACIENTES CON USO DE TAMOXIFENO
En pacientes que utilizan tamoxifeno,** las reco-mendaciones incluyen a pacientes premenopáusicas y posmenopáusicas. El uso de tamoxifeno no debe ser mayor a cinco años (Evidencia A, recomenda-ción 1).
Recomendaciones previas al inicio de uso de tamoxifeno
• Realizar ultrasonido de alta resolución preferen-temente transvaginal para descartar patología endometrial preexistente y obtener dimensión
ba-* Se considera biopsia fraccionada cuando se realiza inicialmente legrado endocervical y posteriormente biopsia endometrial incluyendo las cuatro paredes de la cavidad uterina en sentido de las manecillas del reloj. Las muestras se realizan con instrumentos independientes y se envía el material en recipientes separados para evitar contaminación celular (Evidencia B, recomendación 1).
sal del espesor endometrial para comparaciones ulteriores (Evidencia B, recomendación 1).
Recomendaciones durante el tratamiento con tamoxifeno
Vigilancia anual con ultrasonido de alta resolu-ción para medir espesor endometrial, preferentemen-te ultrasonido transvaginal, punto de corpreferentemen-te 5 mm:
• 1. Endometrio < 5 mm en paciente asintomá-tica.
° 1.1 Continuar con vigilancia anual.
• 2. Endometrio < 5 mm en paciente sintomáti-ca, endometrio ≥ 5 mm en paciente con o sin sangrado transvaginal, optar por una de las si-guientes:
° 2.1 Ultrasonido de alta resolución con Do-ppler, preferentemente transvaginal (en caso de no contar con ultrasonido previo).
° 2.2 Histeroscopia con biopsia dirigida.
° 2.3 Biopsia fraccionada en consultorio. Utili-zar cánula Pipelle o Novak.
° 2.4 Legrado uterino instrumentado bajo anes-tesia (en caso de no lograr realizar la biopsia endometrial en consultorio por dolor, esteno-sis cervical o atrofia).
° 2.5 Histerectomía total abdominal (tipo I) con estudio transoperatorio (HTA+ETO) en caso de no lograr realizar alguno de los procedi-mientos previos.
Resultado del estudio histopatológico de biopsia o pieza quirúrgica
• Negativa a malignidad:
° En pacientes posmenopáusicas cambiar a inhi-bidor de aromatasa para completar cinco años de hormonoterapia (si se cuenta con el recur-so), de lo contrario continuar con tamoxifeno. Se incluyen pacientes con menopausia quirúr-gica en las que se realizó histerectomía total abdominal y salpingooforectomía bilateral (HTA + SOB).
° En caso de preservar útero, se recomienda continuar con ultrasonido anual para medir espesor endometrial y completar cinco años de hormonoterapia con inhibidores de aromatasa (si se cuenta con el recurso).
• Hiperplasia endometrial (cualquier tipo):
° Individualizar caso.
° Ofrecer histerectomía con salpingooforectomía bilateral en pacientes sin contraindicación qui-rúrgica.
° En pacientes posmenopáusicas cambiar a inhi-bidor de aromatasa para completar los cinco años de hormonoterapia (si se cuenta con el recurso), de lo contrario continuar con ta-moxifeno. Se incluyen pacientes con menopau-sia quirúrgica en las que se realizó HTA + SOB.
° En caso de preservar útero, se recomienda continuar con ultrasonido anual para medir espesor endometrial y completar cinco años de hormonoterapia con inhibidores de aromatasa (Evidencia B, recomendación 1).
• Positiva a malignidad:
° Suspender tamoxifeno.
° Tratamiento específico para cáncer de endo-metrio.
° Al término del tratamiento de cáncer endome-trial, reiniciar hormonoterapia con inhibido-res de aromatasa para completar los cinco años de hormonoterapia.
Recomendaciones al
finalizar tratamiento con tamoxifeno
• Continuar vigilancia del espesor endometrial en forma anual.
• Realizar biopsia endometrial en caso de sangrado transvaginal o espesor endometrial ≥ 5 mm.
III. ESTUDIOS DE
EXTENSIÓN CUANDO LA BIOPSIA ES REPORTADA POSITIVA
La estadificación del cáncer de endometrio es qui-rúrgico-histológica. La cirugía estadificadora debe realizarse por cirujano oncólogo o ginecólogo oncó-logo.
• Necesidad de reintervención quirúrgica por dificul-tar técnica en la primera intervención quirúrgica. • Reporte histológico preoperatorio que sugiera
alto riesgo para diseminación extrauterina (gra-do 3 o estirpe seroso papilar, células claras o car-cinosarcoma).
• Estudio histopatológico definitivo de cáncer en-dometrial no esperado posterior a histerectomía realizada por otras indicaciones.
• Evidencia de enfermedad cervical o extrauterina. • Citología de lavado peritoneal positivo a células
malignas.
• Sospecha o diagnóstico de enfermedad recurrente. • Cuando se ha considerado tratamiento no
qui-rúrgico.
Estudios
• Examen clínico completo incluyendo áreas linfo-portadoras (supraclaviculares, axilares, inguina-les) y exploración ginecológica incluyendo tacto recto-vaginal para evaluar parametrios y tabique rectovaginal.
• Ultrasonido de alta resolución preferentemente transvaginal (en pacientes en las que se realizó la biopsia endometrial sin ultrasonido previo). • Citología cervicovaginal.
• Histeroscopia con biopsia dirigida (en caso de contar con el recurso) además de ser útil para de-terminar localización del tumor (afección a ist-mo, canal cervical) y extensión (tamaño).
• Radiografía de tórax.
• Estudios de laboratorio: BH, PFH, QS, TP, TPT, EGO.
• En histologías desfavorables, además solicitar CA-125.
• Resonancia magnética si el hospital cuenta con el recurso y si su realización es a corto plazo y no retrasa la estadificación quirúrgica; no debe ser utilizada para obviar la linfadenectomía pélvica. • Manejo de comorbilidades y valoración preoperatoria.
La tomografía computada tiene poca utilidad en determinar la extensión de la enfermedad, por lo que el consenso no recomienda su uso para evaluación preoperatoria.
IV.
ESTUDIO HISTOPATOLÓGICO
• 1. Debe realizarse estudio transoperatorio (ETO) de útero en forma rutinaria para fines de estadificación.
• 2. Los propósitos del estudio transoperatorio de útero son:
° 2.1. Descartar malignidad en caso de duda diagnóstica histológica en endometrio ≥ 5 mm sin biopsia previa.
° 2.2. En diagnóstico de cáncer de endometrio, la utilidad del estudio transoperatorio es:
∅ ∅ ∅ ∅
∅ 2.2.1. Corroborar histología. ∅
∅ ∅ ∅
∅ 2.2.2. Corroborar grado histológico. ∅
∅ ∅ ∅
∅ 2.2.3. Determinar profundidad de invasión
al miometrio.
∅ ∅ ∅ ∅
∅ 2.2.4. Determinar extensión cervical
(mu-cosa y/o estroma).
∅ ∅ ∅ ∅
∅ 2.2.5. Determinar afección a istmo. ∅
∅ ∅ ∅
∅ 2.2.6. Determinar afección a anexos.
• 3. El estudio transoperatorio debe:
° 3.1 Realizarse por médico patólogo.
° 3.2 En caso de no contar con el servicio de patología, el útero debe ser seccionado por el cirujano (cirujano oncólogo o ginecólogo on-cólogo) mediante corte coronal para obtener un segmento anterior y otro posterior (Evi-dencia C, recomendación 1).
V.
CIRUGÍA ESTADIFICADORA
Histología favorable (endometrioide)
a) Cirugía estadificadora recomendada:
° Laparotomía exploradora mediante incisión infraumbilical media.
° Citología de líquido en caso de ascitis o lavado peritoneal.
° Exploración de cavidad abdomino-pélvica. ° Histerectomía total abdominal y
salpingo-oofo-rectomía bilateral (histesalpingo-oofo-rectomía extrafascial) con estudio transoperatorio (HTA + SOB + ETO).
b) En caso de estar presente uno o más de los si-guientes:
° Cáncer de endometrio de alto grado o poco di-ferenciado.
Realizar además:
• Linfadenectomía pélvica y para-aórtica. • Omentectomía infracólica.
• Remoción de tejido parametrial hasta la pared pél-vica (en el caso de extensión al estroma cerpél-vical).
c) En la presencia de ganglios palpables:
° Todo ganglio(s) palpable(s) debe retirarse y enviar a ETO.
° Con uno ó más ganglios positivos pélvicos en ETO, debe realizarse detumorización y linfa-denectomía para-aórtica (Evidencia C, reco-mendación1).
Histología desfavorable (seroso papilar y células claras)
a) Cirugía estadificadora recomendada:
° Laparotomía exploradora mediante incisión infraumbilical media.
° Citología de líquido en caso de ascitis o lavado peritoneal.
° Exploración de cavidad abdomino-pélvica. ° Histerectomía total abdominal y
salpingo-oofo-rectomía bilateral con estudio transoperatorio (HTA + SOB + ETO).
° Linfadenectomía pélvica y para-aórtica. ° Omentectomía infracólica.
b) En la presencia de ganglios palpables:
° Todo ganglio(s) palpable(s) debe retirarse y enviar a ETO.
° Con uno o más ganglios positivos pélvicos en ETO, debe realizarse detumorización y linfa-denectomía para-aórtica (Evidencia C, reco-mendación 1).
Laparoscopia
Las ventajas de la laparoscopia comparada con laparotomía son varias:
• Facilita la estadificación en pacientes obesas. • Existe menos sangrado transoperatorio. • Disminuye el tiempo estancia postoperatoria. • Existe mejor recuperación del evento quirúrgico.
El consenso recomienda utilizar la laparoscopia con fines de estadificación, sólo al cumplir los si-guientes requisitos:
• Entrenamiento adecuado para esta técnica por parte de los cirujanos oncólogos y ginecólogos oncólogos. • Contar con el equipo adecuado, tanto humano
como técnico.
• Haber completado la curva de aprendizaje, reco-mendando entre 25 y 30 procedimientos de esta-dificación en cáncer de endometrio, especialmente para la disección para-aórtica (Evidencia B, reco-mendación 1).
VI.
ETAPA IA, IB, G1, G2
Etapa I
1. Cirugía estadificadora.
2. Omentectomía (variedad no endometrioide). 3. No tratamiento adyuvante (proporcionar
braqui-terapia en el caso de que se reporte invasión lin-fovascular) (Evidencia C, recomendación 1).
VII.
ETAPA IA, IB, G3
1. Cirugía estadificadora
2. Omentectomía en el caso de variedad no endome-trioide.
3. Braquiterapia vaginal.
• Alta tasa de dosis: Cuatro aplicaciones de 6 Gy cada una, o
• Baja tasa de dosis: 35 Gy a 0.5 cm cúpula va-ginal (Evidencia D, recomendación 1).
4. Radioterapia pélvica externa en variedad no en-dometrioide y factores de mal pronóstico: Radio-terapia con técnica de caja, cuatro campos, 50 Gy (1.8 a 2 Gy/día) 25 a 28 fracciones.
5. Quimioterapia adyuvante (posterior a radiotera-pia) en variedad no endometrioide y factores de mal pronóstico:
• CAP (ciclofosfamida, adriamicina, cisplatino) cada 21 días x cuatro ciclos. (Evidencia B, re-comendación 2), o
• Paclitaxel + carboplatino* cada 21 días x seis ciclos (Evidencia C, recomendación 1).
Se puede administrar quimioterapia como
sibilizador a base de CDDP 50 mg día uno y 28 durante la radioterapia a pelvis externa (Eviden-cia C, recomendación 2).
VIII.
ETAPA II, G1, G2
1. Cirugía estadificadora.
2. Omentectomía en el caso de variedad no endome-trioide.
3. Braquiterapia vaginal.
• Alta tasa de dosis: Cuatro aplicaciones de 6 Gy cada una, o
• Baja tasa de dosis: 35 Gy a 0.5 cm cúpula va-ginal (Evidencia D, recomendación 1).
4. Radioterapia pélvica externa en variedad no en-dometrioide y factores de mal pronóstico: Radio-terapia con técnica de caja, cuatro campos, 50 Gy (1.8 a 2 Gy/día) 25 a 28 fracciones.
Se puede administrar quimioterapia como radio-sensibilizador a base de CDDP 50 mg día uno y 28 durante la radioterapia a pelvis externa (Evidencia C, recomendación 2).
IX. ETAPA II, G3
1. Cirugía estadificadora.
2. Omentectomía en el caso de variedad no endome-trioide.
3. Braquiterapia vaginal.
• Alta tasa de dosis: Cuatro aplicaciones de 6 Gy cada una, o
• Baja tasa de dosis: 35 Gy a 0.5 cm cúpula va-ginal (Evidencia D, recomendación 1).
4. Radioterapia pélvica externa en variedad no en-dometrioide y factores de mal pronóstico: Radio-terapia con técnica de caja, cuatro campos, 50 Gy (1.8 a 2 Gy/día) 25 a 28 fracciones.
5. Quimioterapia adyuvante (posterior a radiotera-pia) en variedad no endometrioide y factores de mal pronóstico:
• CAP (ciclofosfamida, adriamicina, cisplatino) cada 21 días x cuatro ciclos. (Evidencia B,
re-comendación 2), o
• Paclitaxel + carboplatino* cada 21 días x seis ciclos (Evidencia C, recomendación 1).
Se puede administrar quimioterapia como radio-sensibilizador a base de CDDP 50 mg día uno y 28 durante la radioterapia a pelvis externa (Evidencia
C, recomendación 2).
X.
ETAPA IIIA Y IIIB
1. Cirugía estadificadora. (Omentectomía en el caso de variedad no endometrioide).
2. Quimioterapia:
° CAP cada 28 días x seis ciclos (Evidencia B, recomendación 2).
° Paclitaxel + carboplatino* cada 21 días x seis ciclos (Evidencia C, recomendación 1).
3. Radioterapia pélvica externa: radioterapia con técnica de caja, cuatro campos, 50 Gy (1.8 a 2 Gy/día) 25 a 28 fracciones
4. Braquiterapia vaginal:
° Alta tasa de dosis: Cuatro aplicaciones de 6 Gy cada una, o
° Baja tasa de dosis: 35 Gy a 0.5 cm cúpula va-ginal.
No se proporciona quimioterapia a las pacientes que tengan citología positiva, como única evidencia de enfermedad extrauterina.
XI. ETAPA IIIC
1. Cirugía estadificadora (Omentectomía en el caso de variedad no endometrioide)
2. Quimioterapia seguida de Radioterapia. Quimiote-rapia a base de:
° CAP cada 28 días x seis ciclos (Evidencia B, recomendación 2), o