h
c
i
-r
c c
6-
n
t ! b.4
-
I u*c ! u
R
,
Li
'
I...
J
NOMBRE: Maria d e l S o c o r r o G a r c i a R o j a s .TELEFONO: 3-96-57-14
MATRI CULA: 833;24676
NOMBRE: G i s e l a S i l v a G u t i e r r e z .
TELEFONO: 6-70-63-92
MATRICULA: 83323493
c L A v E - - & Z - 3 . W
_____---
7
-cas
/CARRERA: I n g e n i e r i a B i o q u i m i c a I n d u s t r i a l .
TRIMESTRE: 87-0
HORAS SEMANA: 20 HRS
LUGAR DONDE SE LLEVARA A CARO: L a b o r a t o r i o s d e l D e p a r t a m e n t o d e
R i o t e c n o l o g i a e n e l e d i f i c i o S d e e s t a U n i d a d .
FECHA DE I N I C I O : 7 d e s e p t i e m b r e d e 1987.
/FECHA DE TERMINACION: 7 d e f e b r e r o d e 1988
JNüMRRE DEL. TUTOR INTERNO: Jean P i e r r e G u y o t .
/TITULO: C e l e c c i b n d e F u e n t e s P o t e n c i a l e s d e I n b c u l o s N a t u r a l e s
.
/
p a r a D i g e s t o r e s A n a e r o b i o s .
G i s P i a S i i v % G u t i e r r e z .
* SELECCION DE FUENTES POTENCIALES
DE
INOCULOS NATURALES PARA DIBESTOREB ANCHROBIOS.c
1 . ANTECEDENTES.
L a t o t a l i d a d de l a s aguas reBidUale6 producidas en
MBxico en
1985f u e de 160 in3/., de l o s c u a l e s e1 17.5% f u b t r a t a d o y s o l o e l 9.25X
r e s u l t b con l a s e f i c i e n c i a % esperadas (SEDUE 1985).
A h
asi l a gran mayoria cuenta solamente con tratamiento primario.Para t r a t a r 20.5 m5/s en 15 plantas de tratamiento proyectadas para i n s t a l a r s e o? el ‘periodo 1983-2000, NAFINSA (1986) ha calculado que SR necesitarah $ 27,905,000.00 a precio% de 1985, s i n considerar la’s rede8 de a l c a n t a r i l l a d o . Re6pecto d e l a demanda potencial
se
prevben, en e l mismo estudio, 922 plankasde
tratamiento*con una i n v w s i b n d e175,943,000.00 para el rnicmo peribdo.
Ante l a magnitud d b l a i n v w s i b n e5 necesario considerar o t r a s
opciones
a
l o s sistemas convencionales, con o b j e t o de r e d u c i r costos s i n s a c r i f i c a r e f i c i e n c i a s de tratamiento.E l tratamiento anaerobio
se
presenta como una a l t e r n a t i v a apropiada por l a a l t a e f i c i e n c i a de l o s nuevos procesos de tratamiento de aguas negras. Particularmente el proceso de lecho granular de t i p o üüSü que esta bien adaptado para el problema queso
presenta ene1
p a i s : porque t i e n e a l t o s rendimientos,es
de f h c i l instalacibn y mantmimiento, necesita poca mano d e obra, por i o quees
de b a j ocosto.
Este t i p o d e p r a e s o
se
c a r a c t e r i z a p w una a l t a retoncibn de biomasa activa, por medio de l a formacibn de lodos granulados que tienen buenas capacidades de retención.En el
reactor RS disehada unacampana de decantación que f a c i l i t a ademhs l a separaci&n del gas producido, de l a biomasa y del efluente.
r r
.. .
.
......
"_<
.
2.
JUSTIFICACION.
E l arranque de
estos
t i p o sde
d i g e s t o r e ses
d i f i c i l y toma tiempo(2-3
meses), a menudo por f a l t a d e un inoculo bien adaptado.Cldemhs, en
Hbxico
todaviano
se
conocenfuentes
d e abastecimiento de e s t o r inóculos, de donde surge l a necesidad d e determinar l a ractividades metanogbnicas de v a r i a s fuentes potenciales de: e s t i c r c o l , lodos activados de plantas de tratamiento de aguas negras y sedimen- tos.
*-
I
c-
...,.
3.
INTROD!JfXION.3 ,
Los avances en los sistemas de tratamiento anaerobiri de# aguar negras v i a metarro
se
han venido desarrollandoen los
altimosahos.
Estos
sistemas estan basadosen
l a rctencibn de l a micro-f l o r a metanogbnica, especialmente a q u e l l a s que convierten Lcido acetic0 a metano.
E l '
resultadoes
una mayor concentracibn-
dm" --.A-
-__.-- -_^_
E5QüEMA
.
. .
DEL
DIGESTOR
UR50
-J:
.
.
...
.
M a t c r i a OrgAni ca Car bohi dr ato.
P r o t e l n a r
L l
p i dosI
( 1 ) H i d r b l i s i s y Fermentacibn
I
Ac i dos O r asos
'
1'
.
i h r h i d r o g e n a c i bn'icetogbnica. ( 2 )
D e u a r b o x i l a c i b n
Ac e t ato. ( 3 )
For mac i bn
de metano reducido ( 3 )
1
CH,
+
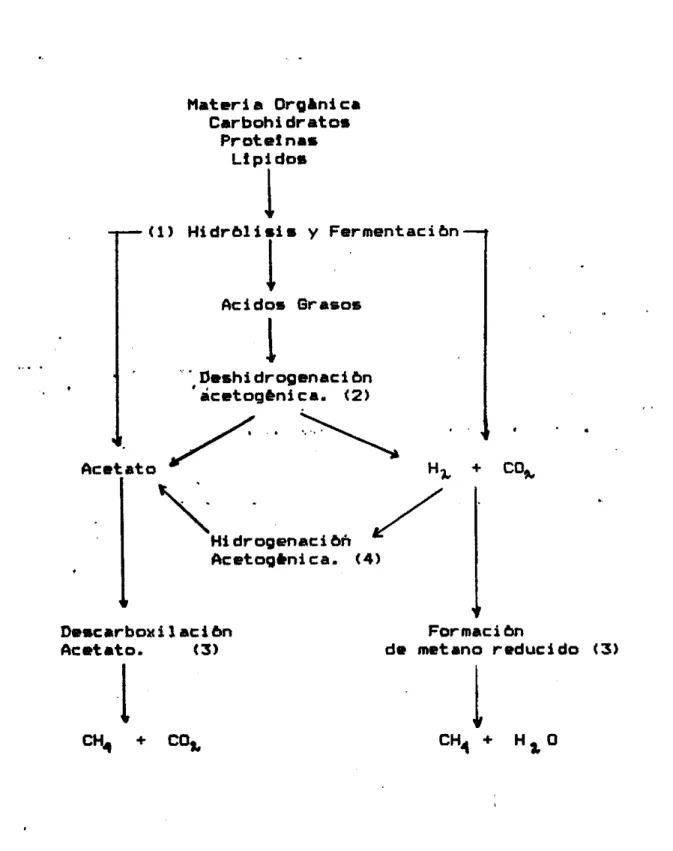
H,,0Fig. Esquema de t r e s artados para l a degradación anaerobia
completa de materie orghnica, muestra una r u t a g m e r a l y presenta l o s
t r e s grupos metabblicos de l a r bacterias: ( 1 ) b a c t e r i a s fermentativas#
.
Etapas de l a fetmentacíon mctanogfmica:
La fermentacíbn metanog&nica ha s i d o separada
dentro
d e v a r i o s esquemas, ínvolucrando difRrRnteS etapaso
grupos metaboiicos de bac-terias
en orden delmls
f A c í l de e x p l í c a r í a microbíologia, qulmica y cínCtíca de 106 procesos. Sí bienestos
grupos de b a c t e r i a s pueden s e r Separadosen
un esquema, SU f i s í o l o e í a y metabolismo esinterdependiente.
Hasta l a fecha se reconoce una degradací&n anaerobia de l a materia organíca que c o n s i s t e
en
tres
etapas:.
La primera etapa involucra l a s b a c t e r i a s h i d r o l l t i c a s fermentati- vas. Estas b a c t e r i a s producen principalmente
a
p a r t í r d e l a . materia w g h n i c a i n i c i a l acidos grasos v o l l t i l e s iAGV'65), etanol, hidropeno y CO*.
Aeste
n i v e l íntervíenen b a c t e r i a s fermentativas c l l s i c a s iclos-t
ri di a, bsci1 1
us,
Q t C ..
.
).
La
segund; etapaes
;calizada por medio de un complejo d e b a c t e r i a s llamadas b a c t e r i a s a c e t o g h i c a s productoras oblígadas de hidrogeno(OHPA).
Este
grupo degrada los. A O V ' s y etanolim
acetato;CO*
e
H s,
pero s e necemíta e s t a r
en
estrecha r e l a c í b n con b a c t e r i a s hidrogeno- f f l i c a s , de t a l manera queno re
acumule el hidrbgeno producido quees
un inhíbídor de l a reacc'ibn acctogLníca. Tal r e l a c í b n de interdependen c i a para el hidropeno.
5e
llama t r a n s f e r e n c i a interespecies db hidrogenoLa
t e r c e r a etapa e s t a c o n r t í t u í d a por b a c t a r í a s iactanogenicas queSR pueden d í h d i r principalmente
en
dos grupos metabblícosr- l a s b a c t e r i a s metanogCnícas h i d r o g e n o f í l í c a r , l a s cuales u t i l i z a n el hídrbgeno producido por l a s etapas
anteriores
para reducir el COIen
CHd
.
- l a s bacteria8 metinog&nícar a c e t í c l l s t í c a s que transforman el acetato en CHq y COc
.
Esta transformacibn cuenta cone1
70%en l a
produccíbnd e metano en
lor
dlgR8tOreS.E l mantenimiento de b a j a s concentraciones de hídrbgeno en
el
e c o r í s tema e5 esencial para l a e f í c í e n c í a de l a fermentacíbn p w dos r a -zones.
Primero,
l a
produccíbn de electrones reducidos d!unínuyeproductos del píruvato t a l e s
como
propíonato, butírato, etanol y l a c t a t o 'e
incrementa l a fwmacíbn de acetato, porlas
b a c t r r í a sfermentativas
a
condícibn de queesten
en
r e l a c í b n con b a c t e r i a s hidrogenof!lícas paral a
remoción permanente del hídrbgeno producido. Segundo, es esencial para e1 catabolísmo de propíonato yotros
acídos graoosa
acetato Q hídrbgmo, para ser tamodínamícamrntr f a v o r a b l e , por ejemplo:se
necesita una presíbn p a r c i a l de hidrbgeno inferior a Id'atm para hacer f a c t i b l e l a degradacíbn del propionato.La destruceibn de l a matería o r g l n i c a e s t a relacionada dirrctamentr
con l a proüuccíbn de metano. La e f í c í r n c í a de
la
fernantacibnesta
vínculada con.ri tiempo de rMtenCibn del n i t R r i i 1en
e1 reactor y l a carga volum&trica w g l n í c a . En casí toda5 l a s fermentacíoner anarro-.
Í‘
i.
r
.
~
L”
T
L
r
L,
cr
BI BL
I
OORAF I ALettinga A. F.
M.
Van Velsen 6. W. Hobwa, W. de Zeeun 81 A. Klapwijk,Use of t h e Sludge Blanket
turn)
Reactor Concept f o r Bi,ological treatment. Wastewater treatment, Especi a l 1 y f o r Anaerobic(Biotechnology and Bioengineering. Vol. XXII. pp. 499-734 (1980)
).
Heinrich F. Kas#ar and .Karl Wuhr.mann. Cinetic parameters and r e l a t i v e turnovers ’
04
some
important c a t a b o l i c r e a c t i o n s i n Digesting Sludge.Applied and Environmental Microbiology, July 1978 p. 1-7.
Heinrich F. Karpar and Karl Wuhrmann. Product I n h i b i t i o n in Sludge Digestion. Microbial Ecology 41241-248 (1978).
Michael J. Mc Inerney ‘and.Marvin P. Bryant. ‘Rmview
o + ’
Mcthsno Fermentation Fundamentals. Cap. 2 FuelGas
Production from Biomass.Mah Robert A-, The Methanogenic Bacteria, their Ecology and Phisiology. Trends i n the Biology of Fermentation f o r Fuels and Chemicals. (1981).
Mah Robert A. and Smith Michael R. T h e Prokaryotes. A Handbook on Habitats, I s o l a t i o n , and I d e n t i f i c a t i o n o+ Bacteria. 1981. Printed
in
M A .
L. Van Den Berg. Developments
i n
Methanogenesis from IndustrialWastewater. CAN. J. Microbiol.
Vol.
30, 1984, p. 975-987.. . .
* I
-.
3 .NOMBRE: Maria del Socorro Garcia hojas
TELEFONO:
3-96-57-14MATRICULA:
83324676NOMBRE: Gisela Silva Gutierrez.
TELEFONO:
6-70-63-92MATRICULA:
83323493CARRERA: Ingenieria Bioquimica Industrial
TRIMESTRE:
87-0HORAS SEMANA:
20HRS
LUGAR DONDE SE LLEVARA A CABO: Laboratorios del Departamento d e
Biotecnologia en el edificio S de esta Unidad.
FECHA DE INICIO:
7de septiembre de
1 9 8 7 .FECHA DE TERMINACION:
7
de febrero de
1 9 8 8 .NOMBRE DEL TUTOR INTERNO: Jean Pierre GUYGt.
TITULO: Selecci6n d e Fuentes Potenciales d e In6culos Naturales
para Digestores Anaerobios.
Ma. del
ro
Garcia hojas.
R
_____
Gisela Silva isutierrez.
SELECCION DE FUENTES POTENCIALES DE INOCULO5 NATURALES PARA DIGECTOFCEC ANAEROBIOS.
INTRODUCCION
Los
digestores anaerobios ofrecen mayores ventajas para los procesos anakrobios, ya que no requieren equipo n i energía parala aereación, -tienen una limitada producción de desecho y
producen metano (McCarty 1964). Los reactores de tipo avanzado tales como e l digestor de lecho de lodos y
el
de pelicula fija, ofrecen buenas alternativas para e l tratamiento de desechoslíquidos (Noyola 1988). ~
.
El reactor anaerobio de lecho de lodos (UACB: Upflow Anaero- bic Sludge Blanket), (Lettinga et a l
.,
1980,1982) de flujo ascendente, ejerce una cierta selectividad sobre los microorgani- smos presentes, favoreciendo l a formación en l a parte inferior de un lodo g r a n u h r con buenas propiedades de sedimentación, l o que = d a una^ alta retención de biomasa activa en e l reactor. Además secaracteriza por tener un colector de gas que asegura una buena sepaEación liquido-gas-sólido.
A 1
arrancar un reactor UACB, loideal es inocularlo con un volumen suficiente de algun inóculo
~. apropiado disponible. (Arias y Noyola, 1987).
El reactor tubular de pelicula fija es un filtro anaerobio empacado en forma ordenada, lo-cual crea canales bien definidos, (Van den Berg y Lentz, 1 9 7 9 ) , como en todo reactor de biomasa
-
fija sobre soporte, los tiempos de arranque son importantes, debido a que l a adhesión y el posterior crecimiento de los mic.roprganismos para formar l a biopelícula son procesos lentos, sobre todo en anaerobiosis.La destrucción de l a materia orgánica esta relacionada directamente con l a producción de metano. La eficiencia de la fermentación . esta vinculada con e l tiempo de retención del mate-
rial en e l reactor y l a carga volumétrica orgánica. En casi todas las fermentaciones anaerobias el paso limitante es l a transforma- ción del acetato en metano. Los parametros del medio ambiente y
nutrientes tienen l a necesidad de mantener un nivel óptimo, para
l a
eficiencia de l a fermentación.Dentro de estos digestores, l a conversión de compuestos orgánicos a productos terminales como
CH4
yC O L
,
consiste en una serie de reacciones realizadas por un consorcio de bacterias.La fermentación metanogénica, ha sido separada dentro de un esquema, involucrando diferentes etapas y grupos metabólicos de bacterÍas por el orden mds'fdcil de explicar l a microbiologia, química y cinética de los procesos. Aunque estos grupos de bacte- rias puedan ser separadas en un esquema, su fisiología y metabo-
Hasta la fecha s e reconoce una degradaci6n anaerobia de
la
materia orgánica que consiste en
tres etapas:
(McInerney
8iBryant,
1980).La primera etapa involucra
l a sbacterias hidroliticas fer-
mentativas.
Estas bacterias producen principalmente
apartir
d e
la materia orgánica inicial ácidos grasos volátiles
CPG~Vs),eta-
nol,
H s yCO$,
'.
A
este nivel intervienen bacterias fermentativas cldsicas
(clos-
tridia, bacillus, etc..
. ) .La segunda etapa
esrealizada por medio de una complejidad
debacterias 'llamadas
bacterias acetog6nica.s producto.ras obliga-
das
d e hidr6gdno ( O H P A ) .Este
grupo degrada los
ñBVs .yetanoi en
acetato,
C o ae
HLpero
se necesita estar en
estrecha
relaci6n con
bacterias hidrogenofilicas,
de tal manera que
nose acumule el
hidr6geno producido que
es un inhibidor de la reacci6n
ace-
togénica.
Tal
relación de interdependencia para
el
hidr6geno se
llama transferencia interespecies de hidr6geno.
-
L a tercera etapa esta constitui&a
por bacterias meta-
nogénicas que s e pueden dividir principalmente en dos grupos
metab6licos:
I -_-
Las bacterias metanogénicas hidrogen-of
ilicas,
las cuales
utilizan
el .hidr6geno
producido-
p o r l a setapas anteriores para
reducir el
C O L en
CH4.
-
Las
bacterias
metanogénicas acetoclásticas que -transforman
e1acetato en CH4
yC O Z .Esta transformaci15n cuenta con el
70%
( S m i t h y Mah, ,1966)
en la producción d e metano en los digestores.
El
mantenimiento de bajas c6ncentraciones de hidr6geno en
el ecosistema!
es esencial para l aeficiencia d e la fermentaci6n
por
dos razones:
Primero,
la producci6n de electrones reducidos
que disminuye los productos-
del piruvato,~tales
como:propionato,
butirato,
etanol
ylactato e incrementa la formaci6n de acetato,
por
las bacterias fermentativas
acondici6n
deque esten
enrelaci6n
conbacterias hidrogenof ilicas para
la
remoción
permanente del hidr6geno producido.
Segundo, es esencial para el
catabolismo d e propionato y otros ácidos grasos
aacetato e
hidrcjgeno,
p a r a sertermodinamicamente favorable, por ejemplo: se
necesita una
'presi6n parcial de hidrógeno inferior
a10"-4
a t m
para hacer factible la degradación del propionato.
.~ ~
-
Mat
e
ri
a
O
rg
án
i c
a
Caibohidra
tos
Proteinas
L i pidos
1
( 1 )
Hidrdlisis
yFermentacidn
Acidos Grasos
Deshidrogenacidn
acetogénica.
(2)$-
I
Acetato
HAHidrogenac i6n
acetogénica.
( 4 )+
coz
- 1
Descarboxilaci6n
d e acetato.
(3)Formacidn de
metano reducido.
( 3 )
3
-
Rasado en el esquema de degradación de la materia orgánica en anaerobiosis, este trabajo se propone analizar- l a composición .
microbiana de posibles fuentes de inóculos para recomendar e l USO
de astos en digestores anaerobios, debido a que existen pocas instalaciones para abastecer de inóculos ya adaptados, es necesario encontrar fuentes de inóculos apropiados para digestores especificos del tipo UACB y Tubular.
.~
MATERIAL Y METODOS
A ) Condiciones experimentales. Las técnicas anaerobias de Hungate (1969) y Balch et al., (1976), fuerón utilizadas a lo .,largo de este estudio, tanto para l a preparación de
los
medios decultivo como para l a transferencia de - sustratos y las inocula-
-
' ciones.
B)
CuantificaCión de I;as bacterras.
Las bacterias anaero- bias fueron cuanCificadas utilizando l a técnica del número más probable(NMP),
con
cinco
tubos, (Garcia et al., 1982). Los medios de Balch et a l (1979)- fueron utilizados para el cultivo deI
las bacterias metanogénicas. Para las bacterias OHPA (obligate hydrogen-producing acetogenic bacteria) (McInerney & Bryant,'
1981) se emplearon los mismos medios, excepto que los sulfatos fueron cambiados por cloruro.;, las muestras de inóculos fueron, procesadas dentro de una recámara anaerobia tipo Coy y homogeni- zadas utilizando un maceradbr-de tejidos.
-
I
La determinación de
los
sólidos suspendidos totales ( S C T ) yvolátiles ( C S V ) , :se determinaron por los metodos estandares (1976).
E l metano se analizó por cromatografía de gas equipado con un detector de ionización de llama.
,
c
^.
=
-
h
r”
TABLA
1.GRUPOS METANOGENICOS CUANTIFICABLES
L
c
Y
NOMBRE
SI
MBOLO
CUCTRATO
CARACTER DETERMINADO
rnB.Fermentativas
FGlucosa,
Crecimiento
B.OHPA
(Obligate
Hydrogen-Producing
OP
r
Propionato
Metano
Acetogenic Bacteria).
B.
OHPAObut
But
irato
Metano
-
- -Metano
I
B.Acetoclásticas
AAcet
at
o
T
-~
-
’ !
B.Hidrogenofilicas
HH i d
r6geno
Metano
4
-
B.Metanogénicas
T
Acetato
+.For-Metano
-
.
Totales
mato+
H z
+ COZ1
L-1
1
TABLA 2. PROCEDENCIAS DE LOS INOCULOS
TIPO DE LODO ~ PROCEDENCIA No.
-Lodo de un tanque de neutraliza- 1ng.Sta Clara,Los Reyes 1
ción de vinazas.. de Salgado Mich.
.
-Lodo de un tanque de separación de grasa.
-Lodo activado
de
planta de tra- tamAento deaguas
negras.-Lodo-activado adaptado.
-Lodo granular, -digestor UACH de 6 meses de operación.
-Liquido de fermentación de desechos de pulpa de café.
Ing.Sta Clara,Los Reyes 2
de Caigado Nich.
UNAN (México D,F) 3
UNAN (México D,F) 4
UAM
-
Iztapalapa 5Ing.Café, Orizaba
Ver.
6
-Sedimento de un rio,recibiendo Kimberly Clarck, Ori zaba 7
desechos líquidos. Ver.
.
-Estiércol fresco de vaca.
-Lodo de Fosa séptica
Iztapalapa, México. 8
Ingenio, Alianza Popular 9
e
."i
F
Y
c TARLA No.3 RELACION DE PROPORCIONES DE CAD6 GRUPO TROFICO DENTRO
1
DE
CADA GRUPO METABOLIC0 POR MUESTRA.i P L
-
Y Bacterias MetanogénicasBac ter1 as Hidrogenof
i
l i c a sOHPPi
..
OHPA Y 3 H+A c_ Ha
T-
No. MUESTRA
Ob
OP
-
H-Ob
+
Qpc:
1
d cL
r
irr
L " F I r. & _ 3 4 3x10 1 i . 6 ~ 1 01 1.8
-
1 1.2x10 1 2.0x100 . 5
16
1 . 6
1 . 4
7 . 4
0. 4
0. 9
4
.. - ..
4 1.5
~
.
1 . 7 17.3
0. 2
-~
-
3
0 . 0 5
~
1
1
1 2 . 8 ~ 1 0
-
1 . 8
1 . 1
1 . 2
7 . 1
6
9.6
,
RESULTADOS
Se analizaron los diferentes grupos microbianos representa- tivos de cada una de las etapas de
la
transformaci6n anaerobica de la materia orgánica, conel
propósito de establecer las poten-.~ cialidades de cada muestra.
En l a primera etapa se comentarán
los
datos obtenidos por~ ~ cada muestra con el fin de caracterizarlas, en una segunda etapa
se analizarán comparativamente cada uno de los grupos metabblicos entre cada una de las muestras, con el fin de mostrar los puntos similares, o las diferencias entre ellas.
.
1. CARACTERIZACION DE CAD& UNA DE LAS MUESTRAS.
-
Lodos de un tanque de neutralizaci6n de vinazas (muestra No. 1 )Se aprecia que las bacterias fermentativas representan el grupo dominante, despues vienen las bacterias metanoghnicas hidrogenofilicas ( H ) y las bacterias OHPA utilizadoras de butira- to (Ob), las bacterias aceto-clásticas ( A ) , estan casi
en
l a misma proporci6n que las anteriores, las bacterias OHPA utiliza- doras de propionato ( O p ) , representan a l grupo minoritario.1-
Lodos de un tanque de decantaci6n y separación de grasa yaceite (muestra NO.^), de los desechos liquidos de un ingenio.
i
En esta muestra, proveniente del ingenio anterior, se nota que l a poblaci6n microbiana dominante esta representada por e l srupo de las bacterias metanogénicas hidrogenofílicas, y después las
Las OHPA se encuentran en una proporci6n más baja, pero ambos grupos (Op y Ob) presentan un número similar de bacterias.
La poblaci6n minoritaria esta constituida de las bacterias metanoghicas -acetoclAsticas, que se encuentran a un nivel muy bajo (3.3 x
lü"3
bacterias/g S S V ) .. bacterias fermentativas.
-
Lodos activados procedentes de l a planta de tratamiento de aguas negras de l a UNAM (muestra N o . 3 ) .La poblaci6n dominante son las bacterias fermentativas,
E l conteo de las OHPA da un número inferior a los anteriores, siguiendole las bacterias hidrogenofilicas.
siendo las de mayor cantidad las utilizadoras de propionato.
De nuevo se encuentra que las bacterias acetoclasticas son e l grupo minoritario.
-
Lodos activados de l a misma procedencia que l a anterior, pero adaptados durante un mes con acetato (muestra N o . 4 ) .La particularidad con
lo
anterior; es-que tenemos una repar- tici6n equivalente de los siguientes grupos metab6licos:Bacterias fermentativas, hidrogenofílicas, acetoclákticas y utilizadoras de but.irato, y no se destaca de manera significativa un grupo dominante.En esta muestra el nivel mds bajo se encuentra con las bacte- ria's OHPA, utilizadoras de propionato.
'
-
Lodos de un UACB de 110 Ltinoculado
c o n - lodos activados y alimentado con aguas negras (muestra NO.^), durante 6 meses.Esta muestra se caracteriza, por provenir de un reactor anaerobio de tipo UASB en operac-i6n y puededervir de punto de referencia; las poblaciones dgminantes son la5 bacterias fermen- tativas, hidrogenofílicas y sorprendentemente
la5
bacterias OHPAuti,lizadoras del prop-ionato, se debe notar -que las bacterias acetoclásticas son numerosas, alcanzando c-asi las cifras obteni- das, con los grupos mencionados. El grupo de menos represen- tabilidad esta constitufdo por losutilizadores de butirato.
-
-
Jugo de fermentación expontánea de desechos de pulpa deI
café (muestra No.6).
~
3 Esta muestra se presenta como un liquido, por l o que no se analizaron los SST y los SCV. Tampoco se determinaron las bacte-
rias fermentativas. El principal intpres delanalisie de ~ esta
muestra'el determinar si habian potencialidades metanogénicas
y acetogénicas (OHPA). .Los datos estan expresados e m particular en este caso, en número de bac*rias p o r - m l de muestra. En esta muestra no se detectaron bacterias metanogénicas acetotlásticas, pero se encuentran bacterias hidrogenofilicas-a un nivel de 2.5 x
10*5 bacterias/ ml y bacterias OHPA a un nivel de 1.7 x 10*4
bacNterias/ ml por cada uno de
los
grupos (Op y Ob).i
-
Sedimentos de un rio recibiendo desechos de una planta de Kimberly-Clarck (muestra N o . 7 ) .Las bacterias fermentativas son las dominantes, después vie- nen' las bacterias metanogénicas hidrogenofilicas.
Se aprecia que las bacterias OHPA se encuentran a un nivel
sup'erior que las bacterias acetoclá<ticasr 6.3 X 10^3 bacterias/ g SSV para cada una de las OHPA y 3.1 x 10*3 bacterias/ 9 SSV
n
.",.
..""
.1.
d .
,?*
L..
-
-
Estiércol fresco de vaca (muestra NO.~).Cdlo'se pudo caracterizar 1.6 x 10".6 fermentativas/ g SCV '',.
y 4.3 x lO"4 acetoclásticasi 9 CSV. Las bacterias hidrogenofí- licas no crecieron y
n o
se detectaron bacterias DHPA.L I- ! L
r
ii r* u r( I , Lin
I-
Lodos de fosa séptica (muestra No.9).Este lodo se caracteriza por un alto nivel en bacterias I fermentativas e hidrogenofilicas.
Después los grupos más representativos son las bacterias acetoclásticas y las bacterias utilizadoras de butirato. Las bacterias utilizadoras de propionato son las menos numerosas.
S i .se analiza en cada muestra, las proporciones relativas para las bacterias metanogénicas entre las hidrogenofilicas y las acetoclásticas (Tabla No.3 y Fig.3) se muestra que en l a mayoría de los casos hay más bacterias hidrogenofílicas que acetoclásti- cas, exceptuando en el caso de los lodos activados adaptados con acetato (muestra No.4) en los cuales se encuentran valores equi- valentes entre ambos grupos. Se ve claramente en l a muestra no. 2
(Lodos de decantor de grasa), un gran desequilibrio entre los dos grupos a favor de las bacterias hidrogenofilicas y en las muis- tras n o . 3, 7 y 9 una relacidn de casi 100 bacterias hidrogeno- filicas por bacteria acetoclástica (Tabla
No.3
y Fig.3). En --la - -literatura se han reportado algunos dige,stores anaerobios una proporción más grande de bacterias metanogénicas hidrogenofilicas que de bacterias metanogénicas acetoclásticas (Guyot, Dolfing).
-
A l analizar l a relación (H
+
AI/T pobemos notar un rango-de valores entre 0 . 4 y 16 (Tabla N o . 3 ) . Las btacterias metanogénicastota'les son #representadas por aquellas que pueden utilizar hidrdgeno, acetato y for-to, dado los sustratos utilizados en
este trabajo. S i estos tres grupos de bacterias estuvieran prese- ntes en l a muestra deberíamos tener una relaci6n del orden de 1,
dado que
los
utilizadores de formato tambi,én consumen hidr6geho; pero se puede notar, por ejemplo en e l caso de Methanococcusthermolithotrophicus (Belay et a l 1986) que el uso del hidr6geno y del formato depende del pH del medio del cultivo, además se sabe que el formato puede inhibir algunas ,bacterias metanoghnicas acetoclásticas, (Guyot 1986) consecuentemente si no hay i o pocas)
bacterias que utilizan el formato en l a muestra, se puede encon- trar este tipo de inhibici6n cuando se requiere cuantificar las
bacterias totales. ñdemás el hidr6geno influye tambien sobre el uso del acetato por las metanogénicas acetoclásticas (Baresi et a l 1978). Por tantas interferencia5 posibles entre el uso de estos sustratos metanogenicos, parece que ía cuantificación d e
la5 metanogénicas totales tal como l o han hecho varios autores (Weimin Wu, 1987) no es confiable y no se puede recomendar excep- to si se requiere conocer un orden muy aproximado en bacterias metanogénicas totales.
A 1 analizar las relaciones entre bacterias OHPA utilizado-
r
u
ra5 de propionato y bubirato se nota que para l a mitad de las muestras reportadas (Tabla No. 2) es decir, cuatro muestras
(No.
1 , 2, 4, 9 ) se encuentra un número mayor de bacte'rias OHPA utili- zadoras de butirato que de propionato, que en dos muestras
(No.6
y
7)
e l número es equivalente yen
las dos restantes(No.3
y 5)hay mbs utilizadoras de propionato que de butirato. Es decir que l a mayoría de las muestras se encuentra un número más grande,
o
igual de bacterias OHPA utilizadoras de butirato.
Dada la relación estrecha sintrófica que ligan las bacte- rias hidrogenofil.icas metanogénicas con las bacterias OHFA (McI- nernery % Bryant 1980), es interesante analizar l a relacidn entre
el número de bacterias metanogénicas hidrogenofilicas y el número de bacterias OHPA (Op
+
Ob). Se aprecia en l a Table No. 3 que en l a mayoria delas
muestras hay un número mayor de bacterias hidrogenofilicas y : las muestras donde se encuentra un nrímero equivalente entre los dos grupos son las que corresponden a los lodos de l a fosa de-neutralización, lodos activados adaptados y10s lodos granulares del reactor UASB.
- ~~
-
' 2 . COWARACION DE LOS DATOS ENTRE CADA UNO DE LOS GRUPOS
METAReLICOS.
~
-
Contenidoen
SSU. .A pesar de un valor indicativo, este dato permite tener una
idea
de l a concentración en biomasa en los lodos. Se supone que :*y. más alto en este valor es el que tiene mayor contenido en biomasa - y - que se agregaran menores cantidades de minerales ymateria inerte en el reactor. A l ver l a gráfica no. 1 los lodos del 'tanque de neutralización tienen
el
porcentaje mák grande en1 SCV (71.5%), siguiendole 10%~ sedimentos
(No.
7 ) . pero en ente caso dado e l número bajo de bacterias que se cuantificd podemos pensar q k gran parte de los CSV es inactivo y podria ser biomasa muerta y materia orgánica no bacteriana.Los
lodos del reactor UACB íNo.5) y de l a fosa séptica-
Bacterias Fermentativas.
Exceptuando para las muestras 7
y 8,se puede apreciar q u e
las bacterias fermentativas s e encuentran distribuidas a niveles
entre
10 * 8bacterias
/ gSSV para la muestra
No. 3 y 9 , y t O " 7bacterias
/ g SSVpara las demás.
La incidencia de la cantidad en las bacterias fermentativas
es de menor importancia, sabiendo que en general no es la etapa
fermentativa que es limitante, sólo en casos de sustratos
.~particulares como telulosa o productos arom8ticos.
-
Bacterias Metanogénicas Hidrogenofilicas.
La gráfica
No.3nos muestra que las muestr-as que contienen
los ntlmeros más ,.grandes
de estas bacterias son los lodos del
tanque de separac,ión
de grasa
yaceite
( N o . 2 ) ylos lodos de:
la
fosa séptica
( l x l O " 8 y4 . 2 ~ 1 0 ~ 8
respectivamente),
después s e
encuentra un nivel similar de hidrogenofilicas en
los lodos
activados adaptados
yno adaptados y
en los lodos
del reactor
UñSB(del orden de
10"7bacterias/
gd e
SSV).El
nivel encontrado
en los lodos del tanque de neutralización y
el l~iquido
de--fer;men-
taci6n d e la
pulpa d e café no es despreciable?
-
Bacterias Metanogénicas acetoclásticas
íFig.3,
Las muestras que contienen la~-mayor cantidad de estas
bacterias de suma importancia para un
inóculo de digestor-anaero-
bio,
son
los lodos activados adaptados,
los lodos de lafosa
séptica
ylos lod,os del digestor
UASB,
en estas muestras estas
"bacterias s e encuentran en el orden de:10^7 bacterias
/ 8 SSV.Se
puede notar que"1os lodos activados
60
adaptados tienen ya
ni-
veles no despreciables.de bacterias metanogOnic.as~
de ambos grupos
yque al adaptar estos lodos con acetato, s e puede incrementar d e
mane,ra sensible el nlimero de -bacterias acetoclásticas, hasta
alcanzar un ntlmero parécido a l o s , l o d o s
del digestor
UASB.Parece
que en este digestor el nbmero de bacterias acetoclásticas perma-
nece constante ya que no es diferente al del i M c u l o después de
seis meses d e operación,
lo que verifica otras observaciones
hechas por Guyot et al
1,988.
Loslodos del tanque d e neutra-liza-
ci6n de vinazas tienen
un buen nhmero de acetoclásticas.
En
el esti&rcol fresco de vaca, en los lodos del tanque de
decantación
de grasa del mismo ingenio que del tanque de neutra-
lizaci6n,
yen los sedimentos del río recibiendo efluentes de
Kimberly-Clarck,
el
nQmer.0
de bacterias acetoclásticas es m u y
bajo (inferior a
1 W 4bacterias
/ gSSV).
En
el
liquido de fermentaci6n de la pulpa de café no se
detectaron bacterias acetoclásticas.
i)
-
Aac%.erias ClHFA u t i 1 i z a d o r a - de p r i k i c ~ n a t o ( F i g . 4 jLas rnuet,t.ra% 3 y 5 present.at-8 10% n i v e l e - 8 rnds srarider,
(0.7i:iCt^7 y 1 . 1:.:10^7 tm=t.erias / g SSV) r e s p ~ c t . i v a m e n t e , l o que
corresponde a los l o d o s a c t i v a d o s
no
adaptados y. alos
l o d n s de1d i g e s t o r LIASB. Despu4s l a s muestras N o . 2 , 4 y
9
tietiers n i v e l e s del orden de 1O””E. b a c t e r i a s / 9 d e SSV. Podernos riotar que eri e lcasci de 1 tarique d e decaritac i ter, í
N o .
2 ) se encuent.ra iur~ n i v e l masgrande 4c44 en e 1 casa
del
t.ansue
de rieut.ralizacibn.
Los corsteos mds b a j o sse
encuent.ranen
los sedimentas ( N o . 7 ) y e l l i q u i d ode
fet-ment.aciht-1 de p u l p a .de cafC NO.^),
en
e l e s t i & r c o l (No. 8 )no
se
detect.aronestas
b a c t e r i a r .--
B a c t e r i a s OHPA u t i l i z a d o r a s d e b u t i r a t o ( F i g . 4 )-
Erieste
casalos
- l o d o %de
l a f o s a s&pt.ica ( N o . ? ) ylos
I o d o s a c t i v a d o s adaptados (No. 4 ) t.ierieri l a rnds a l t a coricent.racibn en
este
grupo h a c t e r i a n o , 4.2:~<10”’7 y 0.9:~10”7 respect.ivamente,Se
puede o h s e r v a r que enl a s
muestras No.6 y 7 t a l como eri41 caso d e l propionat.o
se
tiene
un n i v e l h a j o d e u t i l i z a d o r a s deb u t i r a t o Y que tampoco
se
d e t e c t a r o n Q s t a s eri e l e s t i Q r c o 1 .DISCUSION
-
En t o d a s l a s muestras que
se
c u a n t . i f i c a r o r i pcdemos riotar quesiempre encontramos b a c t e r i a s fermerit.at.ivas, bact.er i a s hidrogeno- f i l i c a s Y bact.er i a s OHPF, exceptuarido p a r a
estos
dos i(4lt.imosgrupos an
el
caso del e s t i h r c o l , aquise
debe i n s i s t . i r que riose
a g r e g o a p r o p t ~ s i t . c ~ l i q u i d a ruminal a los medios de c u l t . i v o para
el
e s t . i & r c o l ;se
sabeq u e
para- l a s tnacteria% h i d r u g e n o f i l i c a sse
r e q u i e r e n unos f a c t o r e s n e c e s a r i o s para s u c r e c i m i e n t o , t a l como
e1 metil but.irat.o e n t r e o t r o s ( B a l c h
et.
a1 1979) y queystos
factm-es
se
encuent.rari.enel
l i q u i d o ruminal. Por l o m i s m o si nopodemos c r e c e r l a s b a c t e r i a s h i d r a g e n o f 1 1 i c a s tampoco l a s bact.e-
- r i a í OHPCI e n
e l
caso que e x i s t i e r a n en e lrumen,
por f a l t a de l arelacitan s i r i t r b f i c a
con
l a s h i d r o g e n o f i l i c a s . En e l s e n t i d o deest&
e s t u d i o ,que se
e n f o c a a d e t e r m i n a r huenos i n h c u l o s parareactores a r ~ a e r o b i o s , e1 e s % . i & r c o l de vaca no puede ser uri huen
i n h c u l o dadas l a s e x i g e n c i a s n u t . r i c i o r i a l e s de
las
b a c t . e r i a s d e l rumen, s o b r e todo e l problema s e r i a a l n i v e l d e l arrarique d e lr e a c t o r :
se
necesitaria
demasiado tiempo p a r a quese
e s t a h l e z c ae n
un mediototalmente
d i f e r e n t e d e l rumen utna p a b l a c i t m e s t a b l ocompuesta de microf l o r a que p u d i e r a i n t e r c a m b i a r f a c t o r e s de
c r e c i m i e n t o .
Hemos . t e n i d o l a oportunidad de checar este punto a n i v e l d e
r e a c t o r e s LIASE de l a b o r a t o r i o i n o c u l a d o s con est.iCrcu1 fresco en
P
L
c
La presencia de hidtmgenofilicas en casi todas las muestras parece ser constante. Se pudo ver que en general las bacterias .
hidrogenofilicas son más numerosas que las bacterias acetoclás- ticas y las iiHPFI.
E l hecho que haya una gran concentracibn de hidrogenofilicas es importante cuando se conoce su papel fisiológico de estas bacterias. Se puede decir que estas bacterias permiten l a aceto- génesis y protegen l a acetoclastia CMacI'nerney y Bryant, 1980;
Hemos podido notar que las con-centraciones en hidrogenofi- licas y OHPFI varian de un inóculo a otro, pero exceptuando en e l caso de las muestras 6, 7 y 8 ( ca.fej sedimentos y estiércol) podemos considerar que las concentraciones son a niveles adecua- dos, si se comparan con los datos del digestor UASB o con los datos de Dolfing (1985) obtenidos igualmente en reactor UASB.
Debemos hacer notar que en e l caso del tanque de separación
, de grasa se~observa un incremento en bacterias hidrogenofilicas y en utilizadoras de propionato, en comparación con el tanque de
neutralización; l o que se puede interpretar por un incremento en l a actividad de las bacterias implicadas en l a degradaci6n de
las
explicar el nivel inferior en bacterGs acetoclásticas a l tanque de neutralización, p o r 4 1 hecho de una inhibición de las bacte- rias por los compuestos que se acumulan en el decaneor: se ha
' reportado (Kostet-y Cramer1987) que-los ácidos grasos de larga
cadena inhiben !a metanogenesis a partir del acetato. FIsi,no se ' pueden recomendar
l o s
Lodos provenientes del decantor como inócu-l o por las bajas concentraci&es en bacteria acetoclásticas meta-
,
nogénicas, exceptuando si se requiere un inóculo adaptado para l a , degradación de las grasas, se necesitaria encontrar una manera de,
incrementar l a concentración en acetoclásticas.t Es interesantg reportar que a l nivel del terreno, en ambos
tanques se pudo apreciar una buena producción de grandes burbujas
' de gas (sin olor de Hk S), pero el análisis de los datos micro-
biológicos (repetido dos veces en este caso), nos ensena las djferencias fundamentales entre-estas dos posibles f.uentes de
i nócul os.
E l punto más relevante es l a gran variación en bacterias
' metanagénicas acetoclásticas. Este grupo es de suma importancia para la metanogénesis dado que 70% de metano de un digestor proviene del acetato y
se
considera q u e - e n general l a degradación del acetato es l a etapa limitante de l a transformación de l a materia orgánica soluble en metano (Kaspar y Wuhrmann, 1978).además este grupo de bacterias tiene tiempo de desdoblamientos muy grandes, entonces el.nive1 inicial de estas bacterias en los
inbculos va a condicionar también e l tiempo de arranque de un reactor hasta un nivel de estabilización.
Se puede observar que en los lodos activados hay una gran concentración de bacterias metanogénicas y que al adaptar estos lodos con acetato durante un mes, se logró montar l a concentración de bacterias ac5tqclásticas 100 veces. Estos lodos activados adaptados y los lodos de l a fosa séptica por sus niveles en bacterias acetoclásticas y en las demás bacterias,
et al, (1987) han utilizado
los
lodos activados con éxito paraGuyot 1986). . .
I
i
i
grasas. &demás en e l tanque de decantación de grasas se puede I
' parecen ser los mejores inóculos para reactores anaerobios. W. W u
.
~ 14
Y -7
u
P
Y
1
Y
m
t l
ii
1
inocular reactores UASB, estos autores mostraron l a presencia de bacterias metanogénicas en este inóculo haciendo una cuantificación de las bacterias metanogénicas totales por NMF en tres tubos.' Nuestros datos confirman los de W. Wu et a l y además ensenan de manera detallada l a influencia de adaptación de los
lodos sobre su composición. microbiana.
Otro detalle interesante para los paises .tropicales productores de café: no se detectaron bacterias acetotlásticas en fosas donde se produce una fermentación expontánea de pulpa de
cafe utilizando este criterio e l liquido de fermentación no debe
ser un buen inóculo, pero se necesitariln más datos de varios ~ .
lugares antes de sacar una conclusión definitiva.
,
CONCLUSION
Como inóculo para reactores anaerobios podemos recomendar=el- uso de los lodos de l a fosa septica y los lodos activados proce-
en este caso se recomienda de adaptar los lodos activados dejan- dolos por l o menos un mes con una alimentación semanal cok aceta-
to en orden de 5
gr/l,
l o que no afectará por otra parte e l nivel de las otras bacterias. además podernos, decir que al final de esta adaptación se obtuvieron lodos granulares con buena capacidad deComo otra fuente de inóculo apare;cen los lodos de un tanque podría ser un; buena dentes de plantas de tratamiento aeróbicas de aguas resi&g.aies, -
-
decantacibn. I
de neutralización de vinazas de un ingenio,
alternativa en el' caso de que 'los .otros no estuvieran
-~
disponibles.
inoculación de reactores anaerobios.
El aso de sedimentos o de estiércol no se recomienda para l a - ~
i
r-
I
**
4 . e.-
...
CI
u
.-
u
CUANTIFICACION DE BACTERIAS ANAEROBIAS ESTRICTAS
Microorganismos/mg d e
SSV
3 w
.~
I
Muestras
%CSV
F
H
A
T
OP
Ob
1
2
3
4
56
7
8
9
I .. -71.54
5.1"7
-4.-1"6
19.2
3.1*7
1 . 1 " 81.1AP -
1.1*7
26.43
25.74
3.1"7
1.1"7
37.81
-1.1"7
--2.1^7
-~
- _ P
3.1"5
64.06
6.1"s
4 . 1 ^ 4
20.49
2.1"6
41.09
4 . 1 A 8
4 .
1 * 8_ -
9 . 1 A 5
3.1"3
4 .
l A 52.1"7
8 . l A 6
3 . 1 A 3
4.1"4
2.1"7
9 . P 6
7.1A6
10.
l"6
2 .
l A 7
3.1^6
6.1*5
4 . 1 " 4
1.1AP
5 . 1 A 5
2.1^6
7.1"6
3.1"6
1.1"7
2.1"4
6.1A3
2.1"6
2.1"6
4. l A 6
1.1"6
9.1"6
€ . l A 5
2 .
l"4
€.1"3
4.
lA7
Las muestras corresponden
-a
l o s
inoculos encontrados en
los
lugares
de muectreo.
7SSV.
Porcentaje d e solidos suspendidos volatiles
F. Bacterias Fermentativas
~
Bacterias Metanogenicas:
A.
Bacterias Acetoclasticas
T.
Bacterias Totales
ANEXOS
MEDIO BASE ( 1 L t )
-Solución 'Mineral 1
(Ralch
et
a l 1975').a -Solución Mineral 2
Balch e t ' a l 1979).
i s i n s u l f a t o s para l a s OHFA
-So
1 LIC i ó n , O 1 i goe lemen tos(Balch e t a l 1979). -Solución Vitaminas
iBalch et a l 1979). -HezarsurPna
- E x t r a c t o , d e levadura
__
-Feptona
qe
c a s e i n a -Bicarbonato d e s o d i o50 m i
50 m l
..
10 m l
-Solución d e N i C l 10 m l (10 mg/lOO m l )
-Solución '
FeSO
( 0 . 2 % ) 1 m l ( N o para l a s- C i s t e i n a 0.5 m l
I
-
OHPfi)
_ -
NOTG: - .
- B a c t e r i a s F e r m e n t a t i v a s se pt-epat-6 una s o l u c i 6 n .concentrada
d e l 25% y
se
a g r e g o 0.1 m l d e e s t a s o l u c i ó n e n cada 5 m i d emedio, se alimento atm normal d e N7.
-&act e r i a.5- OHFG
- U t i l i z a d o r a s d e P r o p i o n a t o : s o l u c i ó n concentrada d e p r o p i o n a t d ( 1 m l d e
ac.
pt-opionico + 0 . 4 g NaOH e n 9 m l d ea g u a ) , se a g r e g 6 0.1 m l e n 5 m l d e medio.
- U t i l i z a d o r a s d e B u t i r a t o : misma solución concentrada, p e r o con ac. b u t i r i c o ,
se
a g r e g a l a misma cantifiad.Se alimentan con atmosfera normal d e N 2 / COZ
.
Y
R
Y
R
u
1
L.
J
6
c
1
2
3
4
J7
3
9
,
F I G .
1
.-
Porcentaje de SEW por muestra.so?idos s cspendidos vo i d t i
ies)
i f
,-.
.,
_II
3
I:
1
i<I
4
5
6
i
0i
MUESTRAS
u
R
r
L
R
L
L
5
v1
F
F-
k
1
i9
J4
5
6
7
8
3
7
MUESTRAS
,
I"
u
r
BIBLIOGHAFIA =
-
Arias Osorio A. y Noyola Robles A.(1987)
"Tratamiento de un agua residual urbana mediante e l reactor anaerobio d e lecho de lodos (UACB)" en Avances de Investigaci6n en Ingeniería Química1987,
en prensa.. . .-
Balch, W.E., &nd R.S. Wolfe.1976.
New approach to the cultiva- tion of methanogenic bacteria: 2-mercaptoethanosulfonic acid iH8-Coil)-dependent growth of Methanobacterium ruminantium in a pres-
surized atmosphere. Appl. Environ. Microbiol.
32: 781-791.
L*
-
Balch, W.E., G.E. Fox, - L.J. Magrum,C.H.
Woese, and R.S. Wolfe. Im
1979.
-Hethanogen.s: reevaluation of a unique biological group.,
I :
Microbiol. Rev.43: 260-296.
Iiii
-
Barresi L., R.A. Mah, D.M. Ward and 1. Kaplan(1978)
Methanoge- nesis from acetate: enrichment studies. Appl. Environ. Microbiol.36: 186--197.
-
q
-
Beiay N., R. Sparling and L. Daniels(1986).
Relationship of formate to growth and methanogenesis by Methanococcus therholi- tho t rob% i cus.
-
Dolfimg, J.1985.
Kinetics of methane formation b y granular sludge-at low substrate concentrations. Appl. Microbíol. Biotec-hnol.
22: 77-81.
-
- .
!A
__
-~-
3
.
.
-
Dolf ing,J.,
A. Griffioen, ñ.H.W. van Neerven, and L.P.T.M. Zevenhuizen.1985.
Chemical and bacteriological composition of granular - methanogenic sludge.31: 744-750.
-
Garcia,J.L.,
J. F.^ Guyot, B.~~Ollivier, M. Trad, and C. Pay- cheng.1982.
Ecologie de l a digestion anaerobie. Cah. ORSTOM,ser. Biol.
45: 3-15.
-
Guyot, J.P., and A. Brauman.1986.
Methane production fromformate by syntrophic association of Methanobacterium brvantii and Desulfovibrio vulcraris
JJ.
Apl. Environ. MicrobioB. 52:1436-
1437.
8 '
rl
. .
L
C~
r
.~ .P
i
c
-
Guyot J.F.; Noyola A., Ramírez F. y Monroy O,(1988)
"Activi- dades metanogénicas de lodos granulares de un digestor de lecho de lodos" en Memorias del Frimer'Simposio Nacional sobre Ingenie- ría Ambiental, Instituto de Ingenieria UNAM.-
Hungate, R.E.1969.
A roll-tube method for the cultivation of strict anaerobes. p.117-132.
In J.R. Norris and D.W. Ribbons(ed.) MetHods in microbiology, vol.
3B.
Academic Press. Inc. New-York.
-
Kaspar, H.F., and K. Wuhrmann. 1978. Kinetics parameters an@ relative turnovers of some important catabolic reactions in d-,9.isting sludge. Appl. Environ. Microbiol. 36: 1-7.
-
Koster, I.W., Cramer A. 1987. "Inhibition of Me.thanogenesis from Acetate in Granular Sludge by Long-chain Fatty Acids. Appl. Environ. Microbiol. p. 403-409-
Lettinga G., Van Velsen CI.F.M., Hobman S.W., de Zeeuw W.y r
~Klapwijk A (1980) "Use of the upflow sludge- blanket
(UASB)
reac- tor concept for biological wastewater treatment, especially foe=
anaerobic treatment" Bioyechnol. Bioeng., Vol. 22, 699-734. .
--
Lettinga G., de Zeeuw W.J., Hulshoff Pol L.A., Hobma S.W., Grin P.C. Wiegant W.N., van Velsen A.F.M. y Koster I.W. (1982,). "Anae- .robic' wastewater treatment using the UASB treatment process". Memorias del Simposio Avances en Digesti.on Anaerobia:
comb us ti-.
bles por Fermentación., UAM-I/ICAITIC, Mexico.-
McCarty P.L. (1964) "Anaerobic waste treatment fundamentals" Pub. Works, Vol. 95, 9, 107-112; 10, 123-126; 11, 91-94; 12, 95-99.
-
-
Mc Inerney, M.J., and M.P. Bryant. 1981. Basic-principles of296. I n S.S. Cofer and O.R. Zaborsky (ed. )-Biomass conversion process for energy and fue.1~. Plenum publishing corporation.
-
Noyola A., CapdevilleE,.
y Roques H. (1988) "Anaerobic treat-- ment of:. domestic sewage with a rotating stationary fixed film reactor". Water Res., en prensa.-
Smith, P.H., and MahR.h.
1966. Kinetics of-acetate metabolism during sludge digestion. Appl..Microbiol. 14: 368-371._~~ -
I
bioconversions in anaerobic digestion and methanogenesis. p. 277- - ~,
~
~-
- _. .
-
-
Standard. methods for the examination-of water and -wastewater.1976. 14 th Edition, American'PPublic Health Association. Washin-
g ton, D. C.
-
Van den Berg L., Lentz C.P. y Armstrong D.W. (1980)~"Anaerobic waste treatment efficiency comparisions between fixed film reac- tors, contac digesters and fully mixed, continuosly fed diges- ters" en Proc 35 th Purdue, Ind. Waste Conf., 788-793.-
Wu, W., 'J.
Hu, X. Gu, Y . Zhao, H. Zang, and G. Gu. 1907.Cultivation of anaerobic granular sludge in UASB reactors with aerobic activated sludge
as
seed. Wat. Res. 21: 789-799.-