CARACTERES ANATOMICOS DEL SEGMENTO CAULINAR DE 3 ESPECIES DEL GENERO Opuntia EN COLOMBIA (MONDOÑEDO, CUNDINAMARCA Y
CAÑON DE CHICAMOCHA SANTANDER)
Lina Rocío Sánchez Roncancio Sebastián González Cadena
UNIVERSIDAD DISTRITAL FRANCISCO JOSÉ DE CALDAS PROYECTO CURRICULAR LICENCIATURA EN BIOLOGÍA
CARACTERES MORFOANATOMICOS EN EL SEGMENTO CAULINAR DE 3 ESPECIES DEL GÉNERO Opuntia EN EL CAÑÓN DE CHICAMOCHA,
SANTANDER Y MONDOÑEDO, CUNDINAMARCA COLOMBIA.
Autor:
Lina Rocio Sánchez Roncancio
Sebastián González Cadena
Director:
Germán Antonio Niño
Trabajo de grado para optar por el título de:
Licenciados en Biología
Universidad Distrital Francisco José De Caldas
Facultad De Ciencias y Educación
Proyecto de Licenciatura en Biología
Bogotá, Colombia. 2019
AGRADECIMIENTOS:
A mis padres cuyo apoyo es incondicional, gracias por enseñarme a perseguir mis sueños e ir conmigo a la montaña a colectar cactus, a la Universidad Distrital, en sus aulas encontré
inspiración en muchos docentes, amistades que hacen parte de mí, pero sobretodo la pasión por la educación y la ciencia que es lo que me hace creer que es posible cambiar el
mundo con pequeñas revoluciones y que vale la pena intentarlo.
Gracias a Sebastián, mi colega, compañero y amor, por la infinita paciencia y por todo lo que aprendimos en el camino.
Y gracias a todos los que le apuestan a la educación y la construcción social en este país.
Lina
TABLA DE CONTENIDO
1. INTRODUCCIÓN……….…6
2. Planteamiento del problema 2.1.Descripción………...7
2.2 Justificación………...7
2.3 Pregunta problema………...7
3. Objetivos 3.1 Objetivo General………...8
3.2 Objetivos específicos……….….8
4. Marco de referencia 4.1 Marco Teórico……….. 9
4.1.1 Tejidos vegetales ……….... 9
4.1.2 Familia Cactácea………... 11
4.1.3 Metabolismo CAM ………... 12
4.1.4 Clasificación ……….... 15
4.1.5 Subfamilia Opuntioideae ……….… 15
4.2 Antecedentes………..… 17
5. Metodología………... 20
5.1 Fase de campo………. 20
5.2 Fase de laboratorio ………..….. 23
5.3 Resultados esperados ... ………... 23
6. Resultados……….…. 24
6.1Tejidos de protección………... 28
6.2 Parénquima……….... 30
6.3 Canales de mucílago………... 32
6.4 Tejidos vasculares……….. 34
8. Conclusiones ………..….. 51
9. Bibliografía ……….. 52
Tabla de figuras Figura 1. Clasificación de la familia Cactaceae………..…..15
Figura 2. Sector 1 de muestreo, desierto de Sabrinsky o alto Mondoñedo, Cundinamarca..21
Figura 3. Sector 1 de muestreo, Cuenca media del río Chicamocha , Santander ……...….22
Figura 4. Ficha técnica O.pennelii ……….…..25
Figura 5. Ficha técnica O.quitensis ………...26
Figura 6. Ficha técnica O.dillenii ……….……...27
Figura 7. Estructura peridermis ………...28
Figura 8. Tejidos de protección. Peridermis y epidermis ………..….29
Figura 9. Hipodermis ……….….29
Figura 10. Parénquima clorofílico de empalizada ……….…….30
Figura 11. Parénquima acuífero ………..31
Figura 12. Células de mucilago ………..31
Figura 13. Canales de mucilago (Especies del sector 1) ………....33
Figura 14. Canales de mucilago ..(Especies del sector 2) ………..33
Figura 15. Haces vasculares en la zona apical del cladodio………....35
Figura 16. Haces vasculares en la zona media del cladodio………...36
Figura 17. Haces vasculares en la basal del cladodio……….37
1. INTRODUCCIÓN
La distribución del género Opuntia en Colombia se vincula principalmente a las formaciones secas del Caribe y valles interandinos, suelen ser bosques secos tropicales
cuya flora abarca cactáceas y otras plantas propias de los bosques deciduos, estas
formaciones secas de tierras bajas están distribuidas en parches aislados en la Costa Caribe
(Ruiz et al; 2002). Se encuentran además en el centro de Colombia, en los valles interandinos del río Chicamocha (Santander); en el nororiente de Colombia, en Boyacá y
Norte de Santander; en el suroccidente de Colombia, en la Cordillera Occidental, en
enclaves de Dagua, Valle del Cauca, Patía, entre Popayán y Pasto, y en La Cordillera
Central, en La Tatacoa en el Huila. En los enclaves del río Chicamocha y La Tatacoa, se
destacan gradientes que alcanzan los 2000 m (Ruiz et al. 2002)
El género Opuntia se caracteriza por la ausencia de hojas verdaderas y espinas en su lugar,
agrupadas en estructuras llamadas areolas, poseen como autapomorfía los gloquidios,
espinas urticantes deciduas de muy corta longitud ubicadas en la base de la areola y un
ovario campilótropo rodeado por un arilo, un tallo fotosintético aplanado que es tal vez una
de las mayores ventajas adaptativas pues modifica la relación área / volumen del cladodio
obteniendo una mayor superficie fotosintética. En relación a los miembros de la subfamilia
Opuntioideae, este grupo es el que posee una mayor diversidad. (Rebman 1995, Rebman &
Pinkava 2001 a, b; Griffith 2004, Griffith & Porter 2009), al género se atribuyen
características particulares que impiden que su clasificación y su delimitación filogenética y
taxonómica esté completa, son principalmente los fenómenos de hibridación asociado a un
incremento de la ploidía (especiación por poliploidía), la clonación vía propágalos,
hibridación interespecífica permite el intercambio de genes entre poblaciones separadas o
parcialmente separadas vía fertilidad del híbrido (Rebman & Pinkava 2001a), y plasticidad
fenotípica frecuente entre linajes que trata de una variación de las estructuras vegetativas
afectadas por el ambiente haciendo que no corresponda totalmente la descripción de las
especies y complicando su determinación, estos mecanismos corresponden a estrategias de
adaptación, no solo dificultan la delimitación del grupo sino que algunas favorecen
también a una distribución más amplia incluyendo lugares que no cumplan con
caracteres vegetativos, sino que involucra sus sistemas y estructuras especialmente aquellas
encargadas del aprovechamiento del recurso hídrico, lo que indica que lo que hace especial
su metabolismo y anatomía no es la capacidad de resistencia a ambientes extremos si no la
capacidad de adaptación para colonizar nuevos hábitats.
Esta investigación aporta una descripción anatómica de las estructuras y tejidos que
conforman el segmento caulinar de O. quitensis, O. dillenii y O. pennellii en dos ecosistemas del territorio colombiano, se evalúa la organización interna de tejidos de
protección, vasculares, fundamentales y estructuras anexas, mediante la comparación de
los tejidos en una especie, examinando cómo responde a presiones ambientales distintas, si
se presentan variaciones estructurales significativas de una especie a otra. Todos estos
caracteres de la anatomía serán considerados en función de su ecosistema, de los
mecanismos de cambio y adaptación para lograr una comprensión más global de su
ecología.
2. PLANTEAMIENTO DEL PROBLEMA
2.1 Descripción:
Muchas características morfológicas de las Cactáceas son respuestas a presiones
ambientales xerofíticas, modificaciones como la pérdida de hojas, tallos fotosintéticos y
metabolismo CAM está enfocado en soportar sequías con un sistema más eficiente de
almacenamiento de agua y regulación de la transpiración. Empero, en el paisaje colombiano
no son exclusivas de ambientes secos, su plasticidad fenotípica le ha permitido colonizar
inclusive ambientes en los que no hay escasez de agua e inclusive ambientes húmedos.
La organización interna responde también a las condiciones ambientales ,estas estructuras
pueden otorgarle una adaptación eficiente que merece ser evaluada para en género Opuntia
2.2 Justificación
El género opuntia, es comúnmente empleado como cerca viva o planta ornamental a lo
siendo sembrada incluso en ambientes fríos o húmedos, este servicio ha traído como
consecuencia una distribución muy amplia del género puesto que en las zonas intervenidas
existe poca competencia. Dicha expansión ha causado que las plantas se vean obligadas a
adaptarse a un espectro de condiciones ambientales más amplio.
El estudio de los tejidos de una planta introducida comparado con el análisis tisular de una
planta nativa puede suscitar las condiciones en las que se encuentra y las necesidades a las
que se enfrenta, destacar las estructuras internas más propensas al cambio, aportar a la
comprensión del sistema fisiológico de las cactáceas y su plasticidad fenotípica.
Así mismo este trabajo pretende aportar a la conservación y manejo adecuado de las
cactáceas del género Opuntia en Colombia.
2.3 PREGUNTA PROBLEMA
En relación a lo anterior, la pregunta a resolver por esta investigación es
¿Existen variaciones en caracteres anatómicos y su organización en el segmento caulinar
entre las especies estudiadas del género Opuntia o en una especie distribuida en dos hábitats como presiones ambientales diferentes
3. OBJETIVOS 3.1 General:
● Identificar si existen variaciones en los tejidos del segmento caulinar de los cactus
del género Opuntia en O. Dillenii, O. Quitensis y O. pennelli a consecuencia de sus condiciones ambientales.
3.2 Específicos:
● Describir la anatomía del segmento caulinar de O. dillenii, O. quitensis y O. pennellii.
● Comparar histológicamente la composición del segmento caulinar de O. Dinelli
● Identificar si existen diferencias significativas en los tejidos del segmento caulinar
entre tres especies del género Opuntia. O. dillenii, O. quitensis y O. pennellii.
4.1 MARCO TEÓRICO
4.1.1 TEJIDOS VEGETALES
Las plantas superiores o cormofitas se caracterizan por presentar una diferenciación celular
verdadera que conforma tejidos. Paniagua Gómez- lvarez, 2 7)
Los tejidos son grupos de células de origen, estructura y funciones comunes () constituyen
sistemas especializados para cumplir funciones específicas, están clasificados de acuerdo a
su estructura, ontogenia y función.
La clasificación por estructura es la más simple tiene como criterio la homogeneidad o
heterogeneidad de los tejidos; encontramos los tejidos conformados por un solo tipo de
células los cuales son denominados como simples en los que se encuentran el parénquima,
colénquima , esclerénquima y los que se conforman por diferentes tipos celulares estos
conocidos como compuestos como el xilema , floema y epidermis.
Existe en las plantas un tejido encargado de la generación de nuevas células, estas nuevas
células son indiferenciadas inicialmente, al culminar su desarrollo se diferenciarán
haciendo parte de tejidos específicos, estos tejidos, llamados meristemáticos, se encargan
del crecimiento continuo de la planta.
Las células generadas a partir de estos tejidos meristemáticos, van a alcanzar su madurez y
su respectiva diferenciación formando parte de tejidos específicos en la planta, estos
conocidos como tejidos adultos, de esta manera presentamos la clasificación referente a la
ontogenia, (desarrollo de las células), entendiéndose a los que poseen células
indiferenciadas y generadoras como tejidos embrionarios, y a los conformados por células
maduras y diferenciadas como tejidos adultos. Paniagua Gómez- lvarez, 2 7)
1. Meristemos: son tejidos constituidos por células proliferantes, con una mayor
velocidad de división mediante la mitosis y se encuentran apicalmente en tallos y
hojas, radicalmente presentes en las raíces y por último corticalmente, estas dos
primeras zonas le permiten a la planta crecer longitudinalmente y la tercer zona es
encargada del ensanchamiento de la planta.
2. Parénquima: es el tejido más primitivo, está formado por células con mayor
diferenciación que pueden cumplir funciones de almacén de sustancias nutritivas
como el hidrenquima que almacena el agua o el parénquima amilífero que guarda
almidón y funciones fotosintéticas como es el caso del colénquima.
3. De sostén: son células que generalmente presentan engrosamientos en su pared
celular con el fin de fortalecer la estructura de la planta. Se trata de dos tejidos, el
colénquima y el esclerénquima este último más especializado. Los tejidos
vasculares también contribuyen al sostén desarrollo de la planta sobretodo el xilema
en las plantas leñosas.
4. Vasculares o conductores: constituyen un sistema especializado en la conducción de
agua sustancias inorgánicas y orgánicas. Representados principalmente por el
xilema que transporta agua y sales minerales provenientes de la raíz al resto de la
planta de manera ascendente y el floema que se compone de células vivas de
transporte de las sustancias carbonatadas producidas por la fotosíntesis, comunican
todos los órganos de la planta por lo que son vías por las que se distribuyen
hormonas además de que proporcionan sostén.
5. De protección o tegumentos: son los tejidos que recubren todo el vegetal, protegen
de la pérdida de agua y de la acción de agentes externos, el primero de estos es la
epidermis el cual recubre externamente la estructura primaria del cuerpo vegetal y
forma una barrera frente al medio externo, en algunos casos está sobre una
hipodermis, en el caso de las raíces bajo esta primera capa se ubica una segunda
llamada epidermis, referente a los tejidos vasculares los cuales se ubican en un
cilindro central en la mayoría de los casos, existe un tejido que los protege llamado
endodermis. Cuando la planta conforme a su desarrollo crece en longitud y grosor
tejido no se multiplican, y es reemplazado por un tejido protector secundario
llamado peridermis.
6. Secretores: Las glándulas o tejidos secretores aparecen en la planta con dos
finalidades particulares, la excreción en la que se liberan sustancias de desecho
metabólico y secreción en donde la glándula libera sustancias producidas por la
planta con el fin de facilitar su relación con otros individuos bien sea para atraerlos
o repelerlos. Algunos forman parte de la epidermis de la planta como los pelos y
glándulas, otros son internos y forman canales o conductos como el resinífero y
laticífero (producción y transporte de, resina y látex).
La disciplina que estudia la organización tisular de las plantas se denomina histología
vegetal. Describe las estructuras y su función.
4.1.2 FAMILIA CACTACEAE
La familia cactácea Juss., 1789 perteneciente al orden Caryophyllales es una familia de
plantas angiospermas dicotiledóneas originarias de América Font i Quer Sierra i R fols,
2001), con una amplia distribución desde Canadá hasta el sur de Latinoamérica en Chile y
Argentina y alcanzando hasta los 4000 msnm a excepción del género Riphsalis que puede
tener presencia en África y en varias islas del océano índico (Home, J. 2015) La zona
tropical seca de Sudamérica es considerada por los especialistas como el probable centro
de origen (Bravo 1978).
Comprenden de 120 a 130 géneros descritos y alrededor de 1900 especies en su mayoría
suculentas de tallos perennes (Loaiza S & Morrone, 2011). Sus flores suelen ser efímeras,
actinomorfas o zigomorfas, comúnmente perfectas, pueden presentar tonalidades amarillas,
rojas, naranjas, rosadas o púrpuras al igual que sus frutos. Estos últimos son redondos
carnosos en su mayoría o secos y huecos en algunos géneros con numerosas semillas, muy
pequeñas o alcanzando varios milímetros, a veces muy duras.
La ornitocoria a manera de diseminación es común en esta familia, por los jugos y frutos
dulces, hay mirmecocoria en algunas especies y otras tienen doble estrategia
espinas las pertenecientes al género Opuntia presentan epizoocoria (mamíferos). La anemócora ocurre ocasionalmente en algunos taxas (Barthlott y Hunt, en Kubitzki, 1993)
Las plantas de ésta familia suelen reconocerse fácilmente por un conjunto de características
morfoanatómicas adquiridas principalmente por procesos de adaptación a ambientes
desérticos o semidesérticos tales como: elevada frecuencia estomática, presencia de córtex
de empalizada, gran cantidad de espacios intercelulares, haces corticales y medulares,
modificaciones en el leño. Sin embargo, una de las más importantes características desde
punto de vista adaptativo y taxonómico se trata del “skin” o piel, que consiste de la
epidermis junto con la hipodermis (Bailey 1961, Gibson y Nobel 1986, Darling 1989), ya
que es la capa más externa representando el límite con el ambiente externo
Las espinas a su vez resultan de la reducción en las hojas típicas con el fin de disminuir o
aminorar la pérdida de agua en la transpiración, también protegen a la planta contra
depredadores, condensan el agua de aire , forman una barrera contra la luz y radiación
directa actuando como “sombrilla” además de contribuir en la dispersión y propagación
vegetativa (Hoffmann, 1989).La homología entre las hojas y las espinas se basa en el
crecimiento de ambas en los puntos vegetativos de la planta y en su desarrollo filogenético,
como consecuencia es en los tallos donde ocurre la fotosíntesis, estos son generalmente
verdes, con o sin espinas, continuos o articulados, globosos, ovoides, planos, cilíndricos,
angulosos, con costillas y mamelones, simples o ramificados, solitarios o cespitosos,
erguidos o decumbentes.( Ceroni & Castro,2013) Se caracteriza por grandes reservas de
agua además del aumento de cera en la cutícula que contribuye al aumento de la resistencia
estomática y cuticular a la pérdida de agua (Herman ,Acevedo & Silva, 2001)
Las espinas nacen en el tallo en grupos de brotes cortos que aparecen en la etapa de
primordios llamadas areolas, tejido meristemáticos homólogo a las yemas, dan origen flores
y nuevos brotes (APG III", 2009). Estas areolas se distribuyen en patrones simétricos en los
cladodios y junto con la distinción en 4 secciones del meristemo apical de la rama y el
ovario sumido en el receptáculo son las tres autapomorfias reconocidas para la familia.
Corresponde a la clasificación CAM (Metabolismo ácido crasuláceo) y es uno de los tres
tipos de fotosíntesis encontrados en los tejidos de las plantas vasculares (Taiz & Zeiger,
2014), el menos común abarcando aproximadamente un 7% de estas. En cuanto a su origen
se cree que una disminución en el CO2 atmosférico durante el mioceno llevó a una
diversificación polifilética, a partir de ancestros C3 (Raven y Spicer, 1996). Paralelamente,
por especialización y colonización de nuevos ecosistemas progresivamente más áridos, la
plasticidad fotosintética llevó a la especiación (Bastide et al., 1993; Lüttge, 2002).
Considerado una adaptación al estrés ambiental provocada por bajos niveles permanentes o
temporales de oxígeno o de CO2 la fotosíntesis en plantas CAM pueden mostrar un
incremento de cinco a diez veces en la eficiencia del aprovechamiento del agua en
comparación a las plantas C4 (Cushman, 2001).
Difiere en la fotosíntesis de plantas C3 Y C4 ya que la fotosíntesis C3 (ciclo C3 o de
Calvin-Benson) se realiza en los cloroplastos de todas las plantas con el uso de la enzima
ribulosa 1, 5- difosfato carboxilasa (RUBISCO) como catalizador de la reacción del CO2
con la ribulosa 1, 5-difosfato, y se llama así porque se producen dos moléculas de tres
carbonos (Andrade et al. 2007).
La fotosíntesis C4 se presenta en plantas con una anatomía foliar llamada „Kranz‟,
caracterizada por la inducción de la maquinaria fotosintética en la vaina vascular, un tipo de
tejido que en las plantas C3 no es fotosintético. La vaina vascular cambia, desarrollando
atípicamente cloroplastos ricos en fotosistema I y una estructura necesaria para asimilar el
CO2 de manera eficiente, como consecuencia de esto las células fotosintéticas del mesófilo
se desarrollan presentando cloroplastos ricos en fotosistema II, aunque no siendo tan
eficientes fotosintéticamente y con deficiencias en Rubisco, estas células se distribuyen
formando una corona alrededor de la vaina.
Este ciclo se desarrolla como una vía de comunicación entre ambos tipos de células (de la
vaina y de mesófilo), y su fin último consiste en concentrar el CO2 en las inmediaciones de
la Rubisco para minimizar las pérdidas ocasionadas por la fotorrespiración (Hatch y Slack,
1970). Otro factor importante y que hace más exitoso el proceso es la fuerte
impermeabilización de la vaina a la difusión del CO2. Como consecuencia las
concentraciones de CO2 atmosféricas. Los metabolitos principales que transportan carbono
y poder reductor desde las células del mesófilo a las de la vaina son el malato o el aspartato
según la modalidad de planta C4 (Hatch y Slack, 1970).
En el citoplasma de las células del mesófilo el CO2 es ligado al aceptor fosfoenol piruvato
(PEP) con el uso de la enzima fosfoenolpiruvato carboxilasa (PEPC) y se producen
compuestos de cuatro carbonos, los cuales son transportados a los cloroplastos de las
células que envuelven el haz vascular, donde se realiza el ciclo C3 (Taiz y Zeiger, 2002;
Larcher, 2003).
En Las plantas CAM también se asimila el CO2 con la participación de las enzimas
Rubisco y PEPC de manera similar a la fotosíntesis C4 con la diferencia que en las plantas
CAM esto ocurre en la misma célula (Parenquimática de empalizada) y la diferenciación es
temporal y no espacial.
La asimilación de CO2 atmosférico mediante apertura estomática ocurre
predominantemente en la noche, el cual es fijado con la ayuda de la enzima PEPC
obteniendo compuestos de cuatro carbonos predominantemente Malato, que son
almacenados en las vacuolas en forma de ácido málico. Durante el día los estomas
permanecen cerrados, los ácidos orgánicos son movilizados, se libera el malato en el citosol
donde presenta una descarboxilación, liberando CO2 y produciendo compuestos de 3
carbonos (Piruvato, PEP), el CO2 liberado en el cloroplasto es asimilado por la enzima
Rubisco, entrando en el ciclo de Calvin-Benson obteniendo de este carbohidratos de
almacén o productos para la gluconeogénesis (Winter y Smith, 1996). De ésta manera
logran una reducción en la tasa de fotorespiración considerable y pérdida mínima de agua
(Herppich y Peckmann, 2000).
El metabolismo CAM está ligado a parámetros del ambiente y puede ser modificado o
perturbado por temperatura, intensidad lumínica, estatus nutricional, humedad ambiental
relativa y disponibilidad de agua (Dodd et al., 2002). Esta capacidad de modificarse es
denominada plasticidad, los estomas, por ejemplo, en el amanecer y el atardecer se abren en
lapsos de tiempo cortos que permiten la fijación de CO2 a carbohidratos cuando el malato
se agota (Lüttge, 2004). La mayoría de plantas CAM establecen una serie de
4.1.4 CLASIFICACIÓN
La familia Cactácea comprende tres subfamilia y nueve tribus ( Figura 1)
1. Pereskioideae: Comprende las especies más basales de la familia y puede llegar a
presentar hojas persistentes no suculentas, tallos con ramificación desde la base o la parte
media, ramas ascendentes o decumbentes y pericarpelo con brácteas foliares .1 género y cerca de 100 especies
2. Cactoideae: La subfamilia más diversa en la familia Cactaceae, comprendiendo más de
90 géneros, posee a veces una diferenciación evidente de la zona fértil denominada en ese
caso cefálio de la infértil, pericarpelo y tubo receptacular desnudo o con brácteas y un
ovario ínfero. Abarca Cerca de 91 géneros y 1300 especies.
3. Opuntioideae: Plantas arborescentes o arbustivas con tallo articulado, erectas o rastreras,
hojas subuladas o con limbo laminar, flores laterales o terminales, numerosos estambres
con gloquidios en sus areolas, un arilo duro rodeando un ovario campilótropo y un tubo
receptacular generalmente inconspicuo. Comprende Aproximadamente 20 géneros y 220 especies.
Figura 1. Clasificación de la familia cactácea (Barthlott y Hunt, 1993) Subfamilias y tribus de la familia Cactáceae.
4.1.5 SUBFAMILIA OPUNTIOIDEAE
Dentro de la familia Cactaceae encontramos una subfamilia llamada Opuntioideae, la
clasificación de esta subfamilia, no ha sido resuelta en su totalidad; actualmente se han
explicado y aclarado inconsistencias sobre su delimitación y origen, relacionadas con su
clasificación, pero la delimitación taxonómica y la filogenia al interior del género Opuntia,
no está claramente concluida, teniendo algunas causas naturales como híbridos
reproduciéndose y plasticidad fenotípica frecuente entre linajes. (Gibson & Nobel 1986)
La subfamilia Opuntioideae contiene cerca de 220-350 especies (Griffith & Porter 2009),
morfológicamente pueden ser diferenciadas al poseer dos caracteres distintivos: espinas
barbadas, deciduas, generalmente pequeñas, naciendo en areolas y un arilo duro rodeando
un óvulo campilótropo (Gibson & Nobel 1986; Stuppy 2002). La presencia de hojas en
estado juvenil y su capacidad fotosintética son características adaptativas relevantes en las
Opuntioideae y más específicamente dentro del género Opuntia como por ejemplo la línea que posee el carácter de tallo aplanado es el más diversa dentro de la subfamilia y puede
haber experimentado una rápida radiación, la proporción área/volumen, que se encuentra en
tallos aplanados de Opuntioides es exitosamente adaptativa y pudo permitir la colonización
de un amplio espectro de hábitats y tipo de climas ( Rebman & Pinkava 2001 a, b; Griffith
2004, Griffith & Porter 2009).
Los tallos planos de los opuntias son un carácter derivado con respecto a los opuntias de
tallo cilíndrico, y el linaje que evolucionó a cladodios planos es muy diverso en especies.
Los Opuntia planos parecen ser un grupo exitoso en su evolución, este carácter sugiere que la evolución de cladodios planos fue un evento relevante para las Opuntioideae (Griffith
2004).
Si se considera que la colonización de nuevos hábitats se debe al tipo de reproducción y
estrategias adaptativas de Opuntia, se debe también tener en cuenta que los caracteres que podrían ser diagnósticos no se pueden considerar aisladamente para separar especies dentro
es probable que tengan repercusión en caracteres vegetativos como areolas, forma, longitud
y ancho de cladodios, a su vez esto puede ser una de las razones que dificultan la
delimitación de las especies de opuntia.
4.2 ANTECEDENTES
En el año 2014 Emilia Arruda, en colaboración con Gladys Melo de Pinna, realizan un
trabajo en el que presentan una caracterización anatómica del segmento caulinar en 4
especies de la familia Opuntioideae enfocándose principalmente en los tejidos que forman
los sistemas de revestimiento, vascular y fundamental, titulado: “Caracteres anatómicos del
segmento caulinar en especies de la subfamilia Opuntioideae (Cactaceae)”. Las especies
examinadas fueron Austrocylindropuntia subulata, Opuntia microdasys, Opuntia monacantha y Opuntia rufida, de las cuales se tomaron muestras de tres segmentos maduros estos subdivididos en tres zonas: basal, media y apical, fijadas posteriormente en
FAA 50 (formaldehído, ácido acético, etanol 50%), luego procedieron a deshidratarlas en
una serie etanol-butanólica 50% - 100% - Butanol Puro, propuesta por Johansen, (1940). A
continuación, se incluyeron en parafina, se formaron los bloques y fueron seccionadas
transversal y longitudinalmente en micrótomo rotativo, donde se obtuvieron los cortes que
fueron teñidos con azul de astra 1% y safranina 1%, finalmente montados para su
observación al microscopio óptico. Las imágenes obtenidas de las estructuras y tejidos
fueron registradas con el sistema de digitalización de imágenes (IM50) acoplado al
microscopio Leica DMLB.
Sus resultados arrojaron que caracteres como la apariencia de la epidermis siendo plana o
sinuosa, presencia de papilas y/o tricomas, tipo de estoma, número de capas de parénquima
de empalizada y de almacenamiento como aspecto general de sus células, aparición de
canales secretores de mucílago adyacentes al floema, configuración de la hipodermis;
permiten distinguir las especies entre ellas y de otras.
En conclusión algunos aspectos de los sistemas de revestimiento, vascular y fundamental,
pueden ser una herramienta útil en el diagnóstico de las especies.
caracterización de secciones de raíces y cladodios en cincos especies de la familia
Cactaceae, Harrisia adscendens, Melocactus horridus, M. zenhtneri, Tacinga inamoena, T. palmadora, analizadas para la verificación de posibles caracteres diagnósticos y adaptativos.
Parte del material vegetativo recogido fue fijado en FAA 50% (Johansen 1940) y
posteriormente conservado en etanol 70% (Sass 1951). A partir de este material, se
realizaron cortes transversales y longitudinales a mano alzada, las secciones se sometieron
a la doble coloración con azul de Astra y fucsina básica según protocolos de coloración de
Kraus et al. (1998).
Las imágenes obtenidas de tejidos y estructuras fueron registradas con ayuda de cámara
clara acoplada al microscopio óptico.
Sus resultados afirman que hay ciertos caracteres que pueden llegar a ser diagnósticos para
las especies y que además influyen en su adaptación a diferentes condiciones, como: tipo de
espina, tipo de estoma, localización del estoma en relación a las demás células
hipodérmicas, apariencia de la epidermis, cristales (drusas) en la hipodermis, estructura de
la hipodermis, tipo de estructura secretora y localización de la misma, aspecto general del
sistema vascular. En términos generales las regiones de la hipodermis e hipodermis
colenquimatosa son importantes en el estudio taxonómico de los representantes de la
familia (Gibson & Horak 1978, Gibson & Nobel 1986), demostrado esto ya que en la
investigación fue posible diferenciar individuos con base en el aspecto de la epidermis, el
espesamiento de las paredes y la forma del lumen de las células de hipodermis.
Como conclusiones los autores afirman que con base a los resultados obtenidos se aprecia
claramente que los caracteres anatómicos mencionados anteriormente tienen relevancia en
cuanto al diagnóstico genérico, y específico de la familia Cactaceae. Las especies
estudiadas
presentan caracteres adaptativos comúnmente atribuidos a la familia y que posiblemente
juegan un papel importante en el éxito de estos individuos ante ambientes adversos, como
la zona de estudio del trabajo.
Ruiz (2013) afirma a partir de los resultados obtenidos en su trabajo titulado
“DISTRIBUCIÓN, VARIACIÓN MORFOLÓGICA Y CORRELACIONES
climáticas tienen un efecto constatable sobre la forma y el desarrollo de los cladodios, la
variación en la longitud y ancho de los cladodios dentro de las poblaciones de las especies
de Opuntia en Colombia, demostró que estaban relacionadas significativamente con la
localidad como se ha propuesto también para otras especies de angiospermas (Ackerly et al.
2002; Godínez-Álvarez et al. 2003; Reyes-Aguëro et al. 2006; Soltis & Soltis 2009).
También se apega a lo mencionado por González y colaboradores (2003) los cuales
deducen que la correlación de los caracteres largo y ancho de cladodios con condiciones
bioclimáticas sugiere plasticidad fenotípica o diferenciación de ecotipos.
Esto nos llevó a cuestionarnos la posibilidad de que, al ocurrir transformaciones externas
determinadas por las condiciones ambientales del punto de distribución, en su interior
también se produjeran variaciones para procurar procesos más eficientes, aprovechando los
recursos existentes y subsistiendo a condiciones adversas.
En el estudio de Silva (2001) dirigida hacia la anatomía interna de los cladodios de los
representantes del género Opuntia, demuestra que los factores del medio, especialmente la
radiación, afectan el grosor de la cutícula, las características epidérmicas y determina los
cambios en las dimensiones celulares del tejido fotosintético.
Sin embargo, la plasticidad, o la capacidad de modificar sus estructuras en respuesta del
medio ambiente no es para nada exclusiva de las cactáceas. Garzón en el 2017 realiza un
estudio histológico de tallo de Gaultheria anastomosans con el fin de realizar una
comparación de los tejidos que conforman la región caulinar de esta especie en dos
ecosistemas diferentes, enfrentándose a presiones ambientales distintas, se pretendió hallar
diferencias significativas en más específicamente en las células xilemáticas y de orden
medular, evidenciando y estableciendo así su plasticidad.
Aplicó Las técnicas de muestreo y protocolos de histología vegetal propuesto por
Sandoval (2005) se llevó a cabo la fase de laboratorio donde se obtuvieron cortes
histológicos, los cuales fueron analizados con ayuda de un microscopio óptico, obteniendo
datos necesarios para realizar la prueba estadística de Wilcoxon, la cual contempló la
medida de las células tanto de xilema como de médula, esta prueba arrojó en sus resultados
que el tamaño de las células en los tejidos estudiados era predominantemente mayor en las
disposición de recursos que ejerce el medio ambiente. Garzón argumenta que Gaultheria
anastomosans desarrolla adaptaciones que le confieren la permanencia en los dos
ecosistemas de estudio, ya sea dando rigidez a la pared celular, o incrementando el tamaño
del área celular para acumular sustancias y tener un mayor flujo hídrico.
5. METODOLOGÍA 5.1 Fase de campo
Área de estudio : Para la selección de las zonas de estudio como primera medida es
indispensable asegurarse que la especie a estudiar está presente en ambas y es accesible
para el muestreo
En Mondoñedo alto se encuentra el desierto de la Herrera conocido como desierto de
Sabrinsky , ésta zona no es un desierto solo es el nombre popular, debido a la apariencia del
suelo muy erosionado que toma un tono rojizo, se encuentra a menos de una hora de la
capital colombiana, hace parte del municipio de Mosquera en la Provincia de Sabana
Occidente, en el Departamento de Cundinamarca, sobre la Cordillera Oriental, su
temperatura promedio es entre 12 y 14 ºC y se ubica a de 2516 m s. n. m, es una zona
relativamente húmeda en especial en las primeras horas de día. Esta región está
relacionada frecuentemente a prácticas agropecuarias e industriales como la minería a cielo
abierto que han llevado a la degradación del suelo principalmente por altas tasas de pérdida
de suelo afectando la disponibilidad de nutrientes para la flora presente (Henao y Gómez
2017).
Esta zona de muestreo será denominada sector (1). La presencia de cactus del género
Opuntia se da por parches de máximo 4 individuos en las zonas altas , más o menos
distanciados entre ellos cercanos a la carretera o sembrados como cercas vivas.
El cañón de Chicamocha en Santander, Colombia es un enclave árido interandino en el que
el género Opuntia se encuentra representado por nueve especies distribuidas en matorrales
subxerofíticos y bosques secos, entre 576 a 1867 m (Porras, Albesiano y Arrieta 2018)
siendo una de las zonas más representativas de Colombia en cuanto a diversidad junto con
la Tatacoa y el Caribe (Galeano y Figueroa,2007). Esta depresión topográfica posee un
régimen climático local muy diferente a sus alrededores, aparentemente relacionado con los
cambios bruscos de altitud y su localización junto a la Sierra Nevada del Cocuy. El
resultado es un clima local semi desértico, con grandes vientos, presiones y temperaturas
locales. Este tipo de clima es muy común en otras partes del mundo junto a grandes sierras
montañosas (C.D.M.B., 2005)
El área de muestreo fue la cuenca media del cañón del río Chicamocha (Los santos, Cepitá
y Pescadero) denominado sector (2) entre los 500 y 1200 m es un ecosistema árido en el
que la vegetación crece en matorrales principalmente, presenta una temperatura de que
oscila entre los 30 y 35° centígrados y una precipitación aproximada de 500 a 700 mm
anuales a diferencia de los verdaderos desiertos cuya precipitación no supera los 250 mm
anuales (Hernández-C. et al. 1995). la cobertura vegetal se ha visto afectada debido al
sobrepastoreo extensivo e incontrolado de ganado caprino, la extracción y construcción y
los deslizamientos de tierra.
Figura 2. Sector (1) de muestreo. Desierto de Sabrinsky o alto
Los individuos fueron determinados mediante las claves El género Opuntia (Opuntioideae– Cactaceae) en el departamento de Santander, Colombia. Porras, Albesiano y Arrieta (2018). Una vez determinado el individuo se realizó el registro de los datos morfométricos,
vegetativos y fotografías correspondientes, se colectó un cladodio por individuo procurando
no sea apical, fue cortado desde la base con un cuchillo, las espinas son retiradas con una
pinza desde la areola. Con un bisturí se obtuvieron cubos de aproximadamente 1 cm3 de la
zona apical media y base del segmento caulinar. Las muestras fueron almacenadas
inmediatamente en frascos previamente preparados y rotulados que contienen dos tipos de
fijador: FAA: Formol (37-40%) 10 ml – Alcohol (96%) 5Oml – Ac. Acético glacial (10%)
5ml (Johansen, 1940) y CRAF fórmula III: Trióxido de cromo (Sol. acuosa al 1%) 30 ml –
ácido acético glacial (10%) 20 ml – Formol (37-40%) 10 ml- agua destilada 10 ml
(Sandoval ,2005). Finalmente transportados en una nevera a una temperatura de -4 °C,
cada 24 horas desde el momento de la colecta hasta la deshidratación debe hacerse un
recambio de fijador, eliminandolo por decantación y volviendo a cubrir el material.
Figura 3. Sector (2) de muestreo, Cuenca media río Chicamocha, en los
5.2 Fase de Laboratorio
Para la estandarización de un protocolo de cortes manuales para Cactáceas se hizo
necesario realizar una deshidratación, si bien en otras plantas este paso no es necesario para
cortar artesanalmente el mucílago impedía una tinción homogénea. Se realizó en series de
alcohol a partir de alcohol al 50% en los individuos fijados en FAA y en los individuos
fijados en CRAF, posterior a un lavado de dos horas a partir de 30% en lapsos de 4 horas
(50%, 70%,96%). Los cortes se ejecutaron a mano alzada empleando cuchillas nuevas
tratando de que estos quedaran lo más finos y parejos posible, Las muestras obtenidas son
teñidas directamente con safranina-verde brillante principalmente, y también se usó fucsina
y azul de metileno, fijadas en láminas de vidrio empleando gelatina glicerinada y
finalmente observadas y fotografiadas en un microscopio Leica y el Programa Image-J
5.3. RESULTADOS ESPERADOS
HIPÒTESIS
Hi: Las características de los tejidos y sistemas vasculares de las plantas del género Opuntia cambian según las Condiciones medioambientales de su hábitat y entre especies.
Ho: Las características de los tejidos y sistemas vasculares de las plantas del género Opuntia no presentan variaciones significativas de una zona de muestreo a otra ni de una especie a otra. .
Los investigadores suponen que se encontrará una variación en la composición y/o organización de los tejidos de la planta y que estas variaciones posiblemente son respuestas
6. RESULTADOS
En el proceso de fijación en consideración de la naturaleza principalmente del hidrenquima
con el fin que este no se rompiera se optó por buscar una alternativa con menos cantidad de
formol empleando CRAF en la tercera fórmula (Sandoval,2005) además del fijador FAA
que es el que suele utilizarse comúnmente para tejidos vegetales. Ambos fijadores
funcionan bien para las cactáceas del género Opuntia con la diferencia que el contenido de cromo en CRAF hace necesario lavar los tejidos, proceso en el cual el flujo de mucílago
aumenta y hace que las series de deshidratación deban ser más largas para ser efectivas. Los
tejidos fijados en FAA no mostraron ningún tipo de daño y mantuvieron su estructura, los
resultados después de dos series de deshidratación fueron favorables, sin embargo, una
tercera serie de alcohol al 96% aumentaba la rigidez del tejido y ocasionaba la lisis de las
células de almacenamiento, por este motivo se recomienda estandarizar el proceso de
fijación con FAA y posteriormente realizar dos series de 4 horas en alcohol al 50% y 70%.
En la fase de colecta En el sector 1, Mondoñedo, Cundinamarca asociado a clima húmedo y
de bajas temperaturas, fueron colectados cladodios de dos individuos de las especies O. quitensis y O. dillenii. En el sector 2, correspondiente a la cuenca media del Río Chicamocha con un ambiente semidesértico más característico de los cactus O. dillenii fue nuevamente colectada con el fin de comparar la misma especie en los dos sectores, junto
con O. pennellii especie endémica colombiana.
(Todas las imágenes utilizadas en este apartado son de nuestra autoría. Imágenes por: González & Sánchez, 2019)
Figura 4.O. pennellii. A. Habito de crecimiento erecto B. Cladodio C. Areolas inmersas con dos espinas. D. Detalle del cladodio curvado, Sector 2, Cañón de Chicamocha, Santander.
Opuntia quitensis
Figura 6. O. dillenii. A. Habito de crecimiento erecto B. Areola expuesta C. Areolas con 6 -7 espinas. D. Detalle del cladodio romboide redondeado, Sector 1, Mondoñedo, Cundinamarca.
(A-C). Sector 2. Cuenca del rio Chicamocha, Santander.
6.1 TEJIDOS
DE
PROTECCIÓN
En las especies O. dillenii y O. Quitensis colectadas en el sector 1 Mosquera, Cundinamarca presentan: cambium felógeno en un rango que varía de 3 a 6 capas de células.
La felodermis se compone mayormente de 3 a 4 capas de células, algunas zonas del
segmento caulinar pueden presentar una mayor producción de células donde la peridermis
es ondulada. En las especies colectadas en el sector 2 del cañón de Chicamocha, Santander,
O. dillenii y O. pennelli está ausente este carácter en su lugar poseen una epidermis uniseriada (figura 8) y de aspecto plano o liso recubierta externamente por una capa cérea
denominada cutícula. (figura 8 )
La hipodermis es de naturaleza colenquimatosa formada por 3 a 5 capas de células, siendo
la media 4 capas (figura 9) , el espesamiento de tipo laminar se presenta uniforme en todos
los individuos observados ,el lumen de estas células toma una apariencia redondeada a
aplanada, en la primera capa se observa una fila de drusas con distribución continua La peridermis es la zona más externa se
deriva del crecimiento secundario y cumple
una función protectora, está en particular
reemplaza la epidermis. Está compuesto
principalmente por cambium felógeno
meristemo secundario del cual se derivan
dos capas, hacia el exterior el súber o
corcho, células muertas a su madurez, hacia
el interior aparece la felodermis formada por
inmediatamente interna a la epidermis o peridermis, esta distribución es muy común en los
representantes de Opuntioideae. En la especie Opuntia pennellii apreciamos cámaras subestomáticas de gran tamaño que atraviesan por completo la capa subepidermica
distribuidas a lo largo de toda la epidermis de forma intermitente, No sé aprecio este
6.2 PARENQUIMA CLOROFILICO
Las células del parénquima clorofílico de empalizada tienen forma alargada, más o menos
rectangulares, poseen un gran número de cloroplastos, una composición compacta, sin
espacios extracelulares. (figura 10) se encarga de la fotosíntesis principalmente, el número
de capas celulares de este tejido puede variar entre un rango 4 a 7 capas de células
dependiendo la especie en cuestión. 5-6 dillenii, 5-7 en O. pennellii y 4-6 en O. quitensis
Figura 10: Parénquima clorofílico de empalizada. A O. dinelli. Sector 2. B. O. pennellii. C. O. dillenii sector 1. PE. Parénquima clorofílico de empalizada. D. drusa. H. hipodermis
PARENQUIMA DE RESERVA
El parénquima acuífero comprende parte del córtex interno y de la médula, su función
principal es la de almacenar agua y sustancias de reserva. constituido por células
isodiamétricas presenta paredes celulares delgadas, vacuolas muy desarrolladas ricas en
agua y en mucílagos, que también pueden estar en las paredes y en el citoplasma. En el
hidrenquima enconramos cristales de oxalacetato de calcio (drusas) en forma de cristales
con prolongaciones. (figura 11)
Este tejido permanece invariable en las 4 especies contempladas en este estudio,
únicamente en la zona basal de los segmentos caulinares de O. diilenni y O. quitensis se observa una diferencia, el parénquima de almacenamiento saturado de partículas sólidas y
células de mucilago, en la zona del cortex,estas retienen más contenido en su interior
generando que se tiña de coloración más oscura, y se ubican en zonas más allá de su
distribución normal apareciendo en el parénquima de empalizada y los rayos de parénquima
ubicados entre los haces vasculares (figura 12) ,estas células secretoras son propias de los
cactus , almacenan el mucilago entre la membrana plasmática y la pared celular y
progresivamente este remplaza el protoplasto, este mucilago se caracteriza por ser rico en
polisacáridos, son concurrentes en todos los individuos colectados, los referentes al sector 2
O. pennelli y O. dillenii poseen una menor cantidad y se restringen al parénquima de
almacenamiento. (figura 11)
6.3 CANALES DE MUCILAGO
Los canales de mucílago se encuentran en el parénquima de almacenamiento, restringidos a
la región pericíclica adyacente al floema primario. Se hallaron en todas las especies
contempladas en este estudio a excepción de O. dillenii en la del sector 2 en la zona base y apical, variando en forma y tamaño entre los sectores de colecta, las zonas del cladodio y
asociados o no a un haz vascular.
En O. dillenii y O. quitensis (sector 1) se evidencia un patrón en la estructura y forma del canal correspondientes a las zonas apical, media y basal del cladodio. En la zona apical esta
estructura se aprecia medianamente desarrollada, el espacio conducto se ve reducido, y
rodeado de varias capas de células de parenquima de reserva que le dan forma, se ven
asociados generalmente a los haces de mayor tamaño y desarrollo siendo proporcionales y
adyacentes al floema primario, acompañándolos se aprecia gran cantidad de drusas
dispuestas en el canal. (figura 13). En la zona media los canales son de mayor tamaño en
comparación con la zona apical , las capas de células que rodean el canal son menos y el
espacio interno aumenta considerablemente y se mantienen proporcionales al haz vascular
asociado. En la zona basal los canales poseen menor diámetro nuevamente presentan un
tamaño reducido en comparación con el haz vascular, con varias capas de células que dan
forma a la estructura y espacio del conducto reducido incluso hasta cerrado. (figura 13)
En O. pennelli (sector 2) vemos como existe una proporción en el tamaño de la estructura referente al ancho del haz vascular más no a su longitud, los conductos presentan la misma
rodean el conducto dándole forma y el espacio interno es reducido, casi cerrado . Estos
conductos se ven más asociados a los haces vasculares de mayor porte.( figura 14). Todos
los canales de mucilago se asocian a un haz vascuar pero no todos los haces vasculares
tienen un canal asociado.
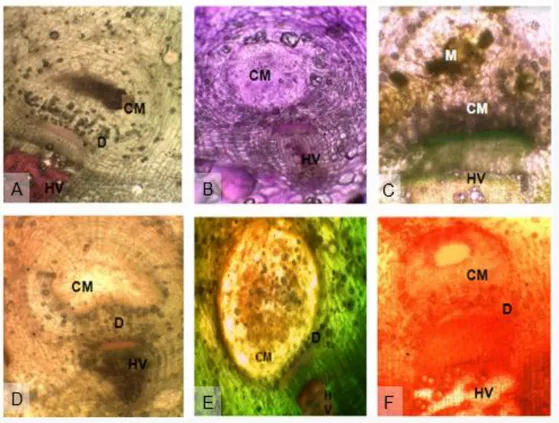
Figura 13. Canales de mucilago en O. quitensis A-C y O. dillenii D-F en cortes transversales. A, D Canal de mucilago en la zona apical del cladodio. B, E Canal de mucilago en la zona media del cladodio. C, F Canal en la
zona basal y O. dillenii. Sector 1. CM. Canal de mucilago. HV. Haz vascular. D. drusa. M. Mucilago Aumento 4X y 10x.
Figura 14. Canales de mucilago en O. pennelli en cortes transversales. A y B. Canal en la zona apical del cladodio. C. Canal de mucilago en la zona media del cladodio. D Canal en la zona basal. CM. Canal de mucilago. HV. Haz vascular. D. drusa. RP. Rayos de parénquima medular.
PA. Parénquima de
6.4TEJIDOS VASCULARES
Las estelas presentes en Opuntioideae son de tipo eustela colateral abierta por lo que se
ubican a la periferia del cladodio en forma de circulo al margen de este.
En O. dillenii (sector 1) los haces vasculares de la zona apical están apenas en desarrollo, de poca longitud, poseen alrededor de 1- 4 hileras de xilema y las fibras distribuidas en este
son escasas en general. En O. quitensis los haces fueron en poco grado más anchos debido esto a una mayor presencia de fibras xilemáticas dispuestas entre los vasos de xilema, que
pueden alcanzar hasta 5 hileras de vasos.
En los individuos del sector 2 los haces vasculares son alargados y delgados las hileras que
lo componen oscilan de 1-3, son pocos los haces vasculares en los que se pueden observar
fibras xilemáticas, en O. dillenii los haces son notoriamente más alargados y delgados que en las otras 2 especies estudiadas, presentan pocas hileras de xilema siendo común
encontrar entre 1 - 2 en la mayoría de haces vasculares con parches de traqueidas pequeños
en poca proporción , algunos más desarrollados alcanzan los 3 y un aumento mínimo en la
presencia de traqueidas acompañando el xilema (figura 15).
Figura 15. Haces vasculares en corte transversal de la zona apical del cladodio en las especies A. O. quitensis. B. O. dillenii (Sector 1). C. O. pennellii. D. O. dillenii (sector 2). CM. Canal de
mucilago. HV1. Haz
vascular primario. HV2. Haz
vascular secundario. D.
drusa. RP. Rayos de
parénquima medular. PA.
Parénquima de
almacenamiento. Cel. M. Células de mucilago. CV.
Cambium fascicular. X.
En la zona media del cladodio se observa un estado más avanzado de desarrollo de haces
vasculares, esto conlleva un mayor tamaño en general de estas estructuras, se encuentran
los haces más separados en la banda de parénquima medular, se compone de más hileras de
xilema y una mayor cantidad de fibras de xilema acompañándolo, esto para los individuos
del sector 1. (figura 16)
En O. quitensis vemos un haz vascular bastante largo y ancho con un aspecto más o menos cónico, pueden poseer más de 7 hileras de xilema, con bastantes fibras de xilema rodeando
las hileras pueden abarcar más o menos la mitad del cordón vascular, esto en los haces
principales, en los secundarios son más cortos con alrededor de 4 hileras de xilema y
parches pequeños de fibras xilemáticas. En la especie O. Dillenii colectada en el sector 1,
encontramos similaridades con O. quitensis, se evidencio un mayor tamaño del haz vascular aumentando más su longitud que su ancho, en los cordones principales se pueden alcanzar
de 5 a 7 hileras de xilema, y fibras xilemáticas presentes en alrededor de la mitad del
cordón vascular, los cordones vasculares secundarios poseen de 1 a 3 hileras de xilema y
pequeños parches de fibras xilemáticas.
En cuanto a las especies colectadas en el sector 2 de igual forma se evidencia desarrollo en
los haces vasculares, pero más en cuanto a su longitud, en el caso de O. penelli tienen una apariencia alargada y delgada tantos los haces principales como los secundarios, las hileras
de xilema varían de 3 a 4 en los haces principales y de 1 a 2 en los haces secundarios,
inclusive se observaron vestigios zonas donde posiblemente aparezca un haz vascular
teniendo su aspecto pero con células muy poco diferenciadas, vemos una presencia de
fibras de xilema que ocupa la mitad de haz vascular en los principales y pequeños parches
en los secundarios en algunos ausentes. La especie O. dinnelli los haces vasculares tiene una apariencia alargada y delgada también con alrededor de 1 a 2 hileras de xilema en los
cordones secundarios y 3 a 4 en los cordones principales, la presencia de fibras en los haces
Figura 16. Haces vasculares en corte transversal de la zona media del cladodio en las especies A, B, O. pennellii. C y D, O. dillenii (Sector 2) E Y F. O. quitensis. G-I. O. dillenii (sector 1) CM. Canal de mucilago. HV1. Haz vascular primario. D. drusas. RP. Rayos de parénquima medular. PA. Parénquima de almacenamiento. Cel. M. Células de mucilago, X. Xilema, F. Floema, f. fibras xilemáticas, P. Parénquima de xilema, CV. Cambium vascular, PF. Floema primario, MF.
Los haces vasculares basales de los individuos del sector 1 (FIGURA 17) en comparación a las
anteriores zonas del cladodio, presentan una mayor aparición de fibras de xilema que pueden llegar
a ocupar casi la totalidad del haz vascular, presentan el mismo número de hileras que en la zona
anterior 6 a 7 o un pequeño incremento en estas, encontrando 7 o más, esto en los cordones
principales, los secundarios pueden presentar entre 3 a 5 hileras, el aspecto de estos es cónico más
pronunciado que en la zona media, en la especie O. quitensis apreciamos colénquima angular
alrededor de los haces vasculares principales, mayormente en la parte final de los mismo, aportando
un mayor sostén.
Figura 18. Haces vasculares en corte transversal de la zona basal del cladodio en las especies A-C, O. pennellii D – F O. dillenii(sector 2 Chicamocha, Santander). HV1. Haz vascular primario, HV D. Haz vascular en desarrollo, D. drusas, RP. Rayos de parénquima medular. PA. Parénquima de almacenamiento, P. Parenquima de xilema, X. Xilema, f. fibras xilematicas, Cel. M. Células de mucilago. f. fibras, MF. Floema secundario, Aumento 4x, 10x,
Los individuos colectados en el sector2, presentan cordones vasculares con aspecto
alargado al igual que en las otras zonas del cladodio, pero aumenta su ancho en poca
proporción en los principales, estos poseen alrededor de 4 a 5 hileras de xilema en la
especie O. pennelli y 5 a 6 en O. dinnelli, presentan fibras xilematicas que abarcan más de la mitad del has vascular en las dos especies, en cuanto a los cordones secundarios
encontramos de 1 a 2 hileras de xilema en las dos especies, O.pennelli presenta fibras xilemáticas en parches que pueden abarcar la mitad del haz vascular o menos , de igual
manera que en O. dillenii.
En las 3 especies analizadas, fueron hallados de dos tipos de drusas, el primero distribuido
en la primera capa de células de la hipodermis colenquimátosa, dispuestas en una hilera
continua a lo largo del segmento caulinar, estas tenían un aspecto redondeado, el segundo
tipo se encontraba distribuido en la zona del córtex que presentaba parénquima de
almacenamiento y parte de la medula, pero principalmente la zona periciclica, adyacente a
los canales de mucilago en general, y en mayor medida en los asociados a los haces
vasculares principales, allí se veía un incremento exponencial de estas estructuras , poseen
prolongaciones de sus cristales en puntas, diferenciándolas de las ubicadas en la capa
7. DISCUSIÓN
La estructura más externa en el segmento vascular perteneciente al sistema de protección
que fue encontrada en los individuos colectados en el sector (1) O. dillenii y O. quitensis , fue la peridermis, Gibson & Nobel (1986) y Soffiatti & Angyalossy (2003) han descrito la
presencia de este carácter en otras especies a nivel de la familia Cactaceae, de igual forma
Gibson & Nobel (1986) mencionan puede ocurrir durante una determinada fase de vida de
la planta o por algún tipo de injuria en el tronco, añaden que aunque este tejido se
desarrolle en gran parte del órgano, nunca lo recubre totalmente, permaneciendo la
epidermis como principal tejido de revestimiento. En el sector (1) de muestreo fue posible
apreciar individuos de las 2 especies con diferente longevidad y por ende tamaño, la
peridermis era un carácter en común a simple vista, los cladodios más basales presentaban
una completa cobertura de peridermis, de igual forma los cladodios más jóvenes
presentaban cobertura en menor medida, esto en plantas adultas, en las plantas juveniles de
pequeño porte evidenciamos presencia de este tejido en parches de reducido tamaño,
corroborando así que un factor evidentemente es la etapa de desarrollo en que se encuentre
el individuo y las diferentes zonas de este, aunque presumimos que las condiciones
ambientales y disponibilidad de recursos en este sector puede estar causando un tipo de
daño en los individuos generando que sea más común este carácter, una de las hipótesis
planteadas también por Gibson y Nobel (1986). En las especies colectadas en el sector (2)
O. dillenii y O. pennelli este carácter no fue evidenciado, al presentarse la especie O. dillenii en ambos sectores y notar la particularidad de que el carácter en el sector (1) esté presente y en el sector (2) ausente, creemos que las condiciones de su punto de distribución
influyen en gran medida. Gibson y Nobel (1990) como también Mauseth (1999) explican
que la formación de esta peridermis en los cactus se da a partir de una transformación de la
epidermis la cual se diferencia para luego originar felógeno, tejido meristemático del cual
se origina la felodermis y el súber, zonas interna y externa, adyacentes al cambium
felógeno que en conjunto constituyen la peridermis, siendo contrario al proceso normal en
que el felógeno se forma en la corteza situada bajo la epidermis. Este tejido surge en
reemplazo de la epidermis en tallos y raíces como consecuencia del crecimiento secundario
de estos órganos. Al observarse este carácter en tallos de individuos juveniles, o tallos
relativamente jóvenes, en parches de variable tamaño y no de manera uniforme, nos indica
que no es un patrón de suberificación común o natural, sino más bien una respuesta de la
planta frente a afecciones y desperfectos superficiales (Salamanca, 2016) la aparición de
este carácter bajo estas circunstancias ha sido descrito también por Fahn (1974)
fortaleciendo nuestra hipótesis.
La epidermis de las especies colectadas en el sector (2) es uniseriada, de aspecto plano o
liso recubiertas externamente por una capa cérea denominada cutícula, la función de esta
capa es la de reducir la desecación de la planta por exposición a la atmósfera terrestre
además de ser una barrera extra para la entrada de bacterias y hongos, contribuye también a
equilibrar el balance energético por reducción de la radiación neta absorbida debido
al aumento de la reflectancia que genera (silva et al 2001). En los cactus que no
pertenecen a la subfamilia Pereskioideae el sistema de revestimiento predominante es la
epidermis en las regiones apical y media del cladodio, esto debido a que el proceso
fotosintético se lleva a cabo en el segmento caulinar (Gibson Y Horak 1978, Mauseth 1996,
1999), según Darling (1989) en estos cactus la epidermis puede conservarse y mantenerse
funcional a lo largo de los años, llevando a cabo de manera exitosa los procesos de
intercambios gaseosos necesarios para la realización de la fotosíntesis.
La hipodermis colenquimatosa es el tejido contiguo interiormente a la capa epidérmica, La
denominación utilizada para hacer referencia a este tejido, fue descrita por Metcalfe &
Chalk (1950), Conde (1975), Gibson & Nobel (1986), Fahn & Cutler (1992) entre
otros, presente en las tres especies colectadas y con características similares, como lo son 3
a 5 capas de células, generalmente 4, la primera de estas presenta una alta cantidad de
drusas dispuestas en una única hilera continua a lo largo del segmento caulinar, estas capas
de colénquima poseen un espesamiento de pared de tipo laminar, el lumen se puede ver de
forma un tanto redondeada a aplanada, muy similar a lo descrito por Salamanca (2016), el
cual afirma que el número de capas que presenta la hipodermis colenquimática es variable,
entre 2 y 6, siendo lo más frecuente 4 o 5, añade que las células de las capas más internas
hipodermis, pudiendo ser un carácter que aporte a la diferenciación de especies, en Harrisia adscendens las capas subepidérmicas están constituidas por células colenquimatosas de tipo laminar, en el caso de Tacinga palmadora son angulares, incluso algunas especies como el caso de Melocactus zehntneri el espesamiento de sus células de hipodermis no encaja en ninguno de los tipos descritos en la literatura, describiendo la hipodermis como colénquima
con células que presentan lumen irregular.
La hipodermis de esta naturaleza es encargada de ejercer funciones de sostén en los
primeros años del cladodio, ayudada por cordones de xilema y en edad más adulta por
fibras de esclerénquima en el xilema. Cuando se presentan aumentos en el volumen de la
corteza subyacente, debido a mecanismos propios de la planta, este tejido es el que
otorga resistencia y la capacidad para contenerlos (Mauseth, 2006) además debido a la
cualidad extensible de sus células, pueden aumentar el espesor y superficie de sus paredes
celulares, es un tejido altamente adecuado para aportar resistencia mecánica a órganos en
crecimiento (Cortés, 1980).
silva (2010) afirma que este tejido también cumple funciones de protección mecánica,
como por ejemplo de barrera frente a patógenos, como también contra la radiación UV
reflejándose en cierta medida.
En O. penelli se encontraron abundantes cámaras subestomaticas que atraviesan totalmente la capa subepidérmica de hipodermis colenquimática, siendo la única de las tres especies,
estas grandes cámaras subestomáticas son mencionadas por algunos autores (Conde 1975,
Gibson Y Horak 1978, Soffiatti & Angyalossy 2003), Arruda (et al, 2005) observó estas
estructuras en las especies; Harrisia adscendens, Melocactus horridus, Melocactus zenhtner, Tacinga inamoena y Tacinga palmadora. Según Darling (1989) , Fahn & Cutler (1992) la localización de estas cámaras asegura rápidos intercambios
gaseosos poco después de la apertura de los estomas, aumentando así la eficiencia
fotosintética.
Tanto la epidermis como el colénquima subepidérmico de las Cactaceae, además de
desempeñar función de protección para el tallo, constituyen regiones importantes en el
estudio taxonómico de representantes de la familia (Gibson y Horak 1978, Gibson y Nobel
1986), esto verificado en el estudio de Arruda en 2004, donde fue posible diferenciar