UNIVERSIDAD A U T ~ N O M A METROPOLITANA
- IZTAPALAPA
D I V I S I ~ N DE CIENCIAS BIOL~GICAS Y DE LA SALUDDIGESTI~N ANAEROBIA DE LACTOSA EN DOS ETAPAS
PROYECTO DE SERVICIO SOCIAL L\C *
ING. BIOQUÍMICA INDUSTRIAL p r e s e n t a
DANIEL VILCHIS
BOLLAS
Asesoria:
OSCAR A. MONROY HERMOSILLO PATRICIA OLGUÍN LORA
LABORATORIO DE MICROBIOLOGÍA AMBIENTAL DEPARTAMENTO DE BIOTECNOLOGÍA
INDICE
RESUMEN ... 1
INTRODUCCI~N ... 1
PROCESO EN DOS ETAPAS ... 2
MODELAMIENTO DE LA DIGESTI~N ANAEROBIA ... 2
ANTECEDENTES Y JUSTIFICACI~N ... 4
OBJETIVOS ... 5
MATERIALES Y METODOS ... 5
REACTORES ...
5
INÓCULO ... 6
MEDIO DE ALIMENTACI~N ... 7
CONDICIONES DE ALIMENTACIóN Y OPERACIóN DEL SISTEMA ... 7
TECNICAS ANALÍTICAS ... 7
MODELO MATEMÁTICO ... 9
COMPORTAMIENTO DEL REACTOR ACIDOGÉNICO ... 11
COMPORTAMIENTO DEL REACTOR METANOGÉNICO ... 15
RESULTADOS Y DISCUSIóN ... 9
ALCALINIDAD, PA Y ESTRATEGIA DE CONTROL ... 17
PRUEBA DE LA ESTABILIDAD: MODELO MATEMÁTICO ... 19
CONCLUSIONES ... 21
RECOMENDACIONES ... 22
BIBLIOGRAFÍA ... 22
APENDICE I: PREPARACI~N DEL MEDIO SINTÉTICO RAMM ... 24
DIGESTI~N
ANAEROBIA DELACTOSA
ENDOS ETAPAS
RESUMEN
Se trabajó en la digestión anaerobia de lactosa en un sistema de dos etapas utilizando reactores UASB (0.34 y 1.35 1) conectados en serie. Se estudió la estabilidad y capacidad de respuesta del sistema ante variaciones controladas de la velocidad de carga (entre 7.9
-
27.5gDQ0A.d para el reactor acidogénico y 1.7
-
6.5 gDQ0A.d para el metanogénico) mediante lacuantificación de variables de respuesta tales como el pH, consumo de DQO, producción de
metano, producción de ácidos grasos volátiles (AGV), y variaciones del potencial de
amortiguamiento-bicarbonato añadido.
Se encontró que en la etapa de acidogénesis (la etapa) hay producción de metano y la pequeña cantidad que se obtiene es independiente de las variaciones en la velocidad de carga del reactor. El predominio de la producción de metano y su clara respuesta al variar la velocidad de carga se observaron en la etapa metanogénica. Siguiendo con el plan de neutralización de los AGV (producidos en la la etapa) con bicarbonatos en la entrada del 2"
reactor, se observó que este representa una buena medida para tener un potencial de amortiguamiento estable y positivo en esta etapa con el cual no se tienen inhibiciones en la eficiencia de conversión de sustrato ni en la metanogénesis por acidificación del reactor; con esta estrategia de control es posible, recomendable y justificable trabajar la digestión anaerobia en las dos etapas para velocidades de carga elevadas: el sistema soportó hasta 6.5 gDQO/I.d siempre con buena eficiencia de remoción de lactosa (98.6%).
En base a los bicarbonatos añadidos, al consumo de la DQO y a la producción de biogás se probó un modelo adaptable para caracterizar la estabilidad de la metanogénesis encontrándose que los parámetros que reflejan dicha estabilidad de esta etapa tienden a ser constantes e independientes de la velocidad de carga a menos que la variación de alimentación sustrato sea demasiado drástica (de 4 gA de diferencia).
La digestión anaerobia es un proceso de degradación natural en el cual un cierto número y tipo de microorganismos actúan en ausencia de 0 2 sobre la materia orgánica dando como productos finales metano y bióxido de carbono. En años recientes este proceso natural ha sido ampliamente estudiado y se ha aplicado en el cuidado ambiental, ya que comprende la remoción de desechos orgánicos de efluentes industriales y domésticos así como la producción del metano como combustible.
El proceso de digestión anaerobia básicamente procede en tres etapas:
l. Etapa de hidrólisis y fermentación: Acidogénesk- Los polimeros naturales y compuestos de
menor peso molecular (aminoácidos, sacáridos, lípidos, compuestos aromáticos, etc.) son hidrolizados y fermentados en ácidos carboxílicos, alcohol,
H2
y COZ. Los ácidosbutírico, isobutírico, valérico e isovalérico. Las principales poblaciones microbianas
involucradas comprenden las bacterias fermentativas en general, entre las que destacan las especies de clostridium y las enterobacterias.
2" etapa: Acetogénesis.- Es realizada por bacterias acetogénicas productoras obligadas de
H2
(OHPA), las cuales convierten los productos de la primera etapa en acetato,
H2
y C02. El pH óptimo de éstas bacterias está cerca de la neutralidad y son inhibidas por H 2 , por lo que es necesario que no se acumule en el medio.3" etapa: Metanogénesís.- Se lleva a cabo a través de las bacterias productoras de metano (metanogénicas), las cuales lo pueden producir a partir de acetato (acetoclásticas, que producen la mayor parte del metano, alrededor del 73%) y otras lo producen a partir de C02 e
H2
(hidrogenotróficas). Es importante observar que esta utilización deH2
evita la inhibición de la acetogénesis: las bacteriasOHPA
y las hidrogenotrofas están en relación sintrófica. El pH óptimo de las bacterias metanogénicas también está cercano a la neutralidad.Existen diferentes tipos de reactores en los cuales la digestión anaerobia se puede llevar a cabo. Uno de los más utilizados para este tipo de proceso es el reactor de lecho de lodos de flujo ascendente (UASB) debido a sus grandes ventajas, entre las que se encuentran que soportan altas cargas de materia orgánica, bajo requerimiento de energía, no requieren medio de soporte, su construcción es simple y es aplicable a pequeña y gran escala.
PROCESO EN
DOSETAPAS
Debido a la interrelación de las bacterias acetogénicas (OHPA) con las metanogénicas hidrogenotrofas y a sus similitudes en condiciones fisicoquimicas (pH=7), se ha propuesto que estas dos etapas operen fisicamente juntas (en un mismo reactor), mientras que la acidogénesis se opere aparte debido a las diferentes necesidades de condiciones fisicoquímicas, nutricionales y fisiológicas de las poblaciones bacterianas involucradas. Esto implica tener dos reactores conectados en serie en donde el primer reactor le da un pretratamiento a la materia orgánica y el segundo le confiere la degradación final convirtiéndola en metano.
MODELAMIENTO DE LA D I G E S T I ~ N
ANAEROBIA
En la digestión anaerobia ocurren varias reacciones bioquímicas, cada una con velocidades diferentes. Asimismo, aunque el metabolismo de las bacterias anaerobias les permite hidrolizar mayores cantidades de materia orgánica sin generar una cantidad de biomasa, las hace más sensibles a las condiciones ambientales, como son el
pH
y la temperatura; a los cambios en la composición del influente, que incluyen cambios bruscos en la materia orgánica los cuales ocasionan la acidificación del medio. Así, puede resultar afectado el metabolismo de laactividad biológica del reactor.
Un sistema de tratamiento adecuado tiene como objetivo lograr que todas las reacciones bioquímicas ocurran simultáneamente a una velocidad aceptable, además de detectar los pasos limitantes en una situación dada, según las características del influente. Dada la complejidad del proceso de la digestión anaerobia y al hecho de que la velocidad de crecimineto de las bacterias limitantes es lenta, sería necesario invertir una gran cantidad de tiempo a la experimentación con la finalidad de estudiar exhaustivamente el comportamento de los digestores anaerobios. El desarrollo de modelos matemáticos ha permitido obtener información del proceso y evaluar estrategias de control.
En 1990 Van Breusegem et al. propuso un modelo matemático dinámico para la digestión anaerobia que considera la actividad biológica de dos poblaciones: bacterias hidrolíticas- acidogénicas y bacterias metanogénicas. El modelo consta de un balance de biomasa, de sustrato, otro para la producción de metano y bióxido de carbono; y para describir la fase fisicoquímica, un balance de bicarbonato, de ácidos grasos volátiles y del bióxido de carbono disuelto; todos actuando sobre la tasa de dilución como variable de control. Con ésto se logró una buena descripción, predicción y simulación del proceso.
Posteriormente Alvarez et al. en 1992 utilizan el modelo de Van Breusegem e introduciendo varios parámetros y consideraciones más lo implementan para la digestión anaerobia en dos etapas; este modelo es el que se utilizará como parte final del proyecto para evaluar una estrategia de control propuesta que se describe a continuación:
Las ecuaciones involucradas para este modelo que resultan del balance de materiales en torno a ambos reactores son:
Al = p ~ X l / Y3
-
Dl(Ao-
Al) para el reactor acidogénico, yA2 =
-
~2x2 / Y2-
DI(A1- A2) para el reactor metanogénico, donde:-
Ai, Xi y pi son las concentraciones de AGV, biomasa y velocidad específica de crecimiento-
D l es la tasa de dilución del reactor 1 (acidogénico)-
Y1 es el rendimiento de la biomasa en el RA respecto al consumo de sustrato,-
Y2 es el rendimiento de la biomasa del RA respecto al consumo de AGV,-
Y3 es el rendimiento de la biomasa del Rh4 respecto al consumo de AGV en el respectivo reactor (Ao son los AGV de entrada al sistema),Zi(t)=Bi(t)+Ai(t) [Eqh], se producciones de biogás Qi y
siguiente ecuación, que ya parametros a:
sustituyen los valores de piXi/Y, por sus correspondientes
se combinan las ecuaciones de la segunda etapa obteniendose la agrupan las constantes de rendimiento desconocidas en los
Usando un modelo estable de referencia de primer orden, puede ser resuelta ésta ecuación diferencial para obtener la expresión dinámica de control:
Con esta ecuación ya es posible caracterizar al sistema asi como su estabilidad.
ANTECEDENTES
Y
JUSTIFICACI~N
En trabajos previos se ha visto que es posible y viable operar la digestión anaerobia en dos etapas y en dos reactores con diferentes condiciones, tanto fisicoquímicas como de operación. Los estudios han medido la cinética de producción de AGV y de metano a diferentes cargas orgánicas volumétricas (COv, ó velocidades de carga), de 0.5 a 4 g/l.d. Se ha observado que la velocidad de producción de ácido acético aumenta con la COv y la de otros ácidos grasos disminuye. Los AGV están directamente involucrados con el potencial de amortiguamiento
(PA)
del medio en el segundo reactor junto con el C02 desprendido y la cantidad de bicarbonato añadido. Este potencial confiere un cierto equilibrio fisicoquímico al medio e influye de manera significativa en la degradación de materia orgánica (lactosa) y en la producción de metano. El potencial de amortiguamiento se calcula mediante la relación:PA = HC03-
-
HAGVDonde HAGV representa los ácidos grasos volátiles protonados.
OBJETIVOS
OBJETIVO GENERAL
-
Estudiar la dinámica de la digestión anaerobia en dos etapas ante variaciones altas de la velocidad de carga de alimentación del sistema.OBJETIVOS
ESPECÍFICOS
-
Estudiar el comportamiento de variables de respuesta tales como el consumo de sustrato, la producción de AGV, la producción de biogás y el pH al hacer variar la velocidad de carga en un rango de 2 a 8 gDQOlactosa/l en relación a la alimentación del sistema.-
Analizar el comportamiento del potencial de amortiguamiento en el reactor metanogénico con relación a la adición de bicarbonatos para la neutralización de los AGV generados por el RA.-
Caracterizar la estabilidad del sistema mediante un modelo matemático adaptable que involucra el consumo de sustrato, adición de bicarbonatos y producción de biogás.MATERIALES
Y
METODOS
REACTORES
Se utilizaron dos reactores tubulares de vidrio de diferentes tamaños; el pequeño con un volumen de operación de 0.34 litros se utilizó como el reactor acidogénico, y el grande
hé
el reactor metanogénico con un volumen de operación de 1.35 1; ambos reactores se usaronSALIDA DE BIOGÁS
t
II
M E T A N O G É N I
C
O
INÓCULO
Los lodos empleados para la operación de los reactores consistieron en una mezcla de 60 %
de lodos que previamente habían sido empleados también para la metabolización de lactosa, y el resto procedíó de la planta piloto de tratamiento de aguas resíduales de la UAM-1.
Para asegurar la completa adaptación de los lodos a sus correspondientes sustratos, se monitoreó la producción de biogás para ambos reactores; y se consideró que ya estaban aptos para la operación como sistema cuando el RM alcanzara su máxima producción teorica de metano, y el RA cuando estabilizara su producción de biogás.
Tanto el volumen del inóculo como la concentración de sus sólidos en ambos reactores se resumen en la siguiente tabla:
Tipo de solidos suspendidos Reactor Reactor
Totales (SST) 98.28 47.39 Fijos (SSF)
43.38
480
140
Volumen del lodo (ml)
23 .O
50.89 Volátiles (SSV)
20.39
Acidogénico
[gA]
Metanogénico[dl
MEDIO DE
ALIMENTACI~N
Se utilizó el medio sintético RAMM (SheltodTiedje), cuya forma de preparación y
composición se menciona en el Apendice 1. La hente de carbono utilizada fbé lactosa de grado farmaceutico industrial; y una vez preparado el medio se esterilizaba en autoclave a 15 libras de presión por solo 10 minutos para evitar su caramelización. Se tuvieron diferentes alimentaciones de sustrato, y para aquellas de 2 , 4 y 6 gDQO/l se procedió a preparar el medio con las cantidades que son requeridas por este medio, pero para preparar una alimentación de sustrato con 8 g/l se hizo una pequeña modificación que consistió en adicionar un exceso de las solución mineral 2 (con NH&l como hente de N) de tal forma que en el medio final quedara una relación de DQORV de 700/15 (con el medio normal solo se consigue una relación DQORV de 700/12).
CONDICIONES
DE
ALIMENTACI~N
Y OPERACI~N
DEL SISTEMA
En estudios previos con un sistema de dos etapas (Lora O./Monroy H. O.), se logró encontrar las condiciones óptimas de operación de este tipo de sistemas; en base a estos resultados se ocuparon las condiciones hidraúlicas recomendadas para que de este modo se tuviera las máximas eficiencias de conversión de sustrato, y la mínima probabilidad de acidificación para el caso del RA; estas condiciones corresponden a utilizar el RA con un
TRH
de 6 h, y al RM con un TRH de 1 día. De este modo para variar la velocidad de carga de alimentación deseada solamente se modificaba la concentración en el medio de alimentación.
TECNICAS ANALÍTICAS
química de oxígeno (DQO), que tiene las ventajas de reproducibilidad y rapidéz en su ejecución. Se usó el método de reflujo cerrado (APHA 1989) modificado: consiste en la digestión de la materia orgánica con dicromato de potasio y ácido sulfürico/sulfato de plata en una parrilla o estufa durante dos horas para su reflujo.
Al
final la muestra desarrolla coloración (verde) cuya intensidad está de acuerdo a la cantidad de materia orgánica, la cuál es cuantificada mediante un colorímetro a una longitud de onda de 620 nm, y esta lectura es comparada con una curva patrón previamente elaborada que se anexa en el Apendice 11.AGV totales. bicarbonatos Y PA.- Todos se determinaror por medio de titulaciones y
retrotitulaciones potenciométricas según el método de PowelVArcher en ambos efluentes de los reactores. Los AGV determinados por éste método procedentes del RA sirven para calcular la cantidad de bicarbonatos con que es necesario neutralizarlos a la entrada del RM
para evitar su acidificación. El potencial de amortiguamiento se calcula como la diferencia de concentración de bicarbonatos cuantificados en cada efluente menos los AGV protonados (ambos en Eq/l).
Composición de AGV.- Se realizó por cromatografia de gases determinandose el ácido acético, propiónico y butirico: 1 m1 de muestra previamente centrifbgada a 13000 rpm durante 10 minutos era acidificada con 10 pl de ácido fórmico puro, y de esta se inyectaban 2 p1 al cromatógrafo
(Hp
5890), el cuál tenía las siguientes condiciones de operación:Detector de ionización de flama integrado
Columna Carbopack 60/80 con 0.3 % de carbowax 20 M en O. 1 % H3P04 Temperatura del inyector de 220 OC
Temperatura de la columna de 120 OC
Temperatura del detector de 220 O C Flujo del gas acarreador (N2) 5 mumin Relación N2/Aire/H2 20/300/30
Para la cuantificación de los diferentes tipos de AGV se construyó una curva patrón de calibración de la concentración vs. areas cromatográficas para cada uno, y se encuentran resumidas en el Apendice 11. Esta determinación también ayudó a verificar los datos obtenidos de la cuantificación de los AGV por titulación.
Producción
v
composición del biogás.- El biogás se determinó mediante un cuantificador digital de flujo DENED CDF-402 que va contando los ciclos que el biogás va dezplazado en relación a un pequeño volumen de calibración dentro de una cámara de vasos comunicantes que es purgada cada vez que se cuenta un ciclo.Detector integrado de conductividad térmica Columna de acero empacada con carbospore Temperatura del inyector de 170 OC
Temperatura de la columna de 140 OC Temperatura del detector de 190 OC
Flujo del gas acarreador (He) 30 d m i n Presión del acarreador de 50 psi aprox. Corriente de los filamentos: 120 mA
La curva de calibración para determinar la composición del biogás (metano y dióxodo de carbono) se anexa en el apendice 11.
MODELO MATEMÁTICO
Se utilizó el modelo matemático propuesto por AlvarezMonroy (1992) para caracterizar la estabilidad del sistema. Este modelo consiste en establecer dos ecuaciones diferenciales algebraicas para cada etapa que se obtienen mediante el balance de materiales, teniendo como
suposición una purga periódica de la biomasa del
Rh4
(ver introducción). La ecuación principal de control derivada del balance de materiales es:D ( t ) = C ( S t r e f - St(t)) - C 1 1 Q C H 4
+
C t 2 Q C O 2 s o - S ( t )Si es conocido D(t), So, S(t), QCH4 y QC02 lo cuál sucede para el experimento, los parámetros a (1 y 2) pueden ser estimados por un algoritmo de mínimos cuadrados. Como los parámetros a tienen involucrados a los coeficientes de rendimiento y son derivados de de las ecuaciones diferenciales del balance de materiales, su estimación refleja la estabilidad del consumo de sustrato y de los bicarbonatos en relación al tiempo. En éste trabajo se realizó la metodología para la estimación de los parámetros al y a2 mediante un algoritmo de mínimos cuadrados implementado en hoja de cálculo electronica.
RESULTADOS Y
DISCUSI~N
Una vez que los reactores heron reinoculados, se procedió a trabajados en forma independiente alimentando al RA 4 gDQO/l de lactosa; durante su adaptación fbé necesario interrumpir su operación una vez por día (durante los primeros 3 días), parando el reactor cerca de 3 horas para asegurar la completa sedimentación de los Iodos. El RM
hé
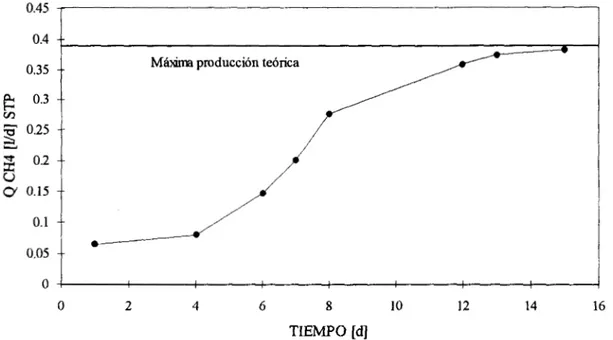
alimentado con 1 gDQOA de acetato de sodio en recirculación.después de alcanzar valores máximos (hasta de 492 d d ) , retornó y se mantuvo en un valor estable de alrededor de 160 mud. En el caso del RM se aseguró una buena adaptación de sus lodos para cuando su producción de metano debido a la DQO de acetato consumida estuviera muy próxima con su valor teórico (con 2.5% de diferencia), de acuerdo a la Figura l .
0.45
0.4 --
e
0.35 -- M A X ~ ~ producción teórica
0.3 -- r/)
0.2
u
Cy 0.15
o.
1 0.05/
f
O 2 4 6 8 10 12 14 16
TIEMPO [dl
Figura l . Acondicionamiento de la metanogénesis con acetato de sodio.
Aproximadamente ambos reactores lograron una buena estabilidad a los 15 días, y a los 20 de ser reinoculados se procedió a conectarlos como un sistema de dos etapas, empezando en sí
el experimento.
Durante los primeros 29 días de iniciado el experimento la neutralización de los AGVt procedentes del RA se realizó con un exceso del 35 % de los bicarbonatos en relación a los necesitados estequiométricamente esperando con esto que no existiera ninguna posibilidad de acidificación del RM y lograr de esta forma su completo acondicionamiento. La Tabla 1 resume las diferentes velocidades de carga operadas asi como el momento en que se realizaron sus variaciones.
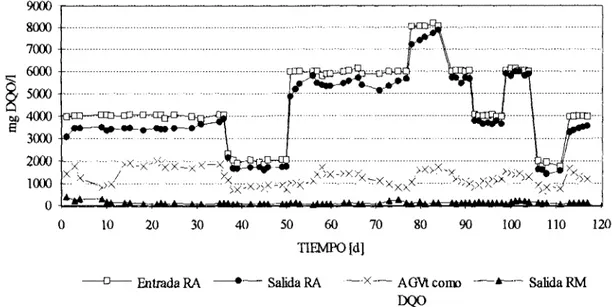
La figura 2 muestra el comportamiento del consumo de DQOlactosa a lo largo de los 117 días de operación del sistema en los cuales se aprecian claramente los cambios de sustrato en la alimentación del sistema (en la entrada del reactor acidogénico) asi como la respuesta de ambos reactores en sus correspondientes salidas.
...
...
-D- Entrada RA "--e--- Salida RA -X- AGVt como
-
Salida RM DQOFigura 2. Seguimiento en el consumo de la DQO.
COMPORTAMIENTO DEL
REACTORACIDOGÉNICO
En la Figura 2 se aprecia claramente como a partir del día 29 se observó un cambio notable en el consumo de la DQO para el caso de la salida del RA: a pesar de que se trabajaba con la misma carga de alimentación la eficiencia de conversión comenzó a disminuir en este punto; este fenómeno con la observación de que la subsecuente eficiencia del remoción de la DQO sigui0 baja marcó la pauta para distinguir que el reactor a partir de éste día alcanzó una buena estabilidad que se mantuvo durante todo el experimento.
cantidad de sustrato (en el día 75) parece tornarse más estable el consumo. Este fenómeno no se manifiesta con el cambio de sustrato de 4 a 6 g/1 ya que en este caso el consumo es estable y desde el principio la eficiencia tiende a permanecer constante y baja (alrededor del 3 %). Es
evidente que aunque se esté operando bajo la misma carga, la magnitud del cambio de carga de la cual se precede (que sea inferior) afecta la actividad de los lodos (la inhibe) lo cual se traduce en estados metabólicos notablemente oscilantes e inestables (la inhibición por sustrato
y el aceleramiento en su consumo se tornan más drásticos).
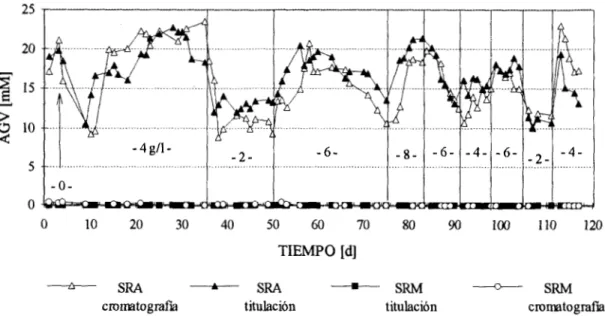
Aunque se repitió varias veces la misma carga, la producción de ácidos grasos totales (AGVt) por el RA no tuvo un valor fijo para una misma carga (Figura 3). Esta producción dependía de la carga que precedía y si ésta provenía de un aumento o una disminución en la concentración de sustrato. Lo que queda claro es la tendencia de que cuando se sube la carga se acelera la producción de AGVTt, y visceversa.
-
SRA -t- SRA-
SRM -0- SRMcmmatografu titulación titulación cmmatografu
Figura 3. Concentración de acidos grasos volátiles en el reactor acidogénico a diferentes velocidades de carga. Los números indican los valores de alimentación; y la flecha muestra una interrupción en la operación.
La figura 3 muestra que cuando en el día 3 se dejó de operar el reactor por 2 días seguidos,
se observó con la subsecuente puesta en marcha que la producción de AGVt bajó drásticamente: antes de esta interrupción se tenía una producción de alrededor de 17.5 mh4 de AGVt y después del paro se registró una caida hasta un valor de 10mM. El reactor tuvo una recuperación rápida (de 5 días) para que la producción de AGVt se volviera a encontrar en el punto original que tenía antes de la interrupción.
cargas se muestran en la Figura
4.
Aunque en realidad es poca la diferencia de consumo de sustrato entre la mayor y menor carga para elRA
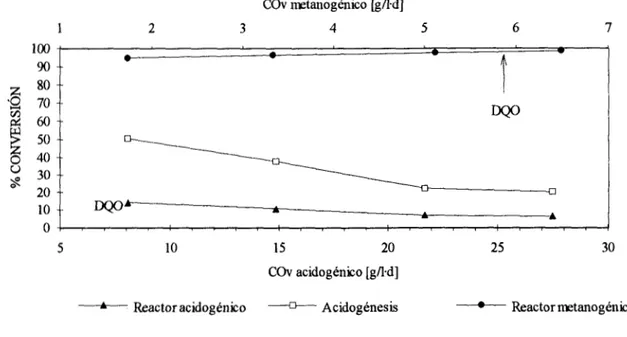
(de 6.5 y 14 %), existe la tenencia que al aumentar la carga se disminuya la eficiencia de consumo; este fenómeno sería favorable al proceso de la la etapa si realmente ese decremento de remoción se tradujera en AGVt, pero no sucede esto como lo muestra la disminución de la acidogénesis en relación a la carga en la misma Figura 4. Por lo tanto, es más probable que dicho pequeño decremento de la eficiencia se deba ensí
a la inhibición de la acidogénesis, y este fenómeno acarrea la ventaja de que el sistema no puede sobreacidificarse y por lo tanto está autorregulado.Con efectos prácticos para el caso del RA en la figura 4, se puede considerar que para altas cargas de más de 20 g/l-d se tiene una eficiencia de remoción de la DQO constante (en este caso un promedio de 7 %) y que ya no es posible que baje más por la completa saturación del sistema.
COv metanogénico [ghd]
1 2 3 4 5 6 7
2 80
*g 70
9
50 40 30 2010
O
260
S
I
DQO
5 10 15 20 25
COv acidogénico [gllsd]
30
-t- Reactor acidogénico "u-- Acidogénesis "-Reactor metanogénico
Figura 4. Eficiencias de conversión de la DQO y de la acidogénesis en relación a
las diferentes velocidades de carga.
La identificación del tipo de AGV producido por el
RA
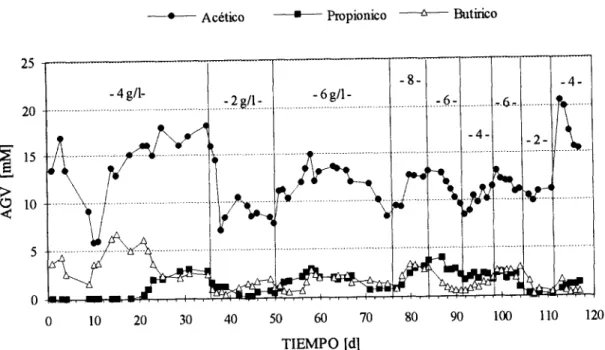
se muestra en la figura 5. La mayor cantidad corresponde al ácido acético y representa el 79 % en promedio de los AGV totales, lo que se considera favorable para la etapa metanogénica.Por otra parte se tiene que tanto
el
comportamiento como la cantidad de producción de los-" Acético Propionic0 -"Butirico
. . . . . . . .
O 10 20 30 40 50 60 70 80 90 100 110 120
TIEMPO [dl
Figura 5. Identificación del tipo de AGV en la salida del
RA
a diferentesvelocidades de carga.
100 I
40
30
20:
:
K
4
10O
6 8 10 12 14 16 18 20 22 24 26 28
COv acidogénico[gA dl
Figura 6. Proporción relativa de los diferentes tipos de AGV en relación a la velocidad de carga de alimentación.
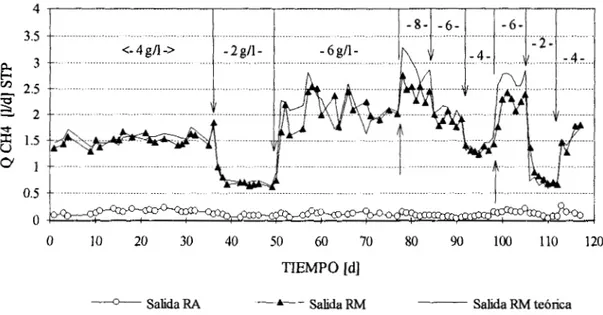
En cuanto a la producción de metano del RA (Figura 7), para todo el experimento y sin importar la carga del reactor se tuvo una producción de metano aproximadamente constante (alrededor de O. 12 Vd); lo que indica que existe en cierta medida la metanogénesis aunque predomine la acidigénesis. Esta producción demuestra que las poblaciones microbianas de los Iodos no están completamente diferenciadas y separadas al menos en este reactor, pero hay la tendencia a que se mantengan constantes y a que no tengan mucho impacto en la producción de metano.
4
3.5
3
2.5
E
2 2
S
u
1.5 a 10.5
O
..."... ~ ... . . .
O 10 20 30 40 50 60 70 80 90 100 110 120
TIEMPO [dl
-Q-SalidaRA
-
Salida RM Salida Rh4 teóricaFigura 7. Producción de metano en ambos reactores. Las flechas indican el momento en que se realizan los cambios de carga de alimentación.
COMPORTAMIENTO
DEL
REACTOR METANOGÉNICO
El tiempo que tardó en estabilizarse el RM fié menor en relación al correspondiente del RA: desde el día 10 alcanzó un consumo casi total de la DQO que mantuvo a lo largo de todo el experimento (Figuras 2 y 4), con una eficiencia media de remoción del 96.7%; sin embargo aún antes de este día se puede decir que la conversión de la DQO de salida de éste reactor fbé alta (90.6%). Debido a que el RM siempre conservó elevadas eficiencias y éstas tendieron a variar dentro de un pequeño rango (Figura 4), se aprecia que al aumentar la velocidad de carga se aumentó la eficiencia. Comparando éstas altas eficiencias de remoción con las obtenidas con el RA que heron bajas (10.7 % en promedio), se aprecia que la eficiencia de conversión global del sistema está gobernada por el RM, y su valor del 96.9 % lo prueba.
consumidos en su totalidad para la producción de biogás.
En cuanto a la producción del RM, la Figura 7 muestra claramente que está en relación directa con la carga trabajada, pero no para todas las cargas se alcanza desde el principio del cambio el valor máximo teórico; tal es el caso al subir la concentración de sustrato del sistema de 2 a 6 , de 6
-
8 y de 4-
6dl.
El fenómeno del retraso en alcanzar la producción teórica
significa justamente lo que pasó con el RA: los cambios hasta una carga superior de
alimentación correspondiente a los 6 u 8 g/l de sustrato resultan en un impacto fberte sobre la
estabilidad del reactor, que para el caso del RA se tradujo en la autorregulación de la acidogénesis, pero para el RM se manifiesta como una incapacidad temporal para transformar la DQO a metano. Además, como el caso del
RA,
el máximo impacto tuvo lugar al cambio más drástico de carga que correspondió al cambio de sustrato de 2-
6 g/l (con 4 gA dediferencia) debido a que le toma más tiempo alcanzar la producción teórica en relación a las otras dos desestabilizaciones.
Una tendencia cercanamente lineal del comportamiento de producción de biogás (R =
0.993), asi como de la producción de metano teórica en relación a la carga trabajada se demuestra mediante la Figura 8.
1 2 3 4 5 6 7
COv [gDQO/l.d]
"E+- Biogás CH4 . . . . . . CH4 teorico C02
Figura 8, Comportamiento de la producción del biogás en relación a la velocidad
de carga.
Este comportamiento se explica fácilmente si se toma en cuenta que el RA tiene un rango
bajo de consumo de la DQO en relación a la carga (Figura 4) y la remanente de su efluente es la mayoría, la cuál es consumida casi en su totalidad por el RM para la producción de biogás.
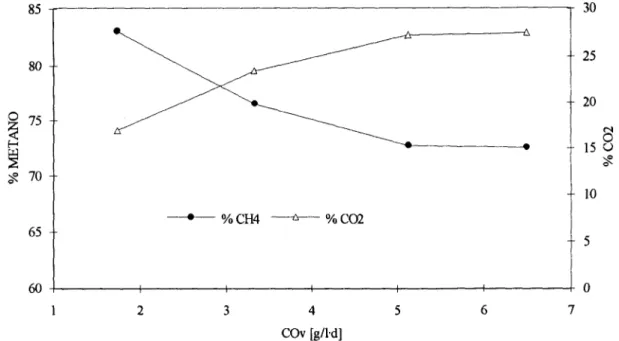
aleja de su correspondiente teórica. El análisis de la composición del biogás en la salida del
RM en la Figura 9 puede explicar la desviación de la producción de metano de su correspondiente teórica: conforme se aumenta la velocidad de carga se disminuye el porcentaje de metano y en la misma proporción de esta disminución se aumenta el de COZ. La tendencia de la disminución en la composición de metano parece no ser permanente ya que al sobrepasar los 5 g1.d tiende a permanecer constante y se muestra como que ya no bajará mas alla de alrededor del 72 %
85
80
75
5
S 7065
60
30
25
20
O"
15 0
S
10
5
O
1 2 3 4 5 6 7
COV [g/l.d]
Figura 9. Composición de biogás en la salida del reactor metanogénico al variar la velocidad de carga.
ALCALINIDAD, PA Y ESTRATEGIA DE CONTROL
Como ya se había mencionado, la adición justa de bicarbonatos para respetar la estrategia de neutralización de los AGV a la entrada del
RM
con el fin de controlar su alcalinidad, comenzó apartir del día 29 del experimento. Para el cálculo de los bicarbonatos añadidos se ocuparon los valores de determinación de AGV totales por tutulación a la salida del RA, que como ya se vió antes (Figura 3) resultó ser un método relativamente preciso para sucuantificación en relación a los resultados obtenidos por el análisis cuomatográfico; ambos solo difirieron en un 8 %.
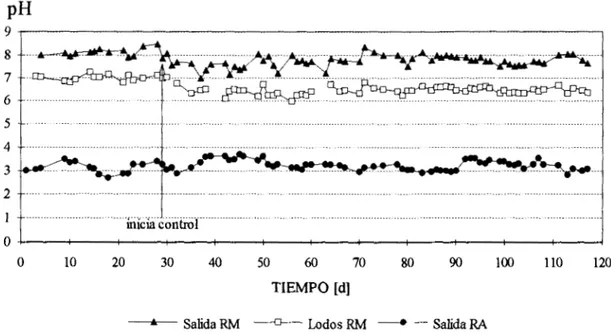
Como resultado de esta adición continua de bicarbonatos al RM, la figura 10 muestra como
9 1 1
... ...
...
2
...
1 ... <..-
I
mica control
O . .I
O 10 20 30 40 50 60 70 80 90 110 120
TIEMPO [dl
--" Salida RM Lodos R M -0- Salida RA
Figura 1 O. Seguimiento del pH en el efluente de los reactores y en los lodos
metanogénicos .
También mediante la Figura 10 se muestra que a pesar de que a lo largo del tiempo se tuvieron variaciones de la velocidad de carga de alimentación al
RA,
su pH no variósignificativamente y se mantuvo en torno a un valor promedio de 3.22 (S=0.22), lo que da prueba que tiene las condiciones para estar autorregulado.
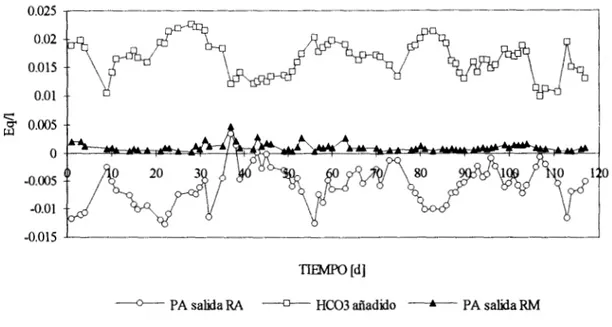
0.025 1 l
e 0.005
O
-0.005
-0.01
O
-0.015 I
e PA salida RA "u-- HC03 añadido -'"PA salida RM
Figura 11. Anulación del potencial de amortiguamiento negativo de la salida
del
RA
con bicarbonato.Tabla 2. Adición media de NaHCO? por carga.
[
AlimentaciónI
Velocidad de cargaI
NaHCO? aiiadidoI
[g DQOA]I
[fled]k 1
2 8.05
I
1.59~
I I
I
4I
14.84I
2.1 16
2.56 27.49
8
2.22 2 1.69
PRUEBA
DE
LA ESTABILIDAD: MODELOMATEMÁTICO
Se utilizaron todos los datos del
R M
de consumo de sustrato, producción de biogás junto con los valores de adición de bicarbonatos para resolver las dos ecuaciones diferenciales que describe el modelo matemático y de esta forma calcular los coeficientes a . Los valores de a a lo largo del tiempo agrupan los valores de rendimiento que son desconocidos, todos ellos involucrados ya seaen
el consumo de sustrato o bien en la producción de metano.estimadores:
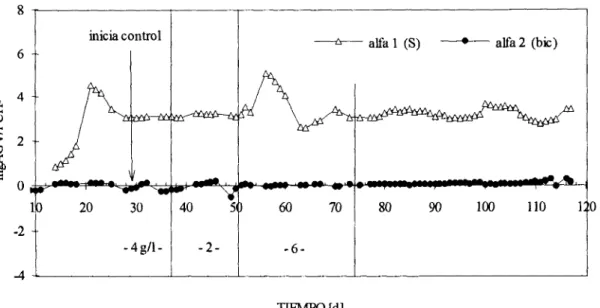
8
-" alfa 1 (S) -" alfa2 (bic)
6
4
8
g 2
E O
d
-2
TIEMPO [dl
Figura 12. Comportamiento de los parámetros de estabilidad alfa.
El parámetro que refleja la estabilidad en relación a la necesidad de bicarbonato a2 tuvo valores sumamente constantes en el riempo y no registró alteraciones significativas que pudieran indicar algún posible peligro de acidificación del sistema, ni cuando se implementó el
control, ni mucho menos antes por la existencia de un exceso de 35 % de bicarbonatos. Estos datos están de acuerdo con los valores de pH de los Iodos y del efluente del RM (Figura 10) los cuales nenca tuvieron alguna caida en sus valores, al igual que el potencial de amortiguamiento (Figura 11) el cuál tuvo una tendencia constante.
generadas en el consumo de DQO del
RA
(Figura 2), con el aceleramiento-disminución de la producción de AGV para la carga cambiada (a 6 g / l , Figura 3), y con el retardo en alcanzar la producción teorica de metano (Figura 7).CONCLUSIONES
-
El sistema soportó bien variaciones de carga hacia valores altos, siendo capaz siempre de degradar la lactosa; pero la dinámica de consumo de sustrato del RA no respondió en forma rápida a variaciones de carga de 4 g/1 de diferencia en la alimentación de sustrato o para más de 6 g / l : en ambos casos tardó hasta 6 días en retornar a las bajas eficiencias previamente mostradas, lo que significa que el RM compensó la falta de dicha capacidad degradativa. Una variación ascendente de carga con 4 g/l de diferencia descompensó el sistema mostrando tendencias oscilatorias en sus variables de respuesta.-
Las bajas eficiencias mostradas a lo largo del tiempo por el RA no necesariamente correspondieron en una buena conversión hacia AGV en relación a la DQO de su efluente: se tuvo un efecto inhibitorio en la producción de AGV por altas velocidades de carga; a pesar de esa disminución en la capacidad de acidificación, el RM tuvo la capacidad de degradar la mayor parte de la DQO no acidificada mostrando elevadas eficiencias de conversión de sustrato a lo largo de todo el experimento.-
Al aumentar la carga dentro de valores altos, el RA aceleró la producción de AGV; pero éste incremento en relación a la DQO de su efluente representa una disminución: más allá de un valor de carga de 13 gDQO/l.d no se acidifica más del 40 % de la DQO. Además es posible que pasando una alimentación de 4g/l
se tenga el inicio de la inhibición.-
Ante variaciones hacia cargas altas, el RA disminuyó la proporción de ácido acético en relación a los AGV totales y aumentó la producción del propiónico y butírico. Con cargas superiores a los 22 g k d predominó la producción de ácido butírico des-acelerandose la de propiónico.-
La producción de metano respondió en forma rápida para alcanzar su valor teórico ante las variaciones de carga; pero a variaciones drásticas de la misma (más alla de 3.S
g/l-d de diferencia) o en valores altos (más de4
g/l-d) la producción no alcanzó a la teórica o le tomó mucho tiempo hacerlo.-
Se confirmó que en el RA coexisten poblaciones microbianas metanogénicas, y que independientemente de la carga producen una pequeña y constante cantidad de metano.-
Con la estrategia de control propuesta que consiste en la neutralización de los AGV en el influente delRM
se tuvo buen control sobre la acidificación del reactor; ésto contribuyó a tener siempre un potecial de amortiguamiento positivo y constante, además de que permitió una elevada eficiencia de remoción de la DQO aún para cargas altas o para cambios drásticos en la misma.-
El modelo matemático adaptable trabajado caracterizó bien el comportamiento de la estabilidad del sistema: los pariunetros a que reflejan dicha estabilidad en relación a laadición de bicarbonatos y de la capacidad de consumo de la DQO reflejaron el comportamiento de otras variables de respuesta tales como el pH, la producción de AGV y de metano.
RECOMENDACIONES
-
Probar el sistema con un sustrato más dificil de acidificar para comprobar si realmente el RM es ahora capaz de compensar la falta de conversión de AGV del RA por las altas velocidades de carga.-
Si se continua con la caracterización de la digestión anaerobia de la lactosa en dos etapas mediante la modelación matemática, sería conveniente trabajar aún mas altas alimentaciones de sustrato para ver la tolerancia límite del RM, ya que en el experimento aunque se alcanzaron altas velocidades de carga másica para la alimentación de 8 gDQO/I (0.81 1 gDQO/gSSVd) es probable que el sistema aún aguante más carga sin bajar significativamente sus eficiencias de conversión.BIBLIOGRAFÍA
-
Alvarez, J.; Monroy, O.; Ruiz,V.
(1992). Model and control strategies of two stage anaerobic digestor. In: Modeling and control of Biotechnical processes. EAC Symposia series; Colorado U. S. A. pp. 191-
194.-
APHA/AWWA/WPCF (1989). Standard Methods for the examination of water wastewater. 17th edition. Joint Editorial Board.-
Cuervo Lopez F. "Digestión anaerobia de lactosa: efecto del potencial de amortiguamiento y comparación con un modelo cinnético". Tesis de maestría, U A " 1 Depto. de Biotecnología; Junio de 1995.Biotecnología; Julio de 1995.
-
Monroy H. O./Guyot J. P./Noyola R. A./et. al. "Bioprocesos Anaerobios para el Tratamiento de Efluentes Industriales". Universidad Autónoma Metropolitana-
Iztapalapa, Depto. de Biotecnología. Curso organizado UAM-ORSTOM-IMP, 6 Y 7 de mayo de 1992.-
Monroy H. 0.Niniegra G. G. "Biotecnología para el Aprovechamiento de los Desperdicios Orgánicos". Ed. AGT, México D. F. 198 l . pp. 65-
93.-
Powel, G. A.; Archer,D.
A. (1989). One line titration method for monitoring buffer capacity and total volatile fatty acid levels in anaerobic digesters. Biotechnol. Bioeng., 33: 570-
577.-
Quintero R. R. "Ingeniería Bioquímica" Ed. Alhambra. 1" edición (2' reimpresión), MéxicoD.
F. 1990. PP. 247 -267.APENDICE
IPREPARACI~N
DEL
MEDIO
SINTÉTICO RAMMConsta de la mezcla de cuatro soluciones minerales en la siguiente proporción: Componentes Volumen /
1
alim. Solución Mineral 1Solución de Oligoelementos
10 ml Solución de FeC13
50 ml
Solución Mineral 2
50 ml
1 m l
siguientes reacl
Las soluciones minerales están preparadas de manera concentrada de acuerdo a los tivos:
REACTIVO Concentración
[g/g
Solución Mineral 1 :KH2P04 7.0
~ Solución Mineral 2:
I
1
I
CaCly2H20 1.5K2HP04 5.4
NH4Cl 10.6
MgC12'6H70 2.0
Solución de FeC12: FeC12~4H20
Solución de oligoelementos:
2.0
0.5 0.05 0.05 0.03 0.01 0.05 0.05
Na2Se0~ 0.05
Para preparar la solución de oligoelementos, se disuelven perfectamente en un vaso las dos primeras sales.
En
otro vaso se disuelven los reactivos restantes excepto el cloruro de cobalto que se disuelve en un recipiente por separado agregando 1 ml de HC1 concentrado. Finalmente se mezclan y se ajusta el volumen a unlitro con agua destilada.El cloruro de hierro se disuelve directamente en 1 m1 de HCl concentrado, y se agrega agua hasta aforar a un litro.
RE
ACTIVO PESOfl solución Buffer de fosfatos (pH = 7)m2po4 K?HPO4
0.27 g
0.35 g
NH4Cl
0.5 mg PulnC12'4H2O
20 mg
FeC12.4H20
75 mg CaCly2H20
0.53 g
Sales minerales
MgC12.6H20 100 mg
Elementos Traza
HRBOB 0.05 mg
ZnC12
0.01 mg Na2SeOq
0.01 mg NiC12.6H20
0.01 mg NaM04*2H20
0.05 mg
cuc12 0.03 mg
APENDICE I1
CURVAS
PATRÓNDE
CALIBRACI~NCURVA PATRÓN DE DQO
1200
1000
800
2
600
400
200
O
O 0.0s o. I 0.15 0.2 0.2s 0.3 0.35 0.4
DO [ABSORBANCIA]
90
-- 80
"
70 --
60 --
50 -- 40 --
30 --
% CH4 CURVA PATRdN DE METANO
1 O0
% CH4 = 93.4505(A CH4lAT) +7.4665 , ...
O o. 1 0.2 O. 3 0.4 0.5 0.6 0.7 0.8 0.9