Contribución al estudio fitoquímico de partes aéreas de la especie vegetal Momordica Charantia (Cucurbitaceae) y evaluación de su capacidad antioxidante
Texto completo
(2) CONTRIBUCIÓN AL ESTUDIO FITOQUÍMICO DE PARTES AÉREAS DE LA ESPECIE Momordica charantia Linn (CUCURBITACEAE) Y EVALUACIÓN DE SU CAPACIDAD ANTIOXIDANTE. GUINNET PAOLA FUQUENE BUSTOS. Proyecto de grado como requisito para optar al título de pregrado en licenciatura en química.. DIRECTORES: WILLIAM FERNANDO CASTRILLON CARDONA Químico, Magíster en ciencias ambientales, Magíster investigación en educación, Especialista en informática para la docencia, Docente Universidad Distrital FJC. JAVIER ANDRES MATULEVICH PELAEZ Licenciado en Química, Especialista en Análisis Químico Instrumental, Magister en Ciencias Biológicas – Fitoquímica, Docente Universidad Distrital FJC. UNIVERSIDAD DISTRITAL FRANCISCO JOSÉ DE CALDAS FACULTAD DE CIENCIAS Y EDUCACIÓN PROYECTO CURRICULAR DE LICENCIATURA EN QUÍMICA Bogotá. D.C 2018.
(3) AGRADECIMIENTOS Agradezco a Dios en primer lugar por haberme acompañado y guiado a lo largo de mi carrera, a mis padres Mauricio y Nidia por su apoyo, fortaleza y amor en cada momento de mi vida, A mis abuelos Beatriz y Antonio, a mis tíos Pilar y Gregori por darme la fuerza y confianza para cumplir mis metas y sueños, siendo cada uno de ellos mi motor de vida. Le agradezco a la universidad Distrital por la formación como profesional, además agradezco al profesor William Castrillón por permitirme estar en el Grupo de investigación de Productos Naturales Vegetales. Le agradezco al profesor Javier Matulevich por él, apoyo, confianza y amistad quien a través de su experiencia y ejemplo a seguir. ha sido parte importante de mi aprendizaje en la carrera y formación en todo el trayecto de mi tesis. Le agradezco a Carlos y a mis amigos por llenar mi vida de alegría y brindarme su apoyo incondicional. A Diego Silva y a todo el grupo de Investigación de productos Naturales por el apoyo, la confianza y amistad formada. A la Pontificia Universidad Javeriana le agradezco por el préstamo de instalaciones y equipos empleados, al igual que al profesor Gonzalo Sequeda por su colaboración en la determinación de la capacidad antioxidante..
(4) TABLA DE CONTENIDO 1. RESUMEN ................................................................................................... 1. 2. INTRODUCCIÓN ......................................................................................... 3. 3. JUSTIFICACIÓN ......................................................................................... 4. 4. OBJETIVOS ................................................................................................ 6 4.1 OBJETIVO GENERAL .......................................................................... 6 4.2 OBJETIVOS ESPECÍFICOS ................................................................. 6 PLANTEAMIENTO DEL PROBLEMA ............................................. 7 4.3 FÓRMULACIÓN DEL PROBLEMA ...................................................... 7. 5. ESTADO ACTUAL DEL TEMA ................................................................... 8 5.1 FAMILIA CUCURBITACEAE ............................................................... 8 Características generales de la familia Cucurbitaceae ................... 8 Características morfológicas de la familia Cucurbitaceae .............. 8 Distribución de la familia Cucurbitaceae ......................................... 9 Usos etnobotánicos de la familia Cucurbitaceae ............................ 9 Actividades biológicas evaluadas en especies de la Familia Cucurbitaceae............................................................................................ 10. Momordica grosvenori. .................................................................................. 11 Estudios Químicos de la familia Cucurbitaceae ............................ 12 5.2 Género Momordica............................................................................ 15 Características morfológicas del género Momordica .................... 15 Distribución del género Momordica .............................................. 16 Usos etnobotánicos del género Momordica .................................. 17 Actividades biológicas en especies del género Momordica .......... 17 Estudios químicos del género Momordica .................................... 19 5.3 Especie Momordica Charantia L. ..................................................... 23 Características morfológicas de la especie Momordica charantia L. …………………………………………………………………………..23 Distribución de la especie Momordica charantia L........................ 24 Usos etnobotánicos de la especie Momordica charantia L. .......... 26 Actividad biológica de la especie Momordica Charantia L. ........... 26 Estudio químico de la especie Momordica Charantia L. ............... 28 5.4 Capacidad antioxidante .................................................................... 30 Determinación de la capacidad antioxidante ................................ 31 Método de 1,1-difenil-2-pricrilhidrazil (DPPH) ............................... 31 Método del ácido 2,2'–azino–bis–[3–etillbenzotiazolin–6–sulfónico] •+ (ABTS ) ..................................................................................................... 32 6. METODOLOGIA ........................................................................................ 34 6.1 GENERALIDADES ............................................................................. 34 Métodos de separación cromatográficos y elucidación estructural34 Espectroscopia de Resonancia Magnética Nuclear...................... 35.
(5) 6.2 L. Estudio fitoquímico de las partes aéreas de Momordica charantia ……………………………………………………………………………….35 Recolección e identificación del material vegetal.......................... 35 Marcha fitoquímica preliminar ....................................................... 36 Obtención del extracto etanólico de las partes aéreas Momordica charantia (E. EtOH.Mc.PA) ........................................................................ 37 Evaluación de la Capacidad antioxidante por los métodos de DPPH y ABTS… ................................................................................................... 41. 7. RESULTADOS Y ANÁLISIS ..................................................................... 45 7.1 Marcha fitoquímica preliminar (MFP) .............................................. 45 7.2 Metabolitos secundarios aislados ................................................... 47 Composición de la mezcla McPA1 ............................................... 47 Composición de la mezcla McPA2 ............................................... 54 Composición de la mezcla McPA3 ............................................... 58 Composición de la mezcla McPA4 ............................................... 64 Elucidación estructural del compuesto McPA5 ............................. 68 Elucidación estructural del compuesto McPA6 ............................. 73 7.3 Evaluación de la capacidad antioxidante ........................................ 78 Curva de calibración para el ensayo DPPH .................................. 78 Cuantificación de la capacidad captadora de radicales libres por DPPH …………………………………………………………………………..80 Estadística para el extracto, y las fracciones para determinar la capacidad antioxidante .............................................................................. 81 Curva de calibración para el ensayo ABTS .................................. 83 Cuantificación de la capacidad captadora de radicales libres ABT …………………………………………………………………………………….85 Estadística para el extracto, y las fracciones ................................ 86 Comparación entre el método de DPPH Y ABTS ......................... 88. 8. CONCLUSIONES ...................................................................................... 92. 9. RECOMENDACIONES.............................................................................. 94. 10. BIBLIOGRAFÍA...................................................................................... 95.
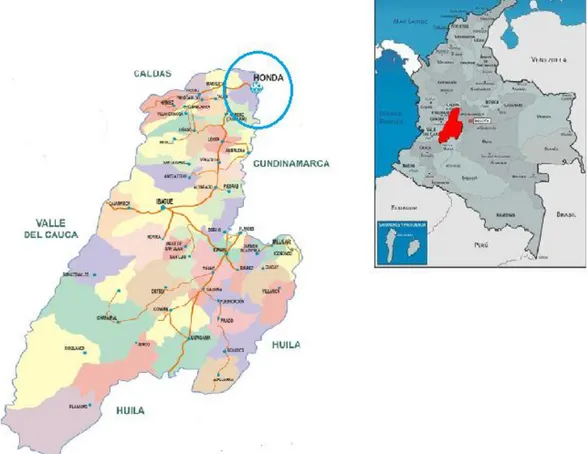
(6) INDICE DE FIGURAS. Figura 5-1 Características morfológicas de la familia Cucurbitaceae . .............. 8 Figura 5-2 Distribución de la familia Cucurbitaceae .......................................... 9 Figura 5-3 Estructuras identificadas en mono y sesquiterpenoides comunes en la familia Cucurbitaceae ................................................................................... 13 Figura 5-4 Ejemplos de triterpenoides de tipos oleanano y lupano comunes en la familia Cucurbitaceae ................................................................................... 14 Figura 5-5 Ejemplos de cucurbitacinas, triterpenóides típicos de la familia Cucurbitaceae .................................................................................................. 15 Figura 5-6 Morfología del género Momordica ................................................. 16 Figura 5-7 Distribución de especie Momordica ............................................... 17 Figura 5-8 Ejemplos de fitoesteroles comunes encontrados en el género Momordica........................................................................................................ 20 Figura 5-9 Ejemplos de triterpenóides encontrados en el género Momordica). ......................................................................................................................... 21 Figura 5-10 Triterpenóides tipo cucurbitanos encontrados en el género Momordica........................................................................................................ 22 Figura 5-11 Características morfológicas de la especie Momordica charantia A. Hojas, B. Flor, C. Frutos............................................................................... 24 Figura 5-12 Distribución de la especie Momordica charantia en el mundo 25 Figura 5-13 Distribución de la especie Momordica charantia en Colombia ..... 26 Figura 5-14 Compuestos químicos más representativos de la especie Momordica charantia ........................................................................................ 30 Figura 5-15 Reacción química del DPPH antes y después de reaccionar con un agente antioxidante. ......................................................................................... 32 Figura 5-16 Reacción química del ABTS antes y después de reaccionar con un compuesto antirradical (AOH) ......................................................................... 33 Figura 6-1 Mapa de localización del área de recolección de la especie Momordica charantia, Colombia (Tolima) municipio de honda. ........................ 36 Figura 6-2 Diagrama de la marcha Fitoquímica preliminar .............................. 37 Figura 6-3 Diagrama general del extracto y fracciones de partes aéreas de la especie Momordica charantia........................................................................... 38 Figura 6-4 Aislamiento y purificación de las mezclas y compuestos. .............. 40 Figura 6-5 Protocolo utilizado para el control de Trolox en los métodos de ABTS y DPPH .................................................................................................. 43 Figura 7-1 Corriente iónica total (TIC) de la mezcla McPA1 ............................ 48 Figura 7-2 (A) Espectro de masas para el compuesto con tiempo de retención 8.30 minutos de la mezcla McPA1. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 49 Figura 7-3 Posibles rutas de fragmentación propuesta para el Epoxylinalool . 50.
(7) Figura 7-4 (A) Espectro de masas para el compuesto con tiempo de retención 11.738 minutos de la mezcla McPA1. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 51 Figura 7-5 Posibles rutas de fragmentación propuesta para la Dihidroactinidiolida ........................................................................................... 51 Figura 7-6 (A) Espectro de masas para el compuesto con tiempo de retención 16.056 minutos de la mezcla McPA1. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 52 Figura 7-7 Posibles rutas de fragmentación propuesta para el Ácido palmítico ......................................................................................................................... 52 Figura 7-8 (A) Espectro de masas para el compuesto con tiempo de retención 23.372 minutos de la mezcla McPA1. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 53 Figura 7-9 Posibles rutas de fragmentación propuesta para el Escualeno ...... 54 Figura 7-10 Corriente iónica total (TIC) de la mezcla McPA2 .......................... 55 Figura 7-11 (A) Espectro de masas para el compuesto con tiempo de retención 13.855 minutos de la mezcla McPA2. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 56 Figura 7-12 Posibles rutas de fragmentación propuesta para 3-Hidroxi-5,6epoxy-beta-ionona............................................................................................ 56 Figura 7-13 (A) Espectro de masas para el compuesto con tiempo de retención 14.014 minutos de la mezcla McPA2. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 57 Figura 7-14 Posibles rutas de fragmentación propuesta para 2-Ciclohexen-1ona-4-hidroxi-3,5,6-trimetil-4-(3-oxo-1-butenil) ................................................. 58 Figura 7-15 Corriente iónica total (TIC) de la mezcla McPA3 .......................... 59 Figura 7-16 (A) Espectro de masas para el compuesto con tiempo de retención 8.415 minutos de la mezcla McPA3. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 60 Figura 7-17 Posibles rutas de fragmentación propuesta para el Ácido benzoico ......................................................................................................................... 60 Figura 7-18 (A) Espectro de masas para el compuesto con tiempo de retención 9.529 minutos de la mezcla McPA3. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 61 Figura 7-19 Posibles rutas de fragmentación propuesta para el indol ............. 61 Figura 7-20 (A) Espectro de masas para el compuesto con tiempo de retención 10.313 minutos de la mezcla McPA3. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 62 Figura 7-21 Posibles rutas de fragmentación propuesta para el óxido de linalool ......................................................................................................................... 63 Figura 7-22 (A) Espectro de masas para el compuesto con tiempo de retención 10.680 minutos de la mezcla McPA3. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 63.
(8) Figura 7-23 Posibles rutas de fragmentación propuesta para el Ácido cinámico ......................................................................................................................... 64 Figura 7-24 Corriente iónica total (TIC) de la mezcla McPA4 .......................... 65 Figura 7-25 (A) Espectro de masas para el compuesto con tiempo de retención 7.184 minutos de la mezcla McPA4. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 66 Figura 7-26 Posibles rutas de fragmentación propuesta para el Eucaliptol ..... 66 Figura 7-27 (A) Espectro de masas para el compuesto con tiempo de retención 8.415 minutos de la mezcla McPA4. (B) Espectro de masas reportado de la librería NIST08 ................................................................................................. 67 Figura 7-28 Posibles rutas de fragmentación propuesta para el Ácido propanoico, 2-metil-, 1-(1,1-dimetiletil)-2-metil-1,3-propanediol ester .............. 68 Figura 7-29 Espectro de RMN 1H (300 MHz, Metanol-d4) del compuesto McPA5 .............................................................................................................. 69 Figura 7-30 Espectro de RMN 13C J-MOD (75 MHz, Metanol-d4) del compuesto McPA5. ............................................................................................................. 70 Figura 7-31 Ampliación de espectro COSY en RMN para el compuesto McPA5. ......................................................................................................................... 71 Figura 7-32 Asignación de los desplazamientos químicos para el compuesto McPA5 .............................................................................................................. 71 Figura 7-33 Espectro de RMN 1H (300 MHz, Metanol-d4) del compuesto McPA6 .............................................................................................................. 74 Figura 7-34 Espectro de RMN 13C J-MOD (75 MHz, Metanol-d4) del compuesto McPA6 .............................................................................................................. 75 Figura 7-35 Ampliación de espectro COSY en RMN para el compuesto McPA6 ......................................................................................................................... 76 Figura 7-36 Asignación de los desplazamientos químicos para el compuesto McPA6 .............................................................................................................. 76.
(9) ÍNDICE DE TABLAS Tabla 5-1 Actividades biológicas de algunas especies vegetales de la familia Cucurbitaceae .................................................................................................. 10 Tabla 5-2 Actividades biológicas de algunas especies vegetales del género Momordica........................................................................................................ 18 Tabla 5-3 Clasificación taxonómica de Momordica charantia L. ...................... 23 Tabla 5-4 Estudios de algunas actividades farmacológicas en la especie Momordica charantia + ..................................................................................... 27 Tabla 7-1 Marcha fitoquímico preliminar del extracto etanólico de las partes aéreas de la especie Momordica charantia. ..................................................... 45 Tabla 7-2 Tiempos de retención y resultados de la comparación con la librería NIST 08 para la mezcla McPA1 ....................................................................... 48 Tabla 7-3 Tiempos de retención y resultados de la comparación con la librería NIST 08 para la mezcla McPA2 ....................................................................... 55 Tabla 7-4 Tiempos de retención y resultados de la comparación con la librería NIST 08 para la mezcla McPA3 ....................................................................... 59 Tabla 7-5 Tiempos de retención y resultados de la comparación con la librería NIST08 para la mezcla McPA4 ........................................................................ 65 Tabla 7-6 Comparación de los desplazamientos químicos del compuesto McPA5 con los de kaguasaponina D . .............................................................. 72 Tabla 7-7 Comparación de los desplazamientos químicos del compuesto McPA5 con los de Momordicina ll .................................................................... 77 Tabla 7-8 Promedio de absorbancias (n=3), %inhibición, IC50 de trolox......... 78 Tabla 7-9 Datos estadísticos para la sustancia patrón Trolox.......................... 79 Tabla 7-10 Lectura del extracto y las fracciones, a los 60 min transcurridos. .. 80 Tabla 7-11 Porcentaje de inhibición, datos estadísticos para el extracto y las fracciones por el método de DPPH .................................................................. 81 Tabla 7-12 Promedio de absorbancias (n=3), %inhibición, IC50 de trolox....... 84 Tabla 7-13 Datos estadísticos para la sustancia patrón Trolox........................ 85 Tabla 7-14 Lectura del extracto y las fracciones, a los 60 min transcurridos. .. 85 Tabla 7-15 % de inhibición por el método de ABTS para el extracto y las fracciones ......................................................................................................... 86 Tabla 7-16 Comparación del método DPPH Y ABTS a partir del IC50 para el extracto y fracciones ........................................................................................ 88. Índice de Gráficas Gráfica 7-1 Curva de calibración para trolox .......................................................... 79 Gráfica 7-2 % de Inhibición para el control positivo, extracto y fracciones ....... 83 Gráfica 7-3 Curva de calibración para Trolox......................................................... 84 Gráfica 7-4 % de Inhibición para el control positivo, extracto y fracciones ....... 88.
(10) LISTA DE ABREVIATURAS 2,2′-azino-bis-3-etilbenzotiazolin-6-. ABTS. Acido. AcOEt. sulfonico. AFP. Acetato de etilo. CC. Análisis fitoquímico preliminar. CCD. Cromatografía en Columna. CCDP. Cromatografía Capa Delgada. CF. Cromatografía en capa delgada preparativa. CG-EM. Cromatografía en columna flash Cromatografía. de. gases. acoplada. a. espectrometría de masas DCM. Diclorometano. DDPH. 1,1-difenil-2-pricril-hidrazilo. EM. Espectrometría de masas. EtOH. Etanol. E. EtOH.Mc.PA. Extracto etanólico de las partes aéreas de Momordica charantia. Fx.AcOEt.Mc.PA. Fracción de acetato de etilo de las partes aéreas de Momordica charantia. Fx.DCM.Mc.PA. Fracción de diclorometano de las partes aéreas de Momordica charantia. Fx.HEP.Mc.PA. Fracción de heptano de las partes aéreas de Momordica charantia. Fx.Hidroalc.Mc.PA Fracción hidroalcohólica de las partes aéreas de Momordica charantia HEP. Heptano. IC50. Concentración inhibitoria del 50%. MeOH. Metanol. MFP. Marcha Fitoquímica Preliminar. m.s.n.m. Metros sobre el nivel del mar. m/z. Relación masa carga. TIC. Corriente iónica total.
(11) 1. RESUMEN. La especie Momordica charantia L. perteneciente al género Momordica de la familia Cucurbitaceae conocida comúnmente como balsamina, bejuco de coje, subicogen, pepinillo y pepino cimarrón es una planta enredadera con fruto amargo; actualmente es utilizada como planta medicinal, reconocida por su actividad hipoglicemiante nativa de la región tropical, teniendo en cuenta la importancia de esta especie en la medicina tradicional ,este trabajo presenta la contribución al estudio químico y biológico de las partes aéreas de la especie Momordica charantia, haciendo una importante contribución a la familia Cucurbitaceae y en especial al género Momordica, ya que presenta pocos estudios en nuestro país. A partir del material vegetal colectado en el municipio de Honda (Tolima) e identificado en el herbario de la Universidad Nacional de Colombia bajo el número de colección COL 596915 se realizó la extracción mediante la técnica de maceración en frio con etanol al 96% obteniéndose 37.1 g (7.4 % p/p) de extracto total (E.EtOH.Mc.PA), donde mediante el estudio fitoquímico preliminar se determinó cualitativamente la presencia de diferentes metabolitos secundarios como: terpenos, taninos, glucósidos cardiotónicos y probablemente alcaloides siendo esto consecuente con estudios fitoquímicos realizados sobre diferentes especies del mismo género como Momordica balsamina (Mussa, 2006) o Momordica grosvenori (Takasaki et al., 2003). Para la determinación y caracterización química de los metabolitos secundarios de la especie vegetal Momordica charantia se realizó un fraccionamiento liquidoliquido continuo al extracto E.EtOH.Mc.PA con solventes de polaridad creciente, obteniendo las fracciones de heptano (Fx.Hept.Mc.PA 1.22%), diclorometano (Fx.DCM.Mc.PA 8.51%), acetato de etilo (Fx.AcOEt.Mc.PA 1.02%) y un residuo hidroalcohólico (Fx.Hidroalc.Mc.PA 89.25%); estas fracciones fueron sometidas a separaciones sucesivas y purificación utilizando técnicas de cromatografía, tales como cromatografía en capa delgada (CCD), cromatografía en capa delgada preparativa (CCDP) y cromatografía en columna (CC), permitiendo identificar dos compuestos denominados Kaguasaponina D y Momordicina ll , 1.
(12) cuatro mezclas de compuestos, la primera conformado por: un terpeno oxigenado Epoxylinalool, un norisoprenoides Dihidroactinidiolida, un ácido graso saturado el Ácido palmítico y un triterpeno alifático identificado como Escualeno, en la segunda mezcla se encontró: un terpenoide biciclico (3-Hidroxi-5,6-epoxybeta-ionona y un norisoprenoide 2-Ciclohexen-1-ona-4-hidroxi-3,5,6-trimetil-4(3-oxo-1-butenil), en la tercer mezcla se encontró: un terpeno oxigenado el Oxido de linalool, dos compuestos fenólicos Ácido cinámico y Ácido benzoico, un compuesto heterocíclico Indol y por ultimo para la cuarta mezcla se encontró un terpeno oxigenado Eucaliptol y un ácido esterificado (ácido propanoico, 2-metil-, 1-(1,1-dimetiletil)-2-metil-1,3-propanediol ester.La identificación de las mezclas obtenidas se realizó mediante la técnica de Cromatografía de gases acoplada a espectrometría de masas, realizando la comparación de los datos con los reportados en la librería NIST08.. La determinación de la capacidad antioxidante se realizó mediante dos métodos por DPPH y ABTS, donde presento efecto inhibitorio al 50% en concentraciones superiores a 1000 ppm, para el extracto total con un IC50 de 5734.1ppm, las fracciones de acetato de etilo con un IC50 de 6178ppm y el residuo hidroalcohólico con IC50 de 7251.8 ppm, por el método del radical DPPH. A diferencia por el método desarrollado ABTS el extracto etanolico presento un IC50 de 5513 ppm para las fracciones de heptano con un IC50 de 5578ppm , la fracción de acetato de etilo con un IC50 de 4282.9ppm y un residuo hidroalcohólico con un IC50 de 4375.2ppm, tomando como referencia la captación antioxidante del trolox como radical libre para ambos métodos, permitiendo establecer así la baja capacidad antioxidante que poseen las partes aéreas de la especie vegetal Momordica charantia debido a las altas concentraciones en que inhibe el radical.. 2.
(13) 2. INTRODUCCIÓN. Colombia ocupa el 0,22 % de la superficie terrestre y alberga cerca del 10% de la biodiversidad del planeta con aproximadamente 28.800 especies catalogado a nivel mundial, como territorio megadiverso dentro del grupo de los 14 con mayor índice de biodiversidad en la tierra (Andrade, 2011) utilizando estas especies con fines medicinales y etnobotánicos. A esta alta diversidad biológica subyacen factores, climáticos, ecológicos, geográficos y evolutivos, cuya interacción resulta en un mosaico de ecosistemas, procesos y especies (Ministerio de ambiente y desarrollo sostenible,2014).. Destacando la diversidad de especies presentes en el país algunos estudios han servido como modelos para la preparación de sustancias bioactivas, siendo materia prima para la síntesis de sustancias de interés farmacológico y/o interés industrial, realizando acciones útiles para la salud en procesos patológicos (Gutiérrez R. y Estévez B.,2009).. En la familia Cucurbitaceae se ha encontrado reportes acerca de la composición química y estudios farmacológicos de varias especies como, por ejemplo, especies del género Cucumis y Cucúrbita que presentan actividades biológicas como antiinflamatoria, antimicrobiana anticancerígena y antioxidante (Pozner, 2010; Mussa, 2006). Actualmente Momordica charantia ha tenido diferentes estudios preclínicos documentando los efectos antidiabéticos e hipoglucémicos a través de diversos mecanismos postulados y por lo que ha sido de gran ayuda en la medicina (Villareal et al., 2015).. De acuerdo con lo descrito anteriormente, el presente trabajo de investigación realiza un aporte al conocimiento químico y biológico de la familia Cucurbitaceae en Colombia, por medio del estudio químico de sus metabolitos fijos y la evaluación de la capacidad antioxidante de sus extractos y fracciones obtenidos de las partes aéreas de Momordica charantia L.. 3.
(14) 3. JUSTIFICACIÓN. En el planeta solo se ha estudiado una pequeña fracción de la flora en pro de la salud humana y animal. Se calcula que un 80% del cuidado primario de la salud en la población de los países en desarrollo depende de la medicina tradicional basada en medicamentos provenientes de plantas y animales (Rodríguez, 2003). Así mismo una sola planta puede presentar miles de metabolitos secundarios diferentes que pueden ser de gran importancia para el desarrollo de productos naturales que combatan diferentes enfermedades en el mundo (Hostettmann Gupta, & Mutis de Serna, 2008).. Colombia al ocupar el segundo lugar con mayor biodiversidad, se constituye como un gran potencial a estudiar, en especial por sus condiciones ambientales en las diversas regiones, lo cual puede representar mayor variedad de compuestos en cuanto a su composición química y actividad biológica (Hostettmann Gupta, & Mutis de Serna, 2008). Por lo anterior, el efecto que han tomado las plantas medicinales y los compuestos presentes en ellas en los últimos años ha sido un nuevo auge para varias investigaciones y estudios que se han expuesto con el fin de mantener viva la tradición herbolaria, encontrando nuevos compuestos activos con diferentes propiedades que actúan contra enfermedades, para el uso en la medicina moderna.. En las últimas décadas se ha generado gran interés en los antioxidantes naturales presentes en las plantas ya que el estrés oxidativo (un desequilibrio entre las sustancias oxidantes y prooxidantes) ha implicado grandes afecciones en la salud. Científicamente se ha demostrado que el daño oxidativo ocasionado por los radicales libres está relacionado con un amplio número de enfermedades y desordenes que incluye: fallo cardíaco, daños celébrales, cataratas, inflamaciones, entre otros (Youngson, 2005). Al contar con un recurso tan amplio como la biodiversidad en nuestro país, se ha permitido realizar el estudio fitoquímico de diferentes especies vegetales. Una de las familias vegetales que se encuentra ampliamente distribuida es la familia Cucurbitaceae, constituye una fuente importante de especies como Cucurbita mostacho, Sechium edule que según estudios reportados en la literatura posee un elevado potencial 4.
(15) antioxidante y otras especies como Cucumis anguria y. Melothria guadalu. presentan actividad antiinflamoria y antimicrobiana (Carlos, 2014) a esta familia también pertenece. la especie vegetal Momordica charantia conocida. comúnmente en las regiones tropicales de Colombia como ¨balsamina¨ se han reportado en los frutos y semillas efectos como febrífugo, dolencias hepáticas, cálculos renales, afecciones de piel, ulceras, quemaduras por contenido de carotenos, además se usa contra el raquitismo y la xeroftalmia (Arango,2006), de acuerdo con estudios realizados puede ser atribuida la capacidad antioxidante. a. compuestos. fenólicos. considerados. marcadores. quimiotaxonómicos de esta familia (Fonnegra & Jiménez, 2007). En la especie Momordica charantia no se tiene antecedentes científicos nacionales que comprueben su propiedad antioxidante y su composición; por esta razón se hace meritorio realizar este estudio contribuyendo de manera importante al conocimiento químico y biológico de esta especie.. 5.
(16) 4 4.1. OBJETIVOS. OBJETIVO GENERAL. Contribuir al estudio químico de las partes aéreas de Momordica charantia L. (Cucurbitaceae) y evaluar su capacidad antioxidante.. 4.2. OBJETIVOS ESPECÍFICOS. Obtener extractos y fracciones de distintas polaridades provenientes de la especie Momordica charantia L. Aislar, purificar y elucidar la estructura química de los metabolitos secundarios mayoritarios presentes en los extractos o fracciones de las partes aéreas de Momordica charantia L. Evaluar la capacidad antioxidante de los extractos y fracciones obtenidos de las partes aéreas de la especie Momordica charantia L.. 6.
(17) PLANTEAMIENTO DEL PROBLEMA En la actualidad el uso de plantas para tratar ciertas enfermedades es bastante reconocida debido a los metabolitos secundarios que posee, por lo que han sido estudiados para aplicarlos en la industria farmacológica en beneficio de la población mundial (Aldana, 2010). Teniendo en cuenta la diversidad vegetal de Colombia es importante hacer el reconocimiento de algunas especies como lo son de la familia Cucurbitaceae que. su. estudio ha sido basado. en la. alimentación balanceada del ser humano y aunque otras de las especies de esta familia hacen parte del estudio en la medicina hace falta contribuir. en el. conocimiento de plantas como Momordica charantia que se ha utilizado como hipoglicemiante y que tiene cantidades de beneficios pero no se han hecho estudios recientes , es por esto que se hace necesario realizar estudios sobre capacidad antioxidante además de la extracción y purificación de metabolitos que pueden llegar a ser importantes para futuras investigaciones en la evaluación de otras actividades biológicas.. 4.3. FÓRMULACIÓN DEL PROBLEMA. ¿Cuál es la composición química de las partes aéreas de Momordica charantia L. y presentan sus extractos y fracciones capacidad antioxidante?. 7.
(18) 5. 5.1. ESTADO ACTUAL DEL TEMA. FAMILIA CUCURBITACEAE. Características generales de la familia Cucurbitaceae La familia Cucurbitaceae se encuentra constituida por 118 géneros y 845 especies distribuidas en el trópico con algunas especies semidesérticas (Stevens, 2009). Esta familia se divide en dos subfamilias: Zanonioideae y Cucurbitoideae generalmente son plantas herbáceas y trepadoras que crecen rápidamente, un gran número de especies en esta familia son utilizadas en la alimentación balanceada del ser humano y animal (Deyo & Malley, 2008).. Características morfológicas de la familia Cucurbitaceae Son plantas típicamente trepadoras (zarcillos) con gruesos rizomas tuberosos, leñosas en la base, sus hojas palmeado-lobuladas, sin estípulas con nectarios extraflorales. Las flores usualmente son unisexuales y regulares monoicas o dioicas, epíginas. Las semillas se pueden encontrar grandes, aplanadas, sin endosperma, cotiledones muy desarrollados y con reservas oleaginosas. El fruto es alargado y rugoso, la mayoría de miembros tienen como característica en su estructura haces vasculares bicolaterales. (Trease & Evans, 2002; Facena, s.f). En la Figura 5-1 se observan algunas características morfológicas descritas anteriormente.. Figura 5-1 Características morfológicas de la familia Cucurbitaceae (Castroviejo et.al, 2005). 8.
(19) Distribución de la familia Cucurbitaceae La familia Cucurbitaceae constituye una variedad de géneros y especies anteriormente mencionado presentándose en distintas zonas continentales. Las plantas se encuentran distribuidas en regiones tropicales y subtropicales de ambos hemisferios, en todo el mundo (Bolaños, 1998). Se desarrollan entre los 50-1500 m.s.n.m, ocupando áreas de bosques siempre verdes, caducifolios, márgenes de ríos, matorrales, sabanas, alrededor de asentamientos humanos y áreas de cultivo (Facena, s.f). Las especies de la familia Cucurbitaceae se encuentran principalmente en, África, sur de Asia, norte de Australia, y en el centro y sur de América como se puede observar en el mapa de la Figura 5-2.. Las Cucurbitáceas en los antecedentes botánicos favorecen el origen sur y centro americano y en los países que más han sido cultivados son (México, Colombia y Guatemala) debido a su gran importancia en la alimentación. En Colombia la distribución de esta familia se centra en las zonas de Sierra nevada, Santa Marta, Costa Atlántica, Antioquia y algunas zonas de la cordillera de los andes (Patiño, 2002).. Figura 5-2 Distribución de la familia Cucurbitaceae (tropicos.org, s.f). *Las zonas de color amarillo corresponden a la distribución de la familia Cucurbitaceae. Usos etnobotánicos de la familia Cucurbitaceae 9.
(20) Diversas especies de la familia Cucurbitaceae son empleadas con fines curativos tradicionales Cayaponia racemosa, Citrullus lanatus, Cucumis sativus, Cucurbita moschata, Gurania spinulosa, Luffa cylindrica, L. sepium, Momordica charantia y Rytidostylis carthagenensis, por sus potenciales propiedades antiálgicas, antiflatulentas, antiinflamatorias, catárticas, febrífugas, otálgicas y vermífugas (Delascio & López, 2007). Como plantas alimenticias o comestibles, bajo la forma de frutas frescas, cocidas, ensaladas, jugos, dulces, arilos y semillas son consumidas Citrullus lanatus, Cucumis anguria, C. melo, Cucurbita sativus, Cucurbita moschata, Cucurbita pepo y Momordica charantia. Incluye además especies con valor alimenticio potencial que a partir de los años 60 se ha esforzado para producir variedades comerciales de las Cucurbitáceas con tolerancia y resistencia a las virosis más comunes y destructivas, ensayando con métodos tradicionales para el mejoramiento genético (Bolaños, 1998).. Actividades biológicas evaluadas en especies de la Familia Cucurbitaceae. Los estudios realizados sobre actividades biológicas en especies de la familia Cucurbitaceae son amplios debido a su distribución geográfica. Dentro de las diversas actividades biológicas evaluadas a extractos y compuestos aislados de especies pertenecientes a esta familia se encuentran reportes de actividad antiinflamatoria, antioxidante, antimicrobiana, antidiabética, y antiandrogénica (Pozner, 2010; Mussa, 2006). En la Tabla 5-1, se ilustran algunos estudios biológicos realizados en especies de la familia Cucurbitaceae.. Tabla 5-1 Actividades biológicas de algunas especies vegetales de la familia Cucurbitaceae Órgano de Especie. la planta o extracto. Actividad/caracterización biológica. evaluado. 10. Referencia.
(21) Cucurbita. Semillas. Actividad Antiandrogénica. pepo L. Bellma A et al., 2006. Cucurbita. Extractos. mostacho. vegetales. Cucumis. Fruta. Actividad Antioxidante. Gutiérrez. et. al., 2007 Actividad Antimicrobiana. anguria. Kumar. &. kamaraj., 2011. Melothria. Tallos y fruta. Actividad Antiinflamatoria. guadalu. Mohamed, Polo. &. Martinez, s. f Sechium. Hojas. edule. semillas. y. Actividad Antioxidante. Ordoñez, Gómez. &. Vattuone, 2006 Ecballium. Extractos. Actividad. Attard,. elaterium. vegetales. inmunomoduladora. Brincat,. &. Cuschieri, 2005 Cucúrbita aff. Semillas. Actividad Vermífuga. máxima. Avila. &. Vásquez, 2011. Lagenaria. Fruta. siceraria Momordica. Fruta. Caracterización. Yetisir, Sakar,. Germoplasma. & Serçe, 2008. Actividad Anti carcinogénica. Takasaki. grosvenori.. al., 2003. 11. et.
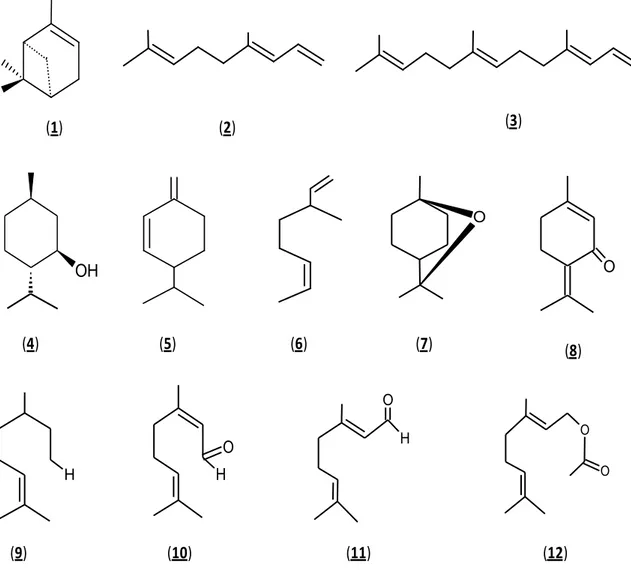
(22) Momordica. Semillas. charantia l. frutos. y. Actividad Anti-diabética. Raman. &. Lau,1996. Estudios Químicos de la familia Cucurbitaceae. De los estudios fitoquímicos realizados sobre las especies de la familia Cucurbitaceae en general se han reportado triterpenoides tetracíclicos oxigenados denominados cucurbitacinas, con efecto purgante y sabor amargo, autores como Takabayashi et al., 1994, reportan en la familia Cucurbitaceae que algunas especies al estar infestadas por arácnidos, elevando los niveles de βocimeno de monoterpenos 4,8-dimetil-1,3E,7-nonatrieno a 25 y 54%, respectivamente, de los compuestos volátiles totales en libertad. Mientras el βocimeno (6) es particularmente un monoterpeno típico en la familia Cucurbitaceae,. el. monoterpeno. 4,8-dimetil-1,3E,7-nonatrieno. (2). y. el. sesquiterpeno 4,8,12-trimetil-1,3E,7E,11-tridecatetraeno (3) es común en muchas especies de diversas familias (Loughrin JH et. al,1994). En esta familia se han identificado los siguientes compuestos químicos: α-pineno (1), βfelandreno (5), (-)-mentol (4) ,1,8-cineol (7), piperitona (8), citronelal (9) ,neral (z-citral) (10), geranial (E-citral) (11), acetato de geranilo (12).. 12.
(23) (1). (3). (2). O. O. OH. (4). (5). (6). (7). (8). O. O. H. H. (9). O. H. O. (10). (11). (12). Figura 5-3 Estructuras identificadas en mono y sesquiterpenoides comunes en la familia Cucurbitaceae (Mussa, 2006). Los compuestos de lupeol (17) y β-amirina (13) cuyos esqueletos de tipo Lupano y oleanano respectivamente se observan en la Figura 5-4, siendo otros alcoholes triterpenoides muy comunes en el reino vegetal. El lupeol actúa a través de un mecanismo diferente en acción de la aspirina y por lo tanto no inhibe la actividad de la ciclooxigenasa y la prostaglandina (Kweifio-Okai et.al ,1955). La actividad citotóxica de triterpenoides pentacíclicos también ha sido demostrada por el ácido Ursólico (16) y el ácido Oleanólico (15). Otros triterpenoides comunes en la familia Cucurbitaceae son: α-amirina (14), Betulinol (18), ácido betulinico (19), y acido 3-acetilbetunilico (20).. 13.
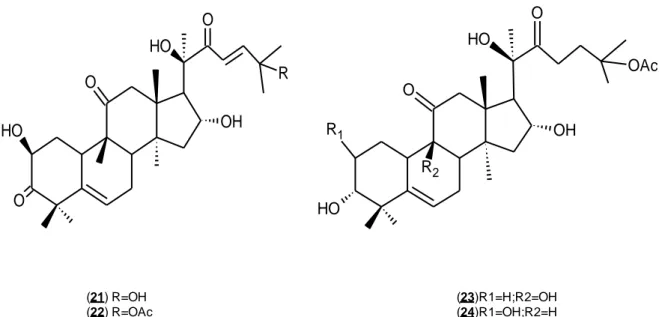
(24) R3. R2. R2. R1. HO. R1. (13) R1=CH3;R2=H;R3=CH3 β-amirina (14) R1=CH3;R2= CH3;R3=H αamirina (15) R1=CO2H; R2=H;R3=CH3 Ac. Oleanólico (16) R1= CO2H; R2= CH3;R3=H Ac. Ursólico. (17) R1=OH; R2=CH3 Lupeol (18) R1=OH; R2= CH2O H Betulinol (19) R1=OH; R2=CO2H Ac. Betulínico (20) R1= OAc; R2= CO2H Ac. 3acetilbetulínico. Figura 5-4 Ejemplos de triterpenoides de tipos oleanano y lupano comunes en la familia Cucurbitaceae (Gershenson & Croteau ,1991; Faldt, 2000). Las cucurbitacinas son derivados bioactivos de triterpenoides tetracíclicos se producen principalmente en la familia Cucurbitaceae (Halaweish, Tallamy & Santana,1999) son conocidos por ser extremadamente amargos, por su alta toxicidad a la mayoría de los organismos (incluyendo seres humanos) y participan directa o indirectamente en los procedimientos de defensa contra las plantas (Miró,1995). Existen una variedad de cucurbitacinas que difieren en cuanto a la aparición de ciertos tipos de ligandos y la presencia de dobles enlaces en ciertas posiciones encontrando los siguientes: cucurbitacina D ó 2β,16α,20β,25-tetra-hidroxicucurbita-5,23-dien-3,11,22-triona. (21). ,. cucurbitacina B ó 2β,16α,20β-trihidroxi-25-acetocucurbita-5,23-dien-3,11,22triona. (22),. di-hidrocucurbitacina. C. ó. 3β,16α,19,20β-tetra-hidroxi-25-. acetocucurbita-5-en-11,22-diona (23) y di-hidrocucurbitacina Q1 ó 3β,3α,20βtetra-hidroxi-25-acetocucurbita-5-en-11,22-diona (24) (Afifi et.al ,1999).. 14.
(25) O. O HO. HO O. OH. HO. OAc. R. O. R1. OH R2. O. HO. (21) R=OH (22) R=OAc. (23)R1=H;R2=OH (24)R1=OH;R2=H. Figura 5-5 Ejemplos de cucurbitacinas, triterpenóides típicos de la familia Cucurbitaceae (Mussa, 2006).. 5.2. Género Momordica. Características morfológicas del género Momordica El género Momordica posee alrededor de 59 especies, en ambientes cálidos y en áreas húmedas. Este género cubre una amplia variedad de plantas silvestres de gran importancia por su funcionalidad en ecosistemas y aplicaciones terapéuticas de igual manera, incluye a la mayoría de vegetales de la familia Cucurbitaceae que se utilizan como alimento (Assubaie & Garawany, 2004).. Las semillas de este género son planas, gruesas sobre la superficie, contiene márgenes afiladas y gruesas en los lados, ampliamente rectangulares, sin distinción entre los extremos con micropilares, esculpidos. Los frutos son pequeños, distantemente blandos, sin protuberancias o crestas, aunque las especies monóicas anuales (M. balsamina y M. charantia) comparten más características morfológicas a diferencia de otras especies. Una característica especifica es el sujetador de la flor macho se encuentra en la base cerca del eje o por debajo del centro del tallo de la flor en M. charantia. Mientras que en M. balsamina se sitúa en el medio superior o hacia la punta del pedúnculo. Los filamentos de anteras se fusionan para dar una apariencia globosa como lo es la 15.
(26) especie M. charantia, mientras que en la otra especie se divide en lóbulos (Bharathi & Jhon, 2013). En la figura 5-6 se presenta la morfología del género Momordica. ores nacen arracimadas en as a i as de os ta os. tallo robusto. Frutos son bayas lisas y globulares. Hojas palmadas y lobuladas. raíz cónica y ramificada. Figura 5-6 Morfología del género Momordica (Poisoner’s, 2018). Distribución del género Momordica Las especies del género Momordica se distribuyen en su mayoría en África tropical, Sudáfrica, Asia, India y algunas en sur América. Principalmente como vegetal están en Gabón, Sudán, y Malawi otras zonas principales donde se encuentran son en Ghana, Kenia, Uganda y Tanzania. La mayoría de los cultivos utilizados en África oriental son importados de países asiáticos. En la actualidad, los criadores de este género se están concentrando en los híbridos y las ventajas de obtener un mayor potencial de rendimiento teniendo una mejor resistencia a una proporción alta de plagas, enfermedades y al grado de amargura (Grubben & Denton, 2004), la distribución del género Momordica se observa en la Figura 5-7.. 16.
(27) Figura 5-7 Distribución de especie Momordica (tropicos.org, s.f). *Las zonas de color amarillo corresponden a la distribución del género Momordica. Usos etnobotánicos del género Momordica Las especies del género Momordica se han utilizado como un purgante drástico incluso hasta tóxico, pero en algunas zonas de distintos continentes los frutos son tradicionalmente comestibles. Las hojas de algunas especies en este género se recogen de la naturaleza y se comen después de hervir por lo general en tiempos de escasez. Las plantas son pastoreadas por el ganado en Sudán, y las hojas se usan como forraje (Kenia, Tanzania). Según la literatura botánica, en la medicina se usa popularmente contra problemas de la piel y parásitos externos, como sarnas y granos también para expulsar parásitos estomacales e intestinales (Grubben & Denton, 2004).. Actividades biológicas en especies del género Momordica. En cuanto a los estudios de la actividad biológica en el género Momordica la literatura reporta principalmente actividades como Antihiperglucemica y Antidiabética como es el caso de la especie Momordica cymbalaria (Rao, Kesavulu & Apparao, 2001). Se reporta en otras especies estudios como Hipoglicemiante, Antioxidante, Anticancerígena y Antiinflamatoria (Maulide, 2012). En la Tabla 5-2, se observa algunos estudios biológicos realizados en especies del género Momordica. 17.
(28) Tabla 5-2 Actividades biológicas de algunas especies vegetales del género Momordica. Órgano de Especie. la planta o extracto. Actividad/caracterización biológica. evaluado Momordica. Semillas. balsamina. Referencia. Actividad. Antiinflamatoria. Actividad. Antiemética. Actividad. Antioxidante. Actividad. Antimicrobiana. Maulide,2012 Mussa,2006 Bot. Propiedades anti-VIH. al.,2006. et. Momordica. Extractos. Actividad. antiovulatoria. Rao,. cymbalaria. vegetales. Actividad. aantidiabética. Kesavulu. Actividad. hipolipidemica. Apparao,. Actividad. &. 2001. antihiperglucémica Momordica. Extractos. grosvenori. vegetales. Actividad anticarcinogénica Actividad antinflamatoria. Takasaki et.al. 2003. Di, Huang y Ho, 2011. Momordica cochinchinen sis. Fruta Semillas Semillas. y. Actividad. Antioxidante. Kubola. &. Actividad. Siriamornpu ,. inmunomoduladora. 2011. Actividad antinflamatoria. Tsoi, NG & Fong, 2006 Jung 2013. 18. et.al.
(29) Momordica foetida. Extracto. Actividad Antipalúdica. Waako. acuoso de. et. al.,2005. la planta. Momordica. Semillas. charantia l. frutos. y. Actividad Antidiabética. Raman. &. Lau, 1996. Estudios químicos del género Momordica Se ha realizado algunos estudios preliminares fitoquímicos, sobre algunas especies de Momordica con el fin de caracterizar algunos metabolitos secundarios determinando su potencial biológico. En el que se atribuye la composición en flavonoides y taninos para propiedades antioxidantes antiinflamatorias antialérgicas y anticancerígenas. Por su contenido en triterpenos, como la momordicina propiedades antioxidantes, antiinflamatorias y vasodilatadoras se encuentra el B-sitoesterol (30), estigmastanol (33) y campesterol (32). Los esteroides también hacen parte de este género el cual se le comprenden una estructura similar a la de triterpenoides, que consta de un sistema de anillo tetracíclico típico (Halaweish, Tallamy & Santana,1999). Los fitoesteroles al tener de 27 a 32 átomos de carbono tienen un grupo hidroxilo en la posición C-3, dos grupos metilos en las posiciones C-10 y C-13 y una cadena lateral de alquilo en la posición C-17 (Novotný, Vachalkova, & Biggs, 2001).También pueden producirse en forma de ésteres y ácidos grasos, por ejemplo, el linoleato de β-sitosterilo (36), E β-sitosterol es el fitosterol más abundante en las plantas como se ilustra en la Figura 5-8. Mientras que a los alcaloides. y. resinas. se. les. atribuyen. propiedades. antimicrobianas. antiinflamatorias, antisépticas y antiinfecciosas. Los glucósidos juegan un papel importante en el tratamiento de la insuficiencia cardíaca, (Mussa, 2006; Thakur et al., 2009). Encontrando así los siguientes compuestos: Colestano (25), ergostano. (26),. estigmastano. (27),. colesterol. (28),. campesterol. (29),. Momordeno ó 3β-hidroxi-estigmasta-5,14-dien-16-ona (31), Espinasterol ó Estigmasta-7,22-dien-3β-ol (34), Estigmasterol (35). 19.
(30) R. R. (25) R=H colestano (26) R=Me ergostano (27) R=Et estigmastano. (28) R=H colesterol (29) R=Me campesterol (30) R=Et sitosterol. HO. R. O. HO. (32)R=Me campesterol (33)R=Et sitostanol o estigmastanol. HO. (31). HO. HO. (34). (35). O H3C. (CH 2)4. (CH 2)7. O. (36) Figura 5-8 Ejemplos de fitoesteroles comunes encontrados en el género Momordica (Mussa, 2006).. 20.
(31) Sin especificar las cantidades y composiciones, algunos estudios publicados muestran que diferentes partes del género Momordica contienen una resina, algunas saponinas y ciertos alcaloides, además de metabolitos tipo triterpenoide como la momordicina en mayor cantidad, el momordol un alcohol triterpenoide monocíclico, y un grupo de triterpenóides tipo pentacíclicos, que comprende momordicina, momordicinina y momordicilina (Figura 5-9) en algunas especies del género Momordica (Begum et.al 1997; Mussa, 2006). Por su amplia variedad se deduce que la diversidad estructural de triterpenoides está relacionada con funciones fisiológicas en lo que estos compuestos son sintetizados por especies, encontramos algunas como : Momordicina ó 13-hidroxi-28-metoxi-urs-11-en-3ona (37), Momordicilina ó 24-(1´-hidroxi-1´-metil-2-penteniloxil)- ursan -3-ona (38) , Momordicina ó 13β,28-epoxi-urs-11-en-3-ona (39) y Momordol ó 1-hidroxi1,2-dimetil-2-(8´,10´-dihidroxi-4´7´-dimetil-11´-hidroximetil-trideca)-3etilciclohex5-en-4-ona (40) .. HO COCH 3. OH. O. O. O. (37). C. CH. CH. CH2 CH3. (38) O. O OH. HO. O. OH. CH2OH. (40). (39). Figura 5-9 Ejemplos de triterpenóides encontrados en el género Momordica (Mussa, 2006).. 21.
(32) Los cucurbitanos constituyen un grupo de triterpenoides tetracíclicos típico de las especies en la familia Cucurbitaceae, especialmente actúan en la actividad biológica antitumoral (Akihisa, Yasukawa, & Tokuda, 2003). En general, el cucurbitano tipo triterpenoide tiene un esqueleto compuesto de un núcleo tetracíclico similar al de esteroides (1,2-ciclopentano-perhidrofenantreno, designados gonano o esterano) y sustituido por dos grupos metilos en el C-4 de posición de otros grupos metilos en las posiciones C-9, C-13 y C-14 cadena lateral alquilo en C-17 como se observa en la Figura 5-10. A continuación las estructuras de los siguientes compuestos químicos encontrados en el género Momordica:. 3β,7β,23α-trihidroxicucurbita-5,24-dien-19-al. (41),. 3β,7β,25-. 3β,7β –trihidroxi-25-metoxicucurbita-. trihidroxicucurbita-5,23-dien-19-al (42),. 5,23-dien-19-al (43) , 3β-hidroxi-7β,25-dimetoxicucurbita-5,23-dien-19-al (44) ,3β-dihidroxi-7β-metoxicucurbita-5,23,25-trien-19-al (45) (Miró ,1995).. OR2. OH H. H. H. CHO. H CHO. HO. HO. OH. OR1. (42)R1=H ; R2=H (43)R1=H ; R2=Me (44)R1=Me ; R2=Me. (41). H. H CHO. HO OMe (45). Figura 5-10 Triterpenóides tipo cucurbitanos encontrados en el género Momordica (Mussa, 2006).. 22.
(33) 5.3. Especie Momordica Charantia L.. Características morfológicas de la especie Momordica charantia L. La especie Momordica charantia L. es una planta tipo enredadera, herbácea anual, es conocida como karela en India, melón amargo (por el sabor amargo de todas sus partes) o Cundeamor en sur América. En Colombia se reconoce por sus nombres comunes balsamina, bejuco de coje, subicogen, pepinillo, pepino cimarrón (Vademecum Colombiano de Plantas Medicinales, 2008) y en el Valle del Cauca, como comidita de culebra. En la tabla 5-3 se presenta la descripción taxonómica de la especie Momordica charantia tomado de (http://www.cabi.org, 2016).. Tabla 5-3 Clasificación taxonómica de Momordica charantia L.. Reino. Vegetal. División. Magnoliofita. Clase. Dicotiledónea. Orden. Violales. Familia. Cucurbitaceae. Genero. Momordica. Especie. Momordica Linn. 23. Charantia.
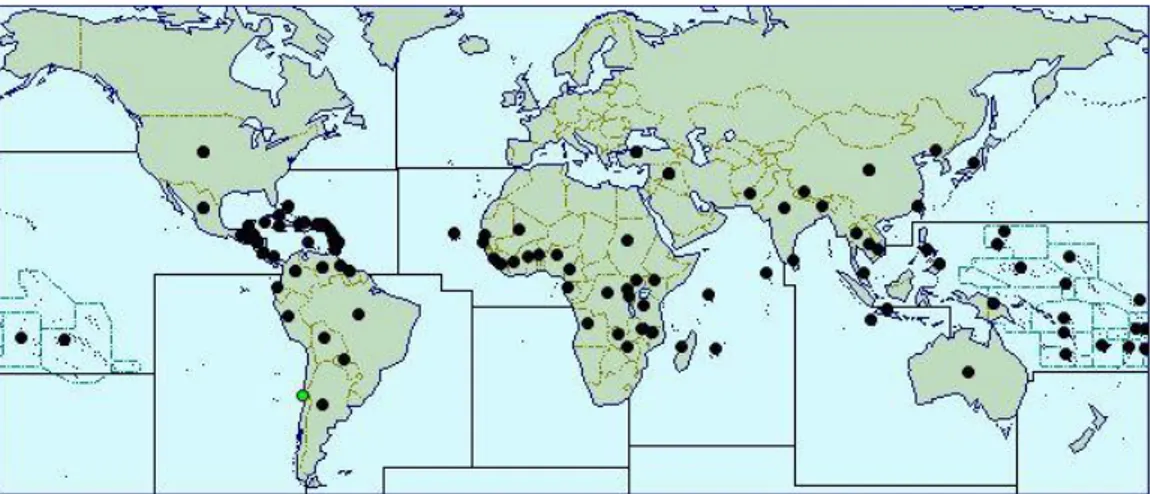
(34) Esta especie se caracteriza por ser bastante ramificada con tallo provisto de zarcillos. Las hojas son lobadas (cinco a siete lóbulos de 3-6 cm ovadooblongos), alternas, membranosas, lisas y aterciopeladas por debajo de la nerviación (Lima, 2008). Las flores son amarillas, axilares, solitarias, pedunculadas y unisexuales; tiene corola de cinco pétalos acompañadas de una gran bráctea. Su fruto es cilíndrico- alargado de aproximadamente 2-3 cm el cual es verde cuando está creciendo y al madurar adquiere una coloración naranja. En la Figura 5-11 Se ilustra un ejemplo de las características morfológicas de la especie Momordica charantia L.. B. A. C Fruto ovoide, color amarillo. Cinco a siete lóbulos oblongos. superficie cubierta por verrugas o tubérculos. lobado-palmadas. Membranosas lisas y aterciopeladas. amarillas, con corola de cinco pétalos y una gran bráctea. Semillas elípticas, planas, color rojizo. Figura 5-11 Características morfológicas de la especie Momordica charantia A. Hojas, B. Flor, C. Frutos (www.shutterstock.com,s.f).. Distribución de la especie Momordica charantia L. La especie Momordica charantia es originaria de China, India, Filipinas y Vietnam. Es un importante mercado de hortalizas en Asia meridional y oriental, y las poblaciones silvestres y cultivadas se puede encontrar en países como la India, Sri Lanka, Tailandia y Malasia, el sur de China y África tropical (Grubben, & Denton, 2004). Se cree que M. charantia se introdujo en América del oeste de África con el tráfico de esclavos. Momordica charantia se registró por primera vez en Puerto Rico en 1885 en el Herbario Nacional de los Estados Unidos (Grubben & Denton, 2004). Esta planta Ha sido usada tradicionalmente como planta medicinal en países como Brasil, Colombia, Haití, Nicaragua, México, Panamá, Perú, Ghana, India, China, Malasia, Nueva Zelanda y Cuba.. 24.
(35) Figura 5-12. Distribución de la especie Momordica charantia en el. mundo (http://www.cabi.org/,2016). *Los puntos negros corresponden a la distribución de la especie Momordica charantia en el mundo. En Colombia crece en los departamentos de Tolima, Magdalena, Antioquia, Bolívar, Santander, Valle del Cauca, entre otros como se puede observar en la Figura 5-13. En zonas de altitud entre 340 y 1000 m.s.n.m, se han registrado ejemplares en el Herbario Nacional Colombiano.. 25.
(36) Figura 5-13 Distribución de la especie Momordica charantia en Colombia (http://www.gifex.com,s.f). *Los puntos morados corresponden a la distribución de la especie Momordica charantia en Colombia. Usos etnobotánicos de la especie Momordica charantia L. Esta especie vegetal posee una larga tradición como planta antidiabética hasta el punto en que su extracto ha sido llamado "insulina vegeta ”. Recientemente, una proteína aislada de las semillas de Momordica, ha demostrado propiedades interesantes como antivírico y antineoplásico. En la medicina folklórica se atribuyen a esta planta multitud de aplicaciones: las hojas secas o la raíz pulverizada sirven para preparar una decocción que alivia las molestias de las hemorroides (aprendeenlinea.udea.edu.co, 2008). El jugo de los frutos se utiliza en la disentería y colitis crónica, mientras que la decocción de las semillas se emplea para las infecciones uretrales. También se dice que las semillas son vermífugas. Sin embargo, científicamente solo ha sido demostrados los efectos hipoglucémicos y antivíricos (Arango,2006). En algunos libros de plantas medicinales en Colombia se nombra esta especie como uso de emenagogo, febrífugo, dolencias hepáticas; también usado en emplastos y cataplasmas contra las hemorroides, afecciones cutáneas, prurito, aftas, afecciones de la piel y quemadura, antimicótico, antimicrobiano. en asma, bronquitis, estreñimiento, fiebre, resfrió, tos, cefalea, hipertensión cálculos renales, desordenes menstruales, afecciones de piel, ulceras, quemaduras (Arango,2006).. Actividad biológica de la especie Momordica Charantia L. A nivel de estudios de actividad biológica se ha demostrado que el extracto de la especie Momordica charantia presenta por electroforesis unas propiedades químicas similares a las de la insulina en algunos animales (Day et al.,1990). Otros hallazgos señalan que puede reducir la gluconeogénesis hepática, aumentar la síntesis hepática de glucógeno y aumentar la oxidación periférica de la glucosa en los eritrocitos y adipocitos, efectos todos ellos que contribuyen a 26.
(37) reducir los niveles de glucosa en sangre ( Basch, Gabardi & Ulbricht, 2003). Aunque esta especie presenta diferentes estudios a nivel internacional, como se describe en la Tabla 5-4 enfocados a la evaluación de diferentes actividades como: la antiinflamatoria, hipoglicemiante, antioxidante a nivel nacional los estudios de esta especie únicamente han sido orientados al establecimiento de parámetros de calidad y rango de variación en el material vegetal (Carlos, 2014).. Tabla 5-4 Estudios de algunas actividades farmacológicas en la especie Momordica charantia (Carlos, 2014).. Partes de la. Actividad. Tipo de. planta. Farmacológica. estudio. Todas las. Actividad. In vivo. partes (fruto,. hipoglicemiante. Referencia. Ali et al., 1993 Bailey, Turner & Leatherdale,. semillas, hojas). 1985 Çakici et al., 1994 Jayasooriya et al., 2000 Shibib, Khan & Rahman,1993 Sarkar, Pranava & Marita,1996. Suspensión de. Actividad. la pulpa del. hipoglicemiante. In vivo. Ahmad et al.,1999. fruto Extracto de. Actividad. Ensayo de. Omoregbe, Ikuebe &. hojas en agua,. Antibacterial. laboratorio. Ihimire,1996. metanol y. Ogata et al.,1991.. etanol). 27.
(38) Extracto de la. Actividad. Ensayo de. Yesilada, Gürbüz &. planta entera. Antimicrobiana. laboratorio. Shibata,1999. Extracto crudo y. Actividad. In vivo. Battelli et al.,1996. fracciones. Anticancerígena. In vitro. purificadas. Ganguly, De & Das,2000 Licastro et al., 1980 Ng et al., 1994 Sun et al., 2001. Extracto de la. Actividad. ensayo de. planta entera. Antiparasitaria. laboratorio. Extractos de. Actividad. In vitro. frutos en agua,. Hipoglicemiante. Khan & Omoloso,1998. Yadav et al., 2010. etanol, metanol cloroformo y hexano. Estudio químico de la especie Momordica Charantia L. La especie Momordica charantia L. cuenta con algunos estudios fitoquímicos reportando en general compuestos fenólicos (ácidos fenólicos), glicósidos triterpenicos, saponinas, glicósidos esteroidales adicionalmente se reportó la presencia de momordicosidos, momordicinas (i, ii y iii) y proteínas (Raman & lau, 1996). En partes de la planta más específicamente en raíces se han aislado algunos compuestos triterpenicos (Chen et al., 2008). En los frutos se han identificado triterpenos, alcaloides, fenoles, taninos, saponinas, además de terpenoides cucurbitanos, siendo coherentes con los reportes en la familia y genero dichos anteriormente (Yadav et al., 2010). Se encuentra los siguientes compuestos: Taiwacina A (46), Momordicosido K (47), Momordicosido L (48), Momordicina (49), Charantina (51), Kuguaglicosido G (54), Charantal (52), Charantin (50), Kuguacina A (53).. 28.
(39) CH3 H3C O CH3. O. O H. H. O OH. O. O. O. O. O. HO. O. OH HO. OH. OH. HO. OH. OH. OH. O. OH. OH. (46). (47). O O. H H. HO. O. H. OH O HO. (48). OH. HO. OH. OH OH. (49). OH OH. H H. H. CHO. HO. Glu. OH. H. O. (51). (50). OH. O H. H H Gl u. HO. O. (52). O. (53). 29.
(40) -. O Glu H H HO. O. Glu. (54). Figura 5-14 Compuestos químicos más representativos de la especie Momordica charantia (Lin, Yang & Lin C., 2011; Liu et al., 2010; Li et al., 2007; keller et al., 2011; Yuan, Gu & Tang, 2008; Chen et al., 2008). 5.4. Capacidad antioxidante. Los Antioxidantes son compuestos que pueden inhibir o retardar la oxidación de otras moléculas inhibiendo la iniciación y/o propagación de las reacciones en cadena de los radicales libres (Orjuela ,2015). La suplementación con antioxidantes está fundamentada en estudios epidemiológicos y clínicos que demuestran la estrecha relación entre factores como: dieta, estilo de vida, exposición a radiación, metales, pesticidas, tóxicos, y algunos medicamentos; con la aparición y desarrollo de enfermedades como cáncer, diabetes, aterosclerosis, desórdenes neurodegenerativos y envejecimiento. Todas estas condiciones patológicas están asociadas a un estado conocido como “estrés o idativo”, es decir, un aumento en as especies o idantes (principa mente Especies Reactivas del Oxígeno–EROs) y/o una disminución en los mecanismos de detoxificación de ellas. (Londoño, 2012).. Se encuentran dos categorías en los antioxidantes que son: sintéticos y naturales. En general los antioxidantes sintéticos son compuestos de estructuras fenólicas con varios grados de sustitución alquílica, mientras que los antioxidantes naturales pueden ser: compuestos fenólicos (tocoferoles, flavonoides y ácidos fenólicos), compuestos nitrogenados (alcaloides, derivados. 30.
(41) de la clorofila, aminoácidos y aminas) o carotenoides, así como el ácido ascórbico. Los antioxidantes sintéticos como el BHA y BHT (Butil – hidroxianisol y Butil - hidroxitolueno) han sido utilizados como antioxidantes desde principios del siglo pasado. Sin embargo, se han impuesto medidas de precaución y se ha restringido su uso debido a su carcinogenicidad (Londoño, 2012). Debido a esto, el interés por los antioxidantes naturales se ha incrementado considerablemente ya que la capacidad de actuar como antioxidante se ha demostrado en especial con los flavonoides, muestra un amplio rango de efectos biológicos incluyendo funciones. antibacteriales,. antivirales,. antiinflamatorias,. antialergénicas,. antitrombóticas y vasodilatadores. Una terapia antioxidante provee una alternativa barata para el tratamiento de enfermedades relacionadas con el estrés oxidativo ya que se ha demostrado el efecto antioxidante de productos naturales provenientes de las plantas (Orjuela, 2015).. Determinación de la capacidad antioxidante La manera más efectiva de evitar el daño producido por los radicales libres es su destrucción o estabilización por parte de antioxidantes, para medir esta capacidad existen diversos métodos entre ellos el ensayo de DPPH* y ABTS+•, el cual determinó la capacidad antioxidante de las fracciones y extractos donde se encuentran los respectivos metabolitos secundarios en las partes aéreas de la especie Momordica charantia basadas en: Método de 1,1-difenil-2-pricrilhidrazil (DPPH) El ensayo DPPH se basa en la estabilidad del radical 1,1-difenil-2-picrilhidrazil (DPPH) la cual se atribuye a la deslocalización del electrón desapareado, esta deslocalización también le otorga una coloración violeta caracterizada por una banda de absorción, en solución etanólica, centrada alrededor de 517 nm de forma que su concentración se puede determinar mediante métodos espectrofotométricos. Cuando una disolución de DPPH entra en contacto con una sustancia que puede donar un átomo de hidrógeno o con otra especie radical (R.) se produce la forma reducida DPPH-H ó DPPH-R con la consecuente pérdida del color y por lo tanto la pérdida de la absorbancia (Muñoz y Gutiérrez,. 31.
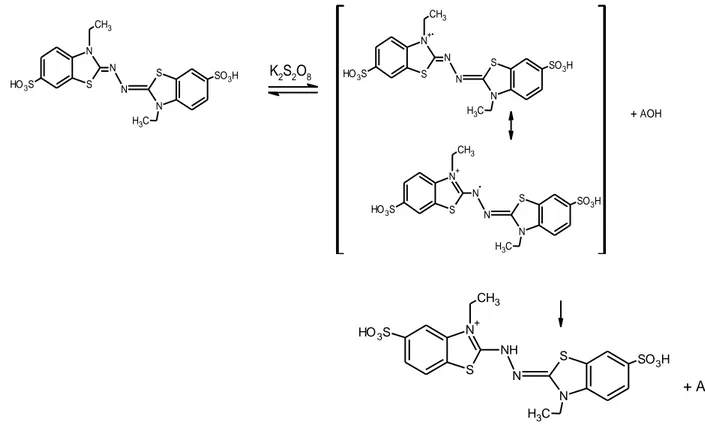
(42) 2009). En la Figura 5-15 se observa la reacción del DPPH con un agente antioxidante. O. O +. N. +. -. N. O. -. O. -. -. O. O. +. N. N. N. +. N. +A-H. NH. O. O +. N. +. N. O. N. +A. .. O. -. -. O. O. Figura 5-15 Reacción química del DPPH antes y después de reaccionar con un agente antioxidante (Muñoz y Gutiérrez, 2009).. Método del ácido 2,2'–azino–bis–[3–etillbenzotiazolin–6–sulfónico] (ABTS•+) El ensayo ABTS●+ es uno de los métodos espectrométricos que han sido aplicados para medir la capacidad antioxidante total de soluciones o sustancias puras y mezclas acuosas (Re et al., 1999). La generación del radical catión ABTS●+, implica la producción directa del cromóforo ABTS●+ verde-azul a través de la reducción del ABTS con persulfato de potasio (K2S2O8). El catión radical resulta en tres máximos de absorción a las longitudes de onda de 645 nm, 734 nm y 815 nm, considerándose mejor para ABTS●+, 734 nm como la longitud de onda de máxima absorbancia. La adición de los antioxidantes al radical pre-formado lo reduce a ABTS. De esta manera el grado de decoloración del radical catión ABTS●+ influye de acuerdo a la concentración de antioxidante como de la duración de la reacción sobre la inhibición de la absorción de catión radical se tienen en cuenta al determinar la capacidad antioxidante (Del Rio, 2013). En la Figura 5-16 se observa la reacción del ABTS con un agente antirradical.. 32.
(43) 2. Método del ácido 2,2'–azino–bis–[3–etillbenzotiazolin–6–sulfónico] (ABTS•+) CH3. CH3. +. N N. N N. HO 3S. S. S. SO 3H. K2S2O8. HO 3S. S. S. SO 3H. N. N. N N. H3C. H3C. + AOH. CH3 +. N. N HO 3S. S. S. SO 3H. N N H3C. CH3 +. N. HO 3S. CH 3 NH HO 3S. S. S. +. N. N S. SO 3H. N SN. SO 3H. NH C 3 N H3C. Figura 5-16 Reacción química del ABTS antes y después de reaccionar con un compuesto antirradical (AOH) (Oliveira et al., 2014).. 33. + AO. .. . + AO.
(44) 6. METODOLOGIA. Este trabajo de investigación se caracterizó por abordar dos aspectos, uno químico y otro biológico. El estudio químico se orientó en el aislamiento, purificación y elucidación estructural de metabolitos fijos presentes en las partes aéreas de la especie Momordica charantia y el estudio biológico se enfocó en evaluar la capacidad antioxidante del extracto y fracciones obtenidas de esta especie.. 6.1. GENERALIDADES. Para el estudio fitoquímico de las partes aéreas de la especie Momordica charantia. se. emplearon. métodos. cromatográficos,. espectroscópicos. y. espectrométricos convencionales utilizados en el aislamiento, purificación y elucidación estructural de metabolitos secundarios. Métodos de separación cromatográficos y elucidación estructural. Los extractos y fracciones obtenidos fueron sometidos a separaciones sucesivas empleando para ello cromatografía en columna (CC) bajo gravedad, cromatografía en capa delgada (CCD) y cromatografía en capa delgada preparativa (CCDP); cada una de las sub-fracciones obtenidas se monitorearon por cromatografía en capa delgada (CCD) utilizando cromatoplacas en sílica gel 60G F-254 Merck y para la CC se utilizó sílica gel 60 Merck (60- 200 Mesh).. El perfil cromatográfico de la CCD y la cantidad de fracción, permitió la selección de las fracciones que se llevaron a purificación, donde el control de pureza se realizó por CCD empleando como reveladores luz ultravioleta y vainillina en ácido sulfúrico. Para determinar las mezclas obtenidas en las diferentes fracciones se utilizó un cromatógrafo con detector selectivo de masas SHIMADZU QP2010 plus, dotado con sonda de inserción directa y analizador de masas cuadrupolar. Utilizando un modo ionización electrónica (IE) a 70eV y una temperatura de la cámara de ionización de 230°C, ubicado en el laboratorio de química de la Universidad 34.
Figure


Outline
Documento similar
This section provides guidance with examples on encoding medicinal product packaging information, together with the relationship between Pack Size, Package Item (container)
Abstract: This paper reviews the dialogue and controversies between the paratexts of a corpus of collections of short novels –and romances– publi- shed from 1624 to 1637:
Entre nosotros anda un escritor de cosas de filología, paisano de Costa, que no deja de tener ingenio y garbo; pero cuyas obras tienen de todo menos de ciencia, y aun
Habiendo organizado un movimiento revolucionario en Valencia a principios de 1929 y persistido en las reuniones conspirativo-constitucionalistas desde entonces —cierto que a aquellas
The part I assessment is coordinated involving all MSCs and led by the RMS who prepares a draft assessment report, sends the request for information (RFI) with considerations,
o Si dispone en su establecimiento de alguna silla de ruedas Jazz S50 o 708D cuyo nº de serie figura en el anexo 1 de esta nota informativa, consulte la nota de aviso de la
De hecho, este sometimiento periódico al voto, esta decisión periódica de los electores sobre la gestión ha sido uno de los componentes teóricos más interesantes de la
Ciaurriz quien, durante su primer arlo de estancia en Loyola 40 , catalogó sus fondos siguiendo la división previa a la que nos hemos referido; y si esta labor fue de