GUÍA DE LABORATORIOS
DE LÁCTEOS
Mónica Obando Chaves
Obando Chaves, Mónica
Guía de laboratorios de lácteos / Mónica Obando Chaves. -- 1ª. Ed. -- Universidad del Tolima, 2019.
136 p. : il. tablas
Contenido: Leche y secreción láctea -- Composición química de la leche bovina -- Toma de muestras de leche cruda -- Guías de laboratorio.
ISBN: 978-958-5569-15-7
1. Procesamiento de productos lácteos 2. Procesos agrícolas 3. Leche – Análisis I. Titulo
637.1 O12g
© Sello Editorial Universidad del Tolima, 2019 © Mónica Obando Chaves
Primera edición electrónica ISBN: 978-958-5569-15-7 Número de páginas: 136 Ibagué-Tolima
Guía de laboratorios de lácteos Facultad de Ingeniería Agronómica Grupo de Investigación CEDAGRITOL Guía de laboratorios de lácteos publicaciones@ut.edu.co mobando@ut.edu.co
Impresión, diseño y diagramación por PROVEER PRODUCTOS Y SERVICIOS S.A.S Corrector de estilo: Carlos Alfonso Quimbayo
Contenido
Prólogo 11
Capítulo 1
Leche y secreción láctea ... 13
1.1. Definición legal ... 15
1.2. Secreción láctea ... 18
1.3. Ciclo de lactación ... 19
1.4. Ordeño ... 21
1.5. Mastitis ... 23
Referencias bibliográficas ... 28
Capítulo 2
Composición química de la leche bovina ...31
2.1. Componentes mayoritarios ... 37
2.1.1. Grasa ... 37
2.1.2. Proteínas ... 40
2.1.3. Lactosa ... 47
2.1.4. Sales ... 49
2.2. Componentes minoritarios ... 49
2.2.1. Vitaminas... 49
2.2.2. Enzimas ... 49
Capítulo 3
Toma de muestras de leche cruda ...53
3.1. Introducción ... 55
3.2. Guía para tomar la muestra ... 56
3.2.1. Aspectos generales ... 56
3.2.2. Protocolo de toma de muestras ... 58
Referencias bibliográficas ... 61
Capítulo 4
Guías de laboratorio ... 63
4.1. Laboratorio No. 1. Análisis organoléptico y fisicoquímico de leche cruda ... 65
4.1.1. Objetivos ... 65
4.1.2. Prueba ... 65
4.1.3. Taller ... 77
Referencias bibliográficas ... 78
4.2. Laboratorio No. 2. Adulterantes y conservantes en leche cruda ... 79
4.2.1. Objetivo ... 79
4.2.2. Pruebas ... 79
4.2.3. Taller ... 82
Referencias bibliográficas ... 83
4.3. Laboratorio No. 3. Coagulación y elaboración de cuajada ... 83
4.3.1. Objetivos ... 84
4.3.2. Procedimiento ... 84
4.3.3. Taller: ... 87
4.4. Laboratorio No. 4. Elaboración de queso costeño
amasado ... 88
4.4.1. Objetivo ... 88
4.4.2. Descripción general del queso costeño amasado ... 89
4.4.3. Pauta de elaboración del queso costeño amasado ... 90
4.4.4. Hoja de control de producción ... 91
4.4.5. Taller ... 95
Referencias bibliográficas ... 95
4.5. Laboratorio No. 5. Elaboración de queso doble crema ... 96
4.5.1. Objetivos ... 96
4.5.2. Descripción general del queso doble crema ... 96
4.5.3. Cuadrado de Pearson ... 98
4.5.4. Pauta de elaboración del queso doble crema ...100
4.5.5. Hoja de control de producción ...101
Referencias bibliográficas ...103
4.6. Laboratorio No. 6. Elaboración de quesillo ...104
4.6.1. Objetivos ...104
4.6.2. Descripción general del quesillo ...105
4.6.3. Pauta de elaboración de quesillo ...106
Referencias bibliográficas ...108
4.7. Laboratorio No. 7. Elaboraciónde queso crema ...108
4.7.1. Objetivos ...108
4.7.2. Definición ...109
4.7.3. Pauta de elaboración del queso crema ...110
Referencias bibliográficas ...113
4.8. Laboratorio No. 8. Elaboración de yogur batido ...113
4.8.1. Objetivos ...114
4.8.3. Definición ...115
4.8.4. Pauta de elaboración de yogur batido ...116
4.8.5. Formulaciones ...117
4.8.6. Costos de elaboración y rendimientos ...118
4.8.7. Hoja de control de producción ...119
4.8.8. Taller ...121
Referencias bibliográficas ...122
4.9. Laboratorio No. 9. Elaboración de mantequilla ...122
4.9.1. Objetivos ...123
4.9.2. Definición ...123
4.9.3. Pauta de elaboración de la mantequilla ...125
Referencias bibliográficas ...128
4.10. Laboratorio No. 10. Elaboración de arequipe ...129
4.10.1. Objetivos ...129
4.10.2. Definición ...129
4.10.3. Ingredientes que pueden emplearse ...131
4.10.4. Pauta de elaboración del arequipe ...132
4.10.5. Formulaciones sugeridas ...133
Listado de figuras
Figura 1.1. Curva de lactación ... 20
Figura 2.1. Esquema de la membrana del glóbulo de grasa de la leche... 38
Figura 2.2. Estructura química de los aminoácidos ... 41
Figura 2.3. Estructura de la micela de caseína ... 46
Figura 3.1. Nevera portátil con muestras de leche cruda ... 57
Figura 3.2. Agitador de émbolo para cantinas (Medidas en milímetros) ... 57
Figura 3.3. Toma-muestras para leche cruda ... 58
Figura 3.4. Flameado de la toma de muestras con alcohol 96 % ... 60
Figura 3.5. Toma de muestras de leche del tanque de enfriamiento. ... 61
Figura 4.1. Coloración de leche cruda con alizarol según pH ... 72
Figura 4.2. Acidímetro para leche ... 73
Figura 4.3. Butirómetro para leche ... 76
Figura 4.4. Cuajada ... 83
Figura 4.5. Prueba de corte ... 87
Figura 4.6. Corte de la cuajada ... 87
Figura 4.7. Queso costeño amasado ... 88
Figura 4.8. Filtración de la leche ... 93
Figura 4.9. Corte de la cuajada con lira ... 93
Figura 4.10. Agitación de la cuajada ... 94
Figura 4.11. Salado y amasado de la cuajada ... 94
Figura 4.12. Prensado del queso costeño amasado ... 95
Figura 4.13. Queso doble crema ... 96
Figura 4.14. Cuadrado de Pearson ... 98
Figura 4.16. Textura de la masa cuando alcanza el
pH 5.1 para hilado ...103
Figura 4.17. Hilado...103
Figura 4.18. Quesillo ...104
Figura 4.19. Hilado ...107
Figura 4.20. Empaque del quesillo ...107
Figura 4.21. Queso Crema ...108
Figura 4.22. Drenaje del queso crema ...111
Figura 4.23. Mezclado y adición de sal ...112
Figura 4.24. Envasado del queso crema ...112
Figura 4.25. Yogur batido...113
Figura 4.26. Adición de sólidos (azúcar, leche en polvo, estabilizantes) ...120
Figura 4.27. Inoculación de la leche con cultivo de adición directa (DVS) ...120
Figura 4.28. Saborización y envasado del yogur ...121
Figura 4.29. Mantequilla ...122
Figura 4.30. Granos de mantequilla ...126
Figura 4.31. Desuerado de los granos de mantequilla ...126
Figura 4.32. Amasado de la mantequilla ...127
Figura 4.33. Moldeo de la mantequilla ...127
Figura 4.34. Corte de la mantequilla ...128
Figura 4.35. Arequipe ...129
Figura 4.36. Adición de sacarosa ...131
Figura 4.37. Adición de glucosa ...132
Listado de tablas
Tabla 1.1. Composición de la leche de diferentes
especies ... 17 Tabla 1.2. Composición de la leche de diferentes razas de ganado lechero ... 17 Tabla 1.3. Definición de los tipos de mastitis con referencia
a sus síntomas ... 25 Tabla 1.4. Principales cambios en la composición de la
leche ocasionados por la mastitis ... 26 Tabla 2.1. Composición química de la leche y sus límites de variación ... 33 Tabla 2.2. Propiedades importantes de los componentes
de la leche ... 36 Tabla 2.3. Principales ácidos grasos en la grasa de la
leche ... 40 Tabla 2.4. Principales proteínas presentes en la leche
bovina ... 44 Tabla 4.1. Pauta de elaboración de cuajada ... 86 Tabla 4.2. Composición media esperada del queso costeño amasado ... 89 Tabla 4.3. Pauta de elaboración del queso costeño
amasado ... 90 Tabla 4.4. Hoja de Control de producción del queso
costeño amasado ... 91 Tabla 4.5. Composición media esperada del queso doble crema ... 97 Tabla 4.6. Pauta de elaboración del queso doble crema ...100 Tabla 4.7. Hoja de control de producción del queso
Tabla 4.10. Composición media esperada del queso
crema ...109 Tabla 4.11. Pauta de elaboración del queso Crema ...110 Tabla 4.12. Pauta de elaboración de yogurt batido ...116 Tabla 4.13. Formulaciones de yogur para los diferentes
grupos de trabajo ...117 Tabla 4.14. Costos del yogur. ...118 Tabla 4.15. Hoja de Control de producción del yogur ...119 Tabla 4.16. Composición media esperada de la
mantequilla ...124 Tabla 4.17. Pauta de elaboración de la mantequilla de
11
Prólogo
La tecnología lechera y la docencia son las pasiones que acompañan mi vida. En este libro guía he querido recoger gran parte del conocimiento y de la experiencia práctica que se ha desarrollado a lo largo de 10 años de trabajo docente en la asignatura “Lácteos” del Programa de Ingeniería Agroindustrial de la Universidad del Tolima, y de más de 13 años de experiencia profesional en la industria lechera privada. La motivación principal es que este libro sirva de guía de laboratorio durante el semestre y que, adicionalmente, sea un material de consulta para aquellos estudiantes y profesionales que se desempeñan en el área. Este libro es relevante para quienes buscan estandarizar procesos de elaboración de derivados lácteos típicos colombianos, puesto que no es fácil encontrar información técnica o protocolos de proceso detallados sobre estos productos. Adicionalmente, contiene una serie de fotografías que enriquecen los protocolos de elaboración de los productos lácteos y hacen que esta guía sea más didáctica.
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
12
componentes, para posteriormente determinar su calidad y aptitud tecnológica.
El capítulo 3 es una guía para la toma de muestras de leche cruda, puesto que este paso es determinante para obtener resultados confiables en los análisis de calidad que se realizarán posteriormente y que serán la base para las bonificaciones económicas que se le reconocen al productor y para el destino de la leche en las líneas de proceso.
En el capítulo 4 se encuentran las guías de los laboratorios que se realizan durante el semestre, incluyendo control de calidad de leche cruda (físico-químico), coagulación y elaboración de derivados lácteos, como cuajada; quesos frescos como: costeño, doble crema, quesillo y queso crema. De igual manera, guías de elaboración de productos fermentados, como yogur; y, finalmente, mantequilla y arequipe.
13
Capítulo 1
LECHE Y SECRECIÓN
LÁCTEA
15
1.1. Definición legal
A
continuación, se presentan varias definiciones de leche, provenientes de diferentes entidades y autores que se complementan muy bien:Leche: “Puede definirse como la secreción mamaria normal de animales lecheros, obtenida mediante uno o más ordeños, sin ningún tipo de extracción o adición, destinada al consumo en forma de leche líquida o a elaboración ulterior” (Codex, 1999).
“Leche es el producto de la secreción mamaria normal de animales bovinos, bufalinos, caprinos lecheros sanos, obtenida mediante uno o más ordeños completos, sin ningún tipo de adición, destinada al consumo en forma de leche líquida o a elaboración posterior” (Ministerio de la Protección Social en Colombia, 2006).
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
16
La leche es un líquido de composición compleja, de color blanco opalescente, con un pH cercano al neutro y de sabor dulce. Su propósito natural es la alimentación de la cría durante sus primeros meses de vida. La leche es la única sustancia natural que puede servir como alimento único. Provee energía y materiales de construcción para el crecimiento del joven mamífero y también contiene anticuerpos para protegerlo de las infecciones.
Las características más importantes de la leche son su
variabilidad, alterabilidad y complejidad. En cuanto a la variabilidad, desde un punto de vista composicional, no es posible hablar de una leche sino de leches debido a las diferencias naturales entre especies o para una misma especie, según la región o lugar (Magariños, 2001). En la tabla 1.1, se puede apreciar la composición de las leches de diferentes especies de animales.
Lec he y sec rec ió n l ác teo
17
Tabla 1.1. Composición de la leche de diferentes especiesEspecie Proteína Total (%) Caseína (%) Sero-proteína (%) Grasa (%) Carbo-hidratos (%) Cenizas (%)
Humana 1.2 0.5 0.7 3.8 7.0 0.2
Caballo 2.2 1.3 0.9 1.7 6.2 0.5
Vaca 3.5 2.8 0.7 3.7 4.8 0.7
Búfalo 4.0 3.5 0.5 7.5 4.8 0.7
Cabra 3.6 2.7 0.9 4.1 4.7 0.8
Oveja 5.8 4.9 0.9 7.9 4.5 0.8
Fuente: Tetra Pak, (2003).
Los otros factores que influyen en la variabilidad de la leche son: la alimentación, la época del año, la temperatura ambiente, la etapa del ciclo de lactancia, las enfermedades como la mastitis y los hábitos de ordeño. La leche de vaca también varía según las diferentes razas de ganado, como se muestra en la tabla 1.2.
Tabla 1.2. Composición de la leche de diferentes razas de ganado lechero
Raza Grasa (%) Proteína (%) Lactosa (%) Cenizas (%)
Sólidos No grasos (%) Sólidos Totales (%)
Ayrshire 4.00 3.53 4.67 0.68 8.90 12.90 Pardo
Suizo 4.01 3.61 5.04 0.73 9.40 12.41
Guernsey 4.95 3.91 4.93 0.74 9.66 14.61 Holstein
F. 3.40 3.32 4.87 0.68 8.86 12.26
Jersey 5.37 3.92 4.93 0.71 9.54 14.91
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
18
1.2. Secreción láctea
La glándula mamaria constituye el punto de partida de la industria lechera, pues allí se forma la leche. Por ello nos interesa conocer el mecanismo de la secreción láctea, ya que cambios de la misma modifican la composición de la materia prima de la industria lechera.
La ubre está integrada por cuatro porciones glandulares más o menos independientes; en la cabra y en la oveja, solamente por dos. Un surco longitudinal las divide en una mitad derecha y una mitad izquierda, cada una de las cuales está subdividida en dos cuarterones por un surco longitudinal. Cada cuarterón posee un pezón y representa una glándula independiente. Los cuartos delanteros producen el 40 % de la leche y los traseros el 60 %.
Lec
he
y
sec
rec
ió
n l
ác
teo
19
de leche son alimentadas con los nutrientes necesarios para la secreción de la leche (Tetra Pak, 2003).
Cuando los alvéolos segregan leche, su presión interna aumenta. Si la vaca no es ordeñada, la secreción de la leche se detiene cuando la presión ejerce cierto límite. La secreción láctea es regida por estímulos que producen reflejos y por hormonas hipofisiarias. La prolactina, que es liberada mientras dura la secreción láctea, tiene un papel esencial.
La hormona oxitocina produce la verdadera eyección de la leche, llamada por los ordeñadores “bajada de la leche”, es decir, la evacuación intensa y breve de dicho líquido, que se encuentra en la ubre. El ordeño requiere el estímulo de la vaca. El mejor estímulo se logra lavando la ubre con agua tibia y limpiándola para prepararla para el ordeño. Esta sensación hace que el animal segregue la oxitocina. Esta acción llega a su máxima intensidad un minuto después del estímulo y va decreciendo hasta hacerse muy débil a los 6 u 8 minutos. Una repentina sensación dolorosa, los sustos o estímulos similares, pueden causar una descarga de adrenalina y, en consecuencia, se interrumpe la secreción de la leche y se inhibe la predisposición para darla. El ordeño debe durar entonces, entre 6 y 8 minutos (ICA, sf.).
1.3. Ciclo de lactación
G uí a d e l ab or at or ios d e l ác te os
20
se detiene para darle a la vaca un período de descanso de aproximadamente 60 días, que se llama “vaca seca”, durante el cual el animal se recupera y se prepara para su siguiente parto. Con el nacimiento del ternero comienza un nuevo ciclo de lactación. Según la fase de dicho período, hemos de distinguir el calostro, la leche correspondiente a la lactación completa y la leche de final de ciclo.
Calostro: Es el fluido que produce la vaca inmediatamente después del parto (hasta 7 días después). El calostro no debe enviarse a la industria de la transformación hasta el día 6 después del parto. Es un líquido ligeramente viscoso, de sabor salino y de color amarillo a pardo, que se coagula por el calor. Su densidad oscila entre 1.033 y 1.094 g/mL (Spreer, 1991).
Leche de lactación completa: Es la materia prima para las plantas lecheras.
Leche del final del periodo de lactación: Unas semanas antes del parto, la leche ofrece características semejantes a las del calostro. Aumenta el extracto seco y los glóbulos grasos son más pequeños. Reacciona con más dificultad al cuajo y coagula de manera defectuosa.
C
on
cen
tració
n de s
ólidos (g/L)
Li
tros de le
ch e 60 50 40 30 20 10 0
1 2 3 4 5 6 7 8 9 10 11 12 13 Meses
grasa lactosa proteina litros leche 60 50 40 30 20 10 0 Periodo seco de rehabilitación del rumen
Figura 1.1. Curva de lactación
Lec
he
y
sec
rec
ió
n l
ác
teo
21
1.4. Ordeño
En este punto se mencionarán solo los principios básicos de la rutina de ordeño, puesto que es el punto de partida para obtener una leche cruda de excelente calidad y, como consecuencia, un producto terminado de alta calidad. Sin embargo, en la mayoría de los casos, el Ingeniero Agroindustrial no tiene injerencia en este proceso y solo recibe la leche en la plataforma de recibo de la planta lechera para su transformación, pero debe estar consciente de que una buena rutina de ordeño, higiénica, rápida y completa,
le garantiza una materia prima de alta calidad en su planta. La rutina debe ser higiénica porque debe realizarse con equipos de ordeña limpios, o en el caso de ordeña manual, manos limpias, utensilios limpios, agua limpia y una sala o lugar de ordeño que minimice la contaminación en la leche. También debe ser rápida porque debe realizarse en el tiempo de acción de la oxitocina (6 a 8 minutos); y completa, para que no queden residuos de leche en los cuarterones que puedan generar problemas como la mastitis.
Una rutina de ordeño realizada correctamente, está relacionada con la calidad higiénica, calidad composicional y la cantidad de leche obtenida. Los pasos en la rutina de ordeño se enumeran a continuación. Aun cuando en algunos casos puede variar, no se debe olvidar la eliminación de los primero chorros de leche y secar muy bien los pezones antes de iniciar el ordeño.
Pasos de la rutina de ordeño:
1. Arrear las vacas con tranquilidad y sin gritos ni ruidos fuertes que estresen al animal.
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
22
3. Mojar los pezones con un mínimo de agua para limpiar el polvo presente y en caso de que se encuentren limpios no mojar los pezones.
4. Eliminar los primeros chorros de leche, utilizando para ello un tazón de fondo oscuro. El objetivo de esta operación es eliminar la leche residual en el canal del pezón que contiene alta carga microbiana; detectar mastitis clínica (pus, grumos, sangre, cuartos afiebrados o endurecidos) y estimular el reflejo de la bajada de la leche.
5. Lavar los pezones y la base inferior de la ubre con agua a baja presión.
6. Opcional: realizar dipping pre-ordeño (pre-dipping).
Solo realizar en caso de incidencia de mastitis ambientales, pero no es reemplazante del lavado de pezones. Debe secarse con toallas desechables para para evitar que los residuos aparezcan como inhibidores en la leche.
7. Secar los pezones con toallas desechables en cada vaca, y de preferencia un cuarto de toalla por cuarterón, no usar la misma toalla para todos los pezones, alguno puede estar enfermo y contaminaría los otros. Es muy importante ordeñar pezones limpios y secos, ya que si se ordeñan mojados se facilita el deslizamiento de las pezoneras y aumentan las unidades formadoras de colonias (UFC), presentes en la leche por efecto del agua contaminada que escurre y que absorben las pezoneras.
Lec
he
y
sec
rec
ió
n l
ác
teo
23
9. Realizar dipping con una solución yodada para sellar los pezones y evitar la entrada de microorganismos al canal del pezón.
Inmediatamente después del ordeño la leche debe ser refrigerada a 4 °C para mantener su carga microbiana inicial baja.
1.5. Mastitis
Un alto recuento de células somáticas es un indicador de mastitis en el ganado lechero y una medida indirecta de la calidad de la leche cruda en la industria láctea. La mastitis es la enfermedad más frecuente en los hatos lecheros y es la principal causa de pérdidas económicas en la producción de leche alrededor del mundo (Hogeveen, Huijps, & Lam, 2011). Si bien, la composición de la leche puede verse afectada por múltiples factores, como raza, edad, etapa de lactación, clima y dieta del animal, entre otros, la mastitis, una reacción inflamatoria de la glándula mamaria a la infección, es también conocida por causar efectos en la cantidad, calidad y aptitud para el procesamiento de la leche. Más allá de la salud del animal y las implicaciones de seguridad alimentaria, la mastitis es un problema de la industria láctea porque induce cambios en la leche que se derivan en menores rendimientos, disminución de la vida útil, baja calidad de los productos lácteos y pérdidas económicas para la industria (Le Maréchal, Thiéry, Vautor, & Le Loir, 2011).
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
24
por muchos factores, como la especie del animal, el estado de lactación, el factor individual y medioambiental, y por supuesto el manejo del animal.
Hay cuatro tipos principales de células somáticas (leucocitos): macrófagos, células neutrófilas polimorfonu-cleares, linfocitos y células epiteliales. La mastitis puede afectar todos o un solo cuarterón de la ubre. Paralelo a la función de defensa de la ubre que cumplen las células somáticas, también proveen numerosas enzimas endógenas (lipasas, oxigenasas, proteasas, glicosidasas) que tienen cierta especificidad y actividad, que son liberadas en la leche y que pueden influenciar los procesos en la industria lechera y la calidad final de los productos (Richoux, Boutinaud, Martin, & Gagnaire, 2014).
El valor normal de células somáticas por cuarterón está entre 68.000 y 187.000 cél/mL en leche bovina (Djabri, Bareille, Beaudeau, & Seegers, 2002). El RCS en leche proveniente de animales enfermos (>200.000 cél/mL) varía, dependiendo del patógeno responsable de la infección. Los principales microorganismos responsables de mastitis son: Corynebacterium bovis, Escherichia Coli, Staphylococcus aureus, Streptococcus uberis y Streptococcus agalactiae. Estos diferentes patógenos inducen diferentes síntomas asociados con diferentes tipos de mastitis. La mastitis puede ser subclínica o clínica en diferentes rangos, que se mencionan en la tabla 1.3.
Lec
he
y
sec
rec
ió
n l
ác
teo
25
acuerdo al país. En Alemania es de 100.000 cél/mL, en Canadá 500.000 cél/mL y en Estados Unidos 750.000 cél/mL.
Tabla 1.3. Definición de los tipos de mastitis con referencia a sus síntomas
Tipo de mastitis Definición
Subclínica Inflamación de la glándula mamaria no visible; requiere test de diagnóstico. Es la enfermedad prevalente en el hato.
Clínica ligera
Anormalidades observables en la leche, generalmente pequeños coágulos, con cambios mínimos no perceptibles en
la ubre.
Clínica moderada
Visibles anormalidades en la leche e hinchazón en el cuarterón afectado, con
ausencia de síntomas de enfermedad sistémica.
Clínica severa Inflamación de la ubre, con graves síntomas locales y sistémicos.
Fuente: Le Maréchal, Thiéry, Vautor, & Le Loir, (2011).
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
26
con altas posibilidades de presentar patógenos o las toxinas de los mismos, lo cual representa un riesgo para la salud del consumidor.
Un incremento en el RCS es normalmente asociado con un decrecimiento en la producción de leche en los animales rumiantes. Después de la mastitis clínica, la producción de leche disminuye en la vaca y nunca regresará a sus niveles normales (antes de la mastitis). El porcentaje de disminución en la producción también depende del patógeno responsable de la infección (Le Maréchal, Thiéry, Vautor, & Le Loir, 2011).
Los principales cambios asociados con un alto recuento de células somáticas se resumen en la tabla 1.4. Se puede observar que las proteínas del suero se incrementan, principalmente seroalbúminas e inmunoglobulinas, las α y β
caseínas disminuyen, no hay una tendencia clara en cuanto a la grasa, pero en algunos estudios el porcentaje de grasa disminuye, con un incremento de los ácidos grasos libres. El pH de la leche se incrementa, al igual que el sodio y los cloruros, y el calcio disminuye.
Tabla 1.4. Principales cambios en la composición de la leche ocasionados por la mastitis
Parámetro Cambio en la leche
Lactosa Disminución
Grasa Disminución, con aumento de los ácidos grasos libres.
Caseína Disminución
Proteínas del
suero Aumento, especialmente seroalbúminas e inmunoglobulinas.
Lec
he
y
sec
rec
ió
n l
ác
teo
27
Parámetro Cambio en la leche
Sodio Aumento
Calcio Disminución
pH Aumento
Fuente: Autora
La actividad enzimática se incrementa, principalmente la actividad de la plasmina, que es una proteasa nativa de la leche y que tiene una actividad óptima a los 37 °C, lo cual hace que el daño a las proteínas de la leche se dé en la ubre, antes incluso de ser ordeñada la vaca. La β y la α–caseínas son principalmente hidrolizadas por esta enzima.
Las lipasas también se incrementan y, como consecuencia, aumentan los niveles de ácidos grasos libres y de los ácidos grasos de cadena corta, lo cual genera defectos como la rancidez en los productos lácteos (Jadhav, Tarate, Bhuvana, Das, & Shome, 2016).
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
28
síntesis de caseína y grasa en la glándula mamaria decrecen. En leches UHT, producidas con leches con altos recuentos de células somáticas, también se presentaron defectos de sabor y rancidez, debido al desarrollo de bacterias, proteólisis y lipólisis de los componentes de la leche (Barbano, Ma, & Santos, 2006).
Referencias bibliográficas
FAO. (05 de marzo de 2016). Producción Lechera. Recuperado de: http://www.fao.org/agriculture/dairy-gateway/milk-production/en/#.Vtjx633hDDc
CODEX Alimentarius. (1999). Norma General del Codex para uso de términos lecheros. Codex Stan 206-1999.
Ministerio de la Protección Social. (2006). Decreto 616 de 2006. Reglamento Técnico sobre los requisitos que debe cumplir la leche para el consumo humano que se obtenga, procese, envase, transporte, comercializa, expenda, importe o exporte en el país.
MAGARIÑOS, H. (2001). Producción higiénica de leche cruda. Producción y servicios incorporados S.A. Guatemala. 93p. FAO. (05 de marzo de 2016). Animales lecheros. Recuperado de:
http://www.fao.org/agriculture/dairy-gateway/produccion-lechera/animales-lecheros/es/#.VvNc6tLhDDc
TETRA PAK. (2003). Manual de Industrias Lácteas. A. Madrid Vicente, Ediciones. Madrid. 436p.
ICA. Manual de Asistencia Técnica No.6: Ganado de Leche. Bogotá. 244 p.
SPREER, E. (1991). Lactología Industrial. Ed. Acribia. España. 617 p. HOGEVEEN, H., HUIJPS, K., & LAM, TJGM. (2011). Economic
aspects of mastitis: New developments. New Zealand
Veterinarian Journal. 59: 16-23.
Lec
he
y
sec
rec
ió
n l
ác
teo
29
91: 247-282.
RICHOUX, N., BOUTINAUD, M., MARTIN, P., & GAGNAIRE, V. (2014). Role of Somatic Cells on Dairy Processes and Products: a review. Dairy Science & Technology, 94: 517-538. DJABRI, B., BAREILLE, N., BEAUDEAU, F., & SEEGERS, H. (2002).
Quarter milk somatic cell count in infected dairy cows: a meta-analysis. Veterinary Research 33: 335-357.
Departamento Nacional de Planeación (DNP). (2010). Política Nacional para mejorar la competitividad del sector lácteo colombiano. Documento Conpes 3675. Consejo Nacional de Política económica y social. Colombia. 50p.
JADHAV, P.V, TARATE, S.B., BHUVANA, M., DAS, D.N., & SHOME, B.R. (2016). Somatic cell count as a monitoring system for hygienic milk production in India: A review. Asian Journal
Dairy and Food Research, 35 (4): 270-277.
MA, Y., RYAN, C., BARBANO, M., GALTON, M., RUDAN, A., & BOOR, J. (2000). Effect of somatic cell count on quality and shelf life of pasteurized fluid milk. Journal of Dairy Science.
83: 264-274.
31
Capítulo 2
33
L
a variabilidad en la composición química de la leche es una característica importante, que debe tenerse en cuenta en la determinación de calidad de leche. La composición química de la leche varía con la raza, las condiciones de manejo, la alimentación e incluso entre animales de una misma raza (individualidad). Los valores que se presentan en la tabla 2.1, son rangos promedio entre los que puede normalmente fluctuar la composición química de la leche.Tabla 2.1. Composición química de la leche y sus límites de variación
Componentes mayoritarios
Límites de
variación (%) Valor promedio (%)
Agua 85.5 - 89.5 87.5
Grasa 3.2 - 4.2 3.9
Proteínas 3.2 - 4.0 3.4
Lactosa 4.0 - 5.5 4.8
Minerales 0.6 - 0.9 0.8
Componentes minoritarios
Enzimas Lipasas, peroxidasas, proteasas, etc. Vitaminas A, D, E, K Células diversas Epiteliales,
34
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os Antes de hacer referencia los componentes mayoritarios de la leche, es importante revisar algunas de sus propiedades físicas. Como fluido, es un sistema polidisperso, esto es, sus distintos componentes forman partículas de diverso tamaño en diferentes grados de dispersión y formas de solución (solución verdadera, coloidal o suspensión).
■ Los glóbulos grasos se encuentran formando una emulsión (1–20µm)
■ Las proteínas se encuentran en solución coloidal (8–200 nm)
■ El azúcar y las sales forman una solución verdadera.
Una dispersión se obtiene cuando las partículas de una sustancia se encuentran distribuidas en un líquido. Hay dos clases de dispersión: suspensión y emulsión.
Suspensión: partículas sólidas dispersas en un líquido. Entre más finas sean las partículas, más estable es la suspensión.
Emulsión: Es una mezcla de dos líquidos no miscibles entre sí. Normalmente consiste en una fase acuosa y una oleosa. La fase oleosa puede hallarse dispersa en forma de pequeñas gotitas en la acuosa: emulsión de aceite/agua o, al contrario, emulsión de agua/aceite. Para mantener la emulsión estable hay que evitar que las gotitas de líquido disperso se unan formando gotas mayores. Esto se puede conseguir añadiendo un agente emulsificante con propiedades hidrófobas e hidrófilas.
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
35
La principal diferencia entre una suspensión y una solución coloidal radica en el tamaño de las partículas. Las partículas de una solución coloidal son mucho menores, razón por la cual son más estables que las suspensiones. Las coloidales pueden ser precipitadas por un cambio de temperatura, un aumento de acidez o por enzimas. Cuando esto ocurre se dice que el coloide gelifica.
Soluciones puras o verdaderas:
■ Soluciones no iónicas: cuando la lactosa de disuelve en agua, no se producen cambios importantes en la estructura molecular de dicho azúcar.
■ Soluciones iónicas: Cuando la sal común se disuelve en agua, los cationes (Na+) y los aniones (Cl-) se
dispersan formando un electrolito.
El agua de la leche se encuentra como agua libre, que actúa como disolvente, y como agua ligada, que está fuertemente retenida por las sustancias insolubles y no actúa como disolvente.
El agua ligada, que constituye menos del 4 % del total del agua, no es fija en proporción, y está en equilibrio con el agua libre. En la leche recién ordeñada aumenta lentamente, afectando la medición de la densidad, fenómeno que se denomina “efecto Recknagel”. La retención del agua ligada en un 50 % es efecto de la caseína; 30 %, de las proteínas solubles; y 15 %, de los fosfolípidos de la membrana del glóbulo graso. Los fosfolípidos pueden retener hasta un 600 % de su peso en agua y la caseína, aproximadamente un 50 %.
36
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os enzimas, y se llama suero (Tabla 2.2). Estas proteínas también se combinan con calcio, pero no forman soluciones coloidales. También hay sales disueltas, como fosfatos, cloruros y bicarbonatos. Las sales presentes en la fase hídrica están en equilibrio entre la fase coloidal y solución, con excepción de los cloruros y los sulfatos.
Tabla 2.2. Propiedades importantes de los componentes de la leche
LECHE
PLASMA
SUERO Glóbulos
de grasa Micelas de Caseína globularesProteínas lipoproteínasPartículas de Componentes Grasa Caseína, agua y
sales
Proteínas
del suero Lípidos, otras proteínas Estado Emulsión dispersiónFina Solución coloidal Dispersión coloidal Contenido (%
materia seca) 4 2.8 0.6 0.01
Diámetro de
partícula 0.1 – 10 µm
20 – 400
nm 3 – 6 nm 10 nm
Densidad
(20°C, Kg/m3) 920 1100 1300 1100
Separable por Descrema-dora
Centrífuga de alta velocidad
Ultrafil-tración Ultrafiltración Punto
isoeléctrico ~ 3.8 ~ 4.6 4- 5 ~ 4
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
37
2.1. Componentes mayoritarios
2.1.1. Grasa
La leche contiene en promedio 3.5 % de grasa, sin embargo, es uno de los parámetros que varía notablemente debido a diversos factores, entre los cuales se incluyen: la raza (Jersey mayor contenido y Holstein la más baja); la edad, la alimentación y la salud del animal, así como la etapa del ciclo de lactación. Como se indicó antes, la grasa también decrece si hay presencia de mastitis.
La grasa se encuentra en la leche en forma de pequeños glóbulos dispersos en emulsión en la fase acuosa. Su diámetro oscila entre 0.1 y 20 μm (1μm = 0.01mm). El tamaño medio es de 3 – 4 μm (Tetra Pak, 2003). Los glóbulos de grasa son las partículas más grandes que tiene la leche y las más ligeras: 0.936 – 0.95 g/cm3 a 15.5 °C, su punto de fusión: 29 – 34 °C y
su punto de solidificación: 24 – 29 °C (Keating, 2002).
38
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os La estabilidad de la membrana del glóbulo de grasa es crítica, porque protege los lípidos que se encuentra en el corazón del glóbulo frente a la lipólisis generada por las lipasas. Esta membrana puede ser dañada por agitación, congelación y, especialmente, por la homogenización, durante la cual la membrana natural es reemplazada por una capa de proteínas de la leche, especialmente caseínas (Fox, 2000).
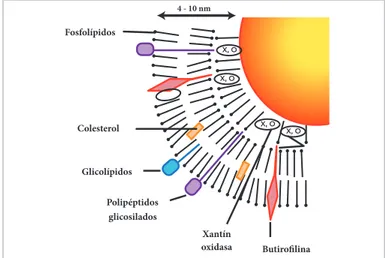
Todas las grasas pertenecen al grupo de sustancias químicas llamadas ésteres, que se forman a partir de alcoholes y ácidos grasos. La grasa de la leche está compuesta por triglicéridos en un 98 % aproximadamente; di- y monoglicéridos, ácidos grasos, esteroles, carotenoides, vitaminas (A, D, E y K), y otros elementos trazas.
X, O X, O
X, O
4 - 10 nm
X, O
Fosfolípidos
Colesterol
Glicolípidos
Polipéptidos glicosilados
Xantín
oxidasa Butirofilina
Figura 2.1. Esquema de la membrana del glóbulo de grasa de la leche
Fuente: Adaptado de Gassi, Famelart & López, (2008).
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
39
unidos en la cadena por enlaces simples, mientras que los ácidos grasos insaturados hay uno o más enlaces dobles en la cadena. La tabla 2.2, muestra los principales ácidos grasos en la grasa de la leche. Los cuatro ácidos más abundantes en la leche son: mirístico, palmítico esteárico y oleico.
A temperatura ambiente los tres primeros son sólidos y el último es líquido. Esta variación afecta la dureza de la grasa (Tetra Pak, 2003). Las variaciones en la composición de los ácidos grasos, especialmente en la longitud de la cadena carbonada y el grado de saturación, originan ciertas características de textura en los productos lácteos, debido a que influyen en el punto de fusión de la grasa: es mayor cuanto mayor es la longitud de la cadena y su grado de saturación más alto.
Algunas características importantes del perfil de ácidos grasos de la leche son: La grasa de los rumiantes contiene altos niveles de ácido butírico (C4) y otros ácidos grasos de cadena corta. El ácido butírico o butanoico se sintetiza en la ubre a partir de ácido acético y ácido hidroxi-butírico que circulan en la sangre provenientes de la fermentación de los alimentos en el rumen.
40
G uí a d e l ab or at or ios d e l ác teos Tabla 2.3. Principales ácidos grasos en la grasa de la leche
Ácidos grasos
% de contenido sobre el total de ácidos grasos Punto de fusión (°C) Número de átomos de carbono Saturados
Butírico 3.0 – 4.5 - 7.9 4
Caproico 1.3 – 2.2 - 1.5 6
Caprílico 0.8 – 2.5 16.5 8
Cáprico 1.8 – 3.8 31.4 10
Ácidos grasos
% de contenido sobre el total de ácidos grasos Punto de fusión (°C) Número de átomos de carbono
Láurico 2.0 – 5.0 43.6 12
Mirístico 7.0 – 11.0 53.8 14
Palmítico 25.0 – 29.0 62.6 16
Esteárico 7.0 – 3.0 69.3 18
Insaturados
Oléico 30.0 – 40.0 14 18
Linoléico 2.0 – 3.0 - 5 18
Linolénico Hasta 1.0 - 5 18
Araquidónico Hasta 1.0 - 49.5 20
Fuente: Adaptado de Tetra Pak, (2003).
2.1.2. Proteínas
La leche contiene en promedio 3.4 % de proteína. Las proteínas son moléculas formadas por unidades más pequeñas, llamadas aminoácidos, en una o más cadenas entrelazadas.
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
41
aquellos que tienen un grupo amino y un grupo carboxílico en el mismo átomo de carbono, que se denomina carbono α.
Cadena lateral
R1
H3N+
Grupo amino
H C C Grupo carboxilo
O
O
-Carbono α
Figura 2.2. Estructura química de los aminoácidos
Fuente: Autora
Los aminoácidos son anfóteros, es decir, están cargados negativamente en soluciones alcalinas; en forma neutra con cargas positivas y negativas, y cargados positivamente en soluciones ácidas. Las proteínas se construyen a partir de 20 tipos de aminoácidos, 18 de los cuales se encuentran en la leche (Tetra Pak, 2003). Los aminoácidos esenciales son aquellos que el organismo tiene que conseguir a través de los alimentos que ingiere, porque no los produce, y la leche los tiene todos.
La estructura primaria de las proteínas está dada por el ordenamiento de la cadena polipeptídica y es estable, gracias al enlace peptídico o de covalencia entre aminoácidos. Esta estructura primaria puede ser alterada por enzimas proteolíticas que liberan aminoácidos de la cadena polipeptídica.
42
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os sobre sí y por fuerzas hidrofóbicas; la estructura cuaternaria se refiere a la unión relativamente frágil de monómeros o de pequeñas unidades moleculares, por enlaces de débil energía.
La desnaturalización de las proteínas es una modificación limitada de la estructura terciaria y secundaria de las proteínas, sin un rompimiento de enlaces covalentes, ni separación de fragmentos que conduce a un reagrupamiento y nueva conformación.
Las proteínas de la leche se dividen principalmente en caseínas (aprox. 78 %) y en proteínas del suero o seroproteínas que son solubles. La leche de bovino contiene seis específicas proteínas: cuatro caseínas, αs1, αs2, β y κ, representando aproximadamente 38 %, 10 %, 36 % y 15 %, respectivamente de toda la caseína, y seroproteínas, β–lactoglobulina y
α–lactalbúmina, las cuales representan el 40 % y el 20 %, respectivamente, del total de las proteínas del suero. La tabla 2.3 muestra las principales proteínas presentes en la leche y su concentración (Fox, 2000).
Las principales diferencias entre caseínas y proteínas del suero son:
■ Las caseínas precipitan a pH 4.6, las seroproteínas, no precipitan a ese pH.
■ El cuajo y otros enzimas coagulantes, causan pe-queños cambios en la caseína, lo que causa su coa-gulación en presencia de calcio. Las proteínas del suero no sufren estos cambios ni la coagulación.
coa-Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
43
gularse. Las proteínas del suero son termo-lábiles y se pueden desnaturalizar completamente a 90 °C por 10 minutos.
■ Las caseínas son fosfoproteínas, contienen 0.85 % de fósforo, mientras que las seroproteínas no con-tienen fósforo. Los grupos fosfatos son importantes porque ellos ligan el calcio, necesario para la nutri-ción y para la aptitud tecnológica de la leche.
■ La caseína es baja en sulfuro (0.8 %), mientras que las proteínas del suero son ricas en sulfuro (1.7 %). Este contenido de sulfuro viene del contenido de aminoácidos que lo contienen; en la caseína es de-bido principalmente al contenido de metionina, mientras en las proteínas del suero, al contenido de cisteína y metionina, lo que los hace responsable de los cambios que sufre la leche durante el calenta-miento, como el sabor a cocido.
2.1.2.1. Caseínas
44
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os caseínas frente al calcio. Esta fracción constituye el sustrato específico del cuajo. Las proteínas forman un sistema coloidal estable, gracias a la acción de dos fuerzas que son: las cargas eléctricas y el agua de hidratación. En las caseínas la principal fuerza de estabilidad la constituyen las cargas eléctricas dadas por el radical ácido (COO-) y básico (NH
3+) de los
aminoácidos, que ayudan a mantener separadas las micelas de caseína. A pH normal de la leche predominan las cargas negativas del radical ácido.
Se han definido entonces tres principales clases de caseínas:
■
■ α– caseína (sensible al calcio)
■
■ β– caseína (sensible al calcio)
■
■ κ– caseína (insensible al calcio)
La caseína en solución coloidal es un complejo asociado con calcio y fósforo que puede ser coagulada por la acción de ácidos, cuajo y/o alcohol.
Cuando la leche se acidifica ocurren dos fenómenos: 1. Disminuyen las cargas eléctricas
2. Disminuye el agua de hidratación
Tabla 2.4. Principales proteínas presentes en la leche bovina
Proteína g/Kg leche g/100 g proteína
Caseína 26 78.3
αs1-Caseína 10.7 32
αs2-Caseína 2.8 8.4
β–Caseína 8.6 26
κ-Caseína 3.1 9.3
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
45
Proteína g/Kg leche g/100 g proteína
Sero-proteínas 6.3 19
β–lactoglobulina 3.2 9.8
α–lactoalbúmina 1.2 3.7
Seroalbúmina 0.4 1.2
Proteosa peptona 0.8 2.4
Inmunoglobulinas 0.8 2.4
IgG1, IgG2 0.65 1.8
IgA 0.14 0.4
IgM 0.05 0.2
Otras 0.9 2.7
Lactoferrina 0.1
-Transferrina 0.01
-Proteínas de membrana 0.7 2
Enzimas -
-Fuente: Adaptada de Walstra, et al. (2006)
Lo anterior resta capacidad a las micelas de caseína de mantenerse separadas, y la leche coagula. La caseína puede ser coagulada únicamente mediante la acción del ácido, si el pH se baja a un valor de 4.6 (punto isoeléctrico) o bien cuando la leche ha experimentado cierta acidificación. La leche puede ser coagulada por acción del alcohol, que actúa como deshidratante. Este fenómeno es la base de la prueba de alcohol usada en la recepción para medir la estabilidad de la leche.
46
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
A: Submicela B: Cadena saliente (Glicomacropeptido) C: Fosfato cálcico D: Kappa caseína E: Interacciones hidrófobas (grupos PO4)
Figura 2.3. Estructura de la micela de caseína
Fuente: Adaptada de Tetra Pak, (2003)
La caseína también puede ser precipitada por la acción de enzimas coagulantes: La cadena aminoácida que forma la molécula de la κ-caseína consta de 169 aminoácidos. La unión entre los aminoácidos 105 (fenilalanina) y 106 (metionina) es fácilmente asequible para muchas enzimas proteolíticas. La parte soluble de esta cadena contiene los aminoácidos 106 a 148, donde predominan los aminoácidos polares y el carbohidrato, que darán a la molécula sus propiedades hidrófilas. Esta parte es conocida como el glico-macropéptido y se elimina en el suero durante el proceso de fabricación del queso. La parte que resta de la κ-caseína (1 a 105) es bastante insoluble, y permanece en la cuajada junto con las caseínas alfa y beta. A esta porción se le llama para-κ-caseína.
2.1.2.2. Proteínas del suero
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
47
superiores a los 70 °C. Estar proteínas comienzan a ser insolubles a pH por debajo de 6.5, si son calentadas. La desnaturalización no resulta en agregación, pero las proteínas del suero precipitan sobre las micelas de caseína y permanecen dispersas. Son proteínas de alto valor nutritivo. La α–lactalbúmina y la β–lactoglobulina son las de mayor importancia tecnológica. La β–lactoglobulina es la más abundante en el suero procedente de leche de vaca. Si la leche se calienta por encima de 60 °C, empieza su desnaturalización. No precipitan por acidificación de la leche.
2.1.3. Lactosa
El principal carbohidrato de la leche es la lactosa. Es un disacárido compuesto por D-glucosa y D-galactosa. La leche proveniente de animales bovinos tiene alrededor de 4.8 % de lactosa. Es importante en el procesamiento de derivados lácteos, por sus propiedades: solubilidad, poder reductor, hidrólisis y fermentabilidad. Debido a que la lactosa es responsable del 50 % de la presión osmótica de la leche, la cual es igual a la de la sangre del animal, es relativamente constante, es decir, la concentración de lactosa es independiente de la raza, y de factores nutricionales e individuales, pero decrece a medida que avanza el ciclo de lactación, especialmente cuando hay presencia de mastitis, por el incremento de NaCl en la sangre.
48
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os ■ El grupo aldehído del C1 de la glucosa existe como un hemiacetal, por lo tanto, el C1 es un carbono asimétrico. Por lo anterior, la lactosa existe como dos anómeros α y β, con diferentes propiedades. Estas diferencias, básicamente, son en solubilidad y en cristalización: α–lactosa cristaliza como monohidrato y la β–lactosa como anhidra.
■ La solubilidad de la α y β–lactosa en agua a 20 °C es, aproximadamente, 7 g y 50 g por 100 mL, respectivamente. En equilibrio en solución acuosa, la lactosa existe como una mezcla de anómeros en un ratio aproximado de α y β de 37:63. La solubilidad es de 18.2 g/100 mL.
■ La lactosa tiene baja solubilidad comparada con otros azúcares. Una vez disuelta, cristaliza y forma soluciones supersaturadas. α–lactosa cristaliza espontáneamente en soluciones altamente supersaturadas. En soluciones saturadas forma cristales agudos (tomahawk), que si sobrepasan los 15 μm son detectables al paladar. Los cristales de β–lactosa son más pequeños. La cristalización es un problema en la industria de las leches concentradas azucaradas y de los helados; este defecto es conocido como arenosidad.
■ La lactosa tiene importancia tecnológica en todos los procesos de acidificación de la leche, como en los productos fermentados.
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
49
2.1.4. Sales
La leche contiene una concentración inferior al 1 % de minerales. Las sales minerales se encuentran disueltas en el suero de la leche o formando compuestos como la caseína. Las sales más importantes son las de calcio, sodio, potasio y magnesio.
Las micelas de caseína contienen sales que no están disueltas, y se encuentran como fosfato de calcio coloidal, las cuales contienen también citratos. El fosfato de calcio es importante en la elaboración de quesos y en la parte nutricional, pues aporta calcio para el mantenimiento de los huesos.
2.2. Componentes minoritarios
2.2.1. Vitaminas
Las principales vitaminas presentes en la leche son: A, D, E y K (liposolubles), y B y C (hidrosolubles). Son susceptibles a destruirse por diversos tratamientos térmicos, por acción de la luz, por oxidaciones, etc.
2.2.2. Enzimas
Algunas de las enzimas más importantes en la leche son:
50
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os con pasteurización HTST, mientras que las lipasas producidas por bacterias son termo-resistentes.
■ Peroxidasa: Se encuentra naturalmente en la leche. Es una enzima oxidante, capaz de liberar oxígeno del peróxido de hidrógeno. Se destruye a temperaturas superiores a 80 °C. Se usa para detectar tratamientos térmicos fuertes en productos lácteos (Prueba de Storch).
■ Catalasa: Está asociada a la membrana del glóbulo graso, micelas y suero. Reacciona con el agua oxigenada liberando agua y oxígeno. Aumenta con los leucocitos, y es usada para detectar mastitis: los leucocitos poseen catalasa. Al adicionar agua oxigenada, el volumen de oxígeno producido es proporcional a la cantidad de leucocitos presentes. La catalasa también es producida por microorganismos. Se destruye a 75 °C durante 60 segundos.
■ Fosfatasa alcalina: Se encuentra el 80 % en la mem-brana del glóbulo graso, y el resto en la fase acuosa. Es natural en la leche, actúa a pH 9 - 10. Existe una fosfatasa ácida a pH 4, pero no tiene importancia tecnológica. La alcalina se inactiva a temperaturas de pasteurización, por lo cual es ampliamente usa-da en la industria lechera como control de pasteu-rización de la leche (Test de fosfatasa de Scharer).
■ Proteasa: Asociada a las micelas. Resistente al calor. Hidroliza las proteínas. Se encuentra en cantidades mínimas en la leche. Algunos microorganismos también producen proteasas como la Pseudomona.
Co
mp
osi
ci
ón q
uím
ic
a d
e l
a l
ec
he b
ov
in
a
51
reductasa que decolora el azul de metileno en presencia de formol.
Referencias bibliográficas
FOX, P.F. (2000). The major constituents of milk. In: Smit, G.Editor. Dairy Processing: Improving quality. (p 2-38). Cambridge, England. CRC PRESS.
TETRA PAK. (2003). Manual de Industrias Lácteas. A. Madrid Vicente. Ediciones. Madrid. 436p.
WALSTRA, P., WOUTERS, J., & GEURTS, T. (2006). Dairy Science and Technology. Second edition. Taylor & Francis. New York. 782p.
HUPPERTZ, T., KELLY, A., & FOX, P.F. (2009). “Milk lipids – Composition, Origin and Properties”. In: A.Y. TAMIME (Ed). Dairy Fats and Related Products. (pp 1-25). United Kingdom. Wiley Blackwell.
53
Capítulo 3
TOMA DE MUESTRAS
DE LECHE CRUDA
55
3.1. Introducción
E
n Colombia, el Ministerio de Agricultura y Desarrollo Rural mediante la Resolución 000017 de 2012, crea un sistema de pago de leche cruda por calidad, para mejorar la competitividad del sector lácteo colombiano. En esta Resolución los departamentos del país son agrupados, desde el punto de vista productivo, en dos regiones lecheras:Región 1: Cundinamarca, Boyacá, Antioquia, Quindío, Risaralda, Caldas, Nariño, Cauca y Valle del Cauca.
Región 2: Cesar, Guajira, Atlántico, Bolívar, Sucre, Córdoba, Chocó, Magdalena, Norte de Santander, Santander, Caquetá, Tolima, Huila, Meta, Orinoquía y Amazonía.
Para efectos del pago de leche cruda por calidad, se tienen en cuenta las valoraciones que realice el laboratorio de análisis, en términos de calidad composicional y calidad higiénica, definidos como sigue:
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
56
Calidad higiénica: es la condición que hace referencia al nivel de higiene mediante el cual se obtiene y manipula la leche. Su valoración se realiza por el recuento total de bacterias, y se expresa en unidades formadoras de colonia por mililitro (UFC/mL).
Para el pago de leche por calidad también se tienen en cuenta las bonificaciones por calidad sanitaria que el agente comprador de la leche cruda debe otorgar al proveedor de leche cuando los hatos se encuentren certificados como libres de brucelosis y/o tuberculosis, así como por buenas practicas ganaderas (BPG). Adicionalmente, el ganadero debe presentar el registro único de vacunación contra la fiebre aftosa y contra la brucelosis.
Por todo la mencionado, la toma de las muestras de leche cruda es determinante para disminuir la variabilidad en el análisis de la composición de la leche y en el recuento bacteriano. De esta manera, la industria puede realizar un pago adecuado de la leche por calidad y el productor recibe un precio justo por su leche. Adicionalmente, el análisis de calidad de leche cruda permite controlar la calidad de la leche que está entrando a la planta procesadora y el direccionamiento de la leche por aptitud tecnológica, a las diferentes líneas de producción.
3.2. Guía para tomar la muestra
3.2.1. Aspectos generales
G
uí
a p
ar
a l
a t
om
a d
e mu
es
tr
as d
e l
ec
he c
ru
da
57
alimentos. También debe portar una indumentaria apropiada: bata, gorro, guantes y tapabocas, y lavarse las manos antes de iniciar el muestreo.
Los materiales y equipos necesarios para la toma de muestra son: frascos estériles (50 mL), rótulos para identificar la muestra y nevera transportable para mantener las muestras refrigeradas con material refrigerante (Fig.3.1). Se requiere de un agitador para toma de muestra en cantina (Fig.3.2), un cucharón o toma-muestra (Fig. 3.3) y un termómetro.
Figura 3.1. Nevera portátil con muestras de leche cruda
Fuente: Autora
Figura 3.2. Agitador de émbolo para cantinas (Medidas en milímetros)
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
58
Figura 3.3. Toma-muestras para leche cruda
Fuente: Norma ISO 707:2008
3.2.2. Protocolo de toma de muestras
3.2.2.1. Agitación de la leche y control de
temperatura
Lo primero que debe hacerse para tomar la muestra es agitar la leche que se encuentra en el tanque, cantina o recipiente, sin hacer espuma.
G uí a p ar a l a t om a d e mu es tr as d e l ec he c ru da
59
y a la asociación de las bacterias con los glóbulos de grasa, lo que hace que ambos, bacterias y grasa, se concentren en la superficie. Por lo tanto, la agitación previa a tomar la muestra es muy importante para tomar una muestra homogénea y representativa (Goodrigde, Hill, & Lenki, 2004)
En el caso de leche en cantinas, debe agitarse con el agitador manual, mínimo un minuto, con movimientos circulares de arriba debajo, de manera pausada (Corpoica, 2008). En el caso de tanques de enfriamiento no hay acuerdo en algunos países; sin embargo, Corpoica menciona que se debe encender el agitador del tanque durante 5 minutos, si el tanque es menor a 5.000 L, o durante 10 minutos si el tanque es mayor a 5.000 L (Corpoica, 2008). En Estados Unidos, en Wisconsin, el tiempo es de 5 minutos, cuando el tanque tiene una capacidad inferior a 3.800 L, y por 10 minutos, para tanques superiores a los 3.800 L (Goodrigde, Hill, & Lenki, 2004). La International Dairy Federation (IDF) menciona que debe agitarse mecánicamente durante 5 minutos hasta obtener una leche homogénea; si el tanque está equipado con agitación periódica, puede realizarse una agitación más corta, de alrededor de 1 a 2 minutos para tomar la muestra (IDF, 1985).
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
60
Las muestras para análisis microbiológico deben recogerse primero usando técnicas asépticas.
Figura 3.4. Flameado de la toma de muestras con alcohol 96 %
Fuente: Autora
3.2.2.2. Toma de muestra
Después de la agitación, cuando la leche aún está en movimiento se sumerge el toma-muestras, se saca la muestra directamente al frasco esterilizado y se cierra herméticamente. El tamaño de la muestra dependerá del tipo de análisis, pero normalmente se toman 50 mL en duplicado. La primera muestra es para análisis microbiológico.
G
uí
a p
ar
a l
a t
om
a d
e mu
es
tr
as d
e l
ec
he c
ru
da
61
La muestra rotulada debe cerrarse herméticamente y colocarse en la nevera portátil para mantener la temperatura durante el transporte al laboratorio de análisis.
Figura 3.5. Toma de muestras de leche del tanque de enfriamiento.
Fuente: Autora
Referencias bibliográficas
GOODRIGDE, L., HILL, A., & LENKI, R. (2004). A review of international standards and the scientific literature on farm milk bulk-tank sampling protocols. Journal of Dairy Science,
8, 3099-3104.
CORPOICA. (2008). Protocolo de toma de muestras de leche cruda IN-R-528. Abril.
ISO 707:2008. Leche y productos lácteos. Directrices para la toma de muestras.
63
Capítulo 4
GUÍAS DE LABORATORIO
Figura 4. Guías de laboratorio65
4.1. Laboratorio No. 1
Análisis organoléptico y
fisicoquímico de leche cruda
4.1.1. Objetivos
Realizar e interpretar las pruebas fisicoquímicas básicas que se practican en la plataforma de recibo de leche cruda en la industria lechera.
Tomar decisiones sobre la compra de leche cruda para una central procesadora.
4.1.2. Prueba
Preparación de la muestra:
Mezcle la muestra, agitando e invirtiendo el recipiente varias veces. Si la mezcla presenta grumos de materia grasa, caliente la muestra a 40 °C en baño María, antes de mezclar.
4.1.2.1. Prueba organoléptica
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
66
en cantinas, esta prueba se debe realizar a cada una de ellas. El olor anormal de la leche aparece cerca de tres (3) horas antes de que la leche coagule a la prueba de ebullición.
En esta prueba organoléptica también se tiene que tener en cuenta el color, pues la presencia de sangre en la leche y el de una coloración amarilla muy intensa son indicios de problemas en la ubre o de presencia de calostro, respectivamente, y dicha leche debe ser rechazada.
4.1.2.2. Densidad (
ρ
)
La densidad de la leche es otra de las pruebas que se realizan en la plataforma de recepción, a diario, en la central lechera. Con esta prueba se pueden detectar rápidamente las adulteraciones más frecuentes que realizan a la leche: el aguado y el descremado.
La densidad de la leche disminuye por la adición de agua, de materia grasa o por aumento de temperatura.
La densidad promedio de la leche oscila entre; 1.027 y 1.033 g/mL, a 20 °C. Se puede determinar por método del picnómetro o termolactodensímetro.
4.1.2.2.1. Picnómetro
Es el método de referencia para determinar la densidad de la leche.
Materiales:
■ Un picnómetro de 25 mL
■ Balanza analítica
■ Una pipeta
G
uía
s d
e l
ab
or
at
ori
o
67
Procedimiento
Calibre la balanza analítica, pese el picnómetro limpio, seco y vacío, luego llene el picnómetro utilizando la pipeta con leche; pese de nuevo el picnómetro.
No olvide tomar la temperatura a la cual se encuentra la leche en el momento de la pesada.
Cálculos:
Densidad de leche = Peso de la muestra (g) / Volumen del picnómetro (mL)
Se debe corregir dicha lectura para tener en cuenta la temperatura a la cual fue tomada la densidad, así:
ρ
c=
ρ
t + (2*
10
-4) (T
°
C)
ρ
c = Densidad corregida a la temperatura de la determinación.ρ
t = Densidad encontrada a la temperatura T°C.T°C = Temperatura de la muestra durante la determinación.
Factor de corrección = (2 * 10-4)
4.1.2.2.2. Termolactodensímetro
G
uí
a d
e l
ab
or
at
or
ios
d
e l
ác
te
os
68
Materiales:
■ Termolactodensímetro de Quevénne 15 °C
■ Una probeta de 250 mL
■ Un platón pequeño plástico
■ Baño María a 40 °C
Procedimiento:
1. Homogenizar la muestra a la temperatura de 40 °C, agitando suavemente, enfriar y dejar en reposo durante unos minutos en un recipiente cerrado a 15 °C.
2. Agregar la leche a la probeta, teniendo esta inclinada con el fin de evitar la formación de espuma. Llenar la probeta.
3. Introducir con cuidado el termolactodensímetro en la probeta con la muestra.
4. Realizar un ligero movimiento rotatorio al densímetro. Esperar que se detenga y realizar la lectura.
5. Determinar la temperatura a la cual se hizo la lectura.
Corregir el valor, en caso de que la temperatura no fuera exactamente 15 °C, así: Sumar a la lectura obtenida 0.2 unidades por cada grado superior a 15 °C; por cada grado por debajo de 15 °C restar 0.2 unidades a la lectura obtenida.