i
UNIVERSIDAD DE GUAYAQUIL
FACULTAD PILOTO DE ODONTOLOGÍA
TRABAJO DE GRADUACIÓN PREVIO A LA OBTENCIÓN DEL
TÍTULO DE ODONTOLOGO
TEMA:
Aplicación del plasma rico en plaquetas (PRP) posterior a la exodoncia de
terceros molares
ANÁLISIS DE CASO
AUTOR:
Christian Alexander Chiluiza Vera
TUTOR:
Dr. Néstor Antepara López. MSc.
ii
APROBACIÓN DE LA TUTORIA
Por la presente certifico que he revisado y aprobado el trabajo de titulación cuyo tema es: “Aplicación del plasma rico en plaquetas (PRP) posterior a la
exodoncia de terceros molares”, presentado por el Sr Chiluiza Vera Christian
Alexander, del cual he sido su tutor, para su evaluación y sustentación, como
requisito previo para la obtención del título de Odontóloga.
Guayaquil, Mayo del 2016
……….
iii
UNIVERSIDAD DE GUAYAQUIL
FACULTAD DE ODONTOLOGÍA
CERTIFICACIÓN DE APROBACIÓN
Los abajo firmantes certifican que el trabajo de Grado previo a la obtención del Título de Odontólogo /a, es original y cumple con las exigencias académicas de la Facultad de Odontología, por consiguiente se aprueba.
……… ……….. Dr. Mario Ortiz San Martín, Esp. Dr. Miguel Álvarez Avilés, Mg.
Decano Subdecano
... Dr. Patricio Proaño Yela, Mg
iv
DECLARACIÓN DE AUTORÍA DE LA INVESTIGACIÓN
Yo, Christian Alexander Chiluiza Vera, con cédula de identidad N° 0941320780,
declaro ante el Consejo Directivo de la Facultad de Odontología de la Universidad de Guayaquil, que el trabajo realizado es de mi autoría y no contiene material que haya sido tomado de otros autores sin que este se encuentre referenciado.
Guayaquil, Mayo del 2016.
……….. Christian Alexander Chiluiza Vera
v
DEDICATORIA
vi
AGRADECIMIENTOS
Agradezco primero a Dios, que me brindo salud y fuerza y que me permitió alcanzar esta meta, agradezco por haberme dado unos abuelos y tías increíbles, que aportaron con todo lo que un hijo puede desear, agradezco a todas las personas que confiaron en mí, ya que fueron un motor durante este trayecto, agradezco por lo aprendido por todos mis docentes de la facultad Piloto de Odontología de la Universidad de Guayaquil, agradezco también a mi hermano, un gran amigo incondicional que me brindo sus experiencias y conocimientos, y a mi gran tutor Dr. Néstor Antepara López. Quien con paciencia y orientación logro este objetivo.
vii
CESIÓN DE DERECHOS DE AUTOR
Dr.
Mario Ortiz San Martín, MSc.
DECANO DE LA FACULTAD DE ODONTOLOGÍA Presente.
A través de este medio indico a Ud. que procedo a realizar la entrega de la Cesión de Derechos de autor en forma libre y voluntaria del trabajo “Aplicación del plasma rico en plaquetas (PRP) posterior a la exodoncia de terceros
molares”, realizado como requisito previo para la obtención del título de
Odontólogo, a la Universidad de Guayaquil.
Guayaquil, Mayo del 2016.
………. Christian Alexander Chiluiza Vera
viii
3.3. Fotos extraorales,intraorales, modelos de estudio, imágenes de RX….. 28
ix
ÍNDICE DE FOTOS
CONTENIDO Pág.
________________________________________________________
Foto 1.Odontograma ... 28
Foto 2.Vista frontal del paciente ... 29
Foto 3.Vista lateral ... 29
Foto 4. Arcada superior ... 30
Foto 5. Arcada inferior ... 30
Foto 6.Vista frontal de la oclusión ... 31
Foto 7.Vista lateral en oclusión ... 31
Foto 8.Vista frontal y lateral de modelo de estudio ... 32
Foto 9.Vista posterior del modelo de estudio ... 32
Foto 10. Radiografía panorámica ... 33
Foto 11.Radiografía panorámica preoperatoria ... 34
Foto 12.Colocación del paciente en el sillón dental ... 35
Foto 13.Extracción de la sangre en el brazo derecho ... 35
Foto 14.Colocación de la sangre en tubo de ensayo con anticoagulante ... 36
Foto 15. Mezcla de la sangre con anticoagulante ... 36
Foto 16. Colocación del tubo de ensayo con el material en la centrifuga ... 37
Foto 17.Centrifugación ... 37
Foto 18.Pipeteado ... 38
Foto 19.Colocación de tubo de ensayo con PRP en una rejilla ... 38
Foto 20.Asepsia extrabucal ... 39
Foto 21.Colocación del campo quirúrgico ... 39
Foto 22. Asepsia intrabucal ... 40
Foto 23. Anestesia troncular ... 40
Foto 24. Anestesia al nervio lingual, y bucal largo ... 41
Foto 25. Incisión (lineal) ... 41
Foto 26. Levantamiento de colgajo ... 42
Foto 27.Osteotomía ... 42
Foto 28.Luxación ... 43
Foto 29. Extracción propiamente dicha ... 43
Foto 30.Eliminación de residuos y lavado del alveolo ... 44
Foto 31. Aplicación del plasma rico en plaquetas ... 44
Foto 32.Sutura a punto separado ... 45
Foto 33. Asepsia intrabucal- extracción de la pieza #38 ... 45
Foto 34. Anestesia ... 46
x
Foto 36.Levantamiento de colgajo ... 47
Foto 37.Osteotomía ... 47
Foto 38. Luxación ... 48
Foto 39. Extracción propiamente dicha ... 48
Foto 40. Eliminación de residuos y lavado del alveolo ... 49
Foto 41. Sutura a punto separado ... 49
Foto 42.Piezas dentarias extraídas ... 50
Foto 43. Radiografía panorámica postquirúrgica ... 50
Foto 44. Inflamación post-quirúrgica ... 51
Foto 45. Instrumentos para la eliminación de los puntos de sutura ... 51
Foto 46. Asepsia extrabucal ... 52
Foto 47. Asepsia intrabucal ... 52
Foto 48. Retirada de los puntos de sutura del lado derecho inferior... 53
Foto 49. Retirada de los puntos de sutura del lado izquierdo inferior ... 53
Foto 50. Radiografía periapical lado derecha inferior ... 54
Foto 51. Radiografía periapical lado izquierdo inferior ... 54
Foto 52. Operador-Paciente ... 55
xi
RESUMEN
La extracción de terceros molares incluidos y retenidos es el procedimiento quirúrgico más frecuentemente realizado en la cirugía bucal y maxilofacial. En la gran mayoría de los casos, el paciente se recupera sin ningún problema, sin embargo, en algunas ocasiones, pueden presentarse complicaciones que pueden ser incomodas para el paciente. Una de esas complicaciones es la cicatrización retardada de la zona intervenida, lo que produce dolor e inflamación y un retraso en el proceso de regeneración del alvéolo. En ese sentido el plasma rico en plaquetas (PRP), se perfila como coadyuvante en los procesos de aceleración, en la cicatrización, regeneración y formación ósea, por lo que el objetivo de este estudio es evaluar el efecto del mismo. A tal efecto se realizó la intervención quirúrgica en un paciente de sexo femenino de 21 años de edad, que presentaba los terceros molares inferiores retenidos, bilateral. Se procedió a realizar la incisión correspondiente para las exodoncias de las piezas dentarias, después de haber hecho la extracción propiamente dicha de la piezas dentarias, se aplicó PRP, en uno de los lados (alveolo de la pieza 48-lado experimental), y al otro lado no se le aplico ningún biomaterial (lado de control).Los resultados obtenidos clínicos y radiográficamente posteriores a la exodoncia de los terceros molares dieron la conclusión que el PRP, acelero el proceso de regeneración ósea moderado y cicatrización de los tejidos blandos en un periodo de 7 días, logrando una regeneración ósea ostensible a los 21 días.
xii
ABSTRACT
The extraction of third molars and retained is the most frequently performed surgical procedure in the oral and maxillofacial surgery. In most cases, the patient recovers without any problems, however, in some cases; there may be complications that may be uncomfortable for the patient. One of these complications is the delayed healing of the surgical site, resulting in pain and inflammation and a delay in the regeneration process of the alveolus. In that sense the platelet-rich plasma (PRP) is emerging as an adjunct in the acceleration process, healing, regeneration and bone formation, so the aim of this study is to evaluate the effect thereof. To this end the surgery on a female patient of 21 years of age, who presented the lower third molars, bilateral performed. He proceeded to make the corresponding incision for extractions of teeth, having made such actual extraction of teeth, PRP was applied on one side (socket of the part 48-side experimental), and the other side will not apply any biomaterial (control side) .The clinical results and radiographically after the extraction of the third molars had the conclusion that the PRP, accelerated the process of moderate bone regeneration and healing of the soft tissues in a 7 day period, achieving an ostensible bone regeneration after 21 days.
1
1. INTRODUCCION
Las retenciones dentarias constituyen un tema importante de la Cirugía Oral, pues suponen una gran parte de las intervenciones quirúrgicas a este nivel. Cualquier diente puede sufrir la interrupción de su erupción, induciendo su retención total o parcial dentro de los procesos maxilares.Existen disímiles denominaciones de las inclusiones dentarias, a partir de las clasificaciones plasmadas por diferentes autores que han abordado el tema, de aquí que encontremos las definiciones de diente incluido, retenido, impactado y enclavado. (Escoda & Aytés, 2004; Medeiros, 2006; Huaygua Arpita & Zeballos López, Tratamiento quirurgico del incisivo retenido, 2012)
Estas retenciones tienen una alta prevalencia, y producen múltiples complicaciones. La fenomenología clínica es muy diversa, incidiendo los accidentes infecciosos, que son los más frecuentes y se deben usualmente a la desinclusión del diente, el cual queda en contacto con la cavidad bucal, siendo la manifestación más habitual la pericoronaritis. Los accidentes mecánicos radican en lisis ósea y radicular, desplazamiento de los dientes adyacentes, o accidentes protésicos. Los accidentes nerviosos son de tipo reflejoneurotrófico y se manifiestan como alergias faciales, placas de alopecia, blefarospasmos, reducción de la agudeza visual, presencia de lagrimeo y zumbidos de oídos. Los accidentes tumorales se refieren fundamentalmente a las formaciones quísticas. (Medeiros, 2006; Chiapasco, 2015)
Los terceros molares, muelas del juicio o cordal son piezas que, por su ubicación en la arcada dentaria, en especial los inferiores no erupcionan correctamente, quedando retenidos. El término muela del juicio se atribuye históricamente a Hieronimus Cardus: descensos, sapiencia e intelectos, haciendo referencia al sentido común.
2
asintomáticas, pero algunas veces participan en distintos procesos patológicos, donde comienzan a incomodar, ocasionando algunas veces fuertes dolores e inflamación en la zona afectada, también se puede presentar caries en la pieza 20 años y encontró que el 17% tenía al menos un diente incluido; de éstos el 47% correspondía a terceros molares (29,9% superiores y 17,1% inferiores) que eran susceptibles de ser extraídos, ya sea por motivos terapéuticos o profilácticos. (Gay Escoda & Aytés, Tratado de cirugia bucal, 2004)
Las frecuencias de patología inducida por el tercer molar son muy elevadas y en nuestro medio sobre todo el cordal inferior, debido a sus condiciones embriológicas y anatómicas. Los terceros molares nacen de un mismo cordón epitelial, con la singularidad de que el mamelón del tercer molar se desase del segundo molar, como si se tratara de un diente de reemplazo; su calcificación comienza desde los 8 a 10 años, su corona no termina hasta los 15 o 16 y la calcificación de sus raíces se completa a los 25 años de edad, erupcionando en un espacio muy limitado. En su crecimiento, el hueso, tiende a tirar hacia atrás las raíces no calcificadas de este molar, lo que explica la oblicuidad del eje de erupción que le hace chocar con la cara distal del segundo molar. (Gay Escoda & Aytés, 2004)
3
segundo molar, repetidos episodios de ricoronitis, lesiones cariosas irreversibles y razones ortodónticas. (Kuffel Vayas, Clasificacion de la posicion de los terceros molares y su mayor incidencia, 2011; Herrera Monteagudo, 2004; Huaygua Arpita & Zeballos López, Tratamiento quirúrgico del incisivo retenido, 2012)
La decisión de extracción del tercer molar en pacientes asintomáticos sigue siendo controversial. Se indica la extracción para reducir riesgos de secuela, morbilidad quirúrgica, complicaciones que involucran los dientes vecinos y mejorar la higiene bucal. Autores han reportado un incremento en la proporción de extracciones profilácticas de un 18 a un 40%, por lo general en pacientes que se encuentran entre 20 y 29 años de edad. La remoción quirúrgica de los terceros molares está asociada a una moderada incidencia de complicaciones, de alrededor de un 10%. Dentro de las más comunes se encuentran factores como el poco entrenamiento y corta experiencia del cirujano para realizar el procedimiento con mínimo trauma, fractura de porciones de raíz del tercer molar complejizando su extracción, en ocasiones desplazándolas al espacio submandibular, canal del nervio dentario inferior o seno maxilar; sangrado, osteítis alveolar o alvéolo seco que se presenta en un 20 a 25%, y con menos frecuencia infecciones post-extracción de terceros molares (1.7 a 2.7%) (Medeiros, 2006; Montilla Balon, 2011; Normando, 2015; Boughner, 2013; Vizuete Terán, 2012)
4
Clasificacion de la posicion de los terceros molares y su mayor incidencia, 2011; Montilla Balon, 2011; Boughner, 2013)
Para prevenir la aparición de complicaciones y obtener un correcto diagnóstico es obligado, previamente a la exodoncia, realizar un estudio radiográfico, que aportará una serie de datos indispensables para el adecuado tratamiento. Para ello, las exploraciones radiológicas habitualmente utilizadas son las intrabucales periapicales, para matizar la morfología, posición y relaciones; las oclusales, para diferenciar una situación vestibular o lingual respecto al segundo molar; y la radiografía panorámica, que proporciona una visión de conjunto. En ciertos casos, pueden también utilizarse la radiografía lateral de cráneo y la oblicua desenfilada. (Palma, García, Larrazabal, & Peñarrocha, 2010; Sanz, Barona, & Martínez, 2011)
Generalmente la remoción del tercer molar genera un impacto negativo durante los primeros 4 a 7 días después de la cirugía, observándose una mejoría en la calidad de vida del paciente al eliminar el dolor crónico e inflamación (comúnmente por pericoronitis). Estos resultados se han detallado en estudios que describen la mejoría que se presenta posterior al procedimiento quirúrgico. (Chiapasco, 2015; Montilla Balon, 2011; Miloro, Larsen, & Waite, 2011)
Las extracciones quirúrgicas del tercer molar incluido, ya sea por el bloqueo de otro diente o de hueso, por falta de espacio, por mal posición o cualquiera de las indicaciones ya mencionadas, es la intervención quirúrgica más frecuente de las que se realizan en la cavidad oral. El tratamiento del cordal incluido incluye tres fases bien diferenciadas: fase preoperatoria, acto quirúrgico y fase postoperatoria. (Montilla Balon, 2011; Herrera Monteagudo, 2004; Huaygua Arpita & Zeballos López, Tratamiento quirúrgico del incisivo retenido, 2012)
5
(Chiapasco, 2015; Gay Escoda & Aytés, Tratado de cirugia bucal, 2004; Montilla Balon, 2011)
En la fase postoperatoria pueden aparecer molestias que pueden ser muy variables, ya que aparecen en relación directa con la forma de manipulación de los tejidos blandos y duros durante el acto quirúrgico. Un mayor despegamiento mucoperióstico, una ostectomía muy amplia, una técnica quirúrgica traumática, un tratamiento previo insuficiente, actuaciones en fase aguda, darán como resultado un postoperatorio más doloroso. El curso postoperatorio normal tras la extracción del tercer molar incluido se caracteriza por ser relativamente molesto y por presentar, en mayor o menor medida, dolor, inflamación, sangrado y trismo; apareciendo incluso en ocasiones algunas décimas de fiebre durante varios días. (Chiapasco, 2015; Gay Escoda & Aytés, 2004; Miloro, Larsen, & Waite, 2011; Guarderas Barba, 2012)
El dolor presentado tras la cirugía del tercer molar es a menudo fácil de controlar con analgésicos como el paracetamol, o medicamentos del grupo AINES. El dolor más fuerte se produce durante las primeras 24-72 horas y disminuye paulatinamente en los días sucesivos, se puede prologar aproximadamente de una semana hasta 10 días. (Miloro, Larsen, & Waite, 2011; Chiapasco, 2015; Gay Escoda & Aytés, Tratado de cirugia bucal, 2004)
Con respecto a la inflamación, por lo general se un grado variable de la misma en la zona maseterina y submaxilar, aumentando durante las primeras 24-72 horas de postoperatorio. Para minimizar esta inflamación, es aconsejable que el paciente se aplique una bolsa de hielo, durante las 6 a 24 horas siguientes a la intervención quirúrgica, y el trauma quirúrgico. (Guarderas Barba, 2012)
6
la paciente ira adaptando su ritmo alimenticio dependiendo del grado de molestia que tenga. (Guarderas Barba, 2012; Chiapasco, 2015)
La extravasación de sangre de los vasos sanguíneos y su fluidez, en un procedimiento quirúrgico, se controla a partir de un proceso fisiológico llamado hemostasia, en el cual intervienen cuatro componentes; respuesta del vaso, actividad plaquetaria, cascada de la coagulación y sistema fíbrinolítico. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012)
La vasoconstricción es la primera respuesta hemostática que tiene lugar tras la lesión de un vaso y se debe fundamentalmente a la acción de la musculatura lisa del vaso. A continuación, ocurre una actividad plaquetaria en la cual las plaquetas como componentes celulares de la sangre se caracterizan por la ausencia de un núcleo y tienen un promedio de vida en la circulación aproximadamente 8 a 12 días. Durante esta fase, las plaquetas liberan gránulos que ayudan a atraer más plaquetas al sitio de la lesión y ayudar así a la estabilización del coagulo inmaduro. En este proceso conocido como desgranulación plaquetaria, se incluyen gránulos densos, gránulos, y Tomboxano A2, las cuales funcionan como agentes quimiotácticos y promueven agregación, desgranulación continua, y más vasoconstricción, lo cual ayuda a la formación de tapón más estable. Los cambios en los receptores de la membrana de las plaquetas, más la conversión de factores de coagulación, consolidan el tapón plaquetario con fibrina, el cual genera un coagulo sanguíneo estable y apropiado. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012)
7
que el factor X es activado y termina con la formación de fibrina. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012)
La fase fibrinolítica es un componente importante de la hemostasia, ya que tiene como función principal la de evitar la oclusión trombólitica de los vasos sanguíneos y la propagación de la coagulación a través de todo el sistema vascular. Este proceso ocurre de manera temprana durante el proceso de coagulación, y consiste en la activación del plasminógeno, el cual es dividido en pequeños fragmentos que se llaman productos degradados de fibrina, y tienen un efecto anticoagulante. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012)
Independientemente de la causa que originó la lesión, en la herida se inicia un proceso llamado cicatrización, el cual tiene como fin trabajar para devolver la integridad al tejido afectado. La cicatrización es el efecto de la regeneración de los tejidos y del cierre de una herida; no es un fenómeno aislado y su evolución está limitada por varios factores bioquímicos a nivel de la solución de continuidad que representa la lesión, por cambios en las estructuras tisulares y por procesos que determinan la formación de la cicatriz. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012; Teller & White, 2010)
8
epitelial. Una vez que la herida está totalmente epitelizada, la costra se ablanda y desprende fácilmente. (Teller & White, 2010)
El proceso de cicatrización de la herida puede ser dividido en tres etapas básicas: inflamación, fibroblástica y remodelación, las cuales tienen lugar de manera progresiva. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012; Lopategui Corsino, 2012; Teller & White, 2010)
La etapa de inflamación comienza inmediatamente después de que el tejido es lesionado y en ausencia de factores que la prolonguen, dura aproximadamente de 3 a 5 días, existiendo dos fases: vascular y celular. La fase vascular ocurre cuando empieza la hinchazón, inicialmente con una vasoconstricción debido a la ruptura celular, con la finalidad de disminuir la pérdida de sangre en el área de la lesión, y a su vez promover la coagulación sanguínea. Varios minutos después, la histamina y las prostaglandinas e1 y e2, elaboradas por los leucocitos causan vasodilatación y aumento de la permeabilidad al crear pequeñas aberturas entre las células endoteliales, lo cual permite el escape de plasma y leucocitos que migran hacia los espacios intersticiales, facilitando la dilución de los contaminantes y generando una colección de fluidos que es conocido como edema. Los signos propios son eritema, edema, dolor, calor y pérdida de la función. El calor y el eritema son causados por la vasodilatación; el edema es producido por la trasudación de líquidos; el dolor y la pérdida de la función son causadas por la histamina, quininas y prostaglandinas liberadas por los leucocitos, así como por la presión del edema. (Teller & White, 2010; Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012)
9
en contacto con el material extraño (por ejemplo, una bacteria) los neutrófilos liberan el contenido de sus lisosomas (desgranulalización). Las enzimas lisosómicas (formadas fundamentalmente por proteasas y proteínas antimicrobianas llamadas defensinas) laboran para destruir las bacterias y otros materiales extraños y para digerir tejido necrótico. Este proceso es también ayudado por los monocitos quienes de la sangre penetran en los tejidos transformándose en macrófagos tisulares, los cuales fagocitan cuerpos extraños y tejidos necróticos. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012; Lopategui Corsino, 2012; Teller & White, 2010)
Con el tiempo aparecen dos grupos de linfocitos: B y T. Los linfocitos B son estimulan a las células β para su proliferación y diferenciación; los T supresores que trabajan para regular a los T ayudadores en su función; y los T citotóxicos, que lisan células que se presentan como extrañas. Durante la inflamación, pequeñas cantidades de fibrina son depositadas para permitir a la herida resistir ciertas fuerzas de tensión. (Teller & White, 2010; Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012)
10
factor quimiotáctico de los fibroblastos, y ayudar a guiar a los macrófagos en su actividad fagocitaría a lo largo de la red de fibrina. (Teller & White, 2010; Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012)
Esta etapa continúa con el incremento de nuevas células. La fibrinólisis ocurre causada por la plasmina, que aparece en los nuevos capilares y remueve la red de fibrina innecesariamente elaborada. Los fibroblastos depositan el tropocolágeno, precursor del colágeno comenzando por debajo y atravesando la herida. Inicialmente el colágeno es producido en exceso y puesto de una manera poco organizada, esta sobreabundancia de colágeno es necesaria para darle cierta fuerza al área de la herida. Debido a la deficiente orientación de las fibras de colágeno la herida no es capaz de resistir fuerzas de tensión durante esta fase, la cual dura de 2 a 3 semanas por lo que, si es sometida a alguna tensión al comienzo de la fase fibroblástica, se tiende a maltratar la línea de la lesión. Clínicamente al final de este período la herida se presenta dura, debido al excesivo acumulo de colágeno y eritematosa por el alto grado de vascularización. La herida alcanza entre 70% y 80% de la resistencia a la tensión respecto al tejido antes de ser lesionado. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012; Lopategui Corsino, 2012; Teller & White, 2010)
11
casos juega un papel importante en la reparación de la herida pues durante este período, los bordes migran hacia el centro y la contracción disminuye el tamaño de la misma, beneficiando al tejido. No obstante, la contracción puede causar problemas, tal es el caso de las quemaduras cutáneas de tercer grado, en las que se produce deformidad y se debilita la piel. Otra desventaja de la contracción se ve en individuos que sufren cortes curvos en su piel, en los que frecuentemente se produce una eversión al ser aproximados los bordes. (Mas, 2008; Teller & White, 2010; Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012) El cirujano bucal puede crear las condiciones que favorezcan o no el normal proceso de cicatrización. Adhiriéndose a los principios quirúrgicos de restablecer la continuidad de los tejidos, minimizando el tamaño de la herida y restaurando posteriormente la función, se facilita el proceso de cicatrización. El cirujano debe dirigir sus esfuerzos a reducir la pérdida de la función y a lograr, en la medida de lo posible, una mínima cicatriz, aunque las heridas de piel, músculos, ligamentos y mucosa bucal nunca sanan sin dejar cicatriz. Los factores que interfieren en el normal proceso de cicatrización de las heridas pueden ser clasificados en dos categorías: factores locales, los cuales son fácilmente controlables por el cirujano bucal, y factores generales, más complejos y difíciles de reconocer, ya que muchas veces pueden actuar de una forma desconocida. (Mas, 2008; Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012; Teller & White, 2010) Entre los factores locales podemos señalar los cuerpos extraños, tejido necrótico, isquemia, tensión; además de infecciones, irradiación previa sobre la piel, mala orientación y manipulación brusca de los bordes de la herida, entre otros. (Mas, 2008; Teller & White, 2010)
12
El tejido necrótico puede causar dos problemas. En primer lugar, sirve de barrera que interfiere en la acción reparativa de las células. La inflamación aumenta debido a que los leucocitos deben eliminar los restos de tejido mediante un proceso de fagocitosis y lisis. El segundo problema que puede generar es que el tejido necrótico es un nicho importante para la proliferación de bacterias, ya que puede contener sangre acumulada en la herida (hematoma) que constituye una excelente fuente de nutrientes para el crecimiento de las mismas. (Mas, 2008) La isquemia de la herida interfiere en su cicatrización por diversas causas; además de promover la necrosis provoca una disminución en la migración de los anticuerpos, leucocitos, antibióticos, entre otros, aumentando las probabilidades de una infección, así mismo reduce el aporte de oxígeno y los nutrientes necesarios para la reparación de la herida. Entre las posibles causas de isquemia podemos indicar: diseño incorrecto del colgajo, presión externa sobre la herida, presión interna sobre la herida (hematoma), anemias, ubicación incorrecta de las suturas, entre otros. (Mas, 2008)
La tensión sobre una herida es un factor que impide su cicatrización. Si la sutura es colocada con una excesiva tensión, va a estrangular los tejidos, produciendo isquemia. Si la sutura es removida antes de tiempo, existe el riesgo de la reapertura de la herida lo que produciría una cicatriz mucho mayor; si esta es removida tardíamente se corre el riesgo de dejar marcas desfigurativas cuando la epitelización sigue la vía de las mismas.
13
tamaño de esta ya que en un área con mayor aporte vascular el proceso de cicatrización será mucho más efectivo, de la misma forma una herida amplia tarda más en recuperarse que una de menor tamaño. (Fernández-Delgado, Hernández-Ramírez, & Forrellat-Barrios, 2012; Teller & White, 2010; Mas, 2008)
Según la unión de los bordes, la cicatrización puede ser por “primera intención” y “segunda intención”. En la cicatrización por primera intención, los márgenes de la herida están en contacto, es decir, tiene los planos cerrados, estando suturada o no, por lo tanto, los bordes de la herida en la cual no ha ocurrido pérdida de tejido son colocados en la posición anatómica exacta en que se encontraban antes de la lesión. La herida se repara con una mínima formación de cicatriz, estrictamente hablando es una teoría ideal, imposible de alcanzar clínicamente; no obstante, el término es generalmente usado para recalcar que los bordes de una herida son reaproximados. Este proceso de cicatrización requiere de una menor epitelización, depósito de colágeno, contracción y remodelación, por lo tanto, la cicatrización ocurre mucho más rápido, con un bajo riesgo de infección y con una menor formación de cicatriz que en las heridas que lo hacen por segunda intención. Ejemplos de este tipo de reparación son, la reducción adecuada de fracturas de hueso, reposición de laceraciones, colgajos y reanastómosis anatómica de los nervios. (Teller & White, 2010; Mas, 2008)
14
cicatrización por primera intención existiendo un mayor riesgo de infección en la herida. Ejemplos de este tipo de cicatrización son la del alvéolo dentario posterior a una exodoncia, fracturas pobremente reducidas y lesiones muy aparatosas con pérdida de tejido. Algunos cirujanos utilizan el término de cicatrización por tercera intención o cierre primario diferido, para referirse a la cicatrización que ocurre cuando se cierra una herida después de un período de cicatrización por segunda intención, la cual se realiza cuando se está seguro de que se ha superado el riesgo de infección. (Mas, 2008; Teller & White, 2010; Lopategui Corsino, 2012) Tras la extracción de un diente, se forma un coágulo de sangre en el alveolo y comienza el proceso de cicatrización, el cual ocurre por segunda intención. Los sucesos de cicatrización temprana incluyen la formación de tejido de granulación en el alveolo, el cual es progresivamente sustituido por hueso neoformado. El proceso de cicatrización se considera finalizado a los 4-6 meses, una vez tiene lugar la remodelación ósea. Paralelamente a este proceso se produce una reabsorción fisiológica del reborde alveolar, reduciendo la cantidad de soporte óseo, la cual puede suponer un problema, ya que la rápida pérdida ósea post-extracción puede afectar a los dientes adyacentes, comprometiendo su estabilidad y causando recesión tisular. La mayor cantidad de pérdida ósea tiene lugar en sentido horizontal, principalmente en la superficie vestibular, causando estrechamiento del reborde alveolar. También tiene lugar una pérdida ósea vertical continuada, más pronunciada en la cortical vestibular. (Boughner, 2013; Chiapasco, 2015; Huaygua Arpita & Zeballos López, Tratamiento quirúrgico del incisivo retenido, 2012)
15
sistemáticos al respecto. (Castillo, y otros, 2010; Fierro-Serna, Martínez-Rider, Hidalgo-Hurtado, Toranzo-Fernández, & Pozos-Guillén, 2011)
La atención en el tema del plasma rico en plaquetas aplicado en cirugía oral ha venido aumentando en las últimas 3 décadas con un gran número de investigaciones que han tratado de soportar su uso para el mejoramiento de los procesos de reparación y regeneración de tejidos blandos y óseos respectivamente. (Castillo, y otros, 2010; Manoochehri, Vielma, & Castillo, Plasma Rico en Plaquetas (PRP) en la regeneración ósea de aleveólos post extracción, 2014)
El plasma rico en plaquetas (PRP) tiene sus antecedentes en 1994 cuando un grupo de cirujanos empleó la adición de un adhesivo de fibrina autógena al hueso esponjoso en una reconstrucción mandibular. Para ello acudieron a la separación de una muestra de sangre en sus componentes y utilizaron la fracción plasmática como crioprecipitado. Observaron una consolidación ósea precoz. (Barona-Dorado, González-Regueiro, Martín-Ares, Arias-Irimia, & Martínez-González, 2014)
Posteriormente Whitman propone el uso de plasma rico en plaquetas y detallaba las diferencias entre el pegamento de fibrina y el gel de plaquetas, destacando que en este último se obtenía un gel con alta concentración de plaquetas por medio de un proceso de sangre extraída del paciente momentos antes de la intervención quirúrgica, las cuales activaban la liberación de factores de crecimiento que promovían una mejor cicatrización. (Whitman, Berry, & Green, 1997)
16
17
El plasma rico en plaquetas autólogo está compuesto por una porción plasmática que posee una concentración elevada de plaquetas superior a 2 a 5 veces al número de plaquetas en sangre periférica. La cantidad de plaquetas que se encuentra en la sangre periférica es alrededor de 200 plaquetas × 103 /μl. Se ha considerado que la concentración de 1000 × 103/μl, es el valor ideal para asegurar un aporte de FC óptimo para estimular la consolidación de huesos y tejidos blandos sin causar ningún efecto negativo. Sin embargo, se ha comprobado que concentraciones menores pueden equiparar los efectos beneficiosos de preparados de PRP con cantidades superiores de plaquetas. (Barona-Dorado, González-Regueiro, Martín-Ares, Arias-Irimia, & Martínez-González, 2014; Castillo, y otros, 2010)
18
Los factores de crecimiento son una familia de señales peptídicas moleculares capaces de modificar las respuestas biológicas celulares, estando involucradas en el control del crecimiento y diferenciación celular. Son mediadores biológicos que regulan la migración, proliferación, diferenciación y metabolismo celular. En cuanto a su clasificación, los FC se pueden clasificar según sea su especialidad: amplia o reducida. Los de especialidad amplia como el PDGF y el EGF actúan sobre muchas clases de células, entre ellas tenemos: fibroblastos, fibras musculares lisas, células neurogliales y el último, además, sobre células epiteliales y no epiteliales. Como ejemplo de FC de especificidad reducida tenemos a la eritropoyetina que sólo induce la proliferación de los precursores de los hematíes. (Mozzati, y otros, 2010; Murga López, 2003)
Los factores de crecimiento actúan de manera local. La estimulación celular se realiza bien por un sistema autocrino, es decir, las células producen y responden al mediador biológico, o por un sistema paracrino en el que la célula que produce el factor se encuentra en las proximidades de las células a las que afecta. En general, los factores de crecimiento son sintetizados en forma de precursores, siendo necesario para la liberación del factor en forma "activa" un proceso específico de proteolisis. (Mozzati, y otros, 2010)
19
factores de crecimiento óseo son activados ante cualquier noxa que altere la morfología estructural o celular del tejido óseo. Se incluyen como desencadenantes de activación de los factores: el traumatismo, accidental o quirúrgico, del tejido óseo como la pérdida dental o la colocación de implantes, la interrupción temporal del aporte vascular asociado a la desvitalización y necrosis del tejido óseo, e incluso las alteraciones humorales con repercusiones en el metabolismo del calcio. (Mozzati, y otros, 2010)
Estudios específicos han identificado al PRP tres importantes factores de crecimiento en los gránulos de las plaquetas obtenidas de los cuales tenemos: FACTOR DE CRECIMIENTO DERIVADO DE PLAQUETAS (PDGF), que favorece la mitogénesis (causando un incremento en el número de células reparadoras), y angiogénesis (generando el desarrollo de nuevos capilares). Se encuentra por primera vez en las plaquetas, donde se almacena dentro de los gránulos alfa, pero también es producido por otros tipos celulares como son los macrófagos, células endoteliales, monocitos, fibroblastos, hallándose también en la matriz ósea. Según las cadenas que formen la estructura del factor de crecimiento, nos encontramos con tres formas: PDGF-AA, PDGF-BB Y PDGF-AB. Entre sus acciones biológicas podemos destacar:
Participación en la glucogénesis.
Regulación del crecimiento y diferenciación celular en el sistema nervioso central durante su desarrollo.
Favorece la cicatrización. Su función en la reparación tisular se basa en inducir la mitogénesis (aumentar el número de células para la cicatrización), estimular la angiogénesis de la mitosis de células endoteliales (lo cual se traduce en la formación de yemas capilares), producción de proteínas de la matriz extracelular y en la quimiotaxis de fibroblastos, monocitos, células musculares y macrófagos. También estimula la fagocitosis en los neutrófilos y monocitos.
20 Se ha involucrado en el desarrollo de agrandamientos gingivales tras la toma de fenitoína. La fenitoína aumentaba la producción de pdgf por los macrófagos y la excesiva producción de este factor en la encía provocaba su hipertrofia.
Puede estimular las somatomedinas.
Aumenta la regeneración periodontal.
FACTOR DE CRECIEMIENTO TRANSFORMANTE-B1 (TGF-B1), favorece la formación matriz colágena de los capilares y matriz ósea.
FACTOR DE CRECIMIENTO TRANSFORMANTE-B2 (TGF-B2), favorece la formación de matriz colágena de los capilares y matriz ósea, y además también la presencia del FACTOR DE CRECIMIENTO SEMEJANTE A INSULINA (IGF-1), que favorece el alineamiento de las trabéculas de hueso injertado. La IGF son mitogénicos para los osteoblastos y estimulan la formación ósea de osteoblastos diferenciados existentes, y su vez promueve la deposición de matriz ósea.
Los métodos de obtención del plasma rico en factores de crecimiento y plasma rico en plaquetas varían en varios aspectos. Para la obtención de plasma rico en plaquetas existen diversos sistemas donde se requieren 60 cc. de sangre (SmartPRep, PCCS, Secquire, Acces, GPS, Magellan) hasta 450 cc. (CATS), aunque algunas de ellas no están estandarizadas o aprobadas. (Castillo, y otros, 2010; Garay, Altuve, Gonzalez, & Yepez, Plasma Rico en Plaquetas en la cicatrización de tejidos blandos de la cavidad bucal, 2014)
Tal vez el más popularizado es el sistema SmartPRep en el que se extrae la sangre del mismo paciente minutos antes de comenzar la cirugía. El hecho de realizar la extracción de sangre de forma previa y no utilizar sangre resultante de la cirugía es porque la cirugía, por si misma, implica la activación de los factores de coagulación. (Rutkowski, Johnson, Radio, & Fennell, 2010; Manoochehri, Vielma, & Castillo, Plasma Rico en Plaquetas (PRP) en la regeneración ósea de aleveólos post extracción, 2014)
21
digital a una velocidad de 2500 revoluciones por minuto a temperatura ambiente. Posteriormente se separa el plasma en fracciones mediante pipeteado muy meticuloso para no crear turbulencias. (Rutkowski, Johnson, Radio, & Fennell, 2010)
Los primeros 0.5 cc (fracción 1), es un plasma pobre en plaquetas y por lo tanto pobre en factores de crecimiento, los siguientes 0.5 cc (fracción 2), corresponde a un plasma con un número similar al de la sangre periférica, y la (fracción 3), corresponde al plasma rico en plaquetas. Como se utilizaron tubos con anticoagulantes no se corre el riesgo de que se solidifique el PRP. Se ha demostrado que las plaquetas más recientemente sintetizadas y, por lo tanto, con una gran actividad, son grandes y están mezcladas con el primer milímetro de la fracción de células rojas, por lo que algunos autores proponen el utilizar también esta pequeña parte. Si cogemos las dos primeras fracciones y las añadimos también cloruro cálcico obtenemos fibrina autóloga que se puede utilizar como membrana o tapón hemostático, dado su alto poder cicatrizante. (Rutkowski, Johnson, Radio, & Fennell, 2010)
Una vez obtenido el PRP coloca el tubo en una rejilla y se procede posteriormente a la extracción de los terceros molares. Realizada las exodoncias es aplicada la solución en el lado que deseamos que haga el efecto la solución.
Las ventajas que presenta el empleo del PRP es que es autólogo, no tóxico, no inmunogénico, no existe ningún riesgo de contagio de infección, de fácil obtención, realza y acelera las vías normales de regeneración y cicatrización de los tejidos blandos y duros, es de bajo costo, respecto a otros procedimientos de regeneración, es una técnica de aplicación sencilla. Ayuda a obtener un efecto hemostático, así como un aumento en la velocidad de cicatrización.
22
de 6 años, los ancianos u otros con determinadas condiciones sistémicas. La incorporación de PRP en el protocolo para el tratamiento de fracasos implantarios acelera la cicatrización y maduración de los tejidos injertados.
El PRP resulta válido absolutamente para todos los pacientes, resultando imprescindible para pacientes de riesgo como fumadores, pues son dos mundos diferentes la epitelización de un fumador con o sin factores de crecimiento. (Barona-Dorado, González-Regueiro, Martín-Ares, Arias-Irimia, & Martínez-González, 2014; Castillo, y otros, 2010; Rutkowski, Johnson, Radio, & Fennell, 2010)
El PRP es el complemento ideal para los injertos, ya que sirve para compactar y retener el material de injerto, tanto autólogo como cualquier biomaterial, aportando estabilidad y adhesión. Además, es un excelente osteoconductor y osteoinductor. Se trata de un material autólogo y por lo tanto con nulo efecto antigénico. No hay riesgo de contagio de ningún tipo de enfermedad y, por último, la fibrina autóloga obtenida con el PRP se puede utilizar a modo de membrana biológica para retener el injerto. (Manoochehri, Vielma, & Castillo, Plasma Rico en Plaquetas (PRP) en la regeneración ósea de aleveólos post extracción, 2014; Rutkowski, Johnson, Radio, & Fennell, 2010)
En este ambiente la cicatrización ósea comienza por la liberación de factores de crecimiento del injerto, inmediatamente después de haber ocurrido la ruptura de los alfa gránulos plaquetarios, quienes actúan como mediadores biológicos, promoviendo la migración, proliferación y dispersión de las células encargadas de la reparación, regeneración y remodelación ósea.
23
maduración de osteoblastos funcionales. El IGF actúa en los osteoblastos endosteales que alinean las trabéculas del hueso injertado.
A pesar de su popularidad, el PRP tiene una pobre evidencia, esto gracias a la pequeña muestra de sujetos de cada estudio, ausencia de estudios controlados, y que la mayoría de estos son reportes anecdóticos o de una pequeña serie de casos. (Hernández, 2008)
Resultados sobre la eficacia del PRP, demuestran que el uso del plasma rico en plaquetas acelera la cicatrización de los tejidos en los primeros días posterior a la extracción de los terceros molares y así como también la formación del hueso alveolar.
Castillo I, y col realizaron un caso de tercer molar retenido, mediante la aplicación del PRP, y llegaron a la conclusión que puede ser utilizado para inducir la cicatrización de tejidos blando y la regeneración ósea, en el caso de problemas de retardada cicatrización, luego de la extracción de los terceros molares. (Castillo,2012)
Fierro-Serna, de la facultad de Estomatología de la Universidad Autónoma de San Luis, sugirió que el uso de plasma rico en plaquetas beneficia el postoperatorio de los pacientes después de la remoción quirúrgica de los terceros molares inferiores, debido a que estos dientes son más complicados para su extracción. (Fierro-Serna, Martínez-Rider, Hidalgo-Hurtado, Toranzo-Fernández, & Pozos-Guillén, 2011)
En sentido general se han establecido varias aplicaciones clínicas del PRP en el campo del campo de la cirugía oral y maxilofacial, a saber:
- Reconstrucción de rebordes alveolares atróficos. - Elevación de seno maxilar.
- Relleno de cavidades quísticas post quistectomía.
- En exodoncias múltiples, para conservar la altura del reborde alveolar.
24
- En defectos óseos periapicales, luego de una apicectomía, por ejemplo.
- Regeneración ósea alrededor de implantes osteointegrados, rellenando el defecto inmediatamente luego de haber colocado el o los implantes.
- En injertos óseos en bloque, para rellenar la zona donante, estimulando su regeneración y para cubrir y ayudar a remodelar el bloque a utilizar, compactándose las zonas limítrofes del injerto, evitando así los escalones óseos.
- Reconstrucción de grandes defectos óseos post cirugía oncológica.
En cuanto a sus desventajas el PRP podemos mencionar que el PRP requiere de material y equipo sofisticado para su procedimiento, así también como el de cumplir rigorosamente los protocolos de Hematología clínica.
En un artículo realizado por el Dr. Martínez - González et al en la revista medicina oral de 2002, se postula una posible relación entre el uso de PRP y la aparición de tumores malignos. Se basan en que es conocido que en la carcinogénesis las sustancias promotoras van a actuar únicamente sobre el aumento de la proliferación celular en los clones de células inicialmente mutadas mediante la modificación de algunos procedimientos bioquímicos celulares. Si no se promoviera la mitogénesis de esas células inicialmente mutadas, los mecanismos de control podrían desencadenar la muerte de esa célula alterada antes de que pudiera llegar a su diferenciación final. Así pues, los concentrados terapéuticos de factores de crecimiento podrían actuar, más que como iniciadores, como promotores en la carcinogénesis, favoreciendo la división y promoción de células previamente mutadas o "iniciadas" en la carcinogénesis. Sin embargo, este fenómeno podría necesitar de dosis más continuadas en el tiempo que las que se aplican en la terapéutica del PRP, teniendo en cuenta que los factores de crecimiento extracelulares se degradan a los 7-10 días. (Martinez-González, 2002)
25
26
2. OBJETIVO
27
3. DESARROLLO DEL CASO
3.1. HISTORIA CLÍNICA DEL PACIENTE (Anexo 2)
3.1.1. Identificación del paciente (Anexo 2)
Nombres: Génesis Teresa
Apellidos: Flores Barzola
Edad: 21
Género: Femenino
Ocupación: Auxiliar de Enfermería
Estado civil: Soltera
3.1.2. Motivo de consulta
La paciente acude a la consulta porque manifiesta: “Tengo virados los dientes y me voy a poner ortodoncia”.
3.1.3. Anamnesis
El paciente no presenta antecedentes familiares, es asintomático y no refiere patologías aparentes. Presenta una presión arterial de 120/83 mm/Hg, una frecuencia cardiaca de 75 latidos por minuto, una temperatura de 38° C, una frecuencia de 20 respiraciones por minuto. Por lo tanto, es un paciente con el sistema inmunitario normal y con un pronóstico favorable para la extracción de los terceros molares.
3.2. ODONTOGRAMA
El examen clínico dental lo registramos en el odontograma, obteniendo los siguientes datos:
-No presenta ningún diente perdido por caries. -Caries en las piezas: 2.7, 3.6, 4.6, 4.7.
-Restauraciones de resina en las piezas: 1.4.
28 Foto 1.Odontograma
-No presenta movilidad dentaria. -No presenta recesión gingival.
-No presenta índice de placa bacteriana.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
3.3. FOTOS EXTRAORALES, INTRAORALES, MODELOS DE ESTUDIO,
IMÁGENES DE RX.
29 Foto 3.Vista lateral
IMAGEN FRONTAL Y LATERAL
Fuente: Propia de la investigación
Autor: Christian Chiluiza
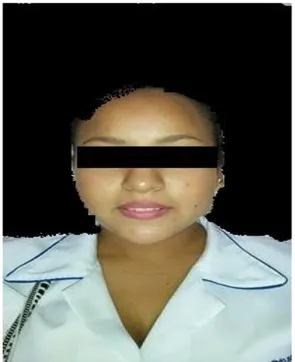
Foto 2.Vista frontal del paciente con un tipo de craneo braquicefalico.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 3. Vista lateral de la paciente donde se observa un perfil convexo
30 Foto 4. Arcada superior
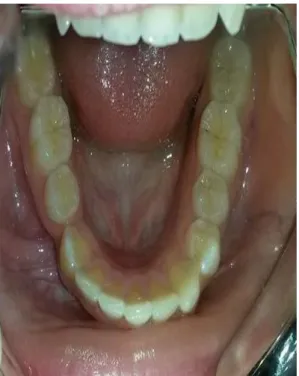
Foto 5. Arcada inferior
FOTOS INTRAORALES: OCLUSALES
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Fuente: Propia de la investigación
Autor: Christian Chiluiza
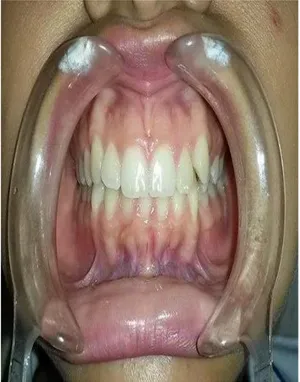
31 Foto 6.Vista frontal de la oclusión
Foto 7.Vista lateral en oclusión IMÁGEN DE ARCADAS EN OCLUSION
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 6. Vista frontal de la oclusión donde se observa una relación oclusal clase I.
IMAGEN DE ARCADAS EN OCLUSION
Fuente: Propia de la investigación
Autor: Christian Chiluiza
32 Foto 8.Vista frontal y lateral de modelo de estudio
Foto 9.Vista posterior del modelo de estudio MODELOS DE ESTUDIO
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 8. Vista frontal y lateral de modelos de estudio que constituyen un elemento fundamental para el diagnóstico.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
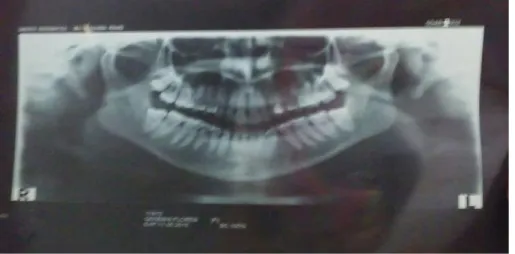
33 Foto 10. Radiografía panorámica
IMÁGENES RADIOGRÁFICAS
.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 10.Radiografía panorámica: Se puede observar la presencia de los terceros molares superiores en posición vertical y los inferiores en posición mesioangular, debajo de la línea de oclusión. Además, presentan sombra radiopaca compatible con material restaurar en las piezas 1.4; 1.7. Trabeculado ósea normal y ápice y periápice normal.
3.4. DIAGNÓSTICO
-El paciente no presenta edentulismo parcial ni total. -Presenta caries en las piezas: 2.7; 3.6; 4.6; 4.7. -No presenta restauraciones defectuosas.
-No presenta tratamiento endodóntico.
-No presenta coronas ni carillas de cerámica. -No presenta retracción gingival.
34 Foto 11.Radiografía panorámica preoperatoria
4. PRONÓSTICO
El pronóstico del paciente es favorable para la extracción de los terceros molares, ya que no presenta ninguna patología ni enfermedades sistémicas que puedan impedir la extracción de dichas piezas.
5. PLANES DE TRATAMIENTO
-Aplicación de la fibrina rica en plaquetas (PRF), en la cirugía de terceros molares retenidos.
-Aplicación de membrana de quitosano para la regeneración osteomucosa posterior a la extracción de terceros molares.
-Aplicación del plasma rico en plaquetas posterior a la exodoncia de terceros molares.
5.1. TRATAMIENTO
Aplicación del plasma rico en plaquetas posterior a la exodoncia de terceros molares.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
35
Fuente: Propia de la investigación
Autor: Christian Chiluiza
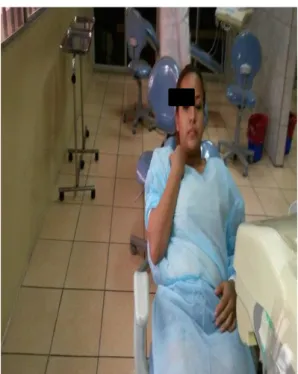
Foto 12. Colocación del paciente en el sillón dental para su posterior intervención.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
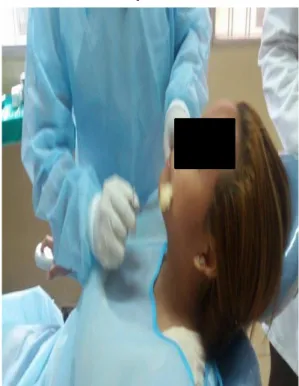
Foto 13. Extracción de sangre en el brazo derecho de la paciente unos minutos antes de iniciar la cirugía de los terceros molares. Se extraerá 10 cc de sangre.
36 Foto 15. Mezcla de la sangre con anticoagulante
Foto 14.Colocación de la sangre en tubo de ensayo con anticoagulante
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 14. Se coloca la sangre en tubo de ensayo con anticoagulante (citrato de sodio)
Fuente: Propia de la investigación
Autor: Christian Chiluiza
37 Foto 16. Colocación del tubo de ensayo con el material en la centrifuga
Foto 17.Centrifugación
Fuente: Propia de la investigación
Autor: Christian Chiluiza
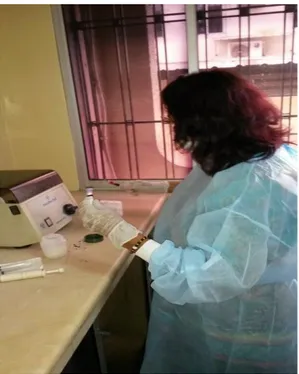
Foto 16. Colocación del tubo a la centrifuga que nos permitirá alcanzar unas 2.500 revoluciones por minuto.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
38 Foto 19.Colocación de tubo de ensayo con PRP en una rejilla
Foto 18.Pipeteado
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 18. Se realiza un pipeteado para retirar el plasma rico en plaquetas y se colocará en otro tubo de ensayo estéril.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
39 Foto 21.Colocación del campo quirúrgico
.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 20. Asepsia extrabucal al paciente con una gasa humedecida con povidine.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 21. Colocación del campo quirúrgico al paciente.
40 Foto 22. Asepsia intrabucal
Foto 23. Anestesia troncular
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 22. Asepsia intrabucal al paciente con una gasa humedecida con povidine.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
41 Foto 24. Anestesia al nervio lingual, y bucal largo
Foto 25. Incisión (lineal)
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 24. Anestesia al 2% al nervio lingual, y bucal largo de la hemiarcada inferior derecha.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
42 Foto 26. Levantamiento de colgajo
Foto 27.Osteotomía
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 26. Se realiza el levantamiento de colgajo con un periostótomo.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
43 Foto 28.Luxación
Foto 29. Extracción propiamente dicha
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 28. Luxación aplicando un elevador recto fino.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
44
Foto 30.Eliminación de residuos y lavado del alvéolo
Foto 31. Aplicación del plasma rico en plaquetas
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 30. Extracción de residuos del saco pericoronario y lavado del alvéolo con suero fisiológico.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
45 Foto 32.Sutura a punto separado
Foto 33. Asepsia intrabucal- extracción de la pieza #38
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 32. Sutura a punto separado con hilo de seda 3.0
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 33. Asepsia intrabucal humedecida con povidine para la extracción de la
46 Foto 34. Anestesia
Foto 35.Incisión lineal
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 34. Anestesia troncular al dentario inferior, lingual, y bucal largo para la extracción de la pieza #38.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
47 Foto 36.Levantamiento de colgajo
Foto 37.Osteotomía
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 36. Se realiza el levantamiento de colgajo con unperiostótomo.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
48 Foto 38. Luxación
Foto 39. Extracción propiamente dicha
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 38. Luxación del tercer molar inferior izquierdo aplicando un elevador recto fino.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
49 Foto 40. Eliminación de residuos y lavado del alveolo
Foto 41. Sutura a punto separado
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 40. Eliminación de residuos del saco pericoronario y lavado del alvéolo con suero fisiológico.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
50 Foto 42.Piezas dentarias extraídas
Foto 43. Radiografía panorámica postquirúrgica
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 42. Piezas dentarias # 3.8; 4.8 extraídas.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
51 Foto 45. Instrumentos para la eliminación de los puntos de sutura
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 44. Inflamación lado izquierdo donde no se aplicó PRP, después de 24 horas.
RETIRADA DE LOS PUNTOS DE SUTURA
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 45. Colocación de los instrumentos en la mesa de mayo.
52 Foto 46. Asepsia extrabucal
Foto 47. Asepsia intrabucal
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 46. Asepsia extrabucal utilizando una gasa humedecida con povidine.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
53 Foto 48. Retirada de los puntos de sutura del lado derecho inferior
Foto 49. Retirada de los puntos de sutura del lado izquierdo inferior
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 48. Retirada de los puntos de sutura del lado derecho inferior donde se aplicó el PRP.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
54 Foto 50. Radiografía periapical lado derecha inferior
Foto 51. Radiografía periapical lado izquierdo inferior
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Foto 50. Radiografía periapical lado derecha inferior posterior a la retirada de los puntos de sutura, donde se observa el proceso de regeneración ósea.
Fuente: Propia de la investigación
Autor: Christian Chiluiza
55 Foto 52. Operador-Paciente
Foto 53. Operador-paciente-tutor-ayudante
Fuente: Propia de la investigación
Autor: Christian Chiluiza
Fuente: Propia de la investigación
56
6. DISCUSION
Después de la cirugía de los terceros molares retenidos, ocurre una respuesta psicológica en el paciente, ya que llega a presentarse ligero sangrado, inflamación, dolor, limitación de la apertura bucal interpretándolo como incomodidad. Por lo anterior mencionado se han sugerido diversos métodos para reducir al máximo estas secuelas que generalmente se presentan. Se ha recomendado el uso de medicamentos como los corticoesteroides, aplicación de hielo en las zonas posteriores a la extracción para reducir la inflamación, y diversos analgésicos para contrarrestar el dolor.
Las cirugías realizadas de los terceros molares es un procedimiento quirúrgico muy común en la práctica de la cirugía bucal y maxilofacial, por lo cual este tipo de cirugías produce una serie de complicaciones como lo antes ya mencionado, además de la cicatrización y formación ósea retardada. Por lo cual el uso de PRP es fundamental para la aceleración del proceso de cicatrización y formación ósea posteriores a las extracciones de los terceros molares.
Babbush y Mancuso han demostrado la capacidad del plasma rico en plaquetas en promover la regeneración ósea en el alvéolo, además de reducir el riesgo de formación de bolsas periodontales o de cualquier condición patológica que comprometa la cara distal de los segundos molares. La ventaja de aplicar el plasma rico en factores de crecimiento en zonas de extracción de las muelas del juicio es promover los procesos de regeneración de la mucosa del área, la formación del tejido óseo y reducir la inflamación y el dolor.
57
izquierdo presento todavía una inflamación de los tejidos blandos. De igual manera a los 15 días se hizo una nueva inspección clínica y radiográfica y se observó una total formación ósea y cicatrización de los tejidos blando.
La revista odontológica mexicana presento un estudio similar, en el cual analizo, el caso de una paciente de 21 años de edad con dolor moderado en la zona del tercer molar inferior izquierdo y derecho, dado el caso se realizó la remoción quirúrgica de ambos terceros molares, luego de extraer 20 cc, de sangre del paciente para obtener el PRP, se colocó en la zona del tercer molar inferior izquierdo, mientras el derecho se irrigo con suero fisiológico. Las observaciones realizadas al tercer día posoperatorio concluyeron que presento una menor inflamación extraoral del lado izquierdo, y el lado derecho presento inflamación y dolor. Así también intraoralmente existe una menor inflamación del lado izquierdo. De igual manera al quinto día de la retirada de los puntos se observó mejor epitelización y menor eritema del lado izquierdo. El estudio concluye que el PRP, puede beneficiar el postoperatorio de los pacientes después de la remoción de los terceros molares inferiores.
Estos estudios si bien pueden ser un importante referente comparativo con la presente investigación realizada sobre la aplicación del PRP posterior a la extracción de los terceros molares. Los resultados son concluyentes y coinciden con el de otros resultados, demostrándose que el dolor e inflamación es menor en el lado donde se aplicó el PRP, además que la cicatrización y formación ósea se realiza de manera rápida, a diferencia del propio ser humano, que la cicatrización y la regeneración ósea es prolongada.
58
7. CONCLUSIONES
La experiencia en el presente caso llegue a la conclusión que el uso del plasma rico en plaquetas o rico en factores de crecimiento tiene un efecto positivo en la regeneración ósea y en la cicatrización de los tejidos blando del paciente después de la remoción quirúrgica de los terceros molares inferiores. Es un tratamiento de bajo costo y es un producto libre de riesgo de reacciones alérgicas o de contaminación.
El uso del plasma rico en plaquetas presenta cambios temprano en el trabeculado ósea observados radiográficamente, y un acelerado proceso de cicatrización.
59
8. RECOMENDACIONES
Se recomienda la aplicación del PRP, en las cirugías de extracciones de terceros molares incluidos o retenidos, pues se ha podido demostrar beneficios para el paciente.
Es importante que al igual que se ha realizado en el presente estudio, se efectué nuevos estudios del uso de PRP, en otras intervenciones quirúrgicas.
Informarse sobre todo lo referente a la utilización del plasma rico en plaquetas ya que es una técnica alcanzable para todos los odontólogos que desean aplicarlo en su vida profesional, conocer más de sus beneficios ir actualizándonos para el bienestar de nuestros pacientes, y con mucha más razón sabiendo que no existe ningún riesgo al aplicar dicho producto ya que es un biomaterial autólogo, de obtención rápida y que puede inducir y mejorar los procesos de cicatrización.