Crecimiento y caracterización de películas delgadas de SnO2 prístino y dopado con Fe al 1% y 5% depositadas por la técnica de pulverización catódica para la aplicación como Sensor de Gas
Texto completo
(2) “CRECIMIENTO Y CARACTERIZACIÓN DE PELÍCULAS DELGADAS DE SnO2 PRÍSTINO Y DOPADO CON Fe AL 1% Y 5% DEPOSITADAS POR LA TÉCNICA DE PULVERIZACIÓN CATÓDICA PARA LA APLICACIÓN COMO SENSOR DE GAS”. Tesis presentada por: Bach. Yessy Bertha Guillen Baca. JURADO:. Dr. Daniel Octavio Roque Roque: _______________________________. Mg. Miguel Angel Vizcardo Cornejo:_____________________________. Dr. David Gregorio Pacheco Salazar: ____________________________. Fecha de Aprobación: 28 de diciembre de 2018.
(3) Dedico este trabajo a Dios, a mis padres Apolonio y Elena, quienes confiaron en mí, dándome fuerza y ánimo para culminar este trabajo..
(4) AGRADECIMIENTOS Agradezco de manera muy especial a Dios y cada uno de los integrantes de mi familia por el apoyo incondicional y desinteresado. Quiero expresar mi agradecimiento a mi asesor de tesis, el Dr. David G. Pacheco Salazar, por su gran aporte al trabajo desarrollado en esta tesis, por haber estado disponible para ayudarme siempre que se lo he pedido, y por haberse esforzado en enseñarme en qué consiste la investigación. También quiero agradecer a la Universidad de Brasilia, al instituto de Física, al Laboratorio del Dr. J.A.H Coaquira y al Dr. Fermín F. Herrera Aragón por la ayuda en varias de las caracterizaciones de Difracción de Rayos X, Espectroscopia Raman, Microscopía Electrónica, Espectroscopia Uv Vis, Mediciones Magnéticas realizadas a las películas delgadas y por su ayuda en todo momento e incondicional, por compartir sus conocimientos y experiencias obtenidas en sus investigaciones similares a este trabajo. Al Dr. Wilmer Sucasaire por compartir sus conocimientos en el programa PeakFit. Al Dr. André Guerra y a sus alumnos del doctorado de la Pontificia Universidad Católica del Perú, por la capacitación en caracterización eléctrica y Uv-vis de películas delgadas. Al Dr. Jorge Ayala Arenas por facilitarme algunos instrumentos y equipos del área al que pertenece. Además, doy gracias a mis amigos del Área de Películas Delgadas por su ayuda en todo el proceso de desarrollo de este trabajo. Por último, les doy las gracias a todas aquellas personas que, aunque no hayan tenido que ver directamente con el trabajo realizado para esta tesis, han hecho que me sintiera a gusto entre ellos durante estos años..
(5) INDICE RESUMEN .................................................................................................................. 1 ABSTRACT................................................................................................................. 2 INTRODUCCIÓN ........................................................................................................ 3 OBJETIVO GENERAL ................................................................................................ 5 OBJETIVOS ESPECÍFICOS ....................................................................................... 5 CAPITULO I: MARCO TEÓRICO ............................................................................... 6 1.1. ANTECEDENTES DE INVESTIGACIÓN ....................................................... 6 1.2. BASES TEÓRICAS ....................................................................................... 9 1.2.1. CRISTALES ............................................................................................... 9 1.2.3. SEMICONDUCTORES ............................................................................ 11 1.2.4. PELÍCULAS DELGADAS ......................................................................... 15 1.2.5. DIÓXIDO DE ESTAÑO ............................................................................ 17 1.2.6. TÉCNICA DE PULVERIZACIÓN CATÓDICA (SPUTTERING) ................ 18 1.2.7. ACETONA ................................................................................................ 20 CAPITULO II: METODOLOGÍA ................................................................................ 22 2.1..PREPARACIÓN DE SUSTRATOS Y BLANCOS METÁLICOS SnO2, SnO2:Fe(1%) y SnO2:Fe(5%) ........................................................................ 22 2.2. CRECIMIENTO DE LAS PELICULAS DELGADAS ..................................... 23 2.3.TRATAMIENTO TÉRMICO: ............................................................................ 26.
(6) 2.4.. TECNICAS DE CARACTERIZACIÓN ......................................................... 26. 2.4.1. DIFRACCIÓN DE RAYOS X .................................................................... 27 2.4.1.1. METODO DE RIETVELD.......................................................... 30 2.4.2. ESPECTROSCOPIA RAMAN .................................................................. 35 2.4.3 MICROSCOPÍA ELECTRÓNICA DE BARRIDO (MEB) ............................ 38 2.4.4. ESPECTROSCOPIA ULTRAVIOLETA-VISIBLE (UV-Vis) ...................... 39 2.4.5. METODO DE VAN DER PAUW ............................................................... 41 2.4.5.1. IMPLEMENTACIÓN DE UN SISTEMA PARA MEDIDAS ELÉCTRICAS ........................................................................... 43 2.4.5.2.DEPOSICIÓN DE CONTACTOS ............................................... 44 2.4.6. MAGNETISMO ......................................................................................... 45 2.4.6.1. TIPOS DE MATERIALES MAGNÉTICOS ................................ 46 2.4.7. SENSIBILIDAD: ..................................................................................... 48 CAPITULO III: RESULTADOS Y DISCUSIÓN ......................................................... 50 3.1. CARACTERIZACIÓN POR DIFRACCIÓN DE RAYOS X .............................. 50 3.2. CARACTERIZACIÓN POR ESPECTROSCOPIA RAMAN ............................ 58 3.3. CARACTERIZACIÓN POR MICROSCOPÍA ELECTRÓNICA DE BARRIDO (MEB) ............................................................................................................. 66 3.4. CARACTERIZACIÓN POR ESPECTROSCOPIA ULTRAVIOLETA-VISIBLE ........................................................................................................................ 70 3.5. CARACTERIZACIÓN ELÉCTRICA................................................................ 74 3.6. CARACTERIZACIÓN MAGNÉTICA .............................................................. 76.
(7) 3.7. PRUEBAS DE SENSIBILIDAD CON GAS DE ACETONA. ........................... 78 CONCLUSIONES ..................................................................................................... 82 TRABAJOS FUTUROS ............................................................................................ 83 BIBLIOGRAFÍA ........................................................................................................ 84 APENDICE 1: REGISTRO DE PELÍCULAS CRECIDAS POR LA TÉCNICA DE SPUTTERING ................................................................................... 90 APÉNDICE 2: REFINAMIENTO RIETVELD ............................................................. 91 APENDICE 3: VALORES OBTENIDOS DE REFINAMIENTO RIETVELD ............... 93 APENDICE 4: VALORES DE DECONVOLUCIÓN RAMAN ..................................... 94 APENDICE 5: DATOS DE LAS CONFIGURACIONES OBTENIDAS CON NUESTRO SISTEMA DE MEDIDAS ELÉCTRICAS ............................................ 95 APENDICE 6: PRUEBAS DE SENSIBILIDAD .......................................................... 96.
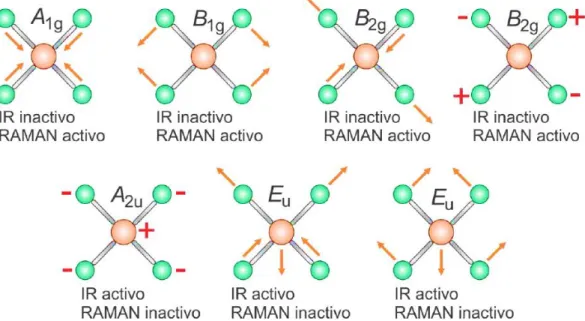
(8) INDICE DE FIGURAS Figura 1.1: Presentación de los defectos de los cristales (Hernández, 2014) (Smith W. F., Fundamentos de la ciencia e ingeniería de materiales, 2006).............................................. 10 Figura 1.2: Representación de las dislocaciones en una red de cristal real: (a) de borde (García, 2008) y b) de tornillo (Shackerlford, 1998)............................................................... 11 Figura 1.3: Representación esquemática de las bandas de energía en un sólido ............... 12 Figura 1.4: Semiconductor intrínseco (Landin, 2014) .......................................................... 13 Figura 1.5: Diagramas de semiconductores tipo-n y tipo-p (Landin, 2014) .......................... 14 Figura 1.6: Representación esquemática del efecto Burstein-Moss (Hernández, 2014) ...... 15 Figura 1.7: Celda unitaria de la estructura del SnO2 ........................................................... 17 Figura 1.8: Proceso de formación de crecimiento de películas delgadas de por la técnica de sputtering (Stanford, 2015) .................................................................................................. 19 Figura 1.9: Descripción general de los compuestos del aliento exhalado (Rydosz, 2018) ... 21 Figura 2.1: Blanco de Sn dopado con Fe al 1% .................................................................. 23 Figura 2.2: Equipo de crecimiento de películas delgadas por Pulverización Catódica DC (Sputtering DC) .................................................................................................................... 24 Figura 2.3: El interior de la Cámara de Vacío del sistema de Pulverización Catódica DC (Sputtering DC). ................................................................................................................... 24 Figura 2.4: Bomba mecánica de vacío. ............................................................................... 25 Figura 2.4: Crecimiento de películas delgadas. La luz violácea corresponde al plasma durante el crecimiento....................................................................................................................... 25 Figura 2.6: a) Horno para el tratamiento térmico de las películas delgadas, b) Rejilla de soporte de las películas delgadas para ser tratadas térmicamente. ..................................... 26 Figura 2.7: Difractómetro de Rayos X, usado para medidas de difracción de rayos X ....... 27 Figura 2.8: Representación de Bragg de una difracción de rayos-X, de acuerdo con reflexiones en fase desde planos sucesivos de un sistema particular. ................................. 28 Figura 2.9: Ficha cristalográfica estándar de difracción de rayos x del SnO2 tetragonal tipo rutilo (JCPDS 41-1445) ........................................................................................................ 29 Figura 2.10: Modos vibracionales del grupo de simetría D4h (Álvarez, 2012). ..................... 36 Figura 2.11: Diagrama de bloques ilustrando el sistema de espectroscopia Raman. (Aragón F. F., 2013) .......................................................................................................................... 37 Figura 2.12: Equipo de espectróscopía Raman ................................................................. 37.
(9) Figura 2.13: Microscopio electrónico de barrido (MEB) ....................................................... 38 Figura 2.14: Espectrofotómetro (UV-Vis) ............................................................................ 40 Figura 2.15: Configuraciones para obtener la resistencia característica RA. ........................ 41 Figura 2.16: Configuraciones para obtener la resistencia característica RB......................... 41 Figura 2.17: Sistema de medidas eléctricas ........................................................................ 43 Figura 2.18: a) Evaporadora Balzers, b) máscara metálica ................................................. 44 Figura 2.19: Deposición de los contactos de aluminio. ........................................................ 44 Figura 2.20: Película delgada con contactos de aluminio, que se encuentran en las esquinas. ............................................................................................................................................ 45 Figura 2.21: Esquema del sistema de mediciones de sensibilidad. ..................................... 48 Figura 2.22: Película con contactos para medidas de sensibilidad...................................... 49 Figura 3.1: Espectros de rayos x para ángulos de 2θ entre 20-80º correspondientes a muestras de películas delgadas de SnO2 y SnO2 dopado con Fe al 1 a 5%. a) Para 30 minutos de crecimiento, b) Para 2 horas de crecimiento y c) Para 4 horas de crecimiento ............... 51 Figura 3.2: Razón de intensidades de los picos correspondientes a los planos (110) y (101) con respecto al tiempo de crecimiento, para muestras de SnO2 y SnO2 dopadas con 1% y 5%. ............................................................................................................................................ 52 Figura 3.3: Comportamiento de los FWHM de los dos picos característicos de la película del SnO2 dopado con 1% de Fe en función del tiempo de crecimiento. ..................................... 53 Figura 3.4: El refinamiento Rietveld del DRX depositadas a 4 horas a) SnO2, b) SnO2:Fe (1%) y c) SnO2:Fe(5%). Los datos experimentales y teóricos calculados se representan con símbolo y líneas continuas, respectivamente. La línea azul continua representa la diferencia entre los datos experimentales y teóricos. .......................................................................................... 55 Figura 3.5: Las representaciones de Williamson-Hall que se usó para estimar el tamaño del cristalito y la deformación residual de la muestra de SnO2:Fe(5%) crecida a 4 horas. ......... 56 Figura 3.6: Comportamiento del volúmen de la celda unitaria en función de la concentración de dopaje para 4 horas. ....................................................................................................... 58 Figura 3.7: Espectros de Raman de las muestras de películas delgadas de SnO2 y SnO2 dopado con Fe al 1 a 5%. a) Para 30 minutos de crecimiento, b) Para 2 horas de crecimiento y c) Para 4 horas de crecimiento.......................................................................................... 60 Figura 3.8: Deconvolución Gausianna del espectro Raman de la películas de SnO2:Fe(5%), crecida a 4 horas. ................................................................................................................ 63 Figura 3.9: Comportamiento del desorden estructural en función de la concentración para películas crecidas por 4 horas. ............................................................................................ 64.
(10) Figura 3.10: Comportamiento del pico A1g de películas de SnO2 no dopadas en función del espesor. ............................................................................................................................... 65 Figura 3.11: Imagen de la superficie de las películas delgadas de SnO2: Fe (5%) con tiempos de crecimiento de a) 2 h, b) 3h. ........................................................................................... 66 Figura 3.12: Imagen transversal de las películas delgadas de SnO2: Fe (5%) con tiempos de crecimiento de a) 2 h, b) 3h.. ............................................................................................... 67 Figura 3.13: Dependencia de espesor (ω) con el tiempo de crecimiento (t). ....................... 67 Figura 3.14: Imagen EDS de la película delgada de SnO2 dopado con Fe al 5% crecida por 2 horas ................................................................................................................................... 68 Figura 3.15: Imagen EDS de la película delgada de SnO2 dopado con Fe al 5% crecida por 3 horas ................................................................................................................................... 69 Figura 3.16: Espectro EDS de la película delgada de SnO2 dopado con Fe al 5% crecida por 2 horas ................................................................................................................................ 69 Figura 3.17: Espectro EDS de la película delgada de SnO2 dopado con Fe al 5% crecida por 3 horas ................................................................................................................................ 70 Figura 3.18: Espectros de Absorción de las películas delgadas de SnO2 y SnO2 dopado con Fe al 1 a 5%. Con crecimientos de a) 30 min, b)2h y c) 4h .................................................. 71 Figura 3.19: Gráficas de (αhυ)2 vs hυ de las películas delgadas de a)SnO2 , b)SnO2 dopado con Fe al 1% y c) SnO2 dopado con Fe al 5% ..................................................................... 72 Figura 3.20: Gap ópico por la concentración de Fe para cada película delgada de SnO2 no dopado y SnO2 dopado con Fe al 1% y 5% ......................................................................... 73 Figura 3.21: Mediciones I-V de ocho configuraciones para la película delgada de SnO2 con 4 horas de crecimiento............................................................................................................ 74 Figura 3.22: Magnetización (M) en función del campo magnético (H), a una temperatura (T) de 300K de las películas delgadas de SnO2 dopado con 1% y 5% de Fe ........................... 76 Figura 3.23: Curva de histéresis de las películas delgadas de SnO2 dopado con 1% y 5% de Fe ........................................................................................................................................ 77 Figura 3.24: Magnetización en función de la temperatura (T) para las películas crecidas a 4 horas de SnO2 dopadas con 1% y 5% de Fe ....................................................................... 78 Figura 3.25: Respuesta de resistencia eléctrica de la película de SnO2 dopada con Fe al 1% de concentración crecida por 30 min., película realizadas a ~ 200ºC en ambiente de acetona. La flecha roja vertical muestra la entrada de acetona. ......................................................... 80 Figura 3.26: Comportamiento lineal de la sensibilidad de las películas de a) SnO2, b) SnO2: Fe (1%), c) SnO2: Fe (5%). ………………………………………………………………………….81.
(11) INDICE DE TABLAS. Tabla 2.1: Masas calculadas de los elementos de Sn y Fe (Silva, 2017) . ....................... 22 Tabla 2.2: Lista de equipos y accesorios usados en el sistema eléctrico. . .............. 43 Tabla 2.3: Temperatura Cure para varias sustancias ferromagnéticas. ........................... 47 Tabla 3.1: Parámetros de red a y c, volumen de la celda unitaria, tamaño de grano o cristalito y estrés de las películas delgadas. ................................................................................ 57 Tabla 3.2: Valores de picos característicos del SnO2, crecido por 4 horas de este trabajo y de otras referencias .................................................................................. 62 Tabla 3.3: Modos de vibración M1, M2 y A1g de las películas de SnO2 prístino y SnO2 dopado con 1% y 5% de Fe, ajustados con el programa PeakFit ................................................ 63 Tabla 3.4: Espesores estimados a partir del ajuste de la dependencia del espesor en función del tiempo. .................................................................................................................. 68 Tabla 3.5: Resultados del Gap óptico de las películas crecidas de SnO2 no dopadas y SnO2 dopadas con Fe al 1% y 5% con tiempos de crecimiento de 30min, 2h y 4h ...................... 73 Tabla 3.6: Resultados de la resistividad de las películas delgadas. ................................... 45.
(12) RESUMEN. El estudio de nuevos materiales que puedan servir como sensores de gases, se encuentra dentro de la investigación dirigida a solucionar la preocupación existente por detectar la cantidad de gases nocivos para nuestra salud. En el presente trabajo, se obtuvieron películas delgadas (PD) de óxido de estaño IV (SnO2) prístino y dopado con hierro (Fe) con concentraciones de dopaje del 1% y 5 %, utilizando la técnica de Pulverización Catódica DC (corriente directa), con una presión base del orden de 10-2 mbar y a una presión de trabajo de 1x10-1 mbar. Los tiempos de crecimiento fueron de 0.5, 1, 2, 3 y 4 horas una vez hecho el crecimiento de las PD de les hizo tratamiento térmico por dos horas a 500°C en ambiente de aire. En la caracterización de Difracción de Rayos X (DRX) donde se encontró una estructura cristalina tetragonal sin fases secundarias para todas las películas, independientemente de la concentración de dopaje, se analizó con el método de Rietveld. los parámetros de red y tamaño de grano,. los resultados fueron. corroborados con caracterizaciones de Espectroscopia Raman. Se caracterizó con Microscopía. Electrónica de Barrido (MEB) donde se encontró un crecimiento. columnar de las PD y una distribución uniforme del dopante, se pudieron obtener los espesores de las películas con las imágenes transversales donde se encontró que la tasa de crecimiento es de ~348 nm/h. La caracterización con espectroscopia ultravioleta visible (UV-Vis) analizando con el método de Tauc el comportamiento de la Energía Gap, se reveló que para dopajes de Fe el gap óptico disminuye en relación al no dopado. Para las caracterizaciones eléctricas se obtuvo la resistividades utilizando la técnica de Van der Pauw para las PD de SnO2 prístino y para las películas dopadas con 1% de Fe. En la caracterización magnética donde se pudo comprobar la presencia de Fe en las PD dopadas con 1% y 5%, por el comportamiento ferromagnético. Se ejecutaron pruebas de sensibilidad en presencia de gas acetona y mostraron respuesta eléctrica al ser sometidas a este gas. Esto implica que este tipo de PD pueden ser utilizadas como sensores de gas acetona.. Palabras Clave: Película Delgada, Pulverización Catódica, Sensibilidad, SnO 2:Fe. 1.
(13) ABSTRACT The study of new materials that can serve as gas sensors, is within the research aimed at solving the existing concern to detect the amount of gases harmful to our health. In the present work, thin films of tin oxide IV (SnO2) were obtained and doped with iron with doping concentrations of 1% and 5%, using the technique of DC Cathode Spraying (direct current) (DC Sputtering), with a base pressure of the order of 10 -2 mbar and a working pressure of 1x10-1 mbar. The growth times were 0.5, 1, 2, 3 and 4 hours after the growth of the thin films had been made for thermal treatment for two hours at 500°C in the air environment. Then, different characterizations were made. In the characterization of X-ray diffraction (XRD) where a tetragonal crystalline structure without secondary phases was found for all the films, regardless of the concentration of doping, the parameters of network and grain size were analyzed with the Rietveld method. Results were corroborated with characterizations of Raman spectroscopy. It was characterized with Scanning Electron Microscopy (SEM) where it was found a columnar growth of the thin films and a uniform distribution of the dopant, it was possible to obtain the thicknesses of the films were obtained with transverse images of SEM where it was found that the growth rate is of ~ 348 nm / h. The characterization with visible ultraviolet spectroscopy (UV-Vis) analyzing with the Tauc method the behavior of the Energy Gap, it was revealed that for doping of iron the optical gap decreases in relation to the non-doped. For the electrical characterizations, a system of electrical. measurements was. designed and constructed, where resistivities were obtained using the Van Der Pauw technique for the pristine SnO2 thin films and for the films doped with 1% iron. Magnetic characterization was also done where check the presence of iron in thin films doped with 1% and 5%, for the ferromagnetic behavior. Sensitivity tests were performed in the presence of acetone gas and showed an electrical response when subjected to this gas. This implies that this type of thin films can be used as acetone gas sensors.. Key Words: Thin Films, Sputtering, Sensitivity, SnO2:Fe.. 2.
(14) INTRODUCCIÓN El estudio de materiales nanoestructurados es de interés actual en diferentes áreas del conocimiento y de la tecnología, siendo estas las componentes esenciales para el mercado del futuro donde sistemas nanométricos desempeñarán funciones específicas. Una de estas tecnologías son las Películas Delgadas (Casella, 2015). La preparación de materiales en forma de películas delgadas han sido objetos de un gran número de investigaciones debido a los enormes intereses tecnológicos de las últimas décadas lo que hace cada vez necesario la investigación en la producción de las PD con el objetivo de modificar sus propiedades físicas. Existen procesos que finalmente influencian la estructura cristalina y morfología lo que a su vez, condicionan las propiedades de las películas delgadas (Albella, 2003). En este sentido, podemos mencionar aspectos tales como: (i) la interacción de la película con sustrato (ii) las modificaciones sufridas de la superficie de la película delgada a la exposición de la atmósfera, (iii) su estabilidad térmica, y (iv) el nivel de impurezas que son incorporados. La. películas. delgadas. se. utilizan. para. la. fabricación. de. catalizadores,. descontaminadores de aire y aguas (Tirado et. al., 2014), filtros para la fabricación de sensores (Tirado et. al., 2011), fotovoltaicas de película delgada (Rey, et. al., 2012). Una de las aplicaciones de importancia para el estudio del medio ambiente y nuestra salud es el conocimiento de los diferentes gases existentes que pueden ser nocivos. (Aragón, 2011). El SnO2 es uno de los materiales más investigados actualmente por su bajo costo y posee una gran capacidad de detección de gases reductores. Actualmente, gran parte de la investigación está dirigida a la búsqueda del incremento de la sensibilidad, selectividad y estabilidad de estos materiales (Delgado,2002.), es un semiconductor ampliamente estudiado para potenciales aplicaciones como sensores de gas (Bahrami et. al., 2008) ya que presenta una conductividad eléctrica variante cuando es sometido a un determinado gas, esta propiedad se debe a que en su superficie se produce procesos de óxido reducción variando la cantidad de electrones libres en la banda de conducción.. 3.
(15) Con la finalidad de producir selectividad a diferentes gases es posible dopar el semiconductor con metales de transición como el Fe (Aragón, 2010), en este trabajo se propone el análisis de películas de SnO2 puro y SnO2 dopadas con Fe para mejorar la aplicación de sensibilidad a diferentes gases, para nuestro caso se inició con gas de acetona.. 4.
(16) OBJETIVO GENERAL: Crecer y caracterizar películas delgadas de SnO2 prístino y dopado con Fe al 1% y 5% depositadas por la técnica de Pulverización Catódica para la aplicación como sensor de gas. OBJETIVOS ESPECÍFICOS: - Crecer películas delgadas SnO2 no dopado y dopados con Fe al 1% y 5% por la técnica de Pulverización Catódica DC (Sputtering DC) - Caracterizar por Difracción de Rayos X - Caracterizar por espectroscopia Raman - Caracterizar por Microscopía Electrónica de Barrido (MEB) - Caracterizar por espectroscopia UV-Visible - Diseñar y construir un sistema de medidas eléctricas. - Caracterización Eléctrica - Caracterización Magnética - Caracterizar sensorialmente con gases biológicos.. 5.
(17) CAPITULO I: MARCO TEÓRICO 1.1.. ANTECEDENTES DE INVESTIGACIÓN Actualmente tenemos varios antecedentes internacionales, en la elaboración de películas delgadas con distintas caracterizaciones y con dopajes diversos.. A. “Characterization of polycrystalline SnO2 films deposited by DC sputtering technique with potential for technological applications” (Aragón, y otros, 2017). Muestran la deposición de películas de SnO2 con diferentes espesores a temperatura ambiente en susstrato de vidrio usando una técnica de pulverización catódica DC; estas películas fueron tratadas térmicamente. Las imágenes de microscopía electrónica de barrido revelaron la formación de superficies agrietadas junto con el crecimiento columnar. Las mediciones de espectroscopia Raman evidenciaron la presencia de modos vibracionales relacionados con un desorden superficial, una reducción progresiva de la tensión y una mejora de la cristalinidad. El análisis de datos UV-vis indica una reducción en la energía de banda prohibida con el grosor de las películas debido a la presencia de estados de deformación. B. “Structural and Optical Properties of Nanostructured Fe-Doped SnO2” (Saleh, Ibrahim, & Mohamed, 2016) Los nanocristalinos. Sn1-xFexO2. en polvo (donde x = 0, 0.01, 0.02, 0.03 y 0.04) se han sintetizado con éxito por el método hidrotermal seguido de sinterización a 1000ºC durante 3 h. La morfología y la estructura de las muestras se analizaron mediante microscopía electrónica de barrido de emisión de campo, y la difracción de rayos X, respectivamente.. Los resultados de difracción de rayos X. muestran que todas las posiciones de picos de difracción concuerdan con una estructura de rutilo tetragonal de la fase de SnO2 sin picos adicionales. Esta estructura fue respaldada por los espectros Raman.. 6.
(18) C. “Structural, Optical and Electrical Properties of Fe Doped SnO2 Prepared by Spray Pyrolysis” (Nassiri, y otros, 2017) En este trabajo, se depositaron películas delgadas de SnO2 dopadas con Fe sobre sustrato de vidrio calentado a 350 °C mediante una técnica de pirólisis por pulverización. El análisis de difracción de rayos X mostró una estructura policristalina con pico característico claro de fases de casiterita de SnO2 en todas las películas. A partir de las mediciones ópticas, se observó que todas las películas presentan una alta transmitancia en el rango visible. En cuanto a las mediciones eléctricas, se encontró que la resistividad aumenta con el incremento de la concentración de Fe. D. “Structural, optical and electrical properties of Fe-doped SnO2 fabricated by sol–gel dip coating technique” (Timonah, Chunhui, & Liang, 2010) Se prepararon películas delgadas de SnO2 dopado con Fe3+ de tamaño nanométrico mediante la técnica de recubrimiento con inmersión en sol y gel sobre sustrato de cuarzo y se sinterizó a 800°C. El espectro DRX muestra la disminución de las alturas de los picos como resultado de la aplicación de Fe3+, mientras que las imágenes MEB revelan una reducción en el tamaño de los cristales con un aumento en el contenido de Fe3+. Los estudios ópticos mostraron una reducción directa de la banda prohibida con un aumento en la utilización de Fe 3+ de 3.87 a 3.38 eV. A partir de las mediciones eléctricas, se encontró que la resistividad inicialmente aumenta con el incremento de la concentración de Fe3+ antes de reducirse a un nivel de dopado más alto. Las mediciones del efecto Hall mostraron una conductividad de tipo n en dopajes bajos de Fe3+ y de tipo p con mayor dopaje. El aumento de la conductividad con la temperatura determinó el comportamiento semiconductor de estas películas.. 7.
(19) E. “Síntese e caracterização das propriedades estruturais e magnéticas de filmes finos de SnO2 dopados com o elemento ferro para a aplicação como sensores do gás metano” (Silva, 2017) Se crecieron películas delgadas de SnO2 con concentración de Fe al 1%, 2%, 3%, 4% y 5%. Las caracterizaciones estructurales mostraron la formación de una única fase correspondiente a la estructura cristalina del dióxido de estaño. Las caracterizaciones ópticas permitieron encontrar el valor del gap óptico, siendo que cada valor encontrado se aproximó al valor correspondiente al SnO2. Las mediciones magnéticas mostraron la coexistencia de los comportamientos paramagnéticos y ferromagnéticos en las películas delgadas con concentración de Fe. Las pruebas de sensores de gas permitieron verificar la influencia del dopaje del hierro en el desempeño de los nanosensores de dióxido de estaño. Los resultados de las pruebas indicaron que la película delgada de SnO2 dopado con 5% de hierro tuvo una mejora significativa en la respuesta como nanosensor del gas metano, en comparación con las películas delgada de SnO2 no dopados y dopados con Fe. F. “Synthesis, structural, and magnetic properties of Fe doped SnO 2 nanomaterials” (Farid, Sufyan, Wahab, Umair, & Saggu, 2015) Las nanopartículas de SnO2 dopadas con Fe se prepararon usando una ruta química.. Las. investigaciones. morfológicas. utilizando. microscopía. electrónica de barrido han demostrado que las muestras preparadas son nanopartículas en el rango de 89-114 nm. La estructura cristalina y la pureza de fase de las nanopartículas de Fe se han examinado utilizando difracción de rayos X. Las nanopartículas preparadas muestran la fase Rutilo del SnO2 y no se observa pico adicional. El tamaño del cristalito se calcula por DRX que está en el rango de nm y va de acuerdo con los resultados del MEB. La inclusión de Fe en el SnO2 se confirma por el cambio de pico en los patrones de XRD. Los picos observados en los espectros de FTIR concuerdan bien con la presencia de un enlace terminal Sn-O de SnO2 y C = O en las impurezas de ácido carboxílico o carbonilo.. 8.
(20) Las nanopartículas de SnO2 preparadas muestran diamagnetismo, mientras que el dopaje de Fe conduce al ferromagnetismo a temperatura ambiente. El lazo M-H para SnO2 no dopado muestra un comportamiento diamagnético típico. El diamagnetismo se debe a la presencia de electrones apareados en su orbital "d".. 1.2. BASES TEÓRICAS 1.2.1. CRISTALES 1.2.1.1. Estructura cristalina Los sólidos se pueden dividir en dos categorías: cristalinos y amorfos. Un sólido cristalino tiene rigidez y orden de largo alcance; sus átomos, moléculas o iones ocupan posiciones específicas. El centro de cada una de las posiciones se llama un punto reticular, y el orden geométrico de estos puntos reticulares se llama estructura cristalina. Las fuerzas que mantienen la estabilidad de un cristal pueden ser iónicas, enlaces covalentes, fuerzas de Van der Waals, enlaces de hidrógeno o una combinación de estas fuerzas (Chang, 1997). El sólido amorfo es un estado, en el que las partículas que conforman el sólido carecen de una estructura ordenada. Estos sólidos carecen de formas bien definidas. 1.2.1.2. Defectos en los cristales El proceso de formación de un cristal puede llevar a que se formen defectos. Su presencia es normal en el equilibrio térmico, por lo tanto les considera intrínsecos en un cristal real. Algunos de los defectos que se presentan en los cristales son vacancias, intersticiales, dislocaciones y fronteras de grano. - Defectos puntuales: son vacancias, substitucionales e intersticiales que consisten en la ausencia o presencia extra de iones como se muestra en la figura 1.1. Estos tipos de defectos son responsables de la conductividad eléctrica de los cristales iónicos y pueden alterar profundamente sus propiedades ópticas. La imperfección más sencilla. 9.
(21) se conoce como vacancias de red o defecto Schottky (vacante + vacante) cuando, en un cristal iónico, faltan simultáneamente un anión y un catión. También se tiene el defecto de Frenkel (intersticial + vacante) cuando, en un cristal iónico, un ion salta su sitio normal a un sitio intersticial dejando una vacante.. Figura 1.1: Presentación de los defectos de los cristales (Hernández, 2014) (Smith W. F., Fundamentos de la ciencia e ingeniería de materiales, 2006). - Defectos lineales, dislocaciones y frontera de grano Los dos tipos más simples de dislocaciones son las dislocaciones de borde y la de tornillo. La dislocación de borde se puede describir como el borde de un plano extra de átomos dentro de una estructura cristalina que se produce cuando un bloque de celdas correspondientes a varias capas superiores se desliza a una distancia atómica respecto de las capas inferiores, mientras que el bloque situado inmediatamente enfrente no se desliza. A lo largo de una dislocación lineal, el cristal se encuentra en un estado de distorsión local muy alto, de modo que la distorsión adicional requerida para mover la dislocación oblicuamente, una constante de red requiere de la aplicación de una tensión adicional relativamente pequeña. La dislocación de tornillo marca el borde entre partes deslizadas y no deslizadas de un cristal. Se puede imaginar la dislocación de tornillo como un corte parcial del cristal el cual es deslizado un espaciamiento atómico paralelo al borde del corte, retomándose el orden cristalino en todas partes excepto cerca de la 10.
(22) línea de dislocación donde termina el plano del corte. En la Figura 1.2 se presentan las dislocaciones en una red en un cristal real: dislocación de borde y dislocación de tornillo. (Hernández, 2014). Figura 1.2: Representación de las dislocaciones en una red de cristal real: (a) de borde (García, 2008) y b) de tornillo (Shackerlford, 1998). 1.2.3. SEMICONDUCTORES Los semiconductores son elementos que se comportan como un conductor o como aislante dependiendo de algunos factores, como el campo eléctrico o magnético, la radiación, la presión o la temperatura del ambiente en el que se encuentre (Orozco, 2012). Los cristales de semiconductores están formados por átomos donde los vecinos más cercanos están enlazados de manera covalente (más o menos polar). Si nos fijamos en su resistividad, los sólidos pueden ser divididos en tres grupos. En los metales la resistividad varía entre 10-6 y 10-4 Ωcm; en los semiconductores la resistividad está entre 10-4 y 1010 Ωcm y las sustancias de resistividad mayor que 1010 Ωcm, corresponden a los dieléctricos (Hernández, 2014).. 11.
(23) TEORIA DE BANDAS En la teoría de bandas, se tiene la banda de valencia, donde se hallan los electrones de valencia y pueden estar llenas o semillenas, dependiendo de la configuración electrónica; la banda de conducción, que puede hallarse vacía o parcialmente vacía, y facilita la conducción de electrones porque es energéticamente accesibles. De hecho, los metales son conductores porque las bandas de valencia y de conducción se superponen, y esto hace que los electrones se muevan con libertad de una a otra.. Figura 1.3: Representación esquemática de las bandas de energía en un sólido. En el caso de los semiconductores, las bandas de valencia y de conducción no se superponen, pero la diferencia energética entre ambas es pequeña, por lo que una pequeña aportación energética hará que puedan ascender electrones de la banda de valencia a la banda de conducción y, por tanto, conducir la corriente eléctrica. En los aislantes, las dos bandas están tan alejadas que la banda de conducción es inaccesible, motivo por el cual son incapaces de conducir la corriente, como se muestra en la figura 1.3. (Quimitube, 2012). 12.
(24) SEMICONDUCTORES INTRÍNSECOS o PUROS: Un semiconductor intrínseco es cuando un semiconductor no contiene impurezas en cantidad suficiente para cambiarle las propiedades. El número de electrones es igual al número de huecos, porque cada vez que una conexión covalente se forma o se rompe, un par del electrón-agujero se genera o se elimina en el proceso. (Mello & Biasi, 1975) Los semiconductores más empleados son el germanio (Ge) y el silicio (Si); siendo éste último el más abundante y se puede trabajar a temperaturas mayores que el germanio. Como ejemplo tenemos la figura 1.4, donde cada átomo de un semiconductor tiene 4 electrones en su órbita externa (electrones de valencia), que comparte con los átomos adyacentes formando 4 enlaces covalentes. De esta manera cada átomo posee 8 electrones en su capa más externa, formando una red cristalina, en la que la unión entre los electrones y sus átomos es muy fuerte. Por consiguiente, en dicha red, los electrones. no. se. desplazan. fácilmente,. y. el. circunstancias normales se comporta como un aislante.. Figura 1.4: Semiconductor intrínseco (Landín, 2014). 13. material. en.
(25) SEMICONDUCTORES EXTRÍNSECOS o IMPUROS La adición de pequeñas cantidades de otras sustancias a un semiconductor puede modificar considerablemente las propiedades del material. Estas impurezas pueden sustituir los átomos de la red cristalina (impurezas substitucionales) u ocupar posiciones vacantes entre los átomos de la red (impurezas intersticiales). (Mello & Biasi, 1975). Según la impureza (llamada dopante) distinguimos: Los semiconductores tipo p se emplean elementos con tres electrones de valencia como el Boro, Indio, o Galio como dopantes. Puesto que no aportan los 4 electrones necesarios para establecer los 4 enlaces covalentes, en la red cristalina éstos átomos presentarán un defecto de electrones (para formar los 4 enlaces covalentes). De esa manera se originan huecos que aceptan el paso de electrones que no pertenecen a la red cristalina. Así, al material tipo p también se le denomina donador de huecos (o aceptador de electrones) (Figura 1.5). (Landin, 2014) Los semiconductores tipo n se emplean como impurezas elementos pentavalentes (con 5 electrones de valencia) como el Fósforo (P), el Arsénico (As) o el Antimonio (Sb). El donante aporta electrones en exceso, los cuales al no encontrarse enlazados, se moverán fácilmente por la red cristalina aumentando su conductividad. De ese modo, el material tipo n se denomina también donador de electrones (Figura 1.5). (Landin, 2014) (Gurrola, 2017). Figura 1.5: Diagramas de semiconductores tipo-n y tipo-p (Landin, 2014). 14.
(26) EFECTO BURSTEIN-MOSS: El llamado efecto Burstein-Moss ocurre en los semiconductores dopados o impurificados (por ejemplo tipo n). En el caso de un semiconductor degenerado, como se le conoce a un semiconductor con una densidad de portadores libres ≥1019 cm-3, un electrón en la parte superior de la banda de valencia solo puede ser excitado a la banda de conducción por encima del nivel de Fermi (que ya se encuentra en la banda de conducción) ya que todos los estados por debajo de nivel de Fermi están ocupados por electrones. El principio de exclusión de Pauli prohíbe la excitación a estados ocupados. Por lo tanto se observa un aumento del gap óptico del semiconductor dopado provocado por el exceso de energía que se debe suplementar a un electrón para que alcance un estado desocupado (Hernández, 2014). Este comportamiento se presenta en forma esquematizada en la Figura 1.6.. Figura 1.6: Representación esquemática del efecto Burstein-Moss (Hernández, 2014). 1.2.4. PELÍCULAS DELGADAS Las películas delgadas (PD) son estructuras sólidas con espesores del orden de nanómetros a micras. Para que un material sea considerado como “película delgada”, el espesor debe tener ciertas características como: conductividad, transparencia óptica de luz, dureza, etc. e incluso la temperatura es importante para ciertas propiedades (Albella, 2003). 15.
(27) El avance en el procesamiento de diversos materiales en película delgada ha permitido el desarrollo de dispositivos que se utilizan en múltiples aplicaciones tecnológicas. Entre los campos tecnológicos donde se hace un uso extensivo de películas delgadas se pueden destacar los siguientes: a. En máquinas, motores y herramientas de corte y piezas sujetas a desgaste (brocas, pistones, turbinas), como recubrimientos duros para aumentar dureza y resistencia a la abrasión, corrosión y deterioro térmico. b. En componentes ópticos (lentes, filtros, vidrios planos o curvos), como recubrimientos para mejorar o modificar las propiedades de reflexión y transmisión de la luz. c. En dispositivos electrónicos como sistemas multicapas (heteroestructuras) que constituyen partes de transistores, diodos, fotodiodos, etc. (Bedoya, 2015) Por la naturaleza de su espesor delgado, las PD depositadas sobre otro material sólido denominado sustrato, pueden ser empleadas para optimizar las propiedades del sustrato y añadir nuevas propiedades. Las PD deben cumplir las siguientes características: . Estabilidad química y térmica respecto al entorno, así como buena adherencia al sustrato.. . Espesor uniforme.. . Composición química controlada.. . Densidad de imperfecciones o defectos controlados.. Al controlar las características de las películas, que pueden ser aislante o semiconductora, poseer propiedades ópticas o magnéticas, o las que se requieran para alguna aplicación en específico. Dadas las exigencias que se precisan en las películas delgadas, se requiere contar con técnicas especializadas para su fabricación y caracterización. La ciencia y tecnología de películas delgadas - de la mano con áreas tan diversas como la ciencia del vacío, la físico-química del estado sólido, la ciencia de las superficies y la física computacional, aunado a los avances en los métodos de caracterización - es lo que ha permitido desarrollar un ambiente propicio para la obtención de Películas delgadas con un alto grado de calidad y especialización. De esta. 16.
(28) manera, la fabricación de películas delgadas es una tecnología tradicional que ha estado presente en las sociedades humanas desde hace siglos, cuyo refinamiento a través del tiempo ha permitido el desarrollo de dispositivos electrónicos, recubrimientos ópticos, celdas solares, circuitos, etc., por lo que su fabricación sigue siendo crucial para el progreso tecnológico actual (Bedoya, 2015). En este contexto, se realza la importancia en la investigación enfocada a la fabricación, caracterización y análisis de materiales en películas delgadas.. 1.2.5. DIÓXIDO DE ESTAÑO El dióxido de estaño (SnO2) tiene una estructura de rutilo tetragonal con grupo 14 espacial 𝐷4ℎ (P42/mnm). En su celda unitaria contiene dos estaños y cuatro. átomos de oxígeno. Cada átomo de estaño está unido a seis átomos de oxígeno en los vértices de un octaedro regular, y cada átomo de oxígeno está rodeado por tres átomos de estaño en las esquinas de un triángulo equilátero (Chan, 2012), como se muestra en la figura 1.7.. Figura 1.7: Celda unitaria de la estructura del SnO2. 17.
(29) Los parámetros de red son a = 4.737 Å (a=b en la estructura tetragonal) y c = 3.186Å. Las posiciones atómicas en la celda unitaria a 300 K con átomos de Sn 1. 1. 1. (0,0,0) and ( 𝑎, 𝑎, 𝑐) 2 2 2. en 1. ± (2 𝑎 + 𝑢𝑎,. 1. 𝑎 − 𝑢𝑎, 2. 1 2. y átomos de oxígeno en ±(𝑢𝑎, 𝑢𝑎, 0) y. 𝑐), con u=0.307 (Chen, Lai, Shek, & Chen, 2003). El. resto de átomos de la celda unitaria pueden obtenerse aplicando la simetría correspondiente a su grupo espacial. El óxido de estaño puro es un semiconductor tipo n debido a la presencia de vacantes de oxígeno, que actúan como donantes de electrones. La conductividad eléctrica del óxido de estaño se origina por la presencia de vacancias de oxígeno o niveles donadores de energía, con un intervalo de gap óptico (𝐸𝑔 ≈ 3.6 − 3.8 𝑒𝑉) (Timonah, Chunhui, & Liang, 2010) y una resistividad eléctrica que varía de 10 a 106 Ω cm dependiendo de la temperatura y de la estequiometria del óxido (Smith W. F., Ciencia e Ingeniería de Materiales, 2004). Se utiliza ampliamente como óxido conductor transparente, como material sensor de gas y como catalizador (Eifert, y otros, 2016).. 1.2.6. TÉCNICA DE PULVERIZACIÓN CATÓDICA (SPUTTERING) La pulverización catódica DC (DC Sputtering) es un proceso que utiliza plasma para extraer los átomos de la superficie de un material objetivo sólido (blanco). Los átomos extraídos se depositan en la superficie del sustrato. Las películas crecidas por esta técnica exhiben buena uniformidad, densidad, pureza y adherencia (Mendivil, 2010). La descarga incandescente de corriente continua que origina las partículas energéticas, puede obtenerse aplicando una diferencia de potencial entre dos electrodos en presencia de un gas inerte (generalmente argón), manteniendo la baja presión dentro de la cámara de vacío. La diferencia de potencial se puede suministrar mediante una fuente de alimentación de corriente continua que puede proporcionar alto voltaje, según la configuración del equipo. En este proceso, se forma un campo eléctrico entre los electrodos separados por una distancia d y que tienen una diferencia de. 18.
(30) potencial V; esto generará una corriente eléctrica en el gas enrarecido, debido a la presencia de electrones e iones formados por procesos como la ionización y por las colisiones entre partículas, como se muestra en la Figura 1.8.. Figura 1.8: Proceso de formación de crecimiento de películas delgadas de por la técnica de sputtering (Stanford, 2015). En el proceso de ionización, un electrón que colisiona con un átomo generará un ion y un nuevo electrón. Bajo el efecto del campo eléctrico, el ion es acelerado hacia el cátodo y los dos electrones se aceleran hacia el ánodo. Una vez que los electrones viajan una distancia suficientemente larga antes de la colisión, adquirirán suficiente energía cinética para promover una nueva ionización. Si se usa argón, las reacciones para la formación de iones (Ar+) y especies excitadas (Ar*) se pueden describir mediante las siguientes expresiones. 𝑒 − + 𝐴𝑟 → 𝐴𝑟 + + 2𝑒 −. (1.1). 𝑒 − + 𝐴𝑟 → 𝐴𝑟 ∗ + 𝑒 −. (1.2). Debido a la aceleración del campo eléctrico, los iones pueden alcanzar el cátodo con una energía lo suficientemente alta como para provocar la emisión de electrones secundarios. Estos electrones pueden acelerarse hacia el ánodo y generar nuevas colisiones, causando un efecto de cascada, estableciendo. 19.
(31) una descarga estable y manteniendo el plasma en una condición de equilibrio. (Gobbi & Nascente, 2013) El argón es un gas inerte, el cual es escogido para actuar como el medio sputtering más común. También tiene un bajo potencial de ionización. La naturaleza inerte de argón inhibe compuestos a formarse en la superficie del blanco. (Mendivil, 2010). 1.2.7. ACETONA La acetona también llamados Dimetil Cetona; 2-Propanona; Beta Cetopropano y su fórmula es C3H6O. Es una sustancia química presente en la naturaleza, contenida en plantas (cebollas, tomates, uvas), en alimentos tales como la leche, árboles, en los gases volcánicos, en incendios forestales; en el cuerpo humano, se encuentra como uno de los metabolitos de la sangre y como un producto de la descomposición de la grasa corporal. Está presente en los gases de combustión de los vehículos, el humo del tabaco y rellenos de seguridad. Los procesos industriales aportan una mayor cantidad de acetona al ambiente que los procesos naturales. Es un líquido incoloro con un olor dulce similar al de las frutas y un sabor característico. Se evapora fácilmente, es inflamable y muy soluble tanto en agua como en solventes orgánicos tales como el éter, metanol, y etanol. La acetona se usa en la fabricación de plásticos, fibras, drogas y otros químicos. También se usa como solvente. El aliento humano exhalado consiste en casi 3500 compuestos orgánicos volátiles diferentes (COV), y un solo aliento consiste en alrededor de 500 diversos COV (Figura 1.9), que generalmente se encuentran en la parte por millón (ppm), parte por billón (ppb) o parte por trillón (ppt). Los biomarcadores presentes en la respiración exhalada se utilizan para indicar varias enfermedades, como el cáncer de pulmón, el asma, la enfermedad pulmonar obstructiva crónica, el cáncer de mama, y la diabetes. El número total de enfermedades que pueden detectarse o controlarse mediante el análisis del aliento exhalado aún se desconoce. (Rydosz, Sensors for Enhanced Detection of Acetone as a, 2018). 20.
(32) La diabetes mellitus (DM) es una enfermedad crónica identificada por los niveles altos de glucosa en la sangre debido a la falta de producción (DM Tipo I) o de consumo (DM Tipo II) de forma adecuada. Como resultado de la reacción bioquímica, la acetona se exhala y es un biomarcador crucial en la respiración para la diabetes mellitus. La concentración promedio de acetona en un aliento humano sano se estimó en menos de 1,8 ppm y en pacientes diabéticos es más de 2 ppm. (Kalidoss, Umapathy, & Sivalingam, 2017). Figura 1.9: Descripción general de los compuestos del aliento exhalado (Rydosz, 2018). 21.
(33) CAPITULO II: METODOLOGÍA 2.1..PREPARACIÓN. DE. SUSTRATOS. Y. BLANCOS. METÁLICOS. SnO2,. SnO2:Fe(1%) y SnO2:Fe(5%) (Silva, 2017) Se utilizaron sustratos de vidrio y de silicio (Si). Los sustratos de vidrio fueron cortados en forma de cuadrados de 1.0x1.0 cm y los de silicio de 0.5x0.5cm. Se lavaron con detergente, frotando regularmente las superficies con hisopo de algodón, se enjuagó con abundante agua y seguidamente con alcohol isopropílico y se procedió a secar con papel fino y secadora. El material a depositar, denominados blancos, se preparó en los laboratorios de la Universidad de Brasilia. Se hicieron cálculos para la determinación de las masas necesarias para los blancos metálicos de los elementos reactivos Sn y Fe, los resultados se muestran en la tabla 2.1. Tabla 2.1: Masas calculadas de los elementos de Sn y Fe (Silva, 2017). Blanco. Masa de Sn (g). Masa de Fe (g). Sn: Fe 1%. 0.9952. 0.0048. Sn: Fe 5%. 0.9750. 0.0250. Se fundió las porciones de los elementos reactivos, en un horno de arco, en atmósfera de argón puro. Seguidamente el compuesto o blanco metálico se prensó con 5 toneladas en la prensa hidráulica, para obtener una superficie horizontalizada y circular. Se pegaron cada compuesto o blanco metálico con tinta plata, en un tubo pequeño de metal, se llevó al horno durante 30 minutos para el tratamiento térmico a 200 °C (Silva, 2017). En la figura 2.1 se muestra el blanco de Sn-Fe dopados al 1%, uno de los blancos utilizados para el crecimiento de películas delgadas.. 22.
(34) Figura 2.1: Blanco de Sn dopado con Fe al 1%. 2.2. CRECIMIENTO DE LAS PELICULAS DELGADAS Para el crecimiento de las películas delgadas de utilizó un sistema de Pulverización Catódica DC como se muestra en la figura 2.2. Este sistema consiste en una cámara de vacío, una bomba mecánica, un medidor de presión, una fuente de alto voltaje y un amperímetro con escala de 20mA. En el interior de la cámara de vacío se tiene los electrodos (ánodo y cátodo), como se muestra en la figura 2.3. El sistema está conectado con un balón del gas de Argón. La figura 2.4 muestra la bomba mecánica de vacío, que reduce la presión de la cámara de vacío. Se procedió a hacer limpieza en el interior de la cámara de vacío y de los electrodos con alcohol isopropílico, seguidamente se colocó el ánodo con los sustratos y en el cátodo con el blanco verificando con un multímetro la conductividad entre el blanco y el cátodo. Se usó la secadora de aire para quitar alguna pelusa en la cámara de vacío. Para iniciar el proceso de crecimiento de las películas delgadas, se cierra la cámara de vacío, se enciende la bomba mecánica. Se espera que en el interior de la cámara alcance una presión base del orden de 10−2 𝑚𝑏𝑎𝑟,. luego se. introduce el gas de argón (𝐴𝑟) a la cámara de vacío, por un instante, regulando el flujo del gas de tal forma que la presión sea del orden de100 mbar, luego se cierra el flujo de gas y se esperó que la presión baje a la presión base del orden de 10−2 𝑚𝑏𝑎𝑟, nuevamente se introduce el gas de argón regulando el flujo de gas de tal forma que la presión de trabajo sea de 1.0 × 10−1 𝑚𝑏𝑎𝑟. Enseguida se. 23.
(35) enciende la fuente de voltaje de forma que la corriente sea de 1mA entre el cátodo y el ánodo donde se observa el plasma generado entre los electrodos como se muestra en la figura 2.5.. Cámara de Vacío Balón del Gas de Argón. Figura 2.2: Equipo de Crecimiento de Películas Delgadas por Pulverización Catódica DC (Sputtering DC). Electrodo (ánodo). Sustratos. Electrodo (cátodo) Blanco. Figura 2.3: El interior de la Cámara de Vacío del sistema de Pulverización Catódica DC (Sputtering DC). 24.
(36) Figura 2.4: Bomba mecánica de vacío.. Figura 2.5: Crecimiento de Películas Delgadas. La luz violácea corresponde al plasma durante el crecimiento.. Las películas de SnO2 prístino y de SnO2 dopado con Fe al 1% y 5% se crecieron en sustratos de vidrio y de silicio con tiempos de 30 min, 1 h, 2h, 3h y 4h. El detalle de estas películas se muestra en la tabla del Apéndice 1.. 25.
(37) 2.3.TRATAMIENTO TÉRMICO: Por los antecedentes en investigaciones de PD, sabemos que las películas crecidas sin tratamiento térmico son amorfas, el tratamiento térmico es importante para mejorar la cristalinidad de nuestras películas. Es por ello que a las películas delgadas se hizo un tratamiento térmico a 500°C por dos horas, en un horno VECSTAR PF2AF Furnace 1200°C - 6KW, Eurotherm. Mostrado en la figura 2.6. (Schneider, 1991).. a) b). Figura 2.6: a) Horno para el tratamiento térmico de las películas delgadas, b) Rejilla de soporte de las películas delgadas para ser tratadas térmicamente.. 2.4.. TECNICAS DE CARACTERIZACIÓN Todas las películas delgadas depositadas en sustratos de vidrio se caracterizaron por Difracción de Rayos X (DRX), espectroscopía Raman, espectroscopía Ultravioleta visible (UV-Vis),. mediciones eléctricas y. sensibilidad. Para la caracterización de Microscopía Electrónica de Barrido (MEB), sólo se pudo caracterizar las películas de SnO2 dopado con 5 % de Fe crecidas por 2h y 3h. Para mediciones magnéticas se utilizaron las películas de SnO 2 dopado con 1% y 5 % de Fe crecidas a 4 h y depositadas en sustratos de silicio.. 26.
(38) 2.4.1. DIFRACCIÓN DE RAYOS X Después del crecimiento de las películas delgadas se realizaron las caracterizaciones estructurales con Difracción de Rayos X (DRX) de los compuestos de SnO2 prístino y SnO2 dopado con Fe al 1% y 5%. Los datos de DRX fueron obtenidos con un equipo de la marca Rigaku que se muestra en la figura 2.7, perteneciente al Laboratorio de Difracción de Rayos X del Departamento de Geología, de la Universidad de Brasilia. Se usó una radiación de Cu Kα = 1.5487 Å, los patrones de difracción 2θ fueron corridos en un rango de 20 a 80 ° con un paso de 0.02°.. Figura 2.7: Difractómetro de Rayos X, usado para medidas de difracción de rayos X.. La difracción de rayos X aplicadas al estudio de materiales cristalinos, permiten obtener, en forma no destructiva, importante información sobre fases presentes, tensiones residuales, micro-deformaciones y orientaciones cristalográficas. En la interacción entre un haz de rayos X y un sólido cristalino, además del proceso de absorción, tiene lugar el fenómeno de difracción. En éste último se cumple la ley de Bragg. Un cristal es considerado como un material donde los átomos del sólido 27.
(39) están ordenados en una forma periódica formando una red. Estos átomos ordenados se convierten en fuente secundarias de radiación de rayos X, que poseen una diferencia de fase definida entre sí, que puede ser destructiva o constructiva según las direcciones. La ley de Bragg dice que se producirá difracción si se cumple la relación. 𝜆𝑛 = 2𝑑𝑠𝑒𝑛𝜃. (2.1). Donde es la longitud de onda de la radiación X utilizada, es el ángulo de difracción definido entre el plano de difracción y el haz incidente, d es la distancia interplanar y n un número entero u orden de la difracción (Figura 2.8). Los haces difractados están caracterizados no sólo por su posición angular respecto del haz incidente sino también por su intensidad y por su forma de línea. Está información se presenta en un gráfico de intensidad en función del ángulo 2, llamado difractrograma de rayos X.. Figura 2.8: Representación de Bragg, de una difracción de rayos-X, de acuerdo con reflexiones en fase, desde planos sucesivos de un sistema particular.. A través de la técnica de DRX podemos obtener información sobre los parámetros cristalográficos tales como; tamaño de cristalito. Un cristalito es un dominio pequeño que produce difracción coherente, por lo cual también es conocido como dominio coherente.. 28.
(40) En los experimentos se observan picos con cierto ancho debido a efectos combinados de un número de factores instrumentales y físicos. La forma y el ancho de un pico dependen fundamentalmente del tamaño medio del cristalito (o distribución de tamaños) y de las imperfecciones particulares que posee la red cristalina, de tal forma que mientras mayores sean estos efectos, mayor será el ancho a media altura del pico de difracción. (Henao, 2010) Con la ecuación de Scherrer (Ecuación. 2.2), se puede determinar el tamaño. promedio del cristalito.. 𝐷(ℎ𝑘𝑙) =. 𝐾𝜆 𝛽𝑐𝑜𝑠𝜃. (2.2). obtenida a partir de la ley de Bragg. Donde es la longitud de onda de la radiación incidente (CuKα=1.5406Å), β es el ancho a media altura del pico de difracción de la muestra (FWHM son siglas en inglés) medido en radianes y es la mitad del ángulo del pico máximo de la posición del pico de difracción, el valor 0.9 es el factor del cristal (K). (Hernández, 2014). En la figura 2.9 se muestra el patrón de DRX estándar del SnO2 tetragonal tipo Rutilo. En ésta se observan los picos principales de esta fase en el rango de 20º a 80º con los índices de Miller, pertenecientes a los planos de difracción respectivos. Las posiciones de mayor intensidad relativa a dos theta (2𝜃). (López, 2012).. Figura 2.9: Ficha cristalográfica estándar de difracción de rayos x del SnO2 tetragonal tipo rutilo (JCPDS 41-1445).. 29.
(41) 2.4.1.1. METODO DE RIETVELD El método de Rietveld o refinamiento de Rietveld, fue desarrollado en 1967 por Hugo Rietveld (Young, 1993), es un método de ajuste o de refinamiento de la estructura cristalina, que en sus inicios fue enfocado a la caracterización de una muestra monofásica y en la actualidad también se aplica a muestras polifásicas, permite evaluar aspectos microestructurales, como tamaño de cristal y microdeformación en diversos materiales. El ajuste engloba algunos criterios como: los parámetros de red (grupo espacial, sitios atómicos, distancias interplanares), del material, así como también los efectos del equipo, conocidos como efectos instrumentales que son ajustados en el refinamiento, el cual se realiza comparando el perfil teórico contra el perfil de difracción experimental (Ståhl, 2008). Para realizar el proceso de refinamiento, se necesita de los datos de intensidad medidos experimentalmente (yi), y datos teóricos de la estructura y así poder realizar la simulación de la estructura, para ajustarla al perfil de difracción experimental. El proceso de refinamiento se realiza, por el método de mínimos cuadrados entre el patrón observado (experimental) y el calculado (modelo inicial), obteniendo el mejor ajuste, es decir cuando el calculado se parezca lo más posible al perfil experimental, es cuando se decide terminar el ajuste. Los programas que desarrollan este método y que están disponibles en forma libre son Fullprof, DBWS y GSAS, entre otros. Nosotros usamos en el presente trabajo el EXPGUI-GSAS. Uno de los parámetros numéricos para evaluar la calidad del ajuste es el residuo Sy, también conocido como función residual cuya expresión es: 𝑆𝑦 = ∑𝑖 𝑤𝑖 (𝑦𝑖 − 𝑦𝑐𝑎𝑙 )2. (2.3). Donde 𝑤𝑖 = 1/𝑦𝑖 , 𝑦𝑐𝑎𝑙 es la intensidad experimental en el paso i-ésimo del difractograma, la sumatoria se extiende a todo el conjunto de puntos del difractograma que se desea ajustar (Young, 1993), 𝑆𝑦 es una función compleja. 30.
(42) que incluye todos los parámetros que dan lugar a un patrón de difracción (parámetros de celda, posición de los átomos, factores Debye-Waller). Además la ecuación no es lineal, por ende se debe obtener un valor mínimo en la ecuación.. Cálculo de la intensidad de los picos de difracción de rayos-X. Esta clase de cálculo mide punto por punto en el patrón de difracción de polvo, tanto picos de difracción como fondos que sobresalen en el difractograma, y esto se debe a factores físicos que son fácilmente cuantificables. Algunos de estos factores son: - Estructura cristalina (geometría de la celda unitaria, posiciones atómicas, vibraciones térmicas) - Características de la muestra (tamaño de cristal, concentración, microtensiones) - Condiciones instrumentales (foco, monocromaticidad del haz, absorción) Para este parámetro se utiliza la siguiente ecuación:. (2.4). Donde tenemos: A. Factor de Escala: SF es la intensidad del haz (depende de la muestra), Fj es la fracción volumen de la fase y Vj es el volumen celda de la fase. B. Factor de polarización de Lorentz: Este factor depende del instrumento de medición en parámetros como: geometría, monocromador (ángulo α), detector, tamaño del haz, volumen de la muestra, posicionamiento de la muestra (angular).. 31.
(43) C. Cálculo del factor de estructura: Es la capacidad de difracción de la celda unitaria, calculado por la dispersión atómica de la fase j y la posición de los átomos en la celda unitaria. El factor de estructura se calcula:. 𝐹𝑘,𝑗 = ∑𝑗 𝑁𝑗 𝑓𝑗 𝑒. −𝐵𝑗. 𝑠𝑒𝑛2 𝜃 𝜆2. 𝑒 2𝜋(ℎ𝑥𝑖 +𝑘𝑦𝑖+𝑙𝑧𝑖 ). (2.5). Nj es el sitio de ocupación de los átomos de la fase j que se encuentran en la unidad asimétrica, fj es el factor atómico de dispersión del j-ésimo átomo, Bj es el coeficiente de temperatura isotrópico y está relacionado con la vibración de los átomos originado por el efecto de la temperatura, h,k,l son los índices de Miller que producen la difracción,. xj, yj, zj son las. coordenadas relativas de las posiciones de los átomos en la celda unitaria, 𝜃 es el ángulo de incidencia del haz de rayos X. (Petrick & Castillo, 2004) D. Factor de forma estructural: Las características de los picos de difracción se determinan por la muestra y el instrumento, y se evalúa como 2θ. De manera que para modelar estos picos de difracción podemos usar las siguientes funciones: a. Gaussiana (G). 𝐺=. 4𝑙𝑛2(2𝜃𝑖 −2𝜃𝑘 )2 ) 𝐻2 𝑘. √4𝑙𝑛2 (− 𝑒 𝐻𝑘 √𝜋. (2.6). Donde Hk es el ancho a media altura del pico de difracción para la késima reflexión y (2θi-2θk) es el ángulo de Bragg para la k-ésima reflexión. b. Lorentziana (L). 𝐿=. 2 𝜋𝐻𝑘. 1 [1+4. (2𝜃𝑖 −2𝜃𝑘)2 ] 𝐻2 𝑘. (2.7). c. Pseudo-Voigt (pV) 𝑝𝑉 = 𝜂𝐿 + (1 − 𝜂)𝐺. (2.8). Esta ecuación trabaja con las ecuaciones de Lorentz y Gauss. 𝜂 = 0 describe la forma del pico de difracción como Gaussiana y 𝜂 = 1 si es Lorentziana. Si está entre 0 y 1 se utiliza la ecuación anterior donde:. 32.
(44) 𝜂 = 𝑁𝐴 + 𝑁𝐵 + 2𝜃. (2.9). NA y NB son variables refinables d. Thompson-Cox-Hastings (TCHZ), Es una variante de la pseudo-Voigt ambas utilizan la misma ecuación, la diferencia radica en la selección de parámetros a refinar y los que se calculan. 𝑇𝐶𝐻𝑍 = 𝜂𝐿 + (1 − 𝜂)𝐺. (2.10) 𝑍. 𝐻𝐺2 = 𝑈𝑡𝑎𝑛2 𝜃 + 𝑉𝑡𝑎𝑛𝜃 + 𝑊 + 𝑐𝑜𝑠2 𝜃 𝑌. 𝐻𝐿 = 𝑋𝑡𝑎𝑛𝜃 + 𝑐𝑜𝑠𝜃. (2.11) (2.12). Los parámetros U, V, W, X, Y e Z son parámetros que determinan la forma del perfil y son refinables por el programa. Con este modelo las componentes Lorentzianas y Gaussianas pueden ser obtenidas separadamente. Los parámetros U y X dan la medida de los alargamientos isotrópicos debido a las microdeformaciones de naturaleza Gaussiana y Lorentziana respectivamente, en cuanto los parámetros Z y Y dan las medida de los alargamientos isotrópicos debido a los efectos de los tamaños de los cristalitos de naturaleza Gaussiana y Lorentziana, respectivamente. Los parámetros V y W describen solamente las medidas de los alargamientos instrumentales. La largura a media altura total H de la línea experimental del perfil de difracción es calculada por medio de un polinomio de quinto grado en las varibles HL y HG.. E. Orientación Preferencial (textura), se usa la fórmula de March-Dollase. 1. 𝑀𝑘 2 𝑃𝑘.𝑗 = 𝑀 ∑𝑛=1 (𝑃𝑀𝐷 𝑐𝑜𝑠 2 𝛼𝑛 + 𝑘. 𝑠𝑒𝑛2 𝛼𝑛 −3/2 ) 𝑃𝑀𝐷. (2.13). Donde PMD es el parámetro de March-Dollase, la sumatoria se trabaja con las reflexiones h, k, l (Mk), 𝛼𝑛 es el ángulo entre el vector de orientación preferencial y el plano cristalográfico hkl.. 33.
Figure




Documento similar
E Clamades andaua sienpre sobre el caua- 11o de madera, y en poco tienpo fue tan lexos, que el no sabia en donde estaña; pero el tomo muy gran esfuergo en si, y pensó yendo assi
Habiendo organizado un movimiento revolucionario en Valencia a principios de 1929 y persistido en las reuniones conspirativo-constitucionalistas desde entonces —cierto que a aquellas
o Si dispone en su establecimiento de alguna silla de ruedas Jazz S50 o 708D cuyo nº de serie figura en el anexo 1 de esta nota informativa, consulte la nota de aviso de la
De hecho, este sometimiento periódico al voto, esta decisión periódica de los electores sobre la gestión ha sido uno de los componentes teóricos más interesantes de la
Como se discutió en la sección 5.3, las películas de BaTiO 3 sobre sustratos de Pt/TiO 2 /SiO 2 /Si presentan grietas como resultado del estrés que se presenta en la película
Products Management Services (PMS) - Implementation of International Organization for Standardization (ISO) standards for the identification of medicinal products (IDMP) in
This section provides guidance with examples on encoding medicinal product packaging information, together with the relationship between Pack Size, Package Item (container)
El Tratado de Maastricht introduce como elemento fundamental de la Unión Europea la cooperación en los ámbitos de la justicia y en los asuntos de interior (JAI) y establece la doble