2 que no usan insulina
Welschen LMC, Bloemendal E, Nijpels G, Dekker JM, Heine RJ, Stalman WAB, Bouter
LM
Reproducción de una revisión Cochrane, traducida y publicada en La Biblioteca Cochrane Plus, 2008, Número 2
Producido por
Si desea suscribirse a "La Biblioteca Cochrane Plus", contacte con:
Update Software Ltd, Summertown Pavilion, Middle Way, Oxford OX2 7LG, UK Tel: +44 (0)1865 513902 Fax: +44 (0)1865 516918
E-mail: info@update.co.uk
Sitio web: http://www.update-software.com
Usado con permiso de John Wiley & Sons, Ltd. © John Wiley & Sons, Ltd.
RESUMEN EN TÉRMINOS SENCILLOS...2
ANTECEDENTES...2
OBJETIVOS...3
CRITERIOS PARA LA VALORACIÓN DE LOS ESTUDIOS DE ESTA REVISIÓN...3
ESTRATEGIA DE BÚSQUEDA PARA LA IDENTIFICACIÓN DE LOS ESTUDIOS...3
MÉTODOS DE LA REVISIÓN...4
DESCRIPCIÓN DE LOS ESTUDIOS...6
CALIDAD METODOLÓGICA...7
RESULTADOS...8
DISCUSIÓN...9
CONCLUSIONES DE LOS AUTORES...10
AGRADECIMIENTOS...11
POTENCIAL CONFLICTO DE INTERÉS...11
FUENTES DE FINANCIACIÓN...11
REFERENCIAS...11
TABLAS...14
Characteristics of included studies...14
Characteristics of excluded studies...18
Table 01 Search strategy...19
Table 02 Methodological quality...20
Table 03 Effects of SMBG in patients with type 2 diabetes who are not using insulin...21
2 que no usan insulina
Welschen LMC, Bloemendal E, Nijpels G, Dekker JM, Heine RJ, Stalman WAB, Bouter
LM
Esta revisión debería citarse como:
Welschen LMC, Bloemendal E, Nijpels G, Dekker JM, Heine RJ, Stalman WAB, Bouter LM. Automonitorización de la glucemia en pacientes con diabetes de tipo 2 que no usan insulina (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, 2008 Número 2. Oxford: Update Software Ltd. Disponible en: http://www.update-software.com. (Traducida de The Cochrane Library, 2008 Issue 2. Chichester, UK: John Wiley & Sons, Ltd.).
Fecha de la modificación más reciente: 23 de febrero de 2005
Fecha de la modificación significativa más reciente: 23 de febrero de 2005
R E S U M E N
Antecedentes
Se descubrió que la automonitorización de la glucemia (SMBG) es eficaz para los pacientes con diabetes de tipo 1 y para pacientes con diabetes de tipo 2 que usan insulina. Existe mucha controversia sobre la efectividad de la automonitorización de la glucemia como herramienta en el automanejo para pacientes con diabetes de tipo 2 que no usan insulina.
Objetivos
El objetivo de esta revisión fue evaluar los efectos de la automonitorización de la glucemia en pacientes con diabetes mellitus de tipo 2 que no usan insulina.
Estrategia de búsqueda
Los estudios se obtuvieron de búsquedas de bases de datos bibliográficas electrónicas y múltiples, complementadas por búsquedas manuales de referencias de artículos recuperados. Fecha de la última búsqueda: Septiembre de 2004.
Criterios de selección
Se incluyeron ensayos controlados aleatorios que investigaron los efectos de la automonitorización de la glucemia en comparación con la atención habitual y con la automonitorización de la glucosa en orina en los pacientes con diabetes tipo 2 que no usan insulina. Los estudios incluidos deben haber usado al menos una de las siguientes medidas de resultado: control glucémico, calidad de vida, bienestar, satisfacción del paciente, o episodios hipoglucémicos.
Recopilación y análisis de datos
Dos revisores extrajeron los datos y evaluaron la calidad de los estudios incluidos de forma independiente. Los datos de los estudios se compararon para decidir si fueron suficientemente homogéneos para combinar en un metanálisis.
Resultados principales
Conclusiones de los autores
A partir de esta revisión se concluye que la automonitorización de la glucemia puede ser eficaz para mejorar el control glucémico en los pacientes con diabetes de tipo 2 que no usan insulina. Para evaluar los efectos beneficiosos potenciales de la SMBG en estos pacientes se requiere un ensayo controlado aleatorio amplio y bien diseñado. Este ensayo a largo plazo también debe investigar los resultados relacionados con los pacientes como calidad de vida, bienestar y satisfacción del paciente, y proporcionar al paciente educación adecuada para permitir que la SMBG sea eficaz.
✦
R E S U M E N E N T É R M I N O S S E N C I L L O S
La automonitorización de la glucemia puede ser eficaz al mejorar el control glucémico en pacientes con diabetes de tipo 2 que no usan insulina
La automonitorización de la glucemia se ha hallado eficaz como herramienta en el automanejo de los niveles de glucosa de los pacientes con diabetes de tipo 1 y pacientes con diabetes de tipo 2 que usan insulina. Los pacientes pueden usar los valores de glucosa para ajustar sus dosis de insulina. Los pacientes con diabetes de tipo 2 que no usan insulina pueden usar los valores de glucosa para ajustar su régimen dietético y estilo de vida. Los resultados de la revisión indican que la automonitorización de la glucemia puede ser eficaz para mejorar el control de glucosa. No hubo pruebas suficientes para estudiar si era beneficiosa para mejorar la calidad de vida, bienestar, satisfacción del paciente, o disminuir el número de episodios hipoglucémicos.
✦
A N T E C E D E N T E S
Diabetes mellitus
La diabetes mellitus es un problema de salud importante. Se calculó que en el año 2000 aproximadamente 177 millones de personas en todo el mundo tenían diabetes y se espera que este número se duplique en el año 2030. Las razones principales de este rápido aumento son el crecimiento de la población, el envejecimiento, los regímenes alimentarios insalubres, la obesidad y el estilo de vida sedentario (Wild 2000).
Las patologías primarias en la diabetes mellitus de tipo 2 incluyen una función beta-célula deficiente y resistencia a la insulina, lo que lleva a una alta concentración de glucosa en sangre. El grado de hiperglucemia y la duración de la diabetes se asocian con un mayor riesgo de aparición de complicaciones principalmente microvasculares; es decir, retinopatía, neuropatía y nefropatía (ADA 2003; Coster 2000a; Stratton 2000). El desarrollo y evolución de las complicaciones diabéticas, especialmente las complicaciones microvasculares, pueden reducirse mediante un mejor control de la glucemia. El Estudio de Diabetes Prospectiva del Reino Unido, por ejemplo, reveló que cada reducción de 1% de la hemoglobina glucosilada (HbA1c) se asoció con una disminución del 37% en el riesgo
relativo de complicaciones microvasculares y con una disminución del 21% en el riesgo relativo de cualquier variable principal de evaluación o muerte relacionada con la diabetes (Stratton 2000).
Automonitorización de la glucemia
Se ha sugerido que la educación en automanejo es una herramienta potente para el adecuado control de la glucemia
(ADA 1997). La automonitorización de la glucemia (SMBG) se recomienda comúnmente como un elemento central del automanejo (Holmes 2002).
La automonitorización procura recopilar información detallada sobre los niveles de glucosa en sangre en diferentes puntos temporales y permite la identificación oportuna de los niveles altos de glucosa en sangre. Se descubrió que la SMBG es eficaz para pacientes con diabetes tipo 1 (Bode 1999; DCCT 1993) y pacientes con diabetes tipo 2 que usen insulina (Nathan 1996; Karter 2001; ADA 1998) ya que la información acerca del nivel de glucosa de un paciente es útil para refinar y ajustar las dosificaciones de insulina, dando lugar a un mejor control glucémico.
Sin embargo, existe una gran controversia sobre si la SMBG es una herramienta eficaz en la automanejo de pacientes con diabetes de tipo 2 tratada sin insulina. Comúnmente, para esta categoría, se recomienda para la evaluación del control glucémico una visita cada tres meses a un médico general o enfermera de diabetes. Se sugirió que la automonitorización para el control de la glucemia puede reemplazar esta visita trimestral (Faas 1997; Coster 2000a; Coster 2000b).
una búsqueda extensa en diferentes bases de datos, halló sólo un nuevo estudio, además de las revisiones de Faas y Coster. Estas revisiones tenían algunas limitaciones metodológicas. Faas 1997 no efectuó búsquedas en otras bases de datos fuera de MEDLINE y no describió claramente los criterios para la calidad metodológica de los estudios y cómo se extrajeron los datos. Coster y cols. sí realizaron un metanálisis, pero informaron que la heterogeneidad entre los estudios incluidos y la calidad deficiente de los estudios eran limitaciones importantes en su análisis (Coster 2000b). Además, Faas 1997 y Coster 2000b también incluyeron un estudio con pacientes con diabetes de tipo 2 que usaron insulina, aunque la educación de automanejo depende del tipo de tratamiento. Probablemente se mantiene lo mismo para la eficacia de la SMBG. Los pacientes que usan insulina pueden usar los valores de las mediciones de glucosa para ajustar sus dosificaciones de insulina.
La cuestión planteada en nuestra revisión es si los pacientes con diabetes de tipo 2 que no usan insulina también pueden beneficiarse con la SMBG. Estos pacientes podrían hacer frente a su enfermedad de forma más independiente cuando usan SMBG, y podrían comprender mejor los factores que afectan su enfermedad y de ese modo percibir una mejora en su calidad de vida. La SMBG también puede mejorar el cumplimiento del tratamiento farmacológico y motivar a los pacientes a realizar cambios apropiados en su estilo de vida (Fontbonne 1989,Karter 2001). Esta cuestión no se ha respondido claramente en las revisiones mencionadas debido a la ausencia de calidad metodológica, así como la heterogeneidad de sus estudios incluidos y debido a la inclusión de los pacientes que usaron tratamiento de insulina. Además, no ha habido una revisión con nuevos estudios publicados desde enero de 2002.
O B J E T I VO S
Evaluar los efectos de la automonitorización de la glucemia en pacientes con diabetes de tipo 2 que no usan insulina.
C R I T E R I O S PA R A L A VA L O R AC I Ó N D E L O S E S T U D I O S D E E S TA R E V I S I Ó N
Tipos de estudios
Sólo se seleccionaron los ensayos controlados aleatorios.
Tipos de participantes
Los estudios se incluían en la revisión si los pacientes se diagnosticaban con diabetes mellitus de tipo 2 y no usaban el tratamiento de insulina.
Tipos de intervención
La intervención principal que se investigó en esta revisión es la automonitorización de la glucemia (SMBG). Los estudios referidos a la comparación entre la glucosa en orina y la monitorización de glucemia también fueron incluidos. En este
caso las intervenciones se compararon entre sí, y de lo contrario, se comparó la SMBG con la atención habitual sin SMBG.
Tipos de medidas de resultado Medidas de resultado principales
1. El control glucémico medido con la concentración de hemoglobina glucosilada (nivel de HbA1c) y el nivel de glucosa
plasmática en ayunas;
2. Calidad de vida, bienestar (p.ej. al usar el SF 36 (Ware 1992) o el cuestionario de bienestar (Bradley 1994a));
3. Satisfacción del paciente (p.ej. al usar el Cuestionario de Satisfacción del Tratamiento de Diabetes (DTSQ) (Bradley 1994b)).
Medidas de resultado adicionales
• Episodios hipoglucémicos; • Morbilidad;
• Efectos adversos; • Costos
Covariables consideradas modificadoras de efecto
• Control glucémico de valor inicial; • Cambio de medicación hipoglucémica; • Duración de la diabetes al inicio del estudio; • Edad;
• Cumplimiento a la intervención.
Momento de la evaluación del resultado
• Corto plazo: hasta seis meses de la intervención; • Mediano plazo: entre seis y doce meses de la intervención; • Largo plazo: más de 12 meses después de la intervención.
E S T R AT E G I A D E BÚ S QU E DA PA R A L A I D E N T I F I C AC I Ó N D E L O S E S T U D I O S
Búsquedas electrónicas
Se utilizaron estrategias de búsqueda electrónica, para identificar los ensayos relevantes (como se especifica en "tipos de estudios"), y las revisiones o metanálisis (para identificación de ensayos adicionales elegibles).
Se hicieron búsquedas en las siguientes bases de datos:
• MEDLINE (hasta septiembre 2004) (http://www.ncbi.nlm.nih.gov/PubMed/);
• The Cochrane Library (Número 4, 2004);
• NHS Economic Evaluation Database (NHS EED) (hasta setiembre de 2004) (www.cochranelibrary.com); • EMBASE (hasta septiembre 2004).
También se realizaron búsquedas en las bases de datos de ensayos en curso:
Current Controlled Trials (www.controlled-trials.com); T h e N a t i o n a l R e s e a r c h R e g i s t e r (http://www.nrr.nhs.uk/search.htm).
Grupo de Revisión Colaborador de Trastornos Metabólicos y Endocrinos. Para los detalles de la estrategia de búsqueda ver (Tabla 01) en "Tablas adicionales".
Búsquedas adicionales
Se buscaron publicaciones adicionales aptas en las listas de referencias de las revisiones identificadas y los estudios incluidos.
Podrían haberse identificado otras palabras clave de relevancia durante cualquiera de las búsquedas electrónicas u otras búsquedas. Sin embargo, este no fue el caso, de manera que las estrategias de búsqueda electrónica no se modificaron para incorporar estos términos.
M É TO D O S D E L A R E V I S I Ó N
Selección de ensayos
Dos observadores (LW, GN) inspeccionaron de forma independiente los títulos y resúmenes de las referencias identificadas para evaluar su potencial elegibilidad. Los ensayos se incluyeron si se cumplían en el estudio todos los criterios siguientes:
1. La población de los participantes constaba de pacientes con diabetes de tipo 2 que no usaban insulina.
2. El diseño era de un ensayo controlado aleatorio.
3. La intervención del ensayo era la automonitorización de la glucemia comparada con la atención habitual sin automonitorización de la glucemia (SMBG). Los ensayos que estudiaban la comparación entre la glucemia y la monitorización de glucosa en orina también fueron incluidos.
4. Los resultados se midieron según al menos una de las mediciones siguientes: HbA1c, glucemia en ayunas, calidad de
vida y bienestar, satisfacción del paciente.
No hubo restricciones de idioma. Si el título no proporcionaba suficiente información para decidir si el ensayo se incluía o no en la selección, se leía el resumen. El artículo completo se recuperaba para la aclaración, si el resumen no proporcionara suficiente información.
Los estudios eran eliminados si ambos revisores estaban de acuerdo en que el ensayo no reunía los criterios de inclusión en la revisión. Un tercero resolvió las diferencias de opinión (JD). El acuerdo entre evaluadores para la selección del estudio se midió con la estadística kappa (Cohen 1960).
En el caso de las publicaciones duplicadas se comprobó la consistencia de ambas y se incluyó la publicación con el período de seguimiento más largo.
Evaluación de la calidad metodológica
Dos revisores (LW, EB) evaluaron en forma independiente la calidad metodológica de los ensayos incluidos con una lista de puntuación. Se utilizó la lista de puntuaciones de Maastricht-Amsterdam (Tulder van 2003) para ensayos clínicos controlados y aleatorios que incluían todos los criterios de las listas de Jadad y cols. (Jadad 1996) y Verhagen y cols. (Verhagen 1998)
La lista original constaba de 19 elementos. De acuerdo con van Tulder y cols. (Tulder van 2003) en la presente revisión sólo se aplicaron los 11 elementos concernientes a la validez interna:
1) ¿El método de asignación al azar fue adecuado? *+ 2) ¿Se ocultó la asignación al tratamiento? *+
3) ¿Los grupos eran similares al inicio del estudio con respecto a los indicadores pronósticos más importantes? *+
4) ¿Estaba cegado el paciente a la intervención? *+ 5) ¿Se cegó al prestador de atención a la intervención? *+ 6) ¿Se cegó al evaluador de resultados a la intervención? *+ 7) ¿Se evitaron las cointervenciones, o éstas fueron comparables? +
8) ¿El cumplimiento fue aceptable en ambos grupos? + 9) ¿Se describió y fue aceptada la tasa de retiro o abandono? + 10) ¿El momento de la evaluación del resultado fue similar en todos los grupos?+
11) ¿El análisis incluyó un análisis del tipo intención de tratar (intention-to-treat analysis)? *+
* Elemento de la lista de Delfos (Verhagen 1998)
+ Elemento recomendado por van Tulder (Tulder van 2003) Los 11 elementos están incluidos en la lista completa de Maastricht-Amsterdam que es una combinación de los elementos de Jadad 1996 y Verhagen 1998.
Cada elemento tenía una escala de calificación de "sí", "no" o "no sabe". Si el sesgo fuera improbable, el elemento se calificaba positivo. Si el sesgo fuera probable, el elemento se calificaba negativo, o si la información respecto al elemento no estaba disponible, se calificaba con "no sabe".
Los estudios que cumplían seis o más de los 11 criterios de calidad se consideraron de "alta calidad". Todos los estudios que cumplían menos de 6 de los criterios se calificaron como "baja calidad". La calidad metodológica de cada estudio se tuvo en cuenta cuando se calculaba el efecto global, al explorar la calidad de los estudios en un análisis de sensibilidad. Ningún estudio se excluyó en función de los criterios metodológicos. El nivel inicial del acuerdo sobre los 11 criterios de calidad entre los dos revisores se informó como Kappa de Cohen (Cohen 1960). Se trataron las discrepancias en el nivel del elemento y si no se alcanzaba el consenso, un tercer revisor (GN) tomaba la decisión final.
Una prueba piloto, mediante dos ensayos excluidos de la revisión, precedió la evaluación de calidad de los ECA para evaluar la factibilidad de usar esta escala. Todos los elementos se definieron claramente y, al calificar los artículos con la lista, ambos investigadores debían obtener consenso en cada elemento de la lista.
Extracción de los datos
El formulario de extracción de datos adaptado incluyó los siguientes elementos:
1. Información general: autores, título, detalles de la revista, año de publicación, país, publicación duplicada.
2. Características de los ensayos: asignación aleatoria, ocultamiento de la asignación, análisis del tipo intención de tratar (intention-to-treat analysis).
3. Pacientes: criterios de inclusión y exclusión, criterios de diagnóstico, edad, sexo, grupo étnico, años de educación, duración de diabetes, peso, índice de masa corporal, glucosa plasmática en ayunas, HbA1c, comedicamentos, otras
características al inicio del estudio.
4. Intervención(es): tipo de intervención en ambos grupos, número de eventos de intervención, número de participantes en cada grupo, duración del estudio y seguimiento, momento de la intervención.
5. Características de la calidad metodológica: cálculo de potencia, semejanza de grupos al valor inicial, cegamiento (paciente, prestador de salud y evaluador de resultados), número de pérdidas o abandonos, cointervenciones, cumplimiento y efectos adversos.
6. Resultados: todas las medidas de resultado disponibles informadas en el ensayo.
7. Notas: otra información disponible revelada en el estudio que pueda ser importante para la revisión.
Una prueba piloto, nuevamente mediante dos ensayos excluidos de la revisión, precedió la extracción de datos del ECA seleccionado. Era probable que esta prueba identificara datos que no se necesitaron o que no se hallaron para optimizar la hoja de extracción de datos. Dos revisores en forma independiente realizaron la obtención y el ingreso de datos. (LW, EB). Cualquier discrepancia entre los revisores fue resuelta a través de la discusión y si no pudo alcanzarse el consenso, un tercer revisor (GN) adoptó una decisión final.
Análisis de los datos
Los resultados de cada ECA se combinaron como estimaciones puntuales con los correspondientes intervalos de confianza del 95%. La heterogeneidad se comprobó mediante la puntuación Z y la estadística de ji cuadrado, y la significación se fijó en p < 0,10. La cuantificación del efecto de heterogeneidad se evaluó por medio de I2, con una variación de un 0-100%, incluido su intervalo de confianza del 95% (Higgins 2002). I cuadrado demuestra el porcentaje de variación total entre los estudios debido a la heterogeneidad y se usó para juzgar la consistencia de las pruebas. Si las pruebas de la heterogeneidad estadística eran apreciables, se investigaban las posibles fuentes de variación entre los ECA. Se exploró la influencia de diferencias específicas entre los ECA, independientemente de cualquier evidencia de heterogeneidad estadística.
Se realizó un análisis cuantitativo (combinación estadística) sólo en los estudios clínicos homogéneos, para los cuales las poblaciones de estudio, intervenciones y resultados se consideraron similares por los revisores al comparar los formularios de extracción de datos de los estudios. Si los
estudios eran clínica y estadísticamente homogéneos, se llevó a cabo un metanálisis mediante el modelo de efectos fijos. Sin embargo, si se hallaba heterogeneidad significativa, era poco razonable suponer que había un efecto "verdadero" subyacente a los datos que fuera constante a través de diferentes poblaciones, y en ese caso se utilizó un modelo de efectos aleatorios. Los metanálisis separados se realizaron para las diferentes medidas de resultado.
Si los estudios eran clínica y estadísticamente heterogéneos o si faltaban datos, se realizaba un análisis cualitativo (síntesis de mejores pruebas) mediante un sistema de clasificación de niveles de las pruebas para resumir los resultados de los estudios respecto a la fuerza de las pruebas científicas. Los hallazgos se consideraban coherentes si más de uno de los estudios informaba sobre la misma dirección del efecto sobre la medida de resultado. El sistema de calificación constaba de cinco niveles de pruebas, basados en la calidad y el resultado de los estudios (Tulder van 2003).
1. Evidencia contundente - hallazgos consistentes entre múltiples ECA de alta calidad.
2. Evidencia moderada - hallazgos consistentes entre múltiples ECA de baja calidad y un ECA de alta calidad.
3. Evidencia limitada - un ECA de baja calidad.
4. Evidencia contradictoria - hallazgos inconsistentes en múltiples ECA.
5. Ninguna evidencia - ningún ECA.
Las posibles fuentes de heterogeneidad también se evaluarían mediante análisis de sensibilidad y de subgrupos, como se describe a continuación.
Los análisis se realizaron con el módulo estadístico en Review Manager 4.2 (software de Cochrane).
Análisis de subgrupos
Si había un efecto estadísticamente significativo para uno o más de las principales medidas de resultado y si la cantidad de datos lo permitía, se procuró realizar los análisis de subgrupos para determinar si había alguna diferencia sistemática entre grupos de pacientes.
Un análisis de subgrupos puede realizarse para:
• Nivel de hemoglobina glucosilada y nivel de glucosa plasmática en ayunas al valor inicial (subdividiéndose en tres grupos de nivel bajo, medio y alto según los datos) • Grupos de edad (menos de 60 años, más de 60 años); • Sexo;
• Duración de la diabetes (según los datos);
• Presencia de complicaciones (p.ej. complicaciones diabéticas);
• Diferentes intervenciones de comparación;
• Tipo de tratamiento: agentes hipoglucemiantes orales, régimen dietético, ejercicio, ningún tratamiento;
• Duración de la intervención (corto, medio y largo plazo, según los datos);
Análisisde sensibilidad
Se planificó un análisis de sensibilidad para investigar la influencia de los siguientes factores en el tamaño del efecto:
• Repetición del análisis con exclusión de los estudios particulares sobre, p.ej., las intervenciones combinadas; • Repetición del análisis en base a la calidad de los estudios,
como se especifica anteriormente;
• Repetición del análisis con exclusión de los estudios con un seguimiento largo o con un gran grupo de pacientes; • Repetición de los análisis con exclusión de los estudios
según los siguientes filtros: criterios diagnósticos, idioma de publicación, fuente de financiamiento (industrial versus otra), país.
La solidez de los resultados también se comprobó mediante la repetición de los análisis que utilizaban diferentes medidas del tamaño del efecto (diferencia de riesgo, odds-ratio, etc.) y diferentes modelos estadísticos (modelos de efectos fijos y aleatorios).
Sesgo de estudio pequeño
Si los estudios proporcionaban datos suficientes, el sesgo de estudio pequeño se evaluaba al usar un gráfico en embudo (funnel plot), mediante el cual las estimaciones de efecto de la medida de resultado común se graficó en coordenada con el tamaño de la muestra. El gráfico en embudo (funnel plot) fue evaluado visualmente. En ausencia de sesgos, el gráfico se asemeja a un embudo simétrico invertido. (Sterne 2001).
D E S C R I P C I Ó N D E L O S E S T U D I O S
La búsqueda en bases de datos computarizadas identificó un total de 572 citas.Figure 01). Después de excluir los títulos que evidentemente no estaban relacionados con el objetivo de nuestra revisión, se consideraron 90 estudios en el procedimiento de selección. El cribaje (screening) de las referencias dio lugar a otras 15 citas. Después de leer los resúmenes de los estudios, si estaban disponibles, se recuperaron 36 artículos de texto completos para la revisión adicional. No se hallaron publicaciones duplicadas. Sólo cinco ensayos controlados aleatorios cumplieron con todos los criterios de inclusión y se incluyeron en la revisión. Durante el proceso de revisión, recibimos la notificación de un artículo en etapa de publicación que también se incluyó en nuestra revisión (Davidson 2005). Cuatro estudios compararon la SMBG con la atención habitual sin monitorización (Davidson 2005; Guerci 2003; Muchmore 1994; Schwedes 2002), un estudio comparó la SMBG con la monitorización de glucosa en orina (Allen 1990) y un estudio era un ensayo de tres brazos que comparaba las tres intervenciones (Fontbonne 1989). Las razones principales de la exclusión de los otros estudios fueron que los ensayos no se asignaron al azar o que el ensayo también incluía pacientes con diabetes de tipo 1, o pacientes con diabetes de tipo 2 que usaban insulina. Estos ensayos distinguieron entre los diferentes grupos de pacientes. Las razones de exclusión de
los estudios aparecen en la tabla "Características de los estudios excluidos".
Figure 01
Diagrama de flujo del estudio
posprandiales. Además, la enfermera, que se cegó a la asignación al azar, siguió los algoritmos detallados para tomar sus decisiones terapéuticas. Los niveles HbA1c se midieron cada dos meses con un valor perseguido de <7,5%. La enfermera realizó cambios en la medicación para alcanzar este objetivo. Si el objetivo no se alcanzaba después de cuatro meses, se comenzaba el tratamiento de insulina.
Fontbonne 1989 estudió los cambios en el control metabólico durante seis meses en 208 pacientes diabéticos tratados sin insulina. El objetivo del estudio fue determinar si el uso de SMBG podría ayudar a este tipo de pacientes a aumentar su concienciación de la enfermedad y su cumplimiento del tratamiento, y también proporcionar al médico nuevas pruebas a partir de las cuales pueda ajustar el régimen dietético y el tratamiento oral. Los pacientes fueron asignados al azar a uno de los tres grupos de monitorización. El grupo A (n=68) tuvo monitorización médica bimestral con hemoglobina glucosilada, el grupo B (n=72) tuvo automonitorización del paciente de glucosa en orina y el grupo C (n=68) tuvo SMBG. En la visita de entrada, los pacientes recibieron una recomendación dietética personal basada en una revisión clínica de HbA1c, niveles de glucosa en sangre en ayunas y posprandiales, altura y peso. Sin embargo, no se proporcionó ningún algoritmo o estrategia predeterminada específicos para los cambios conductuales. Durante los seis meses de estudio, los pacientes se visitaron cada dos meses. En cada visita, se midieron el peso y HbA1c. Además, se le permitió al médico modificar las prescripciones dietéticas e hipoglucémicas orales.
Guerci 2003 realizó un estudio controlado aleatorio en 689 pacientes. El objetivo del estudio fue comparar el control metabólico en pacientes con diabetes deficientemente controlada con el tratamiento antidiabético oral, administrado sólo con recomendación habitual (grupo de evaluación convencional, n=344) o combinado con SMBG (n=345). Los pacientes en el grupo de evaluación convencional recibieron una revisión convencional basada en la evaluación de laboratorio de HbA1c cada 12 semanas. El grupo de SMBG recibió entrenamiento inicial proporcionado por su médico general en la visita de inclusión inicial. Los pacientes se siguieron cada seis semanas durante 24 semanas. En cada reunión, se informó a los pacientes sobre su nivel de glucosa en sangre, la necesidad de un buen control de la diabetes y la importancia de la pérdida de peso en combinación con actividad física. Todo ello fue realizado por médicos generales.
Muchmore 1994 probó la hipótesis que la combinación del uso de SMBG y el cálculo de carbohidratos dietético, mediante los resultados de monitorización sanguínea para configurar las cuotas de carbohidratos dietético, es beneficioso en el tratamiento de diabetes de tipo 2. Veintitrés pacientes con sobrepeso participaron en un programa conductual de control de peso de 28 semanas. Los participantes se asignaron al azar a un grupo de intervención (n=12) que recibió instrucciones individuales y de grupo sobre el cálculo de carbohidratos y SMBG, o a un grupo de control (n=11) que recibió idéntica cantidad de atención; se concentró en los principios generales
sobre nutrición para la diabetes según las recomendaciones de la Asociación de Diabetes Estadounidense. En ambos grupos, se recomendó que la composición de las comidas incluyera un 50% de calorías como carbohidratos, 30% como grasa y 20% como proteína. Las calorías totales se recomendaron individualmente en base a la pérdida de peso del paciente. El grupo de intervención aprendió la SMBG de su educador especializado en enfermería, tanto en sesión de grupo como individualmente. Los grupos se reunieron semanalmente durante cuatro semanas y luego cada cuatro semanas durante 16 semanas.
Schwedes 2002 investigó el efecto de la SMBG relacionado con comida sobre el control glucémico, el bienestar y la satisfacción con los tratamientos, en pacientes con diabetes de tipo 2 tratados sin insulina. En un estudio de seis meses, con seis meses de seguimiento, los participantes se asignaron al azar a dos grupos. El grupo de intervención (n=113) utilizó un dispositivo de monitorización de glucemia, llevó un diario con los datos de la glucemia y de las comidas, y recibió orientación estandarizada. Se les explicó a los pacientes que la SMBG y su diario les proporcionarían la información acerca de su control glucémico diario, permitiéndoles hacer los ajustes apropiados a su régimen dietético y estilo de vida. El grupo de control (n=110) recibió orientación no estandarizada sobre el régimen dietético y el estilo de vida. Los pacientes eran citados cada cuatro semanas. Las enfermeras evaluaron el uso correcto del dispositivo de monitorización en el grupo de intervención. Los pacientes continuaron la monitorización durante el período de seguimiento.
En la tabla con "Características de los estudios incluidos" se resumen datos adicionales sobre los tamaños de la muestra, la edad y la duración de la diabetes y tipo de intervenciones y resultados.
C A L I DA D M E TO D O L Ó G I C A
Para un resumen de la calidad metodológica de los ensayos incluidos ver "Cuadros Adicionales" (Tabla 02)
El acuerdo inicial entre ambos revisores sobre la calidad metodológica general fue un 91%. Las discrepancias se presentaron principalmente debido a errores en la lectura y diferencias en la interpretación de la lista de criterios metodológicos. Después de la reunión de consenso, no persistió la disconformidad. No hubo necesidad de llarmar al tercer revisor para tomar una decisión final.
azar pacientes en grupos de 10 con el uso de una tabla de números aleatorios generada por un ordenador, lo cual se considera un ocultamiento de asignación inadecuado. Los otros cinco estudios no describieron claramente el método de asignación al azar.
Ninguno de los estudios mostró diferencias estadísticamente significativas entre los grupos de pacientes. Davidson 2005 fue el único estudio que cegó al evaluador de resultados. Un dietista y una enfermera proporcionaron supervisión en ambos grupos con decisiones terapéuticas según los algoritmos detallados, sin conocimiento del estado de la SMBG del paciente. Para este tipo de intervención, no fue posible cegar al paciente y al prestador de salud, y por consiguiente estos criterios de evaluación metodológica se consideraron no aplicables. En lo que se refiere a las cointervenciones, como el tratamiento con otros medicamentos o asesoramiento nutricional, Allen 1990 y Guerci 2003 informaron que éstos se evitaron. Davidson 2005 proporcionó la misma información en ambos grupos. Se consideró que el grupo de SMBG en Schwedes 2002 recibió una cointervención por medio de un programa de orientación estructurado, cada cuatro semanas durante el período de intervención. El grupo de control sólo recibió orientación no estandarizada. Además, Muchmore 1994 proporcionó instrucción individual y de grupos sobre el concepto del control de carbohidratos para los pacientes de la intervención. Sin embargo, ya que el grupo de control recibió una cantidad idéntica de atención, aunque con un énfasis en los principios generales de la nutrición para la diabetes según las normas de práctica de ADA, se consideró que no había ninguna cointervención en este estudio. Esta consideración se basó en los hallazgos de que un mejoramiento en los niveles HbA1c se asocia con más atención por los prestadores de salud (DeVries 2003). Fontbonne 1989 no proporcionó información sobre este tema.
El cumplimiento se consideró aceptable en cuatro estudios. En el estudio de Allen 1990, la asistencia a las visitas necesarias excedieron el 98% para ambos grupos y todos los pacientes demostraron el dominio del examen de orina y sangre. El cumplimiento medido por el número de tiras de Fontbonne 1989 fue deficiente en el grupo de automonitorización de glucosa en orina y se obtuvo lo esperado en el grupo de automonitorización de glucemia. Muchmore informó que el cumplimiento del paciente de los requisitos del protocolo fue alto y que todos menos un paciente en el grupo de control completaron las reuniones del grupo. Schwedes 2002 sólo describió el cumplimiento durante el seguimiento. Después del período de intervención de 6 meses, el 87% de los pacientes en el grupo de automonitorización de glucemia todavía monitorizaban sus niveles de glucosa en sangre durante los seis meses del seguimiento. Guerci 2003 no proporcionó información sobre este tema y Davidson 2005 halló que los pacientes realizaron en promedio un 45% del número total de las pruebas necesarias, lo cual se consideró no aceptable. Cinco estudios tenían una tasa aceptable de retiros o abandonos. En el estudio de Allen 1990, 61 pacientes se asignaron al azar
a las intervenciones en competencia y 54 completaron el estudio. Fontbonne 1989 informó que 44 pacientes (21%) se perdieron durante el seguimiento. De los 29 sujetos reclutados para el estudio de Muchmore 1994, seis abandonaron antes o en el momento de la asignación al azar. Schwedes 2002 describió que después de la asignación al azar, se produjeron 27 pérdidas de los 250 pacientes. Davidson 2005 informó que sólo un paciente no volvió a visitar al profesional de enfermería después de ser asignado al azar. Sólo Guerci 2003 informó una tasa de abandonos de más de 40%, que se consideró no aceptable. El momento de la evaluación del resultado en los grupos de pacientes fue similar en todos los estudios.
Allen 1990 y Schwedes 2002 no realizaron un análisis por intención de tratar (intention-to-treat analysis) y Fontbonne 1989 y Muchmore 1994 no fueron claros en este tema. Davidson 2005 y Guerci 2003 incluyeron a todos los pacientes que fueron asignados al azar en uno de sus grupos en el análisis.
R E S U LTA D O S
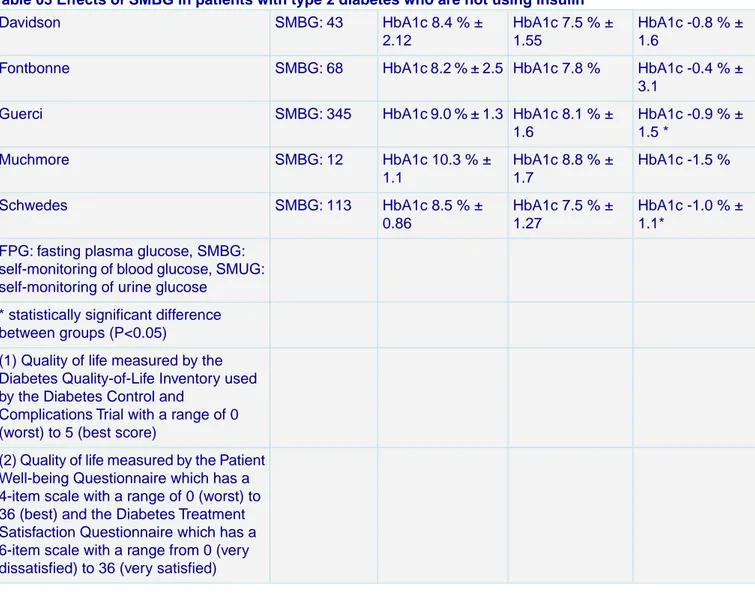
Para un resumen de las características del valor inicial de los pacientes en los estudios y de los efectos de la SMBG sobre medidas de resultado diferentes, consúltese "Cuadros Adicionales" (Tabla 03).
Heterogeneidad
Debido a las diferencias de datos de valor inicial de los pacientes y el tipo de intervenciones entre los estudios, no fue posible realizar un metanálisis ni un análisis de subgrupos o de sensibilidad.
Los datos de valor inicial de los pacientes difirieron en cuanto al control glucémico de 12,4 en Allen 1990 a 8,2 en Fontbonne 1989. Los estudios con un valor inicial mayor de los niveles de HbA1c revelaron una mayor reducción en HbA1c final. Además, la duración de la diabetes al valor inicial varió desde 13,3 años en Fontbonne 1989 a 5,2 años en Muchmore 1994 y Schwedes 2002.
Las intervenciones de los estudios fueron también diferentes. Schwedes 2002 proporcionó instrucción sólo en el grupo de SMBG mientras que los otros estudios proporcionaron la misma cantidad de atención en ambos grupos. Fontbonne 1989 no proporcionó información suficiente sobre el tipo de intervención.
Medidas de resultado principales
Control glucémico medido con HbA1c
de Davidson 2005, HbA1c disminuyó un 0,8% en el grupo de SMBG y un 0,6% en el grupo de control.
Schwedes 2002 halló, al final del estudio, una diferencia estadísticamente significativa de un 0,5% en HbA1c entre los grupos, a favor de la SMBG. Guerci 2003 también halló, al final del estudio, una diferencia estadísticamente significativa de un 0,4% en HbA1c entre el grupo de SMBG y el grupo de control.
Allen 1990 comparó la SMBG con la automonitorización de la glucosa en orina y halló que ambos grupos tuvieron un HbA1c inferior al final del estudio; sin embargo, no se halló ninguna diferencia entre los grupos ya que ambos mostraron una disminución del 2,0%.
Control glucémico medido por glucosa plasmática en ayunas
Sólo los estudios Allen 1990 y Guerci 2003 midieron los niveles de glucosa plasmática en ayunas. Ambos hallaron que los niveles de glucosa plasmática en ayunas disminuyeron como resultado de la SMBG; sin embargo, no había ninguna diferencia estadísticamente significativa entre la SMBG y automonitorización de glucosa en orina o sin monitorización, respectivamente.
Calidad de vida, bienestar y satisfacción del paciente
Muchmore 1994 halló resultados idénticos en el grupo de SMBG y de control para el mejoramiento en las escalas de calidad de vida (satisfacción, repercusión, preocupación-social-vocacional y preocupación relacionada con la diabetes).Schwedes 2002 también halló que el bienestar y la satisfacción con el tratamiento mejoraban en la misma medida en ambos grupos. Ningún estudio halló diferencias estadísticamente significativas entre los grupos.
Medidas de resultado adicionales
Episodios hipoglucémicos
Sólo Guerci 2003 investigó el efecto de la automonitorización de la glucemia en la frecuencia de hipoglucemia asintomática y sintomática (glucemia capilar < 3 mM/L). Hallaron una diferencia significativa en el número de pacientes que informaron al menos un episodio de hipoglucemia asintomática durante el estudio. Este resultado no se consideró válido debido al hecho de que no fue posible medir este tipo de hipoglucemia en el grupo control. Ningún episodio de hipoglucemia grave se notificó durante este estudio.
Niveles de las pruebas
Se realizó un análisis cualitativo (síntesis de mejores pruebas) para dar una recomendación sobre los efectos de la automonitorización de la glucemia, ya que no fue posible realizar un metanálisis debido a la heterogeneidad clínica entre los estudios.
Cuatro estudios hallaron más mejoramiento en los niveles de HbA1c en los grupos de automonitorización de la glucemia que en los grupos de atención habitual (Davidson 2005; Guerci 2003; Muchmore 1994; Schwedes 2002), diferencia que alcanzó significación estadística en dos de estos estudios (Guerci 2003; Schwedes 2002). Uno de estos estudios fue de alta calidad
(Davidson 2005) y los otros estudios fueron de calidad deficiente y por consiguiente se llegó a la conclusión de que actualmente sólo existen pruebas moderados sobre el efecto de la SMBG sobre HbA1c. Además, no existen pruebas de que la SMBG tenga un efecto beneficioso sobre la glucosa plasmática en ayunas, la calidad de vida, el bienestar, la satisfacción del paciente y el número de episodios hipoglucémicos. Estos resultados se midieron en sólo unos pocos ensayos y no alcanzaron significación estadística.
Un estudio comparó la SMBG con la automonitorización de la glucosa en orina y no halló ninguna diferencia en los niveles HbA1c entre los dos grupos (Allen 1990).
D I S C U S I Ó N
En nuestra revisión sólo pudieron incluirse seis ensayos controlados aleatorios para evaluar los efectos de la automonitorización de la glucemia, a partir de varias mediciones de resultado en pacientes con diabetes de tipo 2 que no usaban insulina. Debido a la heterogeneidad clínica de los estudios, no fue posible realizar un metanálisis en los datos combinados. Por consiguiente, se realizó un análisis cualitativo y se concluyó que el nivel de evidencia en esta revisión sobre si la SMBG tuvo un efecto sobre el control glucémico fue moderado. No se encontraron pruebas significativas suficientes de que la SMBG tuviera un efecto beneficioso sobre otros resultados, ya que sólo un estudio informó los datos sobre los episodios hipoglucémicos (Guerci 2003) y sólo dos estudios informaron algunos datos sobre la calidad de vida y la satisfacción del paciente (Schwedes 2002).
conocer que están observándose las medidas de resultado. Este denominado efecto Hawthorne también podría haber dado lugar a una subestimación de la eficacia de la SMBG (DeVries 2003; Renders 2001).
Una limitación de tres estudios fue que no se les dio ninguna instrucción estándar a los pacientes para ajustar su comportamiento y cambiar su estilo de vida, así como la medicación, para modificar sus valores de glucosa (Allen 1990; Fontbonne 1989; Guerci 2003). Muchmore 1994 combinó el uso de SMBG con el control de carbohidratos dietético, lo que alentó el cambio de comportamientos en el régimen dietético y el ejercicio. Su grupo de control recibió idéntica cantidad de atención concentrada en el régimen dietético y el ejercicio. Existió más mejoramiento en el nivel de HbA1c en el grupo de SMBG, pero no fue estadísticamente significativo. Schwedes 2002 proporcionó un diario de comidas y un programa estructurado de orientación sólo en el grupo de SMBG y halló una disminución significativa en HbA1c en el grupo de SMBG. Sin embargo, ya que esto se consideró una cointervención, el efecto aislado de la SMBG no está claro.
Davidson 2005 fue el único estudio cegado, que garantizó que la educación fuera la misma en los grupos. Un dietista y una enfermera proporcionaron supervisión en ambos grupos con decisiones terapéuticas según los algoritmos detallados, sin conocimiento del estado de la SMBG del paciente. Los niveles de HbA1c disminuyeron más en el grupo de SMBG; sin embargo, no había ninguna diferencia estadísticamente significativa entre los grupos. Esto puede deberse al pequeño número de pacientes incluidos en el estudio o a la posibilidad de que la población minoritaria, principalmente de bajo nivel educativo, puede no haber interpretado adecuadamente la información proporcionada por las enfermeras.
Además, Faas 1997 descubrió con anterioridad que la educación sobre cómo los cambios de hábitos del estilo de vida son esenciales para mostrar los efectos positivos de la SMBG sobre el control glucémico. El grupo de control debe recibir los mismos temas sobre el estilo de vida con la misma intensidad para evaluar el efecto de la SMBG.
Aspectos metodológicos
Se realizó una búsqueda extensa de bibliografía en tres bases de datos electrónicas consideradas de la alta calidad; sin embargo, es posible que se hayan pasado por alto algunos ensayos relevantes que no se publicaron o no se incluyeron en estas bases de datos. Estos temas pueden haber causado un efecto sobreestimado de la SMBG debido al sesgo de publicación (Egger 1998). No se buscaron los ensayos no publicados ya que esto es sumamente lento y probablemente conduciría al sesgo de selección, ya que no responderían todos los investigadores. Sí se incluyeron artículos en etapa de publicación, halladas mediante notificaciones de investigadores en nuestra red.
La conclusión de esta revisión debe interpretarse con precaución, ya que la calidad metodológica de los ensayos fue limitada en cuatro de los seis estudios incluidos. El hecho de que el ocultamiento de la asignación de tratamientos no era
claro en todos los estudios es un indicio importante para el sesgo de selección. Schulz 1995 halló que los ensayos con ocultamiento de la asignación inadecuado o poco claro produjeron cálculos desproporcionados de los efectos del tratamiento. Por otro lado, los resultados de la evaluación de la calidad metodológica dependen de una decisión que se tomó a priori con respecto al punto de corte utilizado en la estimación del nivel de las pruebas. Esta decisión sigue siendo arbitraria y puede haber influido en la conclusión de esta revisión (Tulder van 2003). Sin embargo, ya que no fue posible realizar un metanálisis, este método de evaluación de la calidad se seleccionó como un método objetivo y reproducible para poder dar una recomendación metodológica sobre los efectos de la automonitorización de la glucemia.
C O N C L U S I O N E S D E L O S AU TO R E S
Implicaciones para la práctica
A partir de esta revisión se concluye que la SMBG puede ser eficaz en la mejora del control glucémico en pacientes con diabetes de tipo 2 que no usan insulina. Revisiones anteriores (Faas 1997; Holmes 2002; Coster 2000a) informaron que la evidencia existente era insuficiente; sin embargo, en la presente revisión se ha utilizado un protocolo con estrictos criterios de inclusión y exclusión, y se han incluido tres nuevos ensayos realizados tras publicararse las tres revisiones mencionadas (Davidson 2005; Guerci 2003; Schwedes 2002). Dos de estos nuevos ensayos hallaron un efecto estadísticamente significativo de la SMBG sobre HbA1c (Schwedes 2002; Guerci 2003). Sin embargo, uno de éstos tenía una cointervención con educación en el régimen dietético y estilo de vida (Schwedes 2002). Los hallazgos significativos levantaron la expectativa de un efecto beneficioso en ensayos controlados aleatorios futuros, amplios y bien diseñados. Además, se le prestó más atención a medidas de resultado alternativas importantes, como calidad de vida, bienestar, satisfacción del paciente y episodios hipoglucémicos, en comparación con revisiones anteriores. Sin embargo, existían escasos datos sobre estos parámetros. En conclusión, al usar SMBG, los pacientes pueden lograr un tratamiento más individualizado de su enfermedad y en consecuencia una mejor calidad de vida, lo cual puede resultar en una disminución de las consultas con el médico general.
Implicaciones para la investigación
régimen dietético, estilo de vida y medicación, preferentemente con la participación de un dietista. Una enfermera de diabetes para la educación en los aspectos de la SMBG también debe supervisar el grupo de SMBG. Para investigar los efectos a largo plazo, se necesita un período de seguimiento largo. Además, debe evaluarse un rango de resultados. La investigación del control glucémico es importante, ya que resultará en una disminución en el desarrollo de complicaciones micro y macrovasculares (Stratton 2000). La calidad de vida y la satisfacción del paciente, sin embargo, son también muy importantes, ya que el confort y el malestar del paciente desempeñan una función crucial en el éxito de la intervención. Es también importante estudiar los subgrupos de pacientes según edad, duración de diabetes y valores de HbA1c al valor inicial. Con estos análisis puede determinarse si la SMBG es más eficaz en un grupo especial de pacientes, como los pacientes recién diagnosticados o los pacientes deficientemente controlados.
AG R A D E C I M I E N TO S
Se agradece al Dutch Cochrane Centre la provisión de un taller sobre el desarrollo de una revisión sistemática y por su ayuda
con la búsqueda en EMBASE. También se agradece a Ingrid Riphagen su ayuda con la elaboración de la estrategia de búsqueda y a Daniëlle van der Windt por su ayuda en el diseño del metanálisis.
P OT E N C I A L C O N F L I C TO D E I N T E R É S
Ninguno conocido.
F U E N T E S D E F I N A N C I AC I Ó N
Recursos externos
• La información sobre los recursos de apoyo no está disponible
Recursos internos
• Institute for Research in Extramural Medicine NETHERLANDS
✦
R E F E R E N C I A S
Referencias de los estudios incluidos en esta revisión
Allen 1990 {published data only}
Allen BT, DeLong ER, Feussner JR. Impact of glucose self-monitoring on non-insulin-treated patients with type II diabetes mellitus. Randomized controlled trial comparing blood and urine testing. Diabetes Care 1990;13(10):1044-50.
Davidson 2005 {unpublished data only}
Davidson MB, Castellanos M, Kain D, Duran P. The effect of
self-monitoring of blood glucose concentrations on glycated hemoglobin levels in diabetic patients not taking insulin: a blinded, randomized trial..
American Journal of Medicine In press:a blinded, randomized trial. Am J
Med. In press.
Fontbonne 1989 {published data only}
Fontbonne A, Billault B, Acosta M, Percheron C, Varenne P, Besse A et al. Is glucose self-monitoring beneficial in non-insulin-treated diabetic patients? Results of a randomized comparative trial. Diabete & Metabolisme 1989;15(5):255-60.
Guerci 2003 {published data only}
Guerci B, Drouin P, Grange V, Bougneres P, Fontaine P, Kerlan V et al. Self-monitoring of blood glucose significantly improves metabolic control in patients with type 2 diabetes mellitus: the Auto-Surveillance Intervention Active (ASIA) study. Diabetes Metab 2003;29(6):587-94.
Muchmore 1994 {published data only}
Muchmore DB, Springer J, Miller M. Self-monitoring of blood glucose in overweight type 2 diabetic patients. Acta Diabetol 1994;31(4):215-9. Schwedes 2002 {published data only}
Schwedes U, Siebolds M, Mertes G. Meal-related structured self-monitoring of blood glucose: effect on diabetes control in non-insulin-treated type 2 diabetic patients. Diabetes Care 2002;25(11):1928-32.
Referencias de los estudios excluidos de esta revisión
Clua Espuny 1999
Clua Espuny JL, Puig Junoy J, Ciurana Roca E, Garcia Bernal G, Monclus Benet JF, Gonzalez Henares A et al. [Blood glucose self-monitoring (BGSM): an evaluation of its prescription and results in type-2 diabetes. The Research Group in Primary Care of Tortosa]. Aten Primaria 1999;24(6):316-25.
Clua Espuny 2000
Clua Espuny JL, Puig Junoy J, Queralt Tomas ML, Palau Galindo A. [Cost-effectiveness analysis of self-monitoring of blood glucose in type 2 diabetics]. Gac Sanit 2000;14(6):442-8.
Evans 1999
Evans JM, Newton RW, Ruta DA, MacDonald TM, Stevenson RJ, Morris AD. Frequency of blood glucose monitoring in relation to glycaemic control: observational study with diabetes database. BMJ 1999;319(7202):83-6. Franciosi 2001
Franciosi M, Pellegrini F, De Berardis G, Belfiglio M, Cavaliere D, Di Nardo B et al. The impact of blood glucose self-monitoring on metabolic control and quality of life in type 2 diabetic patients: an urgent need for better educational strategies. Diabetes Care 2001;24(11):1870-7. Gallichan 1994
Gallichan MJ. Self-monitoring by patients receiving oral hypoglycaemic agents: a survey and a comperative trial. Pract Diabetes 1994;11(1):28-30. Gallichan 1997
Gimeno Orna 2001
Gimeno Orna JA, Rodriguez Andres M, Enciso Ciriano L, Bosque Luna P, Boned Juliani B. Self monitoring of blood glucose as a predictor of glycated hemoglobin.. Medifam - Revista de Medicina Familiar y
Comunitaria 2001;11(6):325-30.
Goldstein 2003
Goldstein DE , Little RR, Lorenz RA, Malone JI, Nathan DM, Peterson CM. Tests of glycemia in diabetes. Diabetes Care 2003;26 Suppl 1:S106-8. Hanninen 2001
Hanninen J, Takala J, Keinanen-Kiukaanniemi S. Good continuity of care may improve quality of life in Type 2 diabetes. Diabetes Res Clin Pract 2001;51(1):21-7.
Harris 2001
Harris MI. Frequency of blood glucose monitoring in relation to glycemic control in patients with type 2 diabetes. Diabetes Care 2001;24(6):979-82. Jaber 1996
Jaber LA, Halapy H, Fernet M, Tummalapalli S, Diwakaran H. Evaluation of a pharmaceutical care model on diabetes management. Ann Pharmacother 1996;30(3):238-43.
Karter 2001
Karter AJ, Ackerson LM, Darbinian JA, D'Agostino RB, Ferrara A, Liu J et al. Self-monitoring of blood glucose levels and glycemic control: the Northern California Kaiser Permanente Diabetes registry. The American
Journal of Medicine 2001;111(1):1-9.
Kibriya 1999
Kibriya MG, Ali L, Banik NG, Khan AK. Home monitoring of blood glucose (HMBG) in Type-2 diabetes mellitus in a developing country.
Diabetes Res Clin Pract 1999;46(3):253-7.
Klein 1993
Klein CE, Oboler SK, Prochazka A, Oboler S, Frank M, Glugla M et al. Home blood glucose monitoring: effectiveness in a general population of patients who have non-insulin-dependent diabetes mellitus. J Gen Intern
Med 1993;8(11):597-601.
Kwon 2004
Kwon HS, Cho JH, Kim HS, Song BR, Ko SH, Lee JM et al. Establishment of blood glucose monitoring system using the internet. Diabetes Care 2004;27(2):478-83.
Lane 2000
Lane JD, McCaskill CC, Williams PG, Parekh PI, Feinglos MN, Surwit RS. Personality correlates of glycemic control in type 2 diabetes. Diabetes
Care 2000;23(9):1321-5.
Leese 1994
Leese GP , Jung RT , Newton RW. Home glucose monitoring in patients aged over 40 years with diabetes mellitus.. Practical Diabetes 1994;11:32-4. Lehmann 2001
Lehmann R, Kayrooz S, Greuter H, Spinas GA. Clinical and technical evaluation of a new self-monitoring blood glucose meter: assessment of analytical and user error. Diabetes Res Clin Pract 2001;53(2):121-8. Meier 2002
Meier JL, Swislocki AL, Lopez JR, Noth RH, Bartlebaugh P, Siegel D. Reduction in self-monitoring of blood glucose in persons with type 2 diabetes results in cost savings and no change in glycemic control. Am J
Manag Care 2002;8(6):557-65.
Miles 1997
Miles P, Everett J, Murphy J, Kerr D. Comparison of blood or urine testing by patients with newly diagnosed non-insulin dependent diabetes: patient survey after randomised crossover trial. BMJ 1997;315(7104):348-9. Nathan 1996
Nathan DM, McKitrick C, Larkin M, Schaffran R, Singer DE. Glycemic control in diabetes mellitus: have changes in therapy made a difference?.
Am J Med 1996;100(2):157-63.
Newman 1990
Newman WP, Laqua D, Engelbrecht D. Impact of glucose self-monitoring on glycohemoglobin values in a veteran population. Arch Intern Med 1990;150(1):107-10.
Ozmen 2002
Ozmen B, Boyvada S. Can self-monitoring blood glucose control decrease glycated hemoglobin levels in diabetes mellitus.. Endocrinologist 2002;12(4):349-56.
Patrick 1994
Patrick AW, Gill GV, MacFarlane IA, Cullen A, Power E, Wallymahmed M. Home glucose monitoring in type 2 diabetes: is it a waste of time?.
Diabet Med 1994;11(1):62-5.
Rindone 1997
Rindone JP, Austin M, Luchesi J. Effect of home blood glucose monitoring on the management of patients with non-insulin dependent diabetes mellitus in the primary care setting. Am J Manag Care 1997;3(9):1335-8. Rutten 1990
Rutten G, van Eijk J, de Nobel E, Beek M, van der Velden H. Feasibility and effects of a diabetes type II protocol with blood glucose self-monitoring in general practice. Fam Pract 1990;7(4):273-8.
Soumerai 2004
Soumerai SB, Mah C, Zhang F, Adams A, Barton M, Fajtova V et al. Effects of health maintenance organization coverage of self-monitoring devices on diabetes self-care and glycemic control. Arch Intern Med
2004;164(6):645-52. Tattersall 1979
Tattersall RB. Home blood glucose monitoring. Diabetologia 1979;16(2):71-4.
Tattersall 1992
Tattersall R. Self monitoring of blood glucose concentrations by non-insulin dependent diabetic patients. BMJ 1992;305(6863):1171-2.
Watkins 2000
Watkins KW, Connell CM, Fitzgerald JT, Klem L, Hickey T, Ingersoll-Dayton B. Effect of adults' self-regulation of diabetes on quality-of-life outcomes. Diabetes Care 2000;23(10):1511-5. Wing 1986
Wing RR, Epstein LH, Nowalk MP, Scott N, Koeske R, Hagg S. Does self-monitoring of blood glucose levels improve dietary compliance for obese patients with type II diabetes?. Am J Med 1986;81(5):830-6. Referencias adicionales
ADA 1997
American Diabetes Association. Self-monitoring of blood glucose (consensus statement). Diabetes Care 1997;19(Suppl1):S62-S66. ADA 1998
American Diabetes Association. Test of glycemia in diabetes. Diabetes
Care 1998;21:S69-71.
ADA 2003
American Diabetes Association. Standards of medical care for patients with diabetes mellitus. Diabetes Care 2003;26,Suppl (1):S33-S49.
Bode 1999
Bode BW, Gross TM, Thornton KR, Mastrototaro JJ. Continuous glucose monitoring used to adjust diabetes therapy improves glycosylated hemoglobin: a pilot study. Diabetes Research and Clinical Practice 1999;46(3):183-90.
Bradley 1994a
Bradley 1994b
Bradley C. Diabetes Treatment Satisfaction Questionnaire. In Handbook of Psychology and Diabetes: A Guide to Psychological Measurement in Diabetes Research and Practice. Bradley C, Ed. Chur, Switzerland, Harwood Academic. 1994:111-32.
Clarke 2003
Clarke M, Oxman AD. Locating and selecting studies. Cochrane Reviewers'
Handbook 4.2.0 [updated March 2003]. Section 5.
http://www.cochrane.dk/cochrane/handbook/handbook (accessed 30 April 2003)
Cohen 1960
Cohen J. A coefficient of agreement for nominal scales. Educational and
Psychological Measurement 1960;20:37-46.
Coster 2000a
Coster S, Gulliford MC, Seed PT, Powrie JK, Swaminathan R. Monitoring blood glucose control in diabetes mellitus: a systematic review. Health
Technology Assessment 2000;4(12):i-iv,1-93.
Coster 2000b
Coster S, Gulliford MC, Seed PT, Powrie JK, Swaminathan R. Self-monitoring in Type 2 diabetes mellitus: a meta-analysis. Diabetic
Medicine 2000;17(11):755-61.
DCCT 1993
The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. The Diabetes Control and Complications Trial Research Group.
N Engl J Med 1993;329(14):977-86.
DeVries 2003
DeVries JH, Snoek FJ, Kostense PJ, Heine RJ. Improved glycaemic control in type 1 diabetes patients following participation per se in a clinical trial--mechanisms and implications. Diabetes Metab Res Rev 2003;19(5):357-62.
Egger 1998
Egger M, Smith GD. Bias in location and selection of studies. BMJ 1998;316(7124):61-6.
Faas 1997
Faas A, Schellevis FG, Van Eijk JT. The efficacy of self-monitoring of blood glucose in NIDDM subjects. A criteria-based literature review.
Diabetes Care 1997;20(9):1482-6.
Higgins 2002
Higgins JP, Thompson SG. Quantifying heterogeneity in a meta-analysis.
Statistics in Medcine 2002;21(11):1539-58.
Holmes 2002
Holmes V, Griffiths P. Self-monitoring of glucose levels for people with type 2 diabetes. British Journal of Community Nursing 2002;7(1):41-6.
Jadad 1996
Jadad AR, Moore RA, Carroll D, Jenkinson C, Reynolds DJ, Gavaghan DJ et al. Assessing the quality of reports of randomized clinical trials: is blinding necessary?. Controlled Clinical Trials 1996;17(1):1-12. Renders 2001
Renders CM, Valk GD, Griffin SJ, Wagner EH, Eijk Van JT, Assendelft WJ. Interventions to improve the management of diabetes in primary care, outpatient, and community settings: a systematic review. Diabetes Care 2001;24(10):1821-33.
Robinson 2002
Robinson KA, Dickersin K. Development of a highly sensistive search strategy for the retrieval of reports of controlled trials using PubMed.
International Journal of Epidemiology 2002;31:150-3.
Schulz 1995
Schulz KF, Chalmers I, Hayes RJ, Altman DG. Empirical evidence of bias. Dimensions of methodological quality associated with estimates of treatment effects in controlled trials. JAMA 1995;273(5):408-12.
Sterne 2001
Sterne JA, Egger M, Smith GD. Systematic reviews in health care: Investigating and dealing with publication and other biases in meta-analysis.
BMJ 2001;323(7304):101-5.
Stratton 2000
Stratton IM, Adler AI, Neil HA, Matthews DR, Manley SE, Cull CA et al. Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study. BMJ 2000;321(7258):405-12.
Tulder van 2003
Tulder M van, Furlan A, Bombardier C, Bouter L. Updated method guidelines for systematic reviews in the cochrane collaboration back review group. Spine 2003;28(12):1290-9.
Verhagen 1998
Verhagen AP, de Vet HC, de Bie RA, Kessels AG, Boers M, Bouter LM et al. The Delphi list: a criteria list for quality assessment of randomized clinical trials for conducting systematic reviews developed by Delphi consensus. Journal of Clinical Epidemiology 1998;51(12):1235-41. Ware 1992
Ware JE Jr, Sherbourne CD. The MOS 36-item short-form health survey (SF-36). I. Conceptual framework and item selection. Medical Care 1992;30(6):473-83.
Wild 2000
TA B L A S
Characteristics of included studies Allen 1990 Study
Randomised controlled trail. Randomised in groups of 10 with the use of a computer-generated table of random numbers.
Duration: 6 months Methods
Country: USA
Number of participants: 54 Inclusion criteria:
- type II diabetes mellitus, not treated with insulin -a fasting plasma glucose level >8.8 and <22 mM -no history of ketoacidosis
-current treatment with diet alone or diet and an oral hypoglycaemic agent -no active infection or serious illness
-no physical or mental handicap precluding participation in the treatment program (determined by the cognitive-capacity screening examination and a physical-abilities questionnaire)
Exclusion criteria: SMBG devices used previously, serum creatinine level >177 mM - Mean age:
SMBG: 58.2 years ± 9.7 urine testing: 57.9 years ± 10.7 - Diabetes duration:
SMBG: 6.8 years ± 6.5 urine testing: 9.0 years ± 10.3 Participants
1. SMBG group (n=27) and standardized treatment program including diet and exercise counseling. At least 36 blood glucose determinations/month, before each meal every other day.
2. Urine-testing group (n=27) and standardized treatment program including diet and exercise counseling. At least 36 urine glucose determinations/month, before each meal every other day.
Interventions
1. Fasting plasma glucose, obtained monthly by glucose oxidase method. 2. Glycosylated haemoglobin, obtained initially and at 3 and 6 months by affinity chromatography.
3. Total cholesterol and high-density lipoprotein cholesterol, measured by spectrophotometer with Beckman Dri-STAT reagents.
4. Weight, obtained monthly, patients fully clothed. Outcomes
Notes
C Allocation concealment
Davidson 2005 Study
Randomised controlled trial Duration: 6 months
Characteristics of included studies
Country: USA
Number of participants: 89 Inclusion criteria:
-patients not taking insulin - Mean age:
SMBG: 49.8 years ± 11.2 Control: 50.9 years ± 11.0 - Diabetes duration: SMBG: 5.5 years ± 4.7 Control: 5.8 years ± 5.8 Participants
1. SMBG (n=43): measurement of glucose levels before and between one and two hours after eating meals six days a week.
2. Control (n=45)
Patients in both groups were scheduled to meet with dietician five times; at
randomisation and 2, 4, 8 and 12 weeks later. Dietician used glucose levels and meal descriptions in nutritional counseling. A nurse followed detailed algorithms to make therapeutic decisions.
Interventions
1. HbA1c, measured at entry to the study and every two months Outcomes
Notes
B Allocation concealment
Fontbonne 1989 Study
Randomised controlled trial.
Randomisation procedure stratified by clinic. Duration: 6 months
Methods
Country: France
Number of participants: 208 Inclusion criteria:
-non-insulin dependent diabetic patients
-treated with diet and/or oral hypoglycaemic agents
-poorly controlled at entry to trial, FPG >8.8 mmol/l, or postprandial blood glucose level >11.1 mmol/l, 3 times within the preceding year.
Presence of at least occasional glucosuria (renal glucose threshold <11 mmol/l) was to be ascertained. -no rapidly progressing diabetic complications, no severe illness -duration of diabetes: at least 3 years
-first contact to the diabetes clinic at least 6 months before entry to trail -having attended to at least 2 outpatient visits since their first contact - Mean age:
SMBG: 54.5 years ± 10.7 Urine glucose: 54.9 years ± 10.2 Control: 56.3 years ± 9.1
- Diabetes duration: SMBG: 12.2 years ± 6.6 Urine glucose: 13.3 years ± 6.8 Control: 12.7 years ± 0.8 Participants
1. Regular HbA1c determinations every two months, no self-monitoring (n=54). 2. Self-urine glucose monitoring, twice every other day (n=54).
Characteristics of included studies
1. Weight, measured every two months.
2. HbA1c assayed by low-pressure liquid chromatography, measured every 2 months. 3. Number of reactive strips reported in a diary, recorded every two months.
Outcomes
Notes
B Allocation concealment
Guerci 2003 Study
Randomised controlled trial Duration: 6 months
Methods
Country: France
Number of participants: 689 Inclusion criteria:
-type 2 diabetes with a known duration over 1 year
-insufficiently controlled with oral antidiabetic treatment (HbA1c >7.5 and <11.0%) -age between 40 and 75 years
-not previously treated with insulin -not requiring insulin at inclusion -not previously received SMBG -able to carry out SMBG Exclusion criteria:
-type 1 diabetes, MODY and secondary diabetes
-recent weight loss of more than 3 kg during the last 3 months -impending complications of diabetes
-pregnant women -unable to read or write -uncooperative
- Mean age:
SMBG: 60.9 years ± 9.4 Control: 62.2 years ± 9.1 - Diabetes duration: SMBG: 7.7 years ± 6.3 Control: 8.4 years ± 6.6 Participants
1. SMBG (n=345) in addition to the conventional laboratory work-up. Education on weight loss and physical activity; treatment alterations by physician. Measurements at least 6 times per week, on 3 different days, including weekends
2. Control (n=344): conventional laboratory work-up based solely on laboratory measurement of HbA1c every 12 weeks. Education on weight loss and physical activity; treatment alterations by physician
Interventions
1. Weight, SBP, DBP at baseline, 3 and 6 months.
2. HbA1c, determined using the DCA analyser and blood glucose. Measured at baseline, 3 and 6 months.
3. Number of hypoglycaemic episodes Outcomes
Notes
B Allocation concealment
Muchmore 1994 Study
Randomised controlled trial Duration: 28 weeks (-8, 0-20 intervention) and follow-up till 44 weeks.
Characteristics of included studies
Country: USA
Number of participants: 23 Inclusion criteria:
-obese subjects (BMI 27.5-44 kg/m2) -aged 40-75 years
-a history of at least 1 year of non-insulin requiring diabetes
-treated either with diet alone or diet plus oral sulfonylurea hypoglycaemic agents -HbA1c within the range of 9.5%-13.5%
-ability to comply with the protocol
-absence of serious underlying medical or psychiatric illness, drug abuse or alcohol Exclusion criteria: subjects who had performed SMBG within the previous 3 months or those previously instructed in dietary carbohydrate counting.
- Mean age:
SMBG: 57.3 years ± 8.0 Control: 60.1 years ± 7.3 - Diabetes duration: SMBG: 5.7 years ± 4.8 Control: 5.2 years ± 4.6 Participants
Four groups were formed over a period of 6 months, blocking for variables of weight, HbA1c, diet vs. oral agent use, and sex
Weeks -8 to 0: identical run-in for all 4 groups: weekly behavioural weight control program + counselling by diabetes nurse educator + session with dietician. Follow-up session educator at weeks 1, 3 and 24 and dietician at weeks 1 and 3.
Week 0: randomly assignment to control or SMBG interventions.
1. Intervention (n=12): individual and group teaching on CHO counting and SMBG, measured 6 times daily for 4 weeks. Reduced to pre- and postprandial testing of a single meal per day for weeks 4-20. Beyond week 20, individual's election and expense. 2. Control (n=11): identical amount of attention, focus on general principles of diabetes nutrition.Groups continued to meet weekly for weeks 0-4 and then every 4 weeks for weeks 4-20.
Interventions
1. HbA1c, measured at weeks -8, 0, 16, 28 and 44. 2. Body weight measured at every patient encounter. 3. Diabetes Quality of Life Inventory at weeks 0, 24 and 44. Outcomes
Notes
B Allocation concealment
Schwedes 2002 Study
Multicenter, randomised controlled design Randomised in blocks of eight.