Universidad de Colima
FACULTAD DE CIENCIAS BIOLOGICAS
Y AGROPECUARIAS
"VIRULENCIA DE Metarhizium anisopliae (Metsch.) Sor.,
COMOAGENTEDECONTROLBIOLOGICODE
Anastrephaludens (Loew)
T E S I S
COMO REQlJiSiTO PARCiAt PARA
o bwvm
Ei TídodE
MAESTRO EN C IENC IAS
AREA: MICROBIOLOGIA
Esta tesis fue realizada bajo la direccibn del grupo de asesores
abajo indicados, la cual ha sido aprobada por el mismo y aceptada
como requisito parcial para obtener el grado de:
Maestro en Ciencias
En
BIOLOGIA DE LA PRODUCCION AGROPECUARIA
AREA: MICROBIOLOGIA
ASESORES:
Dr. Luis Felipe Bojalil jaber
Dr. Roberto Lezama Gutierrez
Dr. Miguel Arenas Vargas
Dr. Antonio Flores Diaz
Dr. Fausto Sánchez y Garcia-Figueroa
Dr. Hector González Cerezo
AGRADECIMIENTOS
M i agradecimiento al Laboratorio de Producción y cris
masiva de mosca de la fruta, ubicado en Metapa de Domfnguez
Chiapas, por su apoyo brindado para el fortalecimiento de larvas
de A.- ludens, para la realizacibn de la presente investigación.
Tambien, al M.C. Jorge Toledo Arreola, investigador del Centro de
Investigaciones Ecolbgicas del Sureste, de Metapa de Dominguez
Chiapas, por su apoyo durante la realizacibn de esta
investigación, por la revisión y sugerencias aportadas para el
desarrollo del proyecto de investigacibn, ahora terminado en
tesis. Al Dr. Martin Aluja S. investigador del Instituto de
Ecología, A. C. de Xalapa, Veracruz, p o r s urevisión y
recomendaciones, del proyecto de investigaciõn y sus valiosos
comentarios de la tesis terminada; además, por haber aceptado
formar parte en calidad de sinodal en este exámen.
A l Lic. Fernando Moreno Pena, Rector de la Universidad de
Colima; al Ing. Lorenzo Hernandez Arreguin, Secretario General; al
Dr. Luis Felipe Bojalil, Director del Posgrado en Biología de la
Producciõn; al Dr. Carlos E. Izquierdo Espinal, Delegado Regional
No. 2 y al Ing. Emilio SBnchez Arévalo, Director de la Facultad
de Ciencias Biologicas y Agropecuarias, a todos ellos, m i m&s
sincero agradecimiento, por haberme recibido en sus aulas
educativas.
A l Ing. René Alejandro Orosco Santoyo, Delegado Estatal de la
Secretaria de Agricultura Ganaderia y Desarrollo Rural; al Ing.
Eduardo E. Prieto Salazar, Jefe del Distrito 01; al Lic. Jose
Manzo Rosas, Jefe de Capacitación y Productividad; a la Lic.
Alicia Velasco Vaca, también de la Unidad de Capacitaciõn, a todos
depositaron en mi.
Al Dr Miguel Arenas Vargas, profesor del Posgado, por ensenarme
una de las formas de encontrarle sentido a la realidad de las
cosas. Asf mismo, quiero manifestar mi gratitud al Dr. Roberto
Lezama Gutierrez, profesor y Coordinador del Posgrado, por los
conocimientos que compartiõ con paciencia y respeto, para guiarme
en esta investigación.
A los doctores Antonio Flores Diaz, Fausto SBnchez y
Garcia-Figueroa, Judith Licea de Arenas, Hector Gonzalez Cerezo,
asesores del Posgrado, a ellos mil gracias por asesorar mi proceso de formación.
A mis campaneros y amigos gracias por su apoyo y amistad,
Y a todos aquellos que participaron, para hacer posible la realización de este trabajo mil gracias
DEDICATORIA
Dedico este trabajo a la gente de mi pueblo, a la que pertenece
la clase social a la que yo pertenezco, a la que no ha tenido la
oportunidad o los medios para desarrollar su capacidad y
creatividad.
Con todo mi amor, a mis hijas, Thamara y Amarantha.
A mis padres y hermanos.
A Rosario Licea y J. Jesús González
Al Movimiento 24 horas de A.A. que me ha dado vida.
A Lucía Trujillo de la Luz. Mi segunda Madre.
tlVIRULENCIA DE Metarhizium anisopliae (Metsch.) Sor., COMO AGENTE DE CONTROL BIOLOGICO DE Anastrepha ludens (Loew)".
RESUMEN
La fruticultura es una actividad importante para la economia y una fuente de alimento en el mundo; sin embargo, se ve limitada por un complejo de especies de moscas de la fruta. En Mexico representan uno de los m&s grandes
exportacion de frutas y hortalizas, con perdidas anuales estimadasimpedimentos, para la en 30, 000 millones de nuevos pesos.
fruta en el pais se dificulta, por motivo de que tienen al rededorEl manejo de las moscas de la de 700 000 ha de frutales hospederos; dentro de ellos el
citricos, manzano, durazno, guayaba y zapotes, distribuidos enmango, forma irregular en el pais.
Una de las especies de mosca de la fruta, mas distribuidas e n la Replclblica Mexicana, es la conocida como Anastrepha ludens
(LoW , misma que tiene varios cultivos hospederos, pero ataca con mayor frecuencia, a citricos y mango. Sin embargo, los programas de manejo de moscas de la fruta en MCxico, involucran al complejo de especies presentes en cada regibn, como son el trampeo a base d e insecticida-cebo, que captura diferentes especies; íiberacibn de parasitoides, que no son especificos; el uso de feromonas sexuales, que atrapan hasta 10 veces más que las
alimenticias, y la liberaciõn de moscas esteriles, quetrmpasson especificas, entre otros m6todos.
No obstante lo anterior, los logros alcanzados hasta la fecha son alentadores, pero el problema de las moscas en el mundo, no ha sido resuelto;
alternativas, por lo que se tienen que buscar otras
manejo integrado de la plaga. Uno de ellos, lo representa elque permitan utilizarse dentro de programas de unuso potencial
bacterias, que tienen los organismos entornopatógenos,nematodos y hongos. tales como
Dentro de estos altimos, el hongo Metarhizium anisopliae (Metsch.) Sorokin es considerado como un agente potencial de
control biológico de plagas, comercializa
en algunos paises. En moscas de la fruta,al grado de que ya se
capitata (Wiedemann) y Anastrepha striata, este hongo no ha sidoa excepción de Ceratitis evaluado en otras especies, por lo que se hace necesario conocer
desarrollar investigaciones tendientes a demostrar la
potencialidad de uso de este hongo.
S e conoce que la virulencia de los
varia entre especies, e inclusive entre aisladoshongos entornopatógenosde una misma
especie. Lo anterior, evaluen diferentes
aislados para seleccionar el mas virulento. El presente trabajohace necesario que se tuvo como objetivo, evaluar la virulencia de 20 aislamientos del hongo M. aniso liae
laboratõrio. --+.&,~~,;;'y d;~~er~~;u~~~~~;o ;zraA*;;-;g s; efectividad en condiciones de campo.
S e encontró, que todos los aislados de M. anisopliae resultaron virulentos en larvas de A. ludens,- con- mortalidades
aislados, causaron una mortalidad entre 90 y 98.75%. A los tres aislados mejores, que no compartieron igualdad estadistica con el grupo de aislados del segundo nivel de significancia, se les determino su respectiva CL50, que estuvo comprendida entre 3.7 x
5 5
10 y 4.8 x 10 conidios por ml. El tiempo letal 50% de todos los 8
aislados, a la concentración de 1 x 10 conidios por ml, estuvo comprendida entre 1.8 y 14.8 dias; sin embargo, se registró en 13 de los 20 aislados un valor menor de 5 dias.
En base a los resultados anteriores, se seleccion6 al aislado Ma 2, para ser evaluado en campo, en dos localidades y suelos de textura diferente; se encontrá, que el hongo es capaz de reducir la emergencia de adultos, en mas del 50%, con respecto al testigo en suelo de textura franca y en un 31% en suelos con textura arena migajonosa. Esto demuestra que el hongo M. anisopliae puede reducir poblaciones de &. ludens bajo condiciones de campo.
Palabras Clave: Metarhizium anisopliae, Anastrepha ludens, Virulencia, Condiciones de campo, Textura de suelo.
VIRULENCE OF Metarhizium anisopliae (Metchsch.) Sor., AS BIOLOGICAL CONTROL AGENT OF Anastrepha ludens (Loew).
ABSTRACT Laboratory
virulence of 20 isolates of entomopathogenicand field tests were conducted to determine the ;;~~;~li~;oe~¶etsch.) Sor. on third instar larvae offungus Metarhizium
a t the dose of Anastrepha
laboratory,
isolate. fóur groups of
lxlOE+8 conidia per ml. In 20 larvae were inoculated with each Control was formed with others four
larvae immersed in distilled sterile water. groups of 20
The experiment was conducted at 25+loC
1ight:Dark photophase. The percent of mortãlity withand 12:12 hours was recordet each 48 hours. With three of the best isolates,the fungusone
second experiment was conduted to determine the
concentrations. Dilutions of lxlOE+l, lxlOE+2,..., CL50 conidia per ml were made, and four groups of third instarand lxlOE+7
were inoculated with each concentration larvae
mortality was utilised to determine of each isolated. Total
In field conditions, the CL50 by Probit Analysis.
effectiveness of one experiment was conduted, to evalue the ludens, in two texture soils.isolate Ma2, on adults emergence number of A.Four groups of 100 third instãr larvae were placed in plots of 0.25 m2 of soil surface, inoculated
bY aspersion with 200 ml of a conidial concentration of
conidia per ml, of the fungus. lxlOE+8
Others four groups were utilised as
application control, with the
carried in twoof sterile distilled water only. Thesoil textures, Free and sand loand textures.experiment wasThe number of emerged adults was recorded.
Al1 isolates of M.
larvae of A. ludens: anisopliae were virulent on thirdbetween instar 98.75%. However, 8 of the 20Mortality rates variedinsolates 37%, and mortality, with rates between 90% at 98.75%. The lethal timecaused the greater (LT50), was estimated for the isolates, at concentration 5gf lxlOE+8 conidia per ml.
however, Its ranged between 1.8 at 14.8 days;
days. in 13 of the 20 isolates registred a value as lower as 5
With the three best
differents with the second isolates, within statistical utilised to determine their CL50 values.significant 1tsleve1 grow ,betweenwere
3.7xlOE+5 at 4.8xlOE+5 conidia per ml. ranged
Based on the isolate was
selected to evaluate in field conditions,laboratory results, the Ma 2on two different soil
textures, was
to reduce and environmental conditions. The fungus control, the adults emergence, more
capable than 50% with
in the free texture soil, respect toThis
results show that the M. anisopliae and 31% in sandy texture.
adults emergence of A-.-ludens under in field conditions.fungus reduce the populations
Ke Y words: Metarhizium anisopliae, Anastrepha ludens,
Field Conditions, Sol1 Texture. Virulence,
INDICE Agradecimientos ---Dedicatoria __---Resumen __---_--_--_---Abstract -_---Indice
___-__--_-__-__---____________________---Lista de cuadros
__---Lista de figuras
___-__--_-_---1 . INTRODUCCION
-_---II. 2.1 2.2 2.3 2.4 2.5 2.6 2.7 2.8 ANTECEDENTES
-_---Las moscas de la fruta
---Origen y zoogeograffa
---Taxonomia
-_---Descripcidn de Am ludens
-Cultivos hospederos
---Biología y habitos ---Mecanismos de deteccibn
---Control
__---2.8.1 Combate quimico
---2.8.2 Cultural y mecanice
---2.8.3 Legal
___----2.8.4 Liberación de insectos estériles
---2.8.5 Control biológico
---2.9 Los hongos entomopatbgenos
---2.9.1 El hongo Metarhizium
---2.9.2 Insectos hospederos de M. anisopliae ---w--v---
-2.9.3 Mecanismo de infección ---2.9.4 Melanización cuticular
_-2.9.5 Producci6n de metabolitos
2.9.6 Toxinas entomopatõgenas
---2.9.7 Condiciones de temperatura, luz y humedad para la reproduccibn
---2.9.8 Patogenicidad, virulencia y agresividad ---e--w
2.9.9 Virulencia de M. anisopliae-
---III MATERIALES Y METODOS
---3.1 Lugar de la experimentación
---3.1.1 Etapa experimental en laboratorio
---3.1.2 Hongos entomopatõgenos
---3.1.3 Multiplicaciõn de los hongos
---3.1.4 Cuantificacion de conidios
---3.1.5 Insecto prueba
---3.1.6 Experimentos
---3.2 Etapa experimental bajo condiciones de campo
---3.2.1 Pruebas preliminares en un suelo de textura franco, bajo condiciones naturales de campo.
---3.3 Análisis estadfsticos
---IV RESULTADOS
----L---28
28
29
29
32
32
32
32
33
33
35
35
37
37
39
40 4.1 Virulencia de los aislados de M. Anisopliae en larvas
el tercer estadio de A. ludens.---- 40
4.2 Efectividad del aislado M. anisopliae Ma.2, en el control de la emergencia de adultos de A. ludens, en dos locali-dades con texturas diferentes --- 44
V DISCUSION
---5.1 Virulencia de veinte aislados del hongo M. anisopliae de &. ludens. ----L---_
5.2 Efectividad de M. anisopliae en
campo---VI CONCLUSIONES
---VII LITERATURA CITADA
---48
48
51
56
57
LISTA DE CUADROS
[image:11.575.46.532.73.665.2]Páginas
Cuadro No. 1 Posición taxonómica de &. ludens --- 9
Cuadro No. 2 Plantas hospederas de &. ludens segtin varios
autores ---___--- 10
Cuadro No. 3 Mezcla de proteina hidrolizada mas insecticida utilizado en el control de moscas de la fruta en MCxico, ---_--- 17
Cuadro No. 4 Susceptibilidad de A. suspensa a los nematodos Steinernema spp. y H.-bacteriophora. --- 23
Cuadro No. 5 Susceptibilidad de moscas de la fruta al nematodo 2. feltiae. --- 23
Cuadro No. 6 Aislados del hongo M. anisopliae utilizados en la investigaciõn. ---_----_--- 34
Cuadro No. 7 Análisis fisico quimico de dos tipos de suelo--- 37
Cuadro No. 8 Porcentages de mortalidad de larvas del tercer estadio de A. ludens causada por el hongo M.
anisopliae.--- 41
Cuadro No. 9 Análisis de varianza de la mortalidad de larvas de tercer estadio de A. ludens, por diferentes
aislados del hongo M. -anisopliae. --- es--- 42
Cuadro No.10 Tiempos letales 50% del hongo M. anisopliae. en larvas del tercer estadio de &. ludens. ---w---w- 43
Cuadro No.11 Concentraciones letales del hongo M.
en larvas del tercer estadio de &. -lum-- 44
Cuadro No.12 AnAlisis de varianza del ntimero promedio de moscas emergidas de A. ludens, bajo condiciones de campo, tratadas -con M. anisopliae, en dos
localidades con diferentes-tipos de suelo.--- 45
Cuadro No.13 Nnmero promedio de moscas emergidas de &. ludens, bajo condiciones de campo, tratadas con M. anisopliae, en dos localidades con diferente tipo de suelo. --- 45
Cuadro No.14 Temperatura ambiente y humedad del suelo, registradas durante la experimentaciõn, en la
localidad de Villa de Alvarez, Colima.--- 46
Cuadro No.15 Condiciones de temperatura (OC) y humedad (å), que durante el periodo experimental de campo en Tecoman, --- 47
LISTA DE FIGURAS
Pbgina
Figura 1. Caracteristicas morfológicas de A. ludens. . . 11
Figura 2. Ciclo Biolbgico de A. ludens. . . 14
[image:12.575.47.534.104.218.2]1 INTRODUCCION
La fruticultura es una actividad importante para la economia
y una fuente inapreciable de alimento, para la población en el
mundo (Yang et al., 1994). Del cultivo del mango, a nivel
-mundial, se tiene una superficie cultivada de 1 000 000 de ha, con
una producción de 15.7 millones de toneladas de fruta; los
principales paises donde se cultiva son los paises Asiaticos de
Filipinas y Tailandia; Africa del Sur, Australia, Israel, la
Brasil, Perti y Venezuela (Medina, 1993).
En México, la fruticultura se practica en todos los
estados; la diversidad de condiciones climdticas, permite contar
con una temporada de cultivo mas, que en Estados Unidos de Norte
America, CanadB o Europa; ademas, se cuenta con una gran
variedad de frutales (Carreõn, 1993). Se reportan 32 especies
fruticolas, explotadas comercialmente, en una superficie de 1
6102 41 ha; la producción es superior a 12 millones de toneladas
anuales, valuada en 2000 millones de dolares (SAGDR, 1993); lo que
demuestra la importancia de esta actividad agrícola.
Del cultivo de mango, se cuenta con una superficie sembrada
de temporal de 92,347 ha y 45,945 ha de riego; de las cuales,
80,666 ha estan en produccibn bajo condiciones de temporal y
39,698 ha en areas de riego; con una produccion total de
1,151,192.0 toneladas por ano (SARH, 1993). En 1989 se exportaron
40, 000 toneladas de fruta fresca, con un valor de 23 millones de
dolares americanos (Bustos et al., 1993); ademas, este cultivo-
-genera alrededor de 350 mil empleos (SARH-DGSV, 1993).
N o obstante lo anterior, la fruticultura en México se ve
están consideradas como
exportaciõn de frutas y hotalizas (Reyes
el impedimento m&i importante en la
e t al. I 1991,
- Aluja,
1994; Hearth, et al., 1994). Se reporta que en 1994 se decomisaron
291 toneladas de fruta, destinada para exportacibn y se
incineraron y/o se enterraron 387 toneladas, por estar infestada
de mosca (SARH-DGSV, 1994).
Las pérdidas anuales por este concepto se calculan en
30,000 millones de nuevos pesos, lo que ha originado, desde hace
varios anos, la preocupación del gobierno mexicano y de los
propios productores, afectados en la comercialización de sus
productos, especialmente en el mercado internacional (Carreon,
1993) l
U n aspecto que hace difícil el manejo de esta plaga es que
en Mexico, aproximddamente 700 000 ha de frutales, constituyen los
hospederos mas importantes, para la mosca de la fruta, entre
ellos se hayan los citricos, mango, manzano, durazno, guayaba y
zapotes, mismos que estAn distribuidos en diferentes lugares del
psis (Carrebn, 1993).
Del mismo modo, en Mexico se encuentran más de 100 de estas
especies y destacan por su importancia económica y cuarentenaria
los generos Anastrepha, Rhagoletis, Bactrocera, Toxotrypana y
Ceratitis (Bustos et al., 1992).- - Es importante comprender que se
trata de un complejo y que generalmente son varias las especies
que afectan a los frutos (Aluja, 1993a).
En México, existen aproximadamente 30 especies de moscas de
la fruta del genero Anastrepha, cuatro de las cuales son de
importancia económica, debido a su amplia distribuci6n y arboles
mexicana de fruta), A. obliqua (mosca del mango) &.- serpentina
(mosca de los zapotes) y 5. striata (mosca de la guayaba)
(Gutierrez et al., 1992).-
-Los programas de monitoreo y control, utilizados hasta la
fecha, para moscas de la fruta, comprenden desde la aplicacibn de
insecticida en un cebo, por medio del uso de trampas o aspersiones
al árbol (Ehler y Endicott, 1984; Aluja, 1994); realizar ciertas
labores culturales, uso de feromonas, ( P r o k o p y , 1 9 7 2 , 1 9 8 1 ;
Roitberger y Prokopy, 1983; Battiste et al., 1983; Nation, 1983
Robacker, y Hart, 1984; Baker et al.,- 1985; Robaker, 1985;
Robaker y Wolfenbarger, 1988; Robaker, et al., 1990;- - Robaker y
Garcfa, 1990ayb; Aluja y Boller, 1992; Aluja, 1994).
Del mismo modo, efectuar liberaciones de insectos
estériles, mediante irradiaciones gamma (Co60) (Bustos et.- g. t
1993) y de parasitoides (Jirón y Mexzon, 1989; Aluja, 1990, 1994);
asi como someter la fruta a un tratamiento hidrotérmico (Couey y
Hayes, 1986; Sharp, 1986; Sharp et al., 1988; Sharp et al., 1989).-
-Los resultados que se han alcanzado hasta la fecha, son
alentadores; sin embargo, el manejo de esta plaga sigue siendo el
foco de atencibn en el mundo, por la amenaza que representan sobre
la posibilidad de exportar productos libres de moscas. También, se
ha considerado la posibilidad de utilizar agentes entornopatógenos,
para controlar a esta plaga (Poinar et al., 1977; Garcia et al.,-
-1980; Poinar y Hislop, 1981; Beavers y Calkins, 1984; Garcia et
-al. I 1984; Lindegren y Vail, 1986; Lindegren et -al., 1990; Georgis- -y Hom, 1992).
Dentro de ellos, se ha evaluado la patogenicidad de
cucurbitae (coquillet), (Poinar et al., 1977; Poinar y Hislop,
1981; Beavers y Calkins, 1984; Lindegren y Vail, 1986; Lindegren
et
- & I 1990; Georgis y Hom, 1992) y en hongo Metarhizium anisopliae (Metsch.) Sor. en C. capitata (Garcia et al., 1980,- -
-1984). Sin embargo, en &. ludens no se han evaluado hongos
entomopatbgenos, con el fin de contar con otra alternativa de
control biolbgico, no contaminante del medio ambiente, para el
control de moscas de la fruta.
El hongo M. anisopliae es considerado agente de control
biolbgico de plagas agricolas (Maniania, 1991; Zimmermann, 1993) ;
se le ha encontrado en casi todos los paises del mundo y se le
considera como parte de la flora normal del suelo; es capaz de
controlar un gran numero de insectos plaga de raices
(Zimmermann, 1993; Lacey et al., 1994; Villani et al., 1994; Lacey-
-et al.,
- 1994) y follaje (Maniania, 1991), asi como sobre mosca doméstica y mosquitos (Daoust y Roberts, 1983; Barson et al.,-
-1994), lo que demuestra su habilidad de actuar en diferentes
hábitats.
Se reportan más de 200 especies de insectos susceptibles a
M.
- anisopliae (Zimmermann, 1993; Lacey et al., 1994); en el- -mercado, de algunos paises ya se tienen disponibles formulaciones
en forma granulada (Anders 1992), polvos humectables (Zimmermann,
1986; Rodgers, 1993) y en trampas, para el control de plagas
(Roberts, 1991; Riba y Silvy, 1993).
N o obstante lo anterior, son varios los pasos que se deben
seguir, para desarrollar un hongo entornopatógeno como
micoinsecticida (Zimmermann, 1986; Maniania, 1991), uno de los má
importantes es la selección correcta de la cepa o aislado del
hongo entornopatógeno (Soper y Ward, 1981). Se ha demostrado que
existe una gran variabilidad en virulencia, entre especies de
hongos y entre cepas de un mismo hongo (Fargues y Remaudiere,
1977; McCoy, 1990; Maniania, 1991; Lezama, 1993).
L o anterior se debe a la variabilidad genetica entre
aislados de M.- anisopliae de las diferentes regiones geográficas,
de donde se aislan (Riba et al., 1986; Gillespie et al., 1989;
-Jimenez, 1989; Few Y Johnson, 1990; Ribeiro et al.,- - 1992;
Moorhouse et al.,- 1993); del mismo modo, se conoce que la
virulencia de los homgos entomopatõgenos varia entre especies de
hongos y entre aislados de una misma especie de hongo, ya que esta
caracteristica es gobernada por factores poligeneticos (Riba et
-al* I 1982), condiciones ambientales (Roberts y Campbell, 1977; Ferron, 1975, 1981, 1985; Fargues y Remaudiere, 1977).
Lo anterior, pone en manifiesto que se deben realizar
estudios profundos, que permitan evaluar y seleccionar un aislado
que sea capaz de matar a la plaga, con el fin de tener m¿Is probabilidad de exito en campo (Zimmermann, 1986, 1993; Maniania,
1991; McCoy, 1990).
Con base en lo anterior, se proponen una serie d e
actividades experimentales conducentes a tratar de determinar la
virulencia de diferentes aislados del hongo M. anisopliae, con
miras de seleccionar el que mayor potencialidad de uso presente,
como agente de control biolõgico en larvas de &. ludens, plaga de
importancia econbmica en Mexico y Sud America, como otra
alternativa de control biolõgico para esta plaga. Para alcanzar la
meta anterior se parte de la siguiente:
HIPOTESIS
L a virulencia de diferentes aislados del hongo
entornopatógeno M. anisopliae sobre larvas de tercer estadio de A
-ludens no es la misma.
Para demostrar la Hipõtesis anterior, se plantearon los
siguientes, Objetivos:
1) Evaluar la virulencia de 20 aislados del hongo M. anisopliae en,
larvas de tercer estadio de la mosca mexicana de la fruta &.
ludens.
2) Evaluar, en forma preliminar, la efectividad del aislado que
resulte más virulento, en dos localidades y con diferentes
textura de suelo, para el control de la emergencia de adultos
II ANTECEDENTES
2.1 Las moscas de la fruta
En el mundo existen aproximádamente 4,500 especies de moscas
de la fruta (White y Elson-Harris, 1992; Aluja, 1993a; Yang et
-al. t 1994). En Mexico se encuentran mas de 100 especies y destacan por su importancia económica y cuarentenaria, los
generos Anastrepha, Rhagoletis, Bactrocera, Toxotrypana y
Ceratitis (Bustos et al., 1992; Aluja, 1993b).
E s importante comprender que se trata de un complejo y que
generalmente son varias las especies, que afectan a los frutales
(Aluja, 1994).
Del género Anastrepha, en el pais existen aproximadamente 30
especies (Gutierrez et al., 1992; Aluja, 1994); cuatro de las
cuales son de importancia econbmica, debido a su amplia
distribución y Arboles frutales que infestan, Astas son:
Anastrepha ludens, conocida como mosca mexicana de la fruta (CV-=
ataca principalmente, citricos y mango); A. obliqua, que afecta al
-mango; &. serpentina, conocida tambikn como mosca de los zapotes y A.
- striata, que utiliza como hospedero principal, al cultivo de guayaba (Gutierrez et al., 1992; Aluja et al., 1993;- - - - Aluja,
1994).
Los estudios del género Anastrepha se iniciaron con los
trabajos de Herrera et al en 1900,- - quien realizó observaciones en
los gusanos de las naranjas y ante el creciente impacto económico
que ocasionan. En 1928 se estableciõ y di6 inicio un convenio
internacional, entre la Secretaria de Agricultura y Fomento, y el
Departamento de Agricutura de los Estados Unidos Americanos (USDA)
control y erradicacibn de las mocas, convenio que actualmente se
encuentra en funcibn.
2.2 Origen y zoogeografia
Más del 80% de la entómofauna neotropical tiene afinidades
filogenéticas, a nivel de tribu y subtribu, con grupos que
actualmente habitan los continentes del hemisferio sur
(distribucion gondwaniana), sur de Africa, la India, Australia y
Nueva Zelanda, lugares donde se encuentran sus posibles ancestros
(Hernandez-Ortiz, 1992); cuentan con una enorme capacidad de
adaptacibn ambiental; se multiplican en cualquier bioma: clima
frio y templado, semitropical, tropical y desertico.
Las especies del genero Anastrepha son endémicas y estan
restringidas a los climas tropicales y sub tropicales de América
(HernBndez-Ortiz, 1992). De este género se tienen descritas 184
especies, de las cuAles, el 43% se encuentran exclusivamente en
América del sur; el 15%, en Centro America y Panamá; el 49, en
MCxico y USA y el l%, en las pequenas y grandes Antillas (Calza et
-g. t 1988; Jirbn, & al., 1988; Aluja, 1994), constituyendo uno de los grupos de moscas mas importantes desde un punto de vista
agricola.
2.3 Taxonomfa
Las moscas de la fruta pertenecen al orden Diptera y a la
familia Tephritidae (Foote et al., 1993).- - El género Anastrepha es
uno de los grupos americanos más diversos de la familia
Tephritidae, recientemente ubicada en tribu la Taxotrypanini y en
la la subfamilia Trypetinae (Stone, 1942; Steyskal, 1977; Foote,
-L a mosca A. ludens presenta la- siguiente caracterizacibn
taxonomica, de acuerdo con Borror et al.,- (1981), Korykowski,
(1990) y Norrbom y Hernández-Ortiz (1993) (Cuadro 1).
Cuadro 1. Posición taxonbmica de A. ludens.
-Phyllum - - - Artropoda
Subphyllum --- Mandibulata
Clase --_--- Insecta
Subclase --- Pterigota
Orden - - -
Dipter-Suborden --_--- Cyclorrapha
Divisiõn - - -
Schizophor-Seccibn - - - Acalyptrata
Superfamilia --- Tephritoidea
Familia - - - Tephritidae
Subfamilia - - - Trypetinae
Genero --- AnastreDha
Especie --- ludens
2.4 Descripción del A. ludens.
Los primeros estudios morfolbgicos y descriptivos de la
especie A.- ludens se iniciaron en 1933 por Dampf; &. ludens
presenta tamano medio y de color cafe amarillento, en el tórax;
tiene una franja delgada y clara, que se ensancha hacia la parte
posterior y dos franjas a los lados, que llegan hasta la sutura
transversal; frecuentemente con una mancha difusa en la parte
media de la sutura escuto-escutelar, pleura y metano café
amarillento y los dos, con una franja cafe obscuro o negra (Aluja,
1993a).
[image:21.570.33.518.49.687.2]Las alas membranosas presentan bandas pBii.das amarillentas;
las de la región costal en en forma de 'IS" se tocan en la vena
R4+5 o poco más separadas; una banda en forma de W*' es separada
de la banda en aS'w o pueden estar conectadas ligeramente (Aluja,
1993a) (Figura 1).
2.5 Cultivos hospederos
A. ludens e s considerada
- frugivora (Aluja, 1994); es
reportada afectando al menos 23 especies de frutales, pero por el
dano y frecuencia con que se presentan, los cftricos (Citrus spp.)
Y el mango (Mangifera indica L.) son los hospederos m&s importantes (Jirón, 1988; 1991; Hernbndez-Ortiz, 1992; Aluja,
1994). Sin embargo, en el cuadro No. 2 se presentan algunas
especies de frutales que tambien son considerados como plantas
hospederas (Aluja, 1987; Aluja et al., 1987, 1990, 1993; Jirbn y
Norrbom, 1988; Robacker et al., 1990).
Cuadro No. 2 Plantas hopederas de A.ludens seglin varios autores. -
--_---Nombre Cientifico Nombre Coman Familia
-__---Annona . Annona Annona Annona Casmlro Lex. Cltrus Cltrus Citrus cherimola Mill muricata L.
ret iculata L. scuamosa L. ' c aurantium L gra sine
?dulls Llave y
ndis Osbeck Isis Osbeck
Chirimoya Guanabana Annona roja Annona Zapote blanco Naranja agria Toronja Naranja dulce Naranja injerto Tangerina Cidra Pomelo Mandarina criolla Membrillo Pomarosa Jinicuil Mango Durazno Guayaba Granada Pera Manzana
Chapote amarillo
Annonaceae Annonaceae Annonaceae Annonaceae Rutaceae Rutaceae Rutaceae Rutaceae Rutaceae Rutaceae Rutaceae Rutaceae Rutaceae Rosaceae Myrtaceae Leguminosae Anacardiaceae Rosaceae Myrtaceae Punicaceae Rosaceae Rosaceae Rutaceae Citrus S D
Citrus &liciosa Tenore Citrus Medica L.
Citrus maxima(Burm) Mer slata Blco. Citrus ret
Cydonla oblicua Mill. Eugen+a lambos L. Inga -Jlnicuil Schl. Mangifera indica L. Prunus
Psidium-uajava L. Punica granatum L. Pvrus communis L.
sica Batsch.
Pyrus malus L.
Sargentjqreggii Wats. -ril
[image:22.557.30.512.46.718.2]2.6 Biologia y hábitos
A.
- ludens ha sido estudiada en su biologia b&sica desde 1900 (Herrera et al., 1900; McPhail et al., 1933;- - Darby, 1934; Stone,
1942; Baker, 1944; Aluja, 1994). Su ciclo de vida depende de las
condiciones ecológicas (Leyva, 1988); tienen una gran influencia
la disponibilidad de alimento, la temperatura, la humedad, la
vegetaciõn, e l sustrato de pupacion y oviposicibn
(Celedonio-Hurtado et al.,- - 1988; Leyva et al., 1991; Aluja, 199313).
Todas las moscas de la fruta pasan por los estados
biológicos de huevo, larva, pupa y adulto. La hembra fecundada
inserta su ovipositor por debajo de la cascara de los frutos
prõximos a madurar y despues de 2 o 4 dias. La oviposición la
realizan de 3 a 6 dfas despues del apareo y pueden ovipositar
hasta 400 huevecillos, a lo largo de toda su vida
(Celedonio-Hurtado et al., 1988; Aluja, 1994).
-Las larvas recién eclosionadas empiezan a alimentarse de la
pulpa del fruto, de manera que van creciendo y formando una serie
de taneles, que a su vez, contribuyen al desarrollo de
microorganismos que descomponen la fruta, creando zonas
necróticas, fibrosas y endurecidas, de color cafe obscuro (Aluja,
1992; 1993a).
La duración del período larval es de 8 a 13 dias; atraviesan
por tres estadios y presentan dimorfismo sexual; cuando las larvas alcanzan el tercer estadio salen del fruto y se introducen
en el suelo, para pupar. El estado pupa1 tiene una duracibn que va
de 13 a 17 dias; normalmente, este periodo que coincide con la
caida del fruto atacado (Leyva, 1988; Celedonio-Hurtado et al.,-
Cuando el adulto est8 prõximo a emerger de la pupa r este
tiene que romper el pupario y lo hace con el ptilinum, que se
localiza en la parte frontal de la cabeza (Leyva, 1988;
Celedonio-Hurtado et al.,- - 1988; Leyva, et al., 1991; Silvinsky, 1990;
Aluja, 1994) y cuando el adulto logra emerger, no puede volar
inmediatamente, pues sus alas están hñmedas y descoloridas; ellos
buscan lugares poco visibles y cuando se le han secado las alas,
se activan y vuelan hacia el follaje de árboles, para localizar su
alimento, formado principalmente en frutos maduros, que presentan
alguna herida o de secreciones azucaradas de troncos y hojas
(Aluja, 1994).
Los machos vuelan a las ramas sombreadas; prefieren el
enves de las hojas y es su sitio caracteristico de galanteo o en
los pedazos pequenos de corteza u otros sustratos cercanos,
donde inmediatamente asumen una postura de exhibiciãn
caracteristica, resoplan las bolsas en el abdomen, abanican las
alas, en estallidos breves y liberan una feromona sexual, para
atraer a las hembras (Robacker y Hart, 1985).
El apareo ocurre entre los 6 0 12 dias, despues de la
emergencia y generalmente, se lleva a cabo por las tardes (17:0
horas en adelante) (Nation, 1983; Robacker, 1988). El adulto vive
desde 15 dfas a 8 meses, dependiendo de la ecología del lugar
(Celedonio-Hurtado, et al., 1988; Leyva, et al, 1991,- - Aluja,
1993a). Los adultos hembras de A. ludens viven en condiciones de
-laboratorio de 11 a 16 meses y de campo, hasta 12 meses (Leva,
1991; Aluja, 1993a) (Figura 2).
2.7 Mecanismos de detecciõn.
2 5 dias
Pupa
de 20 a 25 dias
Larva
Fi u r a
ubicaciõn de la plaga; proporciona una idea del tamano de l a s
poblaciones, su distribucibn y la fluctuación estacional (Jirbn y
Hedstrom, 1991). Sin embargo, se tiene conocimiento de que este
sistema por si solo no es eficiente, ya que cuando se tienen altas
poblaciones, la trampa Mcphail es capaz de detectar apenas el
31.3% de la poblaciõn original (Aluja y Cabrera, 1989; Aluja,
1994).
Por lo que se recomienda mejorar la efectividad del trampeo,
mediante la estandarizacibn del atrayente alimenticio (Protefna
hidrolizada) (Epsky et al., 1993; Heath et al.,- - 1994), disenar
colores básicos para las trampas (Montero et al., 1990; Duarte et- -
-al. I 1991) e identificar las feromonas (Roitberg y Prokopy, 1983; Robaker y Hart, 1985b; Robaker, et al., 1985; Robaker, 1988;
Robaker y Wolfenbarger, 1988).
2.8 Control
Para el control de las moscas de la fruta se realizan
actividades variadas para disminuir las poblaciones de la plaga,
dentro de ellas se tienen implementadas labores culturales, de
caracter físico como, el uso de plaguicidas aplicados en trampas
junto con un atrayente alimenticio 0 foliar, la liberaci6n de
insectos esteriles, insectos parásitos y depredadores, entre otros
(Cunningham, 1989; Howarth, 1990; Messing y Seiler, 1993; Sales y
Kovaleski, 1990; McDonald et al., 1993; Greany, et al.,- - - - 1994;
Aluja, 1994).
Los modificadores de comportamiento del insecto aplicación
de feromonas disuasivas de la oviposiciõn; el uso de la ciromazina
como reductor de la fecundidad y fertilidad (Moreno et al.,- - 1994)
los frutos, son otras alternativas que están en estudio (Greany et
-a&, 1994).
2. 8.1 Combate quimico
Basado en su comportamiento alimenticio de las moscas, el
uso de productos quimicos ha sido utilizado para el control de
adultos (Diaz et al., 1993), mezclados con un- atrayente
alimenticio, comdnmente llamados insecticida-cebo; aplicados ya
sea en forma de aspersiõn o en trampas. Una gran variedad de
formulaciones y dosis de plaguicidas se han utilizado de manera
extensiva en el mundo. En Israel, la zona mediterranea de
Europa, Estados Unidos de Norte América y MRxico (Cunningham,
1989; Aluja, 1994)
El malathion es uno de los insecticidas más utilizados. Su
modo de acción es por contacto y estomacal; su fórmula quimica es
oxi, oxi-dimetil S (1, 2-dicarbetoxietil) fosforoditioato y
tambien, oxi, oxi-dimetil fosforo ditioato de dietilmercapto
succinato (D.G.S.V. SARH, 1993).
Por su toxicidad el malathion pertenece al grupo III y su
DL50 via oral aguda, en rata macho, es de 2800 mg/kg y para rata
hembra, de 1000 mg/kg. La DL50, via dermal en conejos es de 4100
Wkg; por ingestión, en ratas con 5000 ppm durante 104 semanas, causa depresión de la actividad de colinesterasa. Se reporta que
los residuos de malati6n no se acumulan en los tejidos grasa y
huevo, se degradan en un periodo no mayor de 3 a 7 dias (McEwen,
1979; D.G.S.V. SARH, 1993).
La Organizaciõn Mundial de la Salud (OMS) recomienda el uso
ambiente. Sin embargo, algunos estudios han demostrado que el
malathion tiene efectos detrimentales en el ambiente, suelo y
fauna (artrOpodos), que se encuentran en el suelo, debajo de donde
se colocan las trampas; ya que por efectos de la lluvia u otros
factores, el producto cae y se acumula en el suelo, alcanzando
niveles de hasta 11,700 ppm (Miller et al., 1983; Miles et al.,- -
-1990; Howarth, -1990; Messing y Seiler, 1993).
Actualmente, la Secretaria de Recursos Hidráulicos (Sm) ?
a traves de la Direccibn General de Sanidad Vegetal (DGSV) y los
Tbcnicos del Programa Mosca del Mediterrdneo (MOSCAMED)
recomiendan las siguientes combinaciones del insecticida malathion
y atrayente alimenticio (Gutiérrez et al., 1992) (cuadro' No. 3).
Aluja (1993a) recomienda la adición de un emulsificante a la
[image:29.557.25.519.587.726.2]mezcla.
Cuadro 3. Mezcla de proteína hidrolizada mas
utilizada en el control de moscas de lainsecticida,fruta en MCxico.
---Producto Partes Dosis Aplicación
---Malatibn 57% C. 1 150-300 cc/drbol Terrestre
Proteina hidrolizada 4
Agua 95
Malatión UBV 1 1 Aerea
Proteina hidrolizada 9 lt/ha
---S e recomienda que las aplicaciones se inicien, durante el
periodo de floracibn y fructificación de los arboles, a l
detectarse adultos en las trampas en una densidad promedio de
0.080 MTD (moscas/trampa/dia); en aplicaciones dirigidas a los
Arboles, estas se deben realizar en banda o manchas circulares
las aplicaciones, cuantas veces sea necesario, con intervalos de 7
a 10 dias una de otra (Gutierre2 et al., 1992).
N o obstante lo anterior, mucho se ha documentado sobre los
problemas ecológicos que ocasiona el uso de plaguicidas; en el
mundo se aplican aproximádamente 2.5 millones de toneladas de
insecticidas (Pestic. News, 1990); estos tienen una contribucibn
importante en el mantenimiento de la produccion. En general, por
cada dolar invertido en el control de plagas, genera 4 dolares en
cosechas protegida (Pimentel et al., 1992). Lo anterior, permite
hacer un analisis riguroso, sobre los beneficios de su uso y la
necesidad de utilizarlos de una manera racional, para evitar
efectos mayores sobre la ecología de un lugar.
Estos beneficios no incluyen los costos económicos
ambientales indirectos, ni los costos en la salud humana, ni de la
destrucci6n de enemigos naturales, problemas de polinización,
perdidas de poblaciones de abejas, contaminación de los mantos
freaticos, muerte de peces, de la vida silvestre y de
microorganismos responsables de la fertilidad biológica de los
suelos, la destrucci6n de depredadores naturales y de los
parasitoides (Pimentel et al., 1992).-
-Del mismo modo, se conoce que existe un creciente desarrollo
de resistencia a insecticidas, por parte de las plagas; por
ejemplo, en 1938 siete especies de insectos ya presentaban
resistencia y en 1989, ya se tenian más de 500 especies, con
niveles de resistencia simple, doble y hasta mtiltiple (Brattsten,
1989).
Además, se ha encontrado que tanto las frutas como los
insecticidas, se reporta que el 3% en los alimentos rebasan el
nivel de tolerancia legal (F.D.A., 1990; Hudley et aIJ., 1988).
Los danos causados a la salud son los mas caros; anualmente
se reporta un millón de casos de envenenamientos en el mundo, de
los cuales, 20 000 son casos de muertes y 100 000 son casos de
cáncer, y por si fuera poco, las secuelas de aquellos que han sido
victimas de envenenamiento tienen efectos neurológicos (~O/~,
1989., Escobichon et aJ., 1990; Rosenstock et al., 1991).
Todo lo anterior, hace que actualmente, la sociedad demande
la prohibición del uso de sustancias peligrosas, para la salud y
el medio ambiente, por lo que se ha dado un impulso importante a
otras alternativas de control, dentro de ellas, el biolõgico.
2.8.2 Cutural y mecanice
Dentro de este m6todo se recomienda colectar y destruir,
tanto los frutos que quedaron en el Wbol después de la cosecha,
como los caidos; tambien, se recomienda que se realicen barbechos,
rastreos y que se poden los arboles (Gutiérrez et al., 1992).-
-2.8.3 Legal
Para la regulacibn del movimiento de los frutos que
potencialmenre pueden estar atacados por moscas, está posibilidad
se tiene controlada en Mexico y otros paises, mediante el
establecimiento de medidas cuarentenarias, en las cuales se
requiere la expediciõn de guias fitosanitarias, certificados
internacionales Y d e origen, certificacibn de huertos y
constancias tecnicas, de las medidas de control (Aluja, 1993a).
Ademas, de un tratamiento de postcosecha, hidrotermico
(Couey y Hayes, 1986; Sharp, 1986; Sharp et aJ., 1989) o por
irradiaciones gamma de los frutos con Co60 (Bustos, et. al.,
-1993).
2.8.4 Liberación de insectos estériles
Al Dr. Knipling se le considera el padre de la tecnica del
insecto estéril (Enkerlin, et al., 1993); esta aportacibn a la
ciencia permitiõ obtener, bajo condiciones de laboratorio, machos
y hembras esteriles, al exponerlos a rayos X o bien, a radiaciones
gamma I sin danos a los insectos 0 en su habilidad de apareamiento.
Como resultado del uso de esta tecnica, varias especies de
mosca de la fruta han sido eliminadas de las islas del Pacifico.
Ademds, el gusano barrenador del ganado se logro erradicar con
esta técnica (Weidhaas, 1993).
En moscas de la fruta ha permitido disminuir sustancialmente
las poblaciones de moscas en USA, Mexico y Pera (McDonald et al.,
-1993 ; Aluja, 1994); se ha demostrado que las liberaciones de
moscas estériles son mas efectivas, cuando se tienen bajas
poblaciones de la plaga (Barclay, 1987; Knipling, 1992).
2.8.5 Control biológico.
El control biolõgico es definido como "la utilizacibn de
organismos vivos para el control de plagas" (Rhodes, 1993); ello
contempla la utilizaciõn de insectos depredadores, parasitos y
patbgenos (Ehler, 1991).
Si se pretende
dentro de programas
utilizar insectos par&itos 0 depredadores,
de control biolbgico, se debe conocer el
comportamiento y la ecologia de ellos (Aluja, 1994), como es
contar con alta capacidad de btisqueda y especificidad, en cuanto a
la especie que ataca; tambien, deben poseer un potencial biótico
de reproducción mayor al del hospedero, habilidad de ocupar todos
los nichos habitados y ser facil de reproducir, en condiciones de
laboratorio (Aluja, 1993a).
Aluja (1990, 1994) menciona que los parasitóides, que
atacan a las moscas de la fruta, no son especificos, en cuanto a
la especie que parasitan. Los parasitoides silvestres de
Hymenoptera, que comunmente atacan a Anastrepha SPP* son
Bracanastrepha anastrephae, Doryctobracon aerolatus, -D.
longicaudata 0. brasilensis, D.- crawfodi, D.- zeteki, Opius
hirtus, 0. virecki, 0. tucumanus, 0. arqentinus, Aganaspis
odcarvalhoi, Eucoila pelleranoi (todos los Cynipidae); Odontosema
anastrephae y Cothonaspis sp. (Aluja et al., 1989, 1990; Eskafi,
1990; Jirbn y Mexzon, 1989; Wharton et al-., 1981; Piedra et al.,-
-1993 ; Baranowski, et al., -1993).
Una caracteristica, que muestra la importancia del control
biolõgico de moscas de la fruta con insectos parásitos, es su
respuesta efectiva en regiones donde la poblaciõn de la plaga es
alta y se puede combinar, con la liberaci6n de moscas estériles,
cuando las poblaciones son bajas (Aluja, 1994).
E n México, durante 1954-1955 se introdujeron varios
parAsitos de Hawaii, para control de &. ludens; tambien, se inició
con la producciõn a gran escala y 5 anos mas tarde, ya se habían
liberado mas de 7 millones del himenbptero Aceratoneuromyia indica
(Silvestre) (Eulopihdae). Este parásito se estableci6 rápidamente,
alcanzando niveles de parasitismo de hasta un 80% y reduciendo los
damos a menos del 30% en los estados de Morelos, Veracruz,
Michoacan (Altieri et al., 1993).-
-Actualmente, dnicamente de 0. longicaudata, en el ano de
1993, se liberaron 7.2 millones en el estado de Baja California,
Mexico (SARH-DGSV, 1994).
E n lo que corresponde a los patogenos de moscas de la
fruta, estas pueden ser atacadas por bacterias, nematodos y
hongos, que pueden causarles la muerte, como por ejemplo la
bacteria Serratia marcecens (Aluja, 1993a).
Por otro lado, se han hecho investigaciones c o n Bacillus
thuringensis L. en adultos de la mosca del mediterraneo Ceratitis
capitata, para determinar la efectividad de sus toxinas
(delta-endotoxina y exotoxina), asi como de su espora. La bacteria
mostró patogenicidad hacia las moscas; de 94 aislados probados, 15
causaron una mortalidad de 80%, 9 dlas después de exposiciõn
continua (Gingrich, 1987).
Del mismo modo, se ha encontrado que los nematodos tienen
potencialidad de ser utilizados, como agentes de control biolõgico
para moscas Tephritidae. En larvas de tercer estadio de 5.
capitata, la especie Steinernema feltiae, tiene una CL50 de 38 2
nematodos/cm (Lindegren y McInnis, 1990).
Por su parte, Beavers y Calkins (1984) encontraron que las
especies de nematodos 2. feltiae, Heterorhabditis bacteriophora
Poinar, H.- heliothidis y S. glaseri, son capaces de parasitar
[image:34.563.34.521.62.716.2]larvas y adultos de A. suspensa,- como se puede observar en el
Cuadro No. 4, pero parasitan muy poco el estado biolbgico de
pupa.
Cuadro No. 4. Susceptibilidad de A. Steinernema
Calklns, 1984SPP* Y-g.
suspensa a los nemátodos bacterlophora. Beavers y
---Especies de nematodos
Nematodos (cepas) LarvaPorcentaje de infecci6npupa adulto
---2. feltiae (Mex.) 90.7a 0.4a 91.7a
2. feltiae (all) 88.la l.Oa 93.4a
H. heliothidis. 86.6a l.la 86.7a
2. feltiae (Breton) 83.0a 0.0 70.3ab
H. bacteriphora 78.7a 0.0 75.6ab
S. glaseri 15.7b 0.4a 58.lb
---E n lo que respecta a la suceptibilidad de las moscas del
mediterráneo, del melbn y la mosca oriental de la fruta, al
nematodo entornopatógeno S. feltiae, Lindegren y Vail, (1986)
reportan que las tres especies son sensibles al nematodo (Cuadro
[image:35.567.35.520.133.616.2]No. 5).
Cuadro 5. Susceptibilidad de moscas de la fruta al nematodo 2. feltiae. Lindengrin y Vail, 1986
--_---Mosca del Mosca Mosca del
MediterrzIneo Oriental Melbn
Concentracibn % Mortalidad % Mortalidad % Mortalidad
--_---_---500,000 92.0 85.0 86.0
150,000 70.0 78.0 54.0
50,000 52.0 37.0 28.0
15,000 18.0 9.0 6.0
5,000 9.0 9.0 0.0
___---En cuanto a hongos entornopatógenos, el hongo M. anisopliae
ha sido evaluado en C. capitata, en donde se ha determinado una 6.56
-DL50 de 8 x 10 y un TL50 de ll.4 dias (Garcia et al.,- - 1980;
1984).
2.9 Los hongos entomopatágenos
El uso de hongos entomopatbgenos en el control de plagas
agricolas, se practica en los paises como Brasil, Inglaterra,
Francia, China y USA (McCoy, 1990; Maniania 1991; Zimmermann,
1993).
Las ventajas que los hongos entornopatógenos ofrecen para su
uso son entre otras, su especificidad, su inocuidad, su alta
virulencia, la facilidad relativa de multiplicación masiva, su
rentabilidad (McCoy, 1990).
Actualmente ya se tienen formulaciones comerciales a base de
hongos en varios paises (Reinecke et al., 1990; McCoy, 1990;
Goettel et al., 1990; Rhodes, 1993; Riba y Silvy, 1993). Dentro de
ellos, cinco formulaciones a base del hongo M. anisopllae, tales
como Biomax, Biocontrol, Combio, Metabiol, Metapol y Metaquino,
en Brasil (McCoy, 1990; Goettel et al., 1990; Riba y Silvy, 1990);-
-Biotrol, en USA (McCoy, 1990 Riba y Silvy, 1990); BI0 1020, en
Alemania (Reinecke et al., 1990). Lo anterior, permite- - considerar
la potencialidad de utilizar M.- anisopliae dentro de programas de
control biol6gico de moscas de la fruta.
2.9.1 El hongo Metarhizium
El hongo Metarhizium es un Deuteromycete, que produce
conidios en masa, en conidibforos libres; los conidios son
cilindricos y miden de 5 a 8 micras de ancho y lo-14 de longitud.
Hasta la fecha se tienen 6 especies bien definidas que son:
Metarhizium, que son M. anisopliae, M. flavoviride y M. album, M.
cylindrosporae, M. guizhouense y M. pingshaense (Rombach et al.,
-1987; Zimmermann, 1993). Una descripciõn del mismo se presenta
la Figura No. 3.
2. 9.2 Insectos hospederos de M. anisopliae.
Este hongo parasita a 204 especies de insectos, dentro e n
d e
los ordenes Orthoptera (11 sp.), Dermaptera (1 sp.), Hemiptera
(21 spo), Lepidoptera (27 sp.), Diptera (4 sp.), Hymenoptera (6
spo), Coleoptera (134 sp.) (Zimmermann, 1992; Zimmermann, 1993).
2.9.3 Mecanismo de infeccibn
L a infección, del hongo sobre el insecto, se inicia al
adherirse el conidio, germinar y penetrar el tubo germinativo en
la cutfcula. La penetracion de la hifa, a traves de la
epicuticula, se realiza por medio de un doble proceso, uno
enzimático y otro mecWic0, actuando en forma simult&nea (Fargues,
1983; El-Sayed et al., 1989;- - Fachino y Montero de Barros, 1991).
La epicuticula, que esta constituida por muchas capas, cada
una de ellas, tiene propias caracteristicas; la exterior es muY
fragil, pero presenta resistencia a la degradacion enzimatica y
evita el paso de enzimas degradadoras de la cuticula; esta formada
por lipoproteinas polimerizadas, estabilizadas mediante quinonas.
Esta composicibn la hace dura, pero los hongos poseen
enzimas degradadoras, que les permitem modificar la unidad
estructural del hospedero; ademas, inhiben el proceso selectivo o
enzimatico del hospedero y permiten degradar y asimilar los
materiales del hospedero, utilizando su complejo enzimatico
(quimoelastasa, quitinasas y lipasas (Roberts, 1981; Locke, 1984 ;
Hajek y Leger, 1994).
. .-.:
. ;<+
IIr
,: ‘.I.
a [image:38.566.53.436.217.554.2]00000
c 00000
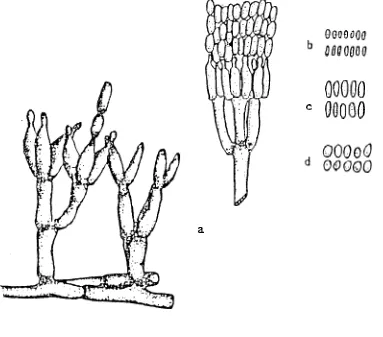
Figura No. 3. Estructuras morfolbgicas del hongo Metarhizium sp. a) ,Conidibforos
Conidias. de g. ani;;y;;aTi,, b;
minor, de M. anisopllae var.
Cuando el hongo logra romper la epicuticula, las estructuras
penetrantes del hongo pueden extenderse y facilitar aun más, la
acción de las enzimas degradantes (Chamley et al, 1991; Goettel et- -
-al., 1989; Locke, 1984).
Tambien, la procutícula acttia como una barrera fisica, que
impide el desarrollo de una infecciõn ftingica, por su
impermeabilidad a secreciones de los patogénos y su resistencia
mecanica a la penetracibn; su grado de resistencia, depende de
efectos combinados del espesor (Lock, 1984; Hassan y Charnley
1989) y el grado de endurecimiento (queratinizaciõn). Los
insectos con segmentos del cuerpo altamente queratinizados son
invadidos via membrana intersegmentales (Hassan y Charnley, 1989;
Magalhaes et aJ., 1990, 1991; Leucona et al., 1991).-
-2.9.4 Melanización cuticular
Este fenómeno es inducido por el dano fisico o por glucanos
B-1,3, en la pared celular ffingica (SoderhAll, 1982; Murrin y
Nolan, 1987; Butt et al., 1988).- - La melanizacion ocurre con
frecuencia demasiado tarde, como para detener el crecimiento
rápido del patógeno (St. Leger, 1991; 1994).
2.9.5 Producciõn de metabolitos
Los hongos patogenos poseen enzimas que permiten degradar y
asimilar los materiales del hospedero, mientras superan los
mecanismos d e resistencia del hospedero (Bidochka y )
Khachatourians, 1992); los metabolitos fñngicos ayudan al patbgeno
a modificar la integridad estructural del hospedero, a inhibir el
proceso selectivo o enzimas del hospedero y a interferir con el
sistema regulador del hospedero.
El dano asociado con los sintomas de la enfermedad, pueden ser
producidos por las enzimas y por sus metabolitos de bajo peso
molecular (toxinas). Las enzimas son las que determinan la
virulencia, porque permiten al patógeno coexistir con los
procesos metabolicos cambiantes, asociados con los estados de
enfermedad del hospedero (Roberts et al., 1992; Hajek y St. Lager,
1994).
2.9.6 Toxinas entomopatbgenas
Una vez que el hongo alcanza el homocele del insecto, este
puede morir por la combinacibn de danos mec&nicos, causados por
crecimiento fangico o por el agotamiento de nutrientes y toxicosis
(Guillespie y Claydon, 1989). Pero tambien, puede morir mediante
la sintesis y accion de sus toxinas; en M.- anisopliae se han
reportado dos familias de toxinas que reciben el nombre de
destruxinas y citocalacinas (Roberts, 1981ab; Samuels et al.,-
-1988).
De las destruxinas se conocen 18 diferentes hasta la fecha
Y son decipeptidos ciclicos, que afectan la estructura y
funcionamiento normal de varios organelos, tales como:
mitocondrias, reticulo endopldsmico y membranas nucleares; de las
citocalacinas se reportan tres diferentes, pero todas paralizan
las céluas y causan una disfunciõn del nervio optico central,
tubos de Malpighio, hemocitos y tejido muscular (Roberts, 1981;
Vey et al., 1985; Samuels et al., 1988ab; Vey y- - - - Quiot, 1989;
Cerenius et al., 1990).-
-2.9.7. Condiciones de temperatura, luz y humedad para la
reproduccion.
esporulacibn y la virulencia son características de los hongos,
que pueden ser afectadas por la temperatura, luz ultravioleta y la
humedad (Zimmermann, 1982; Ferron, 1985; Guillespie y Grawford,
1986; Carruthers, et al- - 1988; Farguez, et al.- - 1988). La
temperatura media bptima de M. anisopliae es de 25gC, para que se
desarrolle; pero pierde su capacidad de matar a los 37gC (Daoust y
Roberts, 1983 ; Garcia, 1984 ; Majchrowiez y Poprawski, 1993 ;
Reinecke, et al 1990,- - Moorhouse et al., 1994).-
-2.9.8 Patogenicidad, virulencia y agresividad
Patogenicidad, virulencia y agresividad son conceptos muY
comunes dentro del lenguaje de hongos entomopatogenos; la
virulencia de hongos entornopatógenos es definida como *'el grado de
patogenicidad con que un organismo mata o causa dano a un insecto
hospedero especifico en condiciones controladasfi' (Aizawa, 1971;
Bigler, 1989 ; Alves, 1986). La patogenicidad es definida como la
capacidad de un microorganismo para causar enfermedad (Shaner, et
-g. I 1992)
A menudo los conceptos de agresividad, patogenicidad y
virulencia son empleados como sinónimos, en patologia de insectos
y se utilizan, para indicar el nivel de enfermedad provocados por
microorganismos. A la agresividad se le define como la habilidad
de un patbgeno para invadir a su hospedero (Shaner et al., 1992)-
-2.9.9 Virulencia de M. anisopliae
-Se ha demostrado que existe una gran variabilidad en
virulencia, entre especies de hongos y entre cepas de un mismo
hongo (Fargues y Remaudiere, 1977; McCoy, 1990; Maniania, 1991;
Lezama, 1993ayb). Lo anterior se debe a la variabilidad genetica
entre aislados de M. anisopliae de las diferentes regiones
geográficas, de donde se aislan (Riba et al., 1986; Gillespie et
-al.,
- 1989; Jiménez, 1989; Feng y Johnson, 1990; Ribeiro et al.,-
-1992; Moorhouse et al., 1993a).
Del mismo modo, se conoce que la virulencia de los hongos
entomopat6genos varia entre especies de hongos y entre aislados,
de una misma especie de hongo, ya que esta caracteristica es
gobernada por factores poligeneticos (Riba et &.,- 1982;
condiciones ambientales (Roberts y Campbell, 1977; Ferron, 1975,
1981, 1985; Fargues y Remaudiere, 1977).
L o anterior, obliga a que se deben realizar estudios
profundos, que permitan evaluar y seleccionar un aislado, que sea
capaz de matar a un insecto plaga determinado, con el fin de tener
mds probabilidad de éxito en campo (Zinunermann, 1986, 1993;
Maniania, 1991; McCoy, 1990).
E n lo que se refiere a dipteros, muchos aislados de M.
-anisopliae, de diferentes regiones geograficas y una gran variedad
de especies de insectos, han mostrado ser virulentas hacia larvas
de mosquitos de los géneros Aedes, Anopheles y Culex (Roberts,
1977; Daoust y Roberts, 1983; Riba y Vey, 1989).
Tambien, e n adultos de la mosca del mediterraneo C.
-Capitata, este mismo hongo presenta potencialidad de uso, con una 6.56
dosis letal 50% estimada en 8 x 10 conidios por ml y un TL50
de ll.4 dias (Garcia et al., 1984).-
-E n lo que respecta, a la virulencia del hongo en moscas de
la fruta del genero Anastrepha, hasta el momento no se han
encontrado publicaciones en revistas internacionales. En el Estado
de Colima, recientemente, se evaluaron 3 aislados de M. anisopliae
-y en larvas de &. striata -y se reporta una mortalidad del 42.5%,
69% y a a .75%, para cada uno, respectivamente (Romero, 1993).
L o anterior muestra, que es posible que las larvas de A.
-ludens sean también sensibles a infecciones de M. anisopliae.
III MATERIALES Y METODOS
3.1 Lugar de la experimentacibn
La presente investigaci6n se desarrolló en dos etapas, una
en el Laboratorio de Control Biolbgico, localizado en el drea de
Posgrado, de la Facultad de Ciencias Biológicas y Agropecuarias
(FCBA) de la Universidad de Colima y otra, en condiciones de
campo, en dos huerto establecidos, con mango, durante el período
comprendido entre los meses de septiembre a diciembre de 1994.
3.1.1 Etapa experimental en laboratorio
A continuación se detalla la metodología de trabajo que se
llev6 a cabo, en el laboratorio.
3.1.2 Hongos entomopatbgenos
Los hongos que se utilizaron en esta investigacibn fueron
aislados en diferentes estados del pafs; uno de Brasil y otro, de
Estados Unidos de Norte Amererica; la mayoria aislados de insectos
y otros, a partir de suelo. Mismos que, actualmente forman parte
de la Colecciõn de Hongos Entornopatógenos, de la Facultad de
Ciencias Biolõgicas y Agropecuarias (FCBA), de la Universidad de
Colima (Cuadro 6).
El aislado originario de Brasil fue proporcionado por
cortesia del Dr. Arthur MendoCa, del IAA/PLANALSUCAR, Alagoas,
Brasil; el de EUA fue obtenido por conducto de la Dra. Raquel
Alatorre Rosas, del Colegio de Postgraduados, Centro de Ciencias
Agricolas, Montecillos, Estado de Mexico y los aislados Ma9, Malo,
Ma18, Mal9 y Ma20, fueron proporcionadas por el Centro Nacional de
Referencia de Control Biológico, de la SARH-DGSV, Mexico; los
FCBA, de la Universidad de Colima, principalmente dentro del
estado de Colima.
Algunos de ellos estAn depositados en la Colección de Hongos
entornopatógenos del USDA y se identifican con el namero de la
colección ARSEF. Las características del origen de las cepas se
muestran en el Cuadro No. 6.
3.1.3 Multiplicacibn de los hongos
Todos los hongos fueron cultivados en medio de agar
dextrosa sabouraud, con 1% de extracto de levadura (Latch, 1976;
Rombach et al., 1987; Samuels et al., 1989ayb; Pereira y- - - - Roberts,
1991; Moorhouse et aJ., 1993ayb), con- 0.005% del antibi6tico
cloramfenicol (Prior y Arura, 1985; Sneh, 1991); mismos que se
incubaron por tres semanas (Latch, 1976; Latch y Fallon, 1976),
bajo condiciones de laboratorio (25+loC) (Riba et al.,- - - - 1986;
Rombach et al., 1987; Lacey et al., 1988; Ravallec et &.,- - - - 1989.,
Reinecke et al., 1990)-
-E n la etapa final y previo a los experimentos en campo, se
multiplicb el aislado del hongo, para obtener inóculo suficiente,
siguiendo la tecnica de arroz como sustrato de multiplicación en
bolsas de polietileno (Barragan, 1994).
3.1. 4 Cuantificacibn de los conidios
Después del período de incubación, los conidios de cada cepa
se recuperaron en agua destilada esteril, con Tween 80 al 0.05%,
para romper la tensiõn superficial de los conidios (Rombach et
-al.,
- 1987; Lacey -et al., 1988; Samuels et al.,- - - 1989ayb); la suspensiõn se agit6 y con el apoyo de una cAmara hematimétrica de
[image:45.555.29.514.93.700.2]Cuadro 6. Aislados del hongo M. anisopliae utilizados en la investigación.
l
---CEPA No. No. ARSEF INSECTO HOSPEDERO LUGAR FECHA
---M. anisopliae:
Mal 3312 Mosca Pinta Brasil 1990
Ma2 Ma3 Ma4 Ma5 Ma6 Ma7 Ma8 Ma9 Mal0 Mal1 Mal2 Mal3 Mal4 Mal5 Mal6 Mal7 Mal8 Mal9 Ma20 (Cercopidae)
3290 D. saccharalis
pyralidae)
FORMULACION COMERCIAL
3291 D2
3292 -D.
3293 S .
saccharalis
fruqiperda (Noctuidae)
saccharalis
3294 -S. frugiperda
3295 emmatalis
boztuidae)
3305 G. senilis
(Curculionidae)
3306 -G. senilis
Suelo M. marinus vcarabaeidae) Phyllophaga sp (Scarabaeidae) Suelo Suelo Suelo
M. marinus
-Sch. piceifrons (Lacustidae)
Sch. piceifrons COLIMA
Sch. piceifrons COLIMA
Neubauer se contabilizaron los conidios (Samuels et- g. I 1989;
Sneh, 1991; Moorhouse et al., 1992; Moorhouse et al., 1993ayb).-
-8 L a suspensibn se ajustb a la concentración de 1 x 10
conidios/ml, la cual fue utilizada como concentración de
comparación, para la evaluación de la virulencia de las cepas
arriba mencionadas (Maniania y Fargues, 1984).
El hongo multiplicado en las bolsas de polietileno fu8
recuperado en agua corriente con 0.1% de Tween 80 y los conidios
se contabilizaron, siguiendo la misma metodología arriba descrita;
una vez hecho &to, por dilución se formó la concentraci6n de 2.5 6
X 10 conidios por ml, misma que se utilizb en los experimentos de
campo.
3.1.5 Insecto prueba
Los insectos de A2 ludens que se utilizaron fueron
proporcinados por el laboratorio de cris de moscas de la fruta de
la SAGDR, ubicado en el municipio de Metapa de Dominguez, Chiapas.
Para este estudio se utilizaron larvas del tercer estadio de menos
de 24 horas de edad, enviadas en lotes de 1000 ejemplares, por
mes, a partir del mes de Septiembre de 1994.
3.1.6 Experimentos
Se realizaron una serie de experimentos independientes para
responder al objetivo planteado.
En una primera etapa se evaluaron los 20 aislados del hongo
a la concentracibn lE+lO en larvas del tercer estadio de 5.
ludens. Para bito, se formaron grupos de 20 larvas del tercer
conidios correspondientes a cada uno de los aislados (Hall, 1976;
Moorhouse et &., 1993). El tratamiento testigo estuvo formado por
el mismo nñmero de larvas, pero con la aplicacibn de agua
destilada estéril al 0.05% de Tween 80 (Ravallec et al., 1989).-
-Una vez infectadas las larvas, se colocaron dentro de una
caja Petri de 100x10 mm de didmetro y alto, respectivamente;
ellas, sobre una capa doble de papel filtro humedo. Las cajas se
sellaron, con cinta adhesiva, para evitar que se escaparan. En
total se utilizaron cuatro grupos de 20 larvas para cada
tratamiento (Lezama, 1993).
Las cajas de Petri con las larvas se colocaron en una camara
obscura, a una temperatura de 25+loC, durante el experimento. Cada
-48 horas se fue registrando el numero de larvas con signos de
infecci6n ftingica, como fue, perdida de movilidad, numero de
larvas muertas, la emergencia de hifas a traves de las membranas
intersegmentales del cuerpo de la larva y la esporulacibn del
hongo sobre la larva muerta) (Almeida, 1983).
U n segundo experimento se realizo para determinar la
concentración letal 50% (CL50) de los aislado que del primer
ensayo, resultaron más sobresalientes en cuanto a virulencia 0
capacidad de matar larvas de A. ludens. Para esto, se prepararon -7
50 ml de una suspensión a las concentraciones de 1 x 10 , 1 x
6 5 4 3 1
10 I 1 x 1 0 , 1 x 1 0 , 1 x 1 0 , 1x102, 1 x 1 0 y 0 conidios por
ml, para cada uno de los aislados seleccionados.
Con cada una de estas concentraciones, se inocularon cuatro
grupos de 20 larvas siguiendo la misma metodologia y condiciones
experimentales del experimento inicial. Las variables que se