Estudio y simulación de la formación de Belita en un horno rotatorio
123
0
0
Texto completo
(2) Dedicatoria Al Sagrado Corazón de Jesús y al Inmaculado Corazón de María por su infinita bondad y amor.. A mi esposa Cintia por su paciencia y comprensión, a mi hija Estefanía la luz de mi vida y al pequeño Emmanuel que viene en camino que con su llegada viene a darle a mi vida un toque muy especial. Te quiero hijo.. A mis padres y hermanos por compartir lo bueno y malo de mi paso por esta etapa.. A todas las personas con las que compartí este ciclo en mi vida…Gracias..
(3) Agradecimiento Uno de los valores que nunca debe perder el hombre es la gratitud, razón por la cual agradezco: A todos mis compañeros que compartieron una etapa similar de sus vidas y por haber hecho mi estancia agradable en el Cimav. Al Grupo Cementos de Chihuahua S.A. de C.V., a su personal por su apoyo y confianza. Al Consejo Nacional de Ciencia y Tecnología (CONACYT), ya que sin su apoyo no hubiera podido realizar estos estudios. Al Centro de Investigación en Materiales Avanzados por dedicarnos a la tarea de estudiar para que comprendamos que la investigación es la ciencia del saber. A mis sinodales Dr. José Martín Herrera Ramírez, M.C. Elías Ramírez Espinoza y M.C. Jaime Valenzuela Grado, que revisaron con paciencia este trabajo. Un sincero agradecimiento a mis Directores, Dr. Antonino Pérez Hernández y Dra. Carolina Prieto Gómez, por todo el tiempo que me han dado, por sus sugerencias e ideas de las que tanto provecho he sacado, por el respaldo y la amistad. A todas las personas que participaron directa o indirectamente en este trabajo. A todos ellos.. ¡Muchas Gracias!.
(4) Índice General Dedicatoria Agradecimientos Índice de tablas ..................................................................................................... vii Índice de figuras ..................................................................................................... ix Lista de símbolos y abreviaturas ........................................................................... xiii Resumen ................................................................................................................ 1 Abstract .................................................................................................................. 2 I.. Introducción ................................................................................................ 3. 1.. Antecedentes .............................................................................................. 4. 2.. Materias primas ........................................................................................... 6. 2.1.. Componente calcáreo ................................................................................... 7. 2.1.1. Caliza ............................................................................................................ 7 2.1.2. Margas ......................................................................................................... 7 2.2.. Componente arcilloso ................................................................................... 7. 2.3.. Correctores ................................................................................................... 7. 2.4.. Componentes adicionales a las materias primas .......................................... 8. 2.4.1. Óxido de magnesio ....................................................................................... 8 2.4.2. Álcalis ........................................................................................................... 8 2.4.3. Azufre ........................................................................................................... 8 2.4.4. Cloro ............................................................................................................. 8 2.4.5. Fluoruros....................................................................................................... 8 2.4.6. Fósforo.......................................................................................................... 9 2.4.7. Metales pesados o elementos traza ............................................................. 9 3.. Composición química.................................................................................... 9 i.
(5) 4.. Proceso de fabricación del cemento Pórtland............................................... 9. 4.1.. Extracción de materias primas.................................................................... 10. 4.2.. Trituración ................................................................................................... 10. 4.3.. Prehomogenización y molienda de las materias primas ............................. 10. 4.4.. Precalentamiento ........................................................................................ 10. 4.5.. Precalcinación ............................................................................................ 10. 4.6.. Producción de clínker en horno rotatorio .................................................... 11. 4.7.. Enfriamiento y almacenamiento .................................................................. 11. 4.8.. Silo de homogenización .............................................................................. 11. 4.9.. Molienda de cemento.................................................................................. 11. 4.10. Silo de almacenamiento.............................................................................. 11 5.. Proceso de clinkerización ........................................................................... 12. 5.1.. Deshidratación de los minerales arcillosos ................................................. 14. 5.2.. Descomposición de los carbonatos. Calcinación ........................................ 14. 5.3.. Cinética de la calcinación ........................................................................... 15. 5.4.. Reacciones entre fases sólidas .................................................................. 16. 5.5.. Reacciones en presencia de fase líquida ................................................... 18. 5.6.. Nodulización ............................................................................................... 18. 5.7.. Formación de clínker .................................................................................. 18. 5.8.. Cinética de la cocción de clínker ................................................................ 19. 6.. Fases del clínker ......................................................................................... 20. 6.1.. Alita ............................................................................................................. 21. 6.2.. Belita ........................................................................................................... 21. 6.3.. Aluminato tricálcico ..................................................................................... 22. 6.4.. Ferrita ......................................................................................................... 22. 6.5.. Otras fases del clínker ................................................................................ 22 ii.
(6) 7.. Justificación ................................................................................................ 23. 8.. Objetivo general .......................................................................................... 24. 9.. Objetivos específicos .................................................................................. 24. 10.. Hipótesis ..................................................................................................... 25. II.. Metodología experimental........................................................................ 26. 1.. Recolección de muestras............................................................................ 26. 2.. Análisis químicos mediante fluorescencia de rayos X ................................ 27. 3.. Densidad..................................................................................................... 28. 4.. Finura.......................................................................................................... 29. 5.. Cal libre....................................................................................................... 29. 6.. Análisis térmicos ......................................................................................... 30. 6.1.. Análisis termo gravimétrico ......................................................................... 30. 6.2.. Análisis térmico diferencial ......................................................................... 31. 6.3.. Calorimetría diferencial de barrido .............................................................. 31. 7.. Difracción de rayos X .................................................................................. 32. 8.. Microscopía óptica ...................................................................................... 33. 9.. Microscopía electrónica de barrido ............................................................. 33. III.. Resultados y Discusión: Laboratorio experimental .............................. 35. 1.. Fluorescencia de rayos X ........................................................................... 35. 2.. Densidad..................................................................................................... 36. 3.. Finura.......................................................................................................... 36. 4.. Cal libre....................................................................................................... 37. 5.. Análisis termogravimétrico .......................................................................... 38. iii.
(7) 6.. Análisis térmico diferencial ......................................................................... 40. 7.. Calorimetría diferencial de barrido .............................................................. 42. 8.. Difracción de rayos X .................................................................................. 43. 9.. Microscopía óptica ...................................................................................... 45. 10.. Microscopía electrónica de barrido ............................................................. 47. IV.. Discusión de resultados: Laboratorio tradicional ................................. 50. V.. Horno rotatorio: Parámetros de control ................................................. 54. 1.. Movimiento de sólidos en el interior del horno rotatorio y tiempo de residencia ................................................................................................... 54. 2.. Modelos para el cálculo del tiempo de residencia en hornos rotatorios ...... 58. 3.. Área de un segmento circular ..................................................................... 59. 4.. Fenómeno de transferencia de calor .......................................................... 60. VI.. Simulación: Dinámica de fluidos computacional .................................. 61. 1.. Ventajas de la simulación ........................................................................... 61. 2.. Limitaciones ................................................................................................ 61. 3.. Técnicas para el análisis de flujos .............................................................. 62. 4.. Discretización ............................................................................................. 63. 5.. Métodos de discretización .......................................................................... 63. 5.1.. Diferencias finitas ....................................................................................... 63. 5.2.. Volumen finito ............................................................................................. 63. 5.3.. Elemento finito ............................................................................................ 64. 5.4.. Discretización temporal............................................................................... 65. 6.. Simulación numérica................................................................................... 65. iv.
(8) 7.. Modelos matemáticos que describen los fenómenos presentes en el proceso de formación de belita ................................................................... 65. 7.1.. Modelos de continuidad, momento y energía ............................................. 65. 7.2.. Modelos de turbulencia ............................................................................... 67. 7.2.1. El modelo de esfuerzos de Reynolds ......................................................... 67 7.3.. Modelo teórico de radiación Rosseland ...................................................... 69. 7.4.. Modelo: Transporte de especies y velocidad finita de reacción .................. 69. 7.4.1. Ecuaciones de transporte de especies ....................................................... 69 7.4.2. Difusión másica en flujos turbulentos ......................................................... 69 7.4.3. El modelo de velocidad de reacción laminar............................................... 70 7.4.4. El modelo disipación-remolino .................................................................... 71 VII.. Laboratorio virtual: Metodología ............................................................. 72. 1.. Recopilación y procesamiento de la información ........................................ 72. 2.. Definición y construcción del modelo .......................................................... 74. 3.. Solución del modelo ................................................................................... 78. 3.1.. Configuración de modelos .......................................................................... 78. 3.2.. Condiciones iniciales y de frontera ............................................................. 79. 3.3.. Ejecución del cálculo .................................................................................. 79. VIII.. Resultados y discusión: Laboratorio virtual .......................................... 81. IX.. Discusión de resultados: Laboratorio virtual ......................................... 86 Conclusiones ............................................................................................ 88 Trabajos futuros ....................................................................................... 90 Bibliografía ................................................................................................ 91 Anexo 1: Fórmulas de Bogue ................................................................ 102 v.
(9) Anexo 2: Plano del horno ...................................................................................... 103. vi.
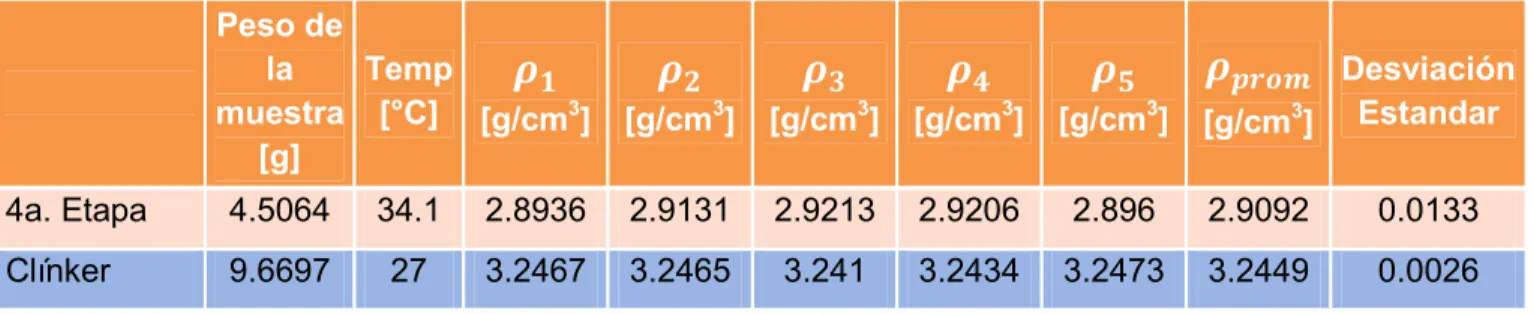
(10) Índice de tablas. Tabla 1. Fórmulas abreviadas ............................................................................. xiv Tabla 2. Composición química del cemento Pórtland ........................................... 9 Tabla 3. Tipos de reacción ................................................................................... 12 Tabla 4. Tipos de reacciones químicas de acuerdo con el estado de la materia .. 12 Tabla 5. Etapas de reacciones en el proceso de clinkerización ............................ 13 Tabla 6. Reacciones de formación de clínker........................................................ 13 Tabla 7. Fases intermedias del proceso de clinkerización ................................... 14 Tabla 8. Principales fases mineralógicas en el clínker Portland. ........................... 21 Tabla 9. Algunos efectos de los óxidos menores ................................................. 23 Tabla 10: Condiciones de prueba para análisis de muestras en TGA .................. 30 Tabla 11. Porcentajes de la composición de óxidos presentes en 4a. etapa y clínker ................................................................................................................... 35 Tabla 12. Densidades de las muestras en diferentes etapas del proceso ........... 36 Tabla 13. Distribución de tamaño de partícula ..................................................... 37 Tabla 14. Cal libre del clínker de proceso ............................................................ 37 Tabla 15. Comparación de cal libre en porcentaje en peso ................................. 38 vii.
(11) Tabla 16. Masa inicial y final de alimentación y de 4a. etapa en TGA ................. 39 Tabla 17. Contenido de fases de 4a. etapa por DRX ........................................... 44 Tabla 18. Contenido de fases del clínker por DRX ............................................... 45 Tabla 19. Número (Fr) y regímenes de movimiento de material sólido ................ 56 Tabla 20. Condiciones de operación del horno .................................................... 57 Tabla 21. Pendiente del horno y grado de llenado ............................................... 58 Tabla 22. Propiedades fisicoquímicas de las especies químicas presentes en la cama de sólidos ................................................................................................... 73 Tabla 23. Propiedades fisicoquímicas de mezcla de material sólido .................... 73 Tabla 24. Configuración de los modelos .............................................................. 78 Tabla 25. Condiciones de frontera ....................................................................... 79. viii.
(12) Índice de figuras. Figura 1. Pirámide de Gizá .................................................................................... 5 Figura 2. Faro de Eddystone ................................................................................. 5 Figura 3. Piedra de Pórtland .................................................................................. 6 Figura 4. Proceso de fabricación del cemento ..................................................... 11 Figura 5. Representación esquemática de la descomposición de una partícula esférica de CaCO3 ................................................................................................ 16 Figura 6. Árbol de reacciones en el horno rotatorio de cemento .......................... 17 Figura 7. Transformación de la harina en clínker ................................................. 20 Figura 8. Toma de muestra de materias primas ................................................... 27 Figura 9. Toma de muestra en la torre de precalentamiento de la 4a. etapa ....... 27 Figura 10. Equipo de fluorescencia de rayos X .................................................... 28 Figura 11. Portamuestra ....................................................................................... 28 Figura 12. Picnómetro Accu Pyc 1330 .................................................................. 28 Figura 13. Equipo Granulómetro Cilas 1180 L ..................................................... 29 Figura 14. Equipo SDT 2960 Simultaneous DSC-TGA ........................................ 31 Figura 15. Equipo Panalytical de DRX ................................................................. 32. ix.
(13) Figura16. Microscopio óptico Axioskop 40 ............................................................ 33 Figura 17. Microscopio electrónico de barrido JEOL JSM 5800 LV ..................... 34 Figura 18. Histograma y acumulado del tamaño de partícula en 4a. etapa ......... 36 Figura 19. TGA de la muestra de alimentación, porcentaje de la pérdida de peso y su derivada ....................................................................................................... 38 Figura 20. TGA de 4a. etapa ................................................................................ 39 Figura 21. Termograma DTA de muestra de 4a. etapa ........................................ 40 Figura 22. Termograma DDTA de muestra de 4a. etapa ..................................... 41 Figura 23. Termograma TGA-DTA-DDTA ............................................................ 41 Figura 24. Termograma TGA–DSC ...................................................................... 42 Figura 25. Termograma TGA–DSC 2 de Noviembre 2012 .................................... 43 Figura 26. Patrones de difracción de 4a. etapa .................................................... 44 Figura 27. Patrones de difracción de clínker ........................................................ 45 Figura 28. Clínker ataque con nital a diferentes amplificaciones .......................... 46 Figura 29. Clínker con ácido salicílico .................................................................. 47 Figura 30. Micrografía de 4a. etapa y clínker ....................................................... 47. x.
(14) Figura 31. Distribución elemental 4a. etapa ......................................................... 48 Figura 32. Distribución elemental clínker ............................................................. 49 Figura 33. Esquema de un horno cementero ....................................................... 54 Figura 34. Capa activa y estacionaria en el movimiento rodante ......................... 55 Figura 35. Esquema de los diferentes regímenes de movimiento de material sólido al interior de un horno rotatorio ............................................................................ 55 Figura 36. Área de la sección transversal ocupada por la cama de sólidos ......... 59 Figura 37. Esquema de los mecanismos de transferencia de calor en el horno rotativo ................................................................................................................. 60 Figura 38. Ejemplo de un volumen de control ...................................................... 64 Figura 39. Modelo de movimiento rodante de la materia en el interior del horno .. 74 Figura 40. Esquema del modelo centrífugo y anillo de material formado en este tipo de movimiento ............................................................................................... 75 Figura 41a. Dimensiones del volumen de estudio. ................................................ 76 Figura 41b. Dominio del modelo y malla ............................................................... 77 Figura 41c. Malla ................................................................................................... 77 Figura 42. Perfil de temperatura de una isosuperficie transversal y axial ............ 81. xi.
(15) Figura 43. Perfil de fracción másica de belita en una isosuperficie transversal y axial ....................................................................................................................... 82 Figura 44. Perfil de fracción másica de sílice en una isosuperficie transversal y axial ...................................................................................................................... 82 Figura 45. Perfil de distribución de la fracción másica de la belita para la componente transversal del dominio .................................................................... 83 Figura 46. Perfil distribución de la fracción másica de la belita para la componente axial del dominio ................................................................................................... 84 Figura 47. Perfil axial de la distribución másica del óxido de calcio y silicio ......... 84 Figura 48. Perfil de la entalpía total del sistema contra la fracción másica de la belita ..................................................................................................................... 85 Figura 49. Comportamiento turbulento del flujo másico ....................................... 85. xii.
(16) Lista de símbolos y abreviaturas. CFD ∆H T Th Ph Ts Ps Tr Pr D L β θ Ṁ R n h Fr g. Computational fluid dinamic. Entalpía de reacción. Temperatura. Temperatura del horno. Presión del horno. Temperatura de la partícula en la superficie. Presión de la partícula en la superficie. Temperatura en el intercara de reacción. Presión en el intercara de reacción. Diámetro del horno. Longitud del horno. Ángulo de inclinación. Ángulo de reposo. Velocidad de flujo másico. Radio del horno. Velocidad de rotación. Altura de la cama de los sólidos dentro del horno. Ángulo de llenado. Número de Froude. Velocidad angular. Aceleración gravitacional. Grado de llenado. P Producción de clínker. (%) Porcentaje de inclinación del horno. t Tiempo de residencia del material. r radio de la trayectoria de la partícula en el lecho de sólidos. C Longitud de la cuerda. Sm Fuente de masa. r Densidad. p Presión estática ⃗ Vector general de velocidad. Operador laplaciano. Tensor de esfuerzos. ⃗ Fuerza externa al cuerpo. Viscosidad molecular. xiii.
(17) I. Tensor unitario. Energía total, energía de activación. Conductividad térmica efectiva. Entalpía.. ⃗. Flujo de difusión de especies. Calor de reacción química. Velocidad fluctuante de los componentes. Energía cinética por unidad de masa.. u′ k ′ ′ ,¡. ¡ ,. Viscosidad turbulenta. Difusión turbulenta. Número de Prandtl turbulento para k. Viscosidad cinemática. Coeficiente de expansión térmica. Velocidad de disipación turbulenta. Función delta. Distribución de esfuerzos normales en la pared. Velocidad media del tensor de rotación. Dilatación en turbulencia compresible. Número Mach de turbulencia. Número de Prandtl turbulento para . Tensor de esfuerzos deviatorico.. τ¡. , ,. ,. Esfuerzos de Reynolds.. Número de Prandtl turbulento. Radiación incidente. Generación de turbulencia por energía cinética. Radiación de flujo. Índice de refracción del medio. Constante de Stefan-Boltzman. Fragmento másico de la especie i. Es la tasa neta de producción de especies i por reacción química. Es la tasa de creación por incremento de la fase dispersa. Coeficiente de difusión másica para las especies i en la mezcla. Coeficiente de difusión térmico (Soret). Número turbulento de Schmidt. Constante de velocidad de reacción. Factor pre-exponencial. xiv.
(18) ,. Energía de activación para la reacción. Constante universal. Función gamma. Concentración molar de especies j en la reacción r.. ,. Velocidad exponencial para especies reactantes j dentro de la reacción r.. ,. Velocidad exponencial para especies reactantes.. R. ,. Peso molecular de especies i. Velocidad molar de Arrehnius de creación/destrucción de especies i en la reacción r. Coeficiente estequiométrico para los reactantes i en la reacción r. , ,. Coeficiente estequiométrico para la reacción i en la reacción r.. ,. ,. ,. ,. Número de especies químicas en el sistema. Coeficiente estequiométrico de los productos de especies. Exponente de temperatura. Velocidad de producción de especies i debido a la reacción r. Constante empírica igual a 4.0 Constante empírica igual a 0.5 Fracción másica de un reactante en particular, ℛ. Fracción másica de cualquier especie de productos, P. Velocidad de reacción reversible. Energía de activación.. xv.
(19) Abreviaturas más utilizadas en la industria cementera. Óxidos C=CaO M=MgO T=TiO2 SIO2 K=K20 P=P2O5 A=Al2O3 Ŝ=SO3 H=H2O F=Fe2O3 N=Na2O Ĉ=CO2. Tabla 1. Fórmulas abreviadas Fases del cemento C3S = 3CaOSiO2 C2S = 2CaOSiO2 C3A = 3CaOAl2O3 CA = CaOAI2O3 C2AS = 2CaOAI2O3SiO2 C2F = 2CaO Fe2O3 C4AF = 4CaOAI2O3Fe2O3 C3MS2 = 3CaOMgO2Si02 KC33S12 = K2O23CaO12SiO2 NC8A3 = Na2O8CaO3AI2O3 CSH= CaO ŜO32H2O C-S-H = 3CaO2SiO28H2O. xvi.
(20) RESUMEN Se desarrolló un modelo para la formación de belita dentro de un horno para clinker de cemento Pórtland, haciendo uso del software Ansys-Fluent. Para ello se dividió en dos partes: laboratorio experimental y laboratorio virtual. Utilizando materiales industriales y para evaluar algunas características físicas y químicas del proceso. En lo cual se aplicaron varias técnicas como fluorescencia de rayos X, densidad, finura, cal libre, análisis termogravimétrico, térmico diferencial y calorimetría diferencial de barrido; difracción de rayos X, microscopía óptica y electrónica. Se realizó la simulación de la formación de belita utilizando los modelos de continuidad, momento y energía; el modelo de turbulencia de esfuerzos Reynolds, el modelo de radiación Rosseland, el modelo de transporte de especies y velocidad finita de reacción. El modelo es una representación en 3D, en él se involucra el movimiento de material sólido dentro del horno, tiempo de residencia, fenómenos de transferencia de materia y energía entre el lecho de sólidos, gases de combustión y las paredes internas del horno rotatorio. El modelo es capaz de predecir la distribución de temperatura en cualquier posición axial así como la composición del lecho de sólidos en un estado estable. Basados en la literatura revisada se encontraron algunas discrepancias en las reacciones de clinkerización. Se recomienda el diseño de un mecanismo para la recolección de muestra a la entrada del horno, finalmente el modelo matemático propuesto constituye una buena base inicial para ampliaciones del mismo encaminadas a incluir el comportamiento de las transformaciones de fase en el clínker.. 1.
(21) ABSTRACT This paper shows the development of a model which describes the Belite formation into a rotatory kiln by using Ansys-Fluent. The work was divided in two issues: experimental and virtual work. By using industrial materials we applied different techniques as (x ray fluorescence analysis, specific gravity, fineness, and free lime tests, thermogravimetric analysis, differential thermal analysis and differential scanning calorimetry, optical microscopy and scanning electron microscopy, in order to evaluate some chemical and physical characteristics of the process. We simulated the Belite reaction´s formation in continuity model, momentum and energy; the turbulence stress Reynolds model and the Rosseland radiation model. Besides the species transporting model and the finite velocity were used. The 3D model involves de solid material movement inside the furnace, residence time, mass transfer and energy between packed solids, combustion gases and the internal walls of the furnace. The model can predict the temperature distribution at any axial position so as the composition of the packed in steady state. Based on the literature revised we discovered some no agreements in the clinkerization reactions. We suggest the design of a mechanism to gather the sample at the input of the furnace. Finally the mathematical model proposed constitutes a good platform to spread out the same phenomenon, and to deal them to include the behavior of the phase transformations in the clinker.. 2.
(22) CAPITULO I. I.. INTRODUCCIÓN.. En la actualidad, toda empresa cementera tiene entre sus objetivos optimizar su proceso de producción, con el fin de reducir el consumo de combustible, disminuir los costos de producción y mejorar la calidad de su producto; la clinkerización es una de las etapas más importantes en el proceso de producción de cemento. Por esta razón, se plantea la necesidad de realizar esta investigación en esta parte del proceso. Esto implica la caracterización fisicoquímica y mineralógica de los materiales intermedios del proceso y del clínker, al igual que el control estricto del proceso de producción, pautas para desarrollar la identificación de acciones óptimas en cada etapa, etc. Hasta la fecha se dispone de pocos modelos matemáticos, en los hornos rotatorios en la industria del cemento [1-2], que se han enfocado a la predicción de flujo de materia [3-6], balance de energía [7-32], altura de la cama y movimiento del material sólido dentro del horno [33-39], tiempo de residencia y perfil de la flama [40-44], el efecto de la formación de costra [45-46], los fenómenos de transferencia de materia y energía entre los gases de combustión, lecho y pared interna del horno [47-49]. El proceso de clinkerización referido a las transformaciones fisicoquímicas de la materia prima dentro del horno para producir clínker, es muy complejo y poco conocido [50-51], aunado a esto, el flujo de energía y temperatura dentro del horno [8,52-56]. El proceso comprende una serie de reacciones, activadas por temperatura y tiempo de residencia, mediante las cuales la mezcla cruda se transforma en clínker para cemento Pórtland. Mezcla Cruda. Temperatura (T) Tiempo (t). Clínker Pórtland. El clínker Portland se fabrica a partir de una mezcla cruda, de aluminosilicatos que puede estar constituida por caliza-arcilla-hematita-ignimbrita, entre otros, la cual debe elevar su temperatura hasta 1450°C. Las reacciones que se llevan a cabo son en su balance global endotérmicas, afectadas tanto por su composición química-mineralógica en la mezcla cruda así como su tamaño de partícula y homogeneidad. La obtención del clínker exige energía mecánica, térmica y eléctrica, su velocidad de reacción es lenta por ser un sistema heterogéneo (gas-líquido-sólido) en sus diversas combinaciones hasta su clinkerizado. Finalmente, para buscar mantener los minerales deseados en el clínker, éste se enfría rápidamente.. 3.
(23) Capítulo I. Introducción. La simulación de operación de hornos rotatorios mediante las herramientas computacionales, ha cobrado especial interés en los últimos años. Esta alternativa presenta las ventajas de reducir el costo e inconvenientes operativos en planta, ya que la producción típica de un horno cementero es mayor a 1700 toneladas de clínker por día. La energía necesaria para estas reacciones es suministrada por gases calientes, producto de la combustión (carbón, gas, aceite y otros combustibles alternos). 1. Antecedentes. Breve Historia del cemento Pórtland [57-61]. 5,600 A.C. Una de las construcciones más antiguas en las que se empleó una mezcla primitiva semejante al cemento, es el suelo de una cabaña en Lepenski Vir (Serbia), se trataba de un compuesto formado por cal roja y aditivos. 3,000 A.C. En Chile se usaba un conglomerante hidráulico procedente de la calcinación de algas. 2,500 A.C. Los egipcios emplearon morteros a base de yeso y cal en sus construcciones (Figura 1). 27 A.C. Los romanos en sus construcciones emplearon concreto, elaborado con puzolanas, cal y áridos ligeros. 75-80 D.C. También con este producto se construyeron las paredes del Anfiteatro de Pompeya (año 75) y los cimientos y las paredes internas del Coliseo (año 80). 500–1200 La calidad de los morteros disminuye. Se emplean morteros con arena gruesa y cal, mezclada con carbón de madera o yeso puro. 1300 La calidad de los cementantes se mejora al reintroducir la técnica de incinerar cal y agregarle puzolana. 1756 El ingeniero británico John Smeaton redescubre el cemento romano, y reconstruye el faro de Eddystone (Reino Unido, Figura 2), capaz de soportar las condiciones marítimas, mismo que permaneció de pie por 126 años. Concluyó y reconoció por vez primera la acción de las arcillas, en la calidad del cemento, en sus propiedades hidráulicas. Sin embargo su éxito no fue reconocido en su momento. 1756–1830 Se usaban grandes cantidades de cemento natural, el cual era producido al incinerar una mezcla natural de cal y arcilla, cuyas propiedades variaban ampliamente por ser un elemento natural. 1796 James Parker patenta un cemento hidráulico producido al calcinar módulos de cal impuros que contienen arcilla, el cual se denomina Cemento Parker o Cemento Romano. 1812 Louis Vicat de Francia prepara una cal artificial al calcinar mezclas sintéticas de arcilla y cal.. 4.
(24) Capítulo I . . . . Introducción. 1824 Joseph Aspdin, un constructor de Wakefield (Reino Unido), calcinó en un horno una mezcla de tres partes de piedra caliza por una de arcilla. Éste fue el padre del cemento moderno y se llamó Pórtland porque su aspecto era similar al de las calizas de la isla de Pórtland. 1845-1847 Isaac Johnson logra temperaturas suficientemente altas para clinkerizar la materia prima y descubre la necesidad de quemar los materiales hasta su punto de fusión. 1885 F. Ransome patenta un horno horizontal que podía ser rotado, de modo que el material podía moverse gradualmente de un lado al otro dentro del horno. 1909 Thomas Alba Edison obtiene una patente para los hornos rotatorios. 1940 Se desarrollan los primeros hornos de vía húmeda, los cuales eran el doble de eficientes a los hornos rotativos anteriores. 1970 Se desarrollan los hornos largos vía seca. Actualidad Evolución y mejora del cemento y de su proceso de fabricación. Uso de algunos residuos industriales como materia prima del cemento. Desarrollo de conglomerantes inorgánicos fabricados con cemento, como el cemento geopolimérico.. Con los trabajos de John Smeaton dejan de ser los yesos y las cales, los conglomerantes base en la construcción, es durante el siglo XVIII cuando se despierta un interés notable por el conocimiento de los cementos. J. Parker, en base a los descubrimientos de Smeaton y utilizando las margas de las orillas del Támesis, obtuvo una cal hidráulica a la que denominó “cemento romano” y que patentó en 1796. Esta cal, que. Figura 1. Pirámide de Giza, ejemplo de la ingeniería Egipcia Figura 2.muy Faro de hidráulica, Eddystone. era fraguaba rápidamente y alcanzaba una resistencia relativamente considerable.. Figura 2. Faro de Eddystone.. Las investigaciones de L. J. Vicat encontraron que un contenido de arcilla en la caliza del orden del 27 al 30 % o bien una parte de arcilla por tres de cal, constituían la composición más favorable para la fabricación del clínker de cemento [62]. Esto permitió preparar una 5.
(25) Capítulo I. Introducción. cal hidráulica artificial mediante la calcinación de una mezcla de piedra caliza y arcilla, triturada previamente en un molino húmedo. Este proceso se considera el precursor principal en la fabricación de cemento Pórtland. Con dicha cal se construyó el primer puente sobre el rio Dordoña en Francia. El 21 de Octubre de 1824 Joseph Aspdin patenta “Producing an artificial stone”, estaba familiarizado con las piedras de construcción y en su patente describe su material como “Cemento Pórtland”. La elección de este nombre fue porque en ese momento la piedra de Pórtland tenía una alta reputación por su calidad y durabilidad y semejanza del color (Figura 3). Su hijo William Aspdin descubrió que el material sobrequemado incrementaba la resistencia del cemento [61]. Se atribuye la producción a escala industrial del cemento moderno a Isaac Johnson, quien en 1845 logra temperaturas suficientemente altas para clinkerizar a la mezcla de arcilla y caliza empleada como materia prima. Los estudios científicos del cemento Pórtland empezaron a ganar Figura 3. Piedra de Pórtland impulso hacia finales del siglo XIX. Le Chatelier propone teorías de fraguado y endurecimiento del cemento Pórtland. El cemento Pórtland se aplica, a partir de 1900, en las obras de ingeniería y al mismo tiempo desciende el consumo de cementos naturales. Hoy en día es éste el material industrializado de construcción de mayor consumo [63].. 2. Materias primas. Para fabricar cemento pueden utilizarse minerales de origen natural lo mismo que productos industriales. Como materiales de partida sirven: cal, sílice, alúmina y óxidos de hierro. Estos componentes raramente se encuentran en proporciones deseadas en un solo compuesto. Por tanto, la mayoría de las veces se ha de elegir la mezcla de un componente rico en cal (caliza) con un componente arcilloso (alúmina, silicatos y óxidos de hierro). Para fabricar una tonelada de cemento son necesarias 1.6 toneladas aproximadamente de materias primas [64]: . Componente calcáreo. Componente arcilloso. Correctores. Componentes minoritarios. Óxido magnésico. Álcalis. 6.
(26) Capítulo I . 2.1 .. Introducción Azufre. Cloruros. Fluoruros. Fósforo. Metales pesados o elementos traza.. Componente calcáreo.. Es el componente formado en su mayor parte por carbonato de calcio (caliza o marga). 2.1.1 Caliza. La caliza, por lo general, son rocas de grano fino. La dureza viene determinada por su edad geológica, cuanto más antigua es la formación, conlleva más dureza. Los yacimientos de la caliza pura son de color blanco. Por lo general, contiene otros materiales referentes a sustancias arcillosas o minerales de hierro que influyen en su color. 2.1.2. Margas. A las calizas que van acompañadas de sílice y de productos arcillosos, así como de óxido de hierro, se les denominan margas. 2.2.. Componente arcilloso.. La segunda materia prima importante para la fabricación del cemento es la arcilla. Tiene una textura de grano fino. Su composición química varía desde minerales puros de arcilla hasta los que contienen agregados de hidróxido de hierro, sulfuro de hierro, arena, carbonato de calcio, etc. El hidróxido de hierro es el componente colorante más frecuente de las arcillas. También pueden producirle distintas coloraciones las sustancias orgánicas. La principal fuente de álcalis en los cementos es el componente arcilloso del crudo. 2.3.. Correctores.. Estos compuestos tienen un alto porcentaje de alguno de los óxidos principales, por lo que agregado en pequeñas cantidades, ayuda a corregir la composición química de la mezcla de materias primas. Por ejemplo, arena como material adicional para elevar el contenido en anhídrido de silicio, mineral de hierro o también arcillas de muy alto contenido en SiO2 [63].. 7.
(27) Capítulo I 2.4.. Introducción. Componentes adicionales de las materias primas (Componentes minoritarios).. Dependiendo del tipo y cantidad, influyen de forma decisiva sobre el proceso de fabricación. 2.4.1. Óxido de magnesio. En las calizas el MgO se encuentra como dolomita (CaCO3MgCO3). Los niveles de MgO no deben de ser muy altos, ya que podrían aparecer cristales de periclasa en el cemento y originar grietas durante el proceso de hidratación del cemento. El óxido de magnesio se encuentra combinado hasta en un 2% en las fases principales del clínker. Cuando su cantidad es superior al 5 %, tiene carácter expansivo [66]. 2.4.2. Álcalis. Provienen en general de la arcilla. Los K2O y Na2O proceden de los materiales margosos y arcillosos, y en pequeña cantidad en las cenizas del carbón. En el interior del horno rotatorio se volatiliza una parte de los álcalis en la zona de sinterización y da lugar a un ciclo cerrado de álcalis. 2.4.3. Azufre. El azufre entra en el horno por medio de combustibles y por la materia prima (sulfato o sulfuro). El azufre se oxida a SO2 y se libera a la atmósfera. Por exceso de SO2 puede ocurrir que éste todavía reaccione con el CaCO3 en el intercambiador para dar CaSO4. Es favorable que el azufre reaccione con los álcalis para que éstos salgan del horno en el clínker [67]. 2.4.4. Cloro. Entra con el combustible (carbón) o con arcillas de origen marino. Al reaccionar con los álcalis, forman cloruros transportables por los gases y precipitan en el intercambiador de calor. Retorna con el material en reacción y en la zona de sinterización, son vaporizados de nuevo, formando un circuito cerrado. 2.4.5. Fluoruros. Existe en cantidades pequeñas en las rocas carbonatadas y está presente como fluorita ó fluorapatito. El contenido está situado entre los límites del 0.03 % al 0.08 %. En algunos casos se añade de 0.5 % a 1.5% de fluorita con el fin de mejorar la aptitud de cocción del clínker.. 8.
(28) Capítulo I. Introducción. 2.4.6. Fósforo. Contenidos mayores de 0.5 % pueden tener como consecuencia fuertes retrocesos en las resistencias iniciales, impide la formación del C3S y forma solución sólida con el C2S, se deben buscar materias primas que contengan la menor cantidad posible de óxidos de fósforo. 2.4.7. Metales pesados o elementos traza. Aportados por minerales conteniendo Pb, Zn, Cu, Ba, aun en pequeñas cantidades, inhiben el fraguado del cemento, por lo que deben de eliminarse. Su presencia se asocia a impurezas en el combustible o en las propias arcillas. El clínker Pórtland consta principalmente de cuatro fases cristalinas: alita, belita, aluminato cálcico y ferritoaluminato cálcico. Contiene además cal libre (CaO sin combinar), así como magnesia libre (periclasa).. 3. Composición química. La composición química del cemento Pórtland se muestra en la Tabla 2. Tabla 2. Composición química del cemento Pórtland [67-71]. Óxidos Rango de concentración (%) CaO 58-68 SiO2 18-26 Al2O3 3-8 Fe2O3 1-6 MgO 0-5 K2O 0-1 Na2O 0-1 SO3 0-2.5 Otros 0-1. 4. Proceso de fabricación del cemento Pórtland (Vía Seca). Las normas ASTM C150 [72] y C219 [73] definen al cemento Pórtland como un cemento hidráulico producido por pulverización del clínker Pórtland que consiste esencialmente de silicatos de calcio hidráulicos y por lo general contiene sulfato de calcio. Para el proceso de fabricación se requiere una serie de operaciones separadas y continuas (Figura 4). Los procesos son básicamente definidos por la forma de preparar el crudo.. 9.
(29) Capítulo I 4.1.. Introducción. Extracción de Materias primas.. El proceso de fabricación del cemento comienza con la obtención de las materias primas necesarias para conseguir la composición deseada de óxidos para la producción de clínker. Las materias primas esenciales, caliza y arcilla, son extraídas de las canteras, a menudo situadas cerca de la planta de cemento. Pequeñas cantidades de material correctivo como mineral de hierro (Ignimbrita), bauxita o arena pueden ser necesarias en proporcionar óxidos adicionales de hierro (Fe2O3), alúmina (Al2O3) y sílice (SiO2) para adaptar la composición química de la mezcla cruda al proceso. 4.2.. Trituración.. La trituración es la primera etapa de la operación de reducción de tamaño de las materias primas. La materia prima es transportada a una trituradora y son quebradas en piezas hasta alcanzar el tamaño conveniente y eficientar la operación de molienda. 4.3.. Prehomogeneización y molienda de las materias primas.. La prehomogeneización se produce en las diferentes materias primas que son mezcladas en las debidas proporciones, a fin de mantener una composición química necesaria para terminar moliéndolas hasta formar la mezcla cruda. Para asegurar un cemento de alta calidad, la química de la materia prima y la mezcla cruda son cuidadosamente monitoreadas y controladas. 4.4.. Precalentamiento.. La torre de precalentamiento es una serie de ciclones verticales, a través de los cuales se hace pasar la harina cruda. En los ciclones la energía térmica es recuperada de los gases de combustión y el crudo es precalentado con una descarbonatación parcial (hasta el 40-60 %) antes de entrar al horno, de esta manera las reacciones químicas ocurren rápidamente y son más eficientes. El tiempo aproximado que tarda el crudo desde que es alimentado en el precalentador hasta que llega al horno es de 25-30 segundos. Durante dicho tratamiento la temperatura del crudo pasa de 50°C a 780-830ºC [74]. 4.5.. Precalcinación.. La calcinación es la descomposición de carbonato de calcio (CaCO3) en óxido de calcio (CaO) y dióxido de carbono (CO2), mediante calor suministrado: CaCO3 ↔ CaO + CO2. Parte de la reacción se lleva a cabo en el precalentador. La tarea del precalcinador es calentar y calcinar el crudo, así como asegurar la completa combustión del combustible alimentado en él [75]. 10.
(30) Capítulo I 4.6.. Introducción. Producción de clínker en horno rotatorio.. La harina caliente entra al horno, el combustible es quemado dentro del horno y el material alcanza hasta una temperatura de 1450°C, el material se desliza y cae progresivamente hacia las zonas calientes de la flama. La intensidad del calor causa reacciones químicas y físicas que funden parcialmente la harina caliente. 4.7.. Enfriamiento y almacenamiento.. El propósito del enfriador es intercambiar el aire del ambiente con el clínker caliente. El clínker caliente cae en los enfriadores donde es enfriado por el aire entrante de combustión, minimizando la pérdida de energía del sistema. El clínker se almacena en silo o en una nave cerrada. 4.8.. Silo de homogeneización.. El clínker es mezclado con otros componentes minerales, típicamente los cementos contienen de 4-5% de yeso para controlar el tiempo de fraguado del producto. 4.9.. Molienda de cemento.. El cemento Pórtland se produce moliendo juntos clínker y sulfatos tales como yeso o anhidrita que actúan como retardadores del fraguado. 4.10. Silo de almacenamiento. El producto final es homogeneizado así como almacenado en silos y enviado desde ahí a una estación de empaque.. Figura 4. Proceso de fabricación del cemento. Adaptado de [76].. 11.
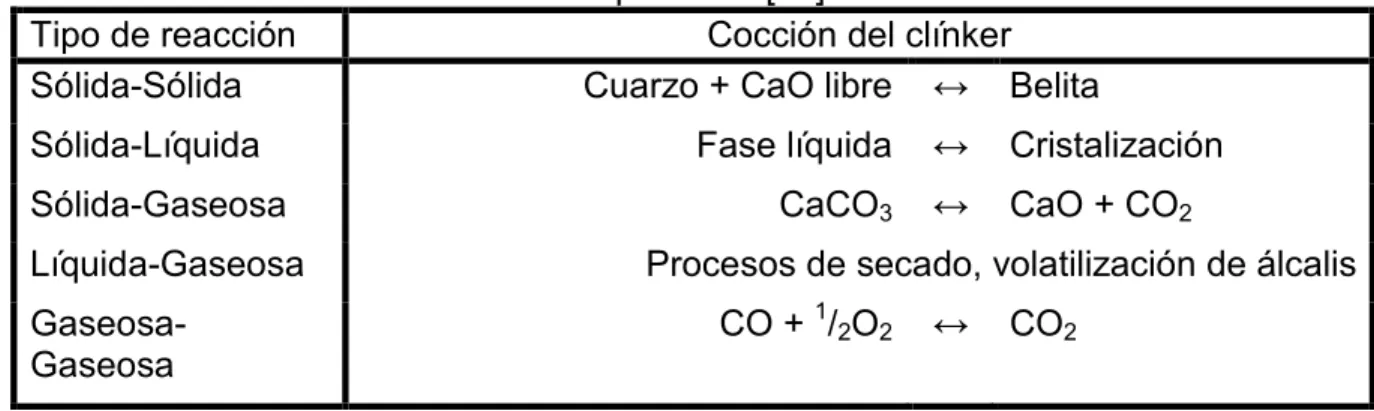
(31) Capítulo I. Introducción. 5. Proceso de Clinkerización. La secuencia de reacciones en la cocción del crudo no es todavía clara, debido a la amplia variación de las características físico-químicas de las materias primas, condiciones de operación del horno y a la dificultad práctica de tomar muestras calientes de las diferentes partes del horno para su estudio [52-54, 77]. Las reacciones químicas que se producen durante la cocción del crudo pueden clasificarse por su tipo de reacción (Tabla 3), o de acuerdo con los tipos de fases (Tabla 4). Las reacciones pueden ser clasificadas de acuerdo con la etapa que controla la velocidad (Tabla 5). Para muchas reacciones, sin embargo, no se conoce la etapa que controla la velocidad. La Tabla 6 muestra los detalles de las reacciones principales de clinkerización propuesta por Locher [1-2].. Tabla 3. Tipos de reacción. Adaptado de [78]. Tipo de reacción Cocción del clínker Cambio Cuarzo de la forma estable ↔ Cuarzo de la forma estable estructural a alta temp. a baja temp. Descomposición Combinación. CaCO3 ↔ CaO + CO2 2CaO + SiO2 ↔ C2S. Tabla 4. Tipos de reacciones químicas de acuerdo con el estado de la materia. Adaptado de [79]. Tipo de reacción Cocción del clínker Sólida-Sólida Cuarzo + CaO libre ↔ Belita Sólida-Líquida Sólida-Gaseosa Líquida-Gaseosa GaseosaGaseosa. Fase líquida. ↔. Cristalización. CaCO3. ↔. CaO + CO2. Procesos de secado, volatilización de álcalis CO + 1/2O2. ↔. CO2. 12.
(32) Capítulo I. Introducción. Tabla 5. Etapas de reacciones en el proceso de clinkerización. Adaptado de [80] Tipo de mecanismo de reacción. Cocción del clínker. Difusión. Formación de alita. Contorno de fase. Cuarzo + cal libre. Belita. Fase líquida. . Nucleación. Cristalización de aluminato y ferrita. Formación de alita. Tabla 6. Reacciones de formación de clínker. Reacción H2Oliq H2Ovapor. Rango de Temperatura [°C] 0 a 100. Entalpía estándar de reacción [kJ/kg] + 2446. CO + ½O2 CO2. 620 a 670. - 10100. C + O2 CO2. 450 a 750. - 32786. C + ½O2 CO. 450 a 750. - 9200. S + O2 SO2. 400 a 500. - 9276. H2 + ½O2 H2O. 530 a 580. - 121000. CaCO3 CaO + CO2. 550 a 960. + 1780. MgCO3 MgO + CO2. 550 a 960. + 1395. CaO + Al2O3 CA. 800 a 1100. - 100. 2CaO + Fe2O3 C2F. 800 a 1100. - 114. 2CaO + SiO2 C2S. 600 a 1300. - 732. CA + C2F + CaO C4AF. 1200 a 1280. + 25. CA + 2CaO C3A. 1200 a 1280. + 25. C2S + CaO C3S. 1200 a 1280. + 59. >1280. + 600. Clínkersól Clínkerliq. 13.
(33) Capítulo I 5.1.. Introducción. Deshidratación de los minerales arcillosos.. En general, el agua adsorbida y la interlaminar se pierden en el intervalo de temperatura de 100 °C a 300 °C, es decir, durante el secado. Por su parte, el agua combinada químicamente comienza a perderse en forma de grupos hidroxilo (deshidroxilación) entre 300 °C y 400 °C y de forma rápida entre 500 °C y 600°C. Al calentar la harina cruda a temperaturas superiores (entre 350 °C y 750ºC), se desprende el agua combinada de los componentes arcillosos (descomposición de los materiales arcillosos). 5.2.. Descomposición de los carbonatos. Calcinación.. La reacción da lugar a un óxido y un producto volátil; CaO, MgO y CO2 En la descomposición de la caliza, su entalpía de reacción es de ∆H = 1644 kJ/ kg [81] siendo esta reacción fuertemente endotérmica. Esto significa que ha de suministrarse calor para descomponer el carbonato de calcio, considerándose como la reacción que consume más calor durante el proceso. Al aumentar la temperatura de 550 ºC a unos 700 ºC, se produce la disociación del carbonato magnésico. Esta reacción es mucho menos importante en la fabricación de cemento que la calcinación de carbonato cálcico. La descomposición del carbonato cálcico reaccionando con la arcilla, empieza alrededor de los 600ºC; de esta manera, se realiza un juego de reacciones más complejo entre la cal y la arcilla, formándose una serie de compuestos que incluyen: CaOAl2O3 (CA), 2CaOFe2O3 (C2F), CaOSiO, (CS) y 2CaOSiO2 (C2S). Las reacciones de estado sólido se llevan a cabo a partir de los 800°C. Se considera que estas reacciones son muy lentas, y pueden acelerarse reduciendo el tamaño de las partículas y elevando la temperatura de quemado. La Tabla 7 muestra un conjunto de los minerales intermedios reportados durante la producción de clínker [82-84]. Tabla 7. Fases intermedias del proceso de clinkerización Nombre del mineral Composición química Anhidrita CaSO4 Arcanita K2SO4 Espurrita de sulfato 2(C2S)CaSO4 Langbeinita de calcio K2Ca2(SO4)3 Espurrita 2(C2S)CaCO3 Silvina KCl Mayenita 12CaO7Al2O3 Aluminato monocálcico CaOAl2O3 Ferrita dicálcica 2CaOFe2O3 Gehlenita 2CaOAl2O3SiO2 14.
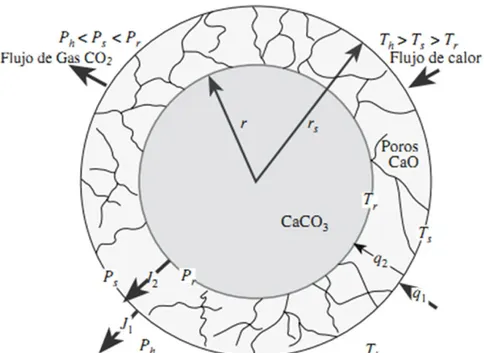
(34) Capítulo I. Introducción. La descomposición de la espurrita tendrá lugar en las zonas del horno donde el contenido de CO2 en los gases es bajo. La espurrita es térmicamente más estable que la calcita, ya que tiene una temperatura de disociación de 912 ºC. Puede formarse como un producto intermedio durante el calentamiento de la mezcla cruda del CaCO3 y SiO2, o por reacción entre el CaO, el Ca2SiO4 y el CO2. Sólo es estable en la gama de temperaturas entre la descomposición de calcita y la descomposición de espurrita, es decir entre 890ºC y 912ºC y a presión atmosférica. Durante la calcinación, la formación de mineral de C2S también continuará, ya que el CaO liberado inmediatamente se combinará con el SiO2. La formación de C2S es un proceso exotérmico, sin embargo no resulta en un aumento de la temperatura, ya que el proceso de calcinación, que se desarrolla simultáneamente, es un proceso endotérmico. La temperatura de la harina sólo aumenta lentamente durante la calcinación debido al alto nivel de absorción de calor, pero tan pronto como haya sido expulsado todo el CO2, la temperatura aumenta rápidamente. Otra reacción que tiene lugar durante la calcinación es la formación de 12CaO7Al2O3 (C12A7), que empieza a temperaturas de 800-900 ºC durante la cual se desarrolla un calor de 80 kJ/ mol. 5.3.. Cinética de la calcinación.. El mecanismo y cinética de la descomposición de la caliza ha sido ampliamente estudiado [82-87]. Se ha mostrado que la reacción comienza en la superficie exterior de la partícula y prosigue hacia adentro, de la intercara de reacción. Detrás de dicha intercara el material se ha convertido en óxido de calcio, dando lugar a una zona calcinada más o menos porosa. Este modelo se muestra en la Figura 5 [88]:. 15.
(35) Capítulo I. Introducción. Figura 5. Representación esquemática de la descomposición de una partícula esférica de CaCO3 que da lugar a un producto poroso (CaO) y un gas (CO2). La reacción es endotérmica, requiriendo la transferencia de calor. Las fuerzas motrices para el calor y el transporte de masas para la descomposición en estado estacionario son expresadas como temperaturas y presiones en el horno (Th, Ph), en la superficie de la partícula (Ts,Ps), y en la intercara de reacción (Tr, Pr). 5.4.. Reacciones entre fases sólidas (a temperaturas inferiores a las de clinkerización).. A partir de temperaturas entre 550 y 600ºC comienzan a producirse reacciones entre fases sólidas, en las cuales se combinan los productos de descomposición del CaCO3 con los de la arcilla, formándose primero compuestos de menor contenido de cal, como por ejemplo aluminato monocálcico, CA, y silicato dicálcico, C2S. El CA se combina con cal libre, lo que resulta la formación de la fase intermedia C12A7. La descomposición de la“gelenita” 2CaOAl2O3SiO2 ocurre a temperaturas más elevadas (alrededor de 1100 ºC), y comienza la formación de 3CaOAl2O3, y 4CaOAl2O3Fe2O3. Se ha propuesto que la gelenita es el producto de reacción entre los refractarios del horno y los materiales formadores del clínker.. 16.
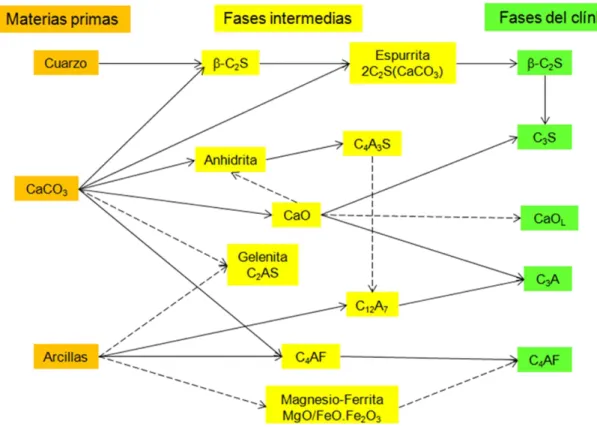
(36) Capítulo I. Introducción. Las primeras fases detectadas a 700ºC son: CA+C12A7+C2S y su cantidad aumenta con la temperatura hasta 900 – 1000 ºC. También se ha sugerido que las primeras fases detectadas son: CF + CA + CS. La presencia de espurrita se ha detectado en muestras retiradas del horno en el intervalo de temperatura de 680–1000ºC, particularmente en presencia de haluros y álcalis. En general, las reacciones entre fases sólidas transcurren muy lentamente, pero se pueden acelerar mediante: 1.- Reducción del tamaño de partícula en la materia prima (aumento de la superficie específica). 2.- Buena homogeneización. 3.- Aumento de la temperatura. 4.- Distorsión de las redes cristalinas. A partir de los 900ºC, la temperatura sube rápidamente, lo que hace que los granos de cuarzo todavía existentes, se transformen en silicato dicálcico (Belita). A 1300ºC las reacciones en estado sólido prácticamente se han completado. Una secuencia de reacciones propuesta puede verse en la Figura 6 [Adaptado de 89]:. Figura 6. Árbol de reacciones en el horno rotatorio de cemento.. 17.
(37) Capítulo I 5.5.. Reacciones en clinkerización).. Introducción presencia. de. fase. líquida. (sinterización. o. La formación de fase líquida (fundida) indica el comienzo de la sinterización o clinkerización, y tiene lugar a temperaturas comprendidas entre 1250 y 1300°C. Su proporción aumenta muy rápidamente en un pequeño intervalo de temperatura y después permanece prácticamente constante, oscilando entre el 20 % y el 25 % [90]. Con la formación de fase líquida, empieza la formación del silicato tricálcico (C3S), compuesto principal hidráulico del clínker de cemento Pórtland. Los procesos y reacciones que ocurren en presencia de fase fundida entre 1300°C y 1450°C son los siguientes: 1.- Formación física del clínker. Nodulización. 2.- Formación de la alita. Reacción de la cal libre, de la sílice que pueda quedar sin reaccionar y de la belita, para dar alita (silicato tricálcico). 5.6.. Nodulización.. La nodulización de clínker se refiere a los procesos de aglomeración física en el horno rotatorio y es deseable que el material caliente que sale del horno tenga una granulometría en la gama de tamaños de 2 a 20 mm con gránulos de una porosidad apropiada. Esta distribución de los granos de clínker por tamaño, es adecuada para el enfriamiento y resulta en una molturabilidad satisfactoria en el molino de cemento. Los problemas relacionados con la formación y la granulometría del clínker (distribución de tamaños) se deben a falta de cocción, pudiendo causar dificultades en la operación del horno y del enfriador, además de que el producto resultante puede resultar muy difícil de moler en el molino de cemento y en ese sentido sí puede tener una influencia en la calidad del cemento. La formación de los nódulos de clínker y costra en la zona de cocción de un horno de cemento, son procesos de aglomeración que vienen influidos por la fase fundida del clínker. Existen otros factores que tienen influencia en la aglomeración, por ejemplo la composición de dicha fase fundida y la uniformidad del material de alimentación al horno. El tamaño de las partículas es un parámetro crítico en la nodulización. Es mucho más difícil nodulizar las partículas grandes que las pequeñas. En cualquier proceso de nodulización, una alimentación uniforme, finamente molida, forma nódulos mayores y más resistentes. 5.7.. Formación de clínker.. La formación de clínker en los hornos rotatorios es un complejo de fenómenos de aglomeración y química de clínker. Los silicatos tricálcico y dicálcico (C3S y C2S) se encuentran como fases sólidas en la parte fundida. Al alcanzar la temperatura 18.
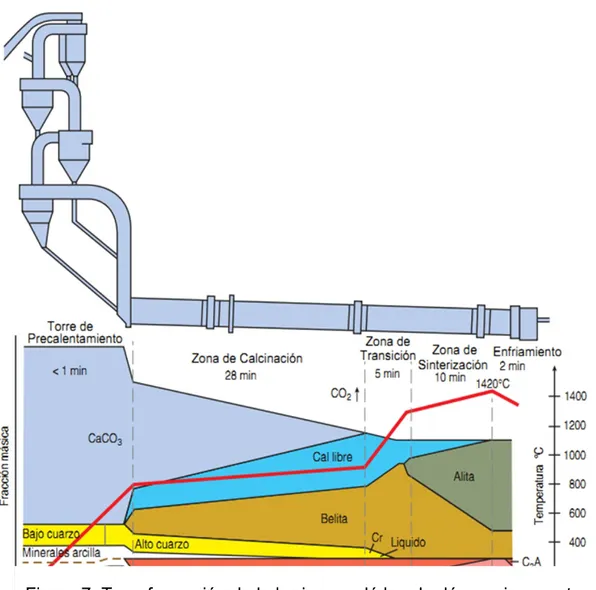
(38) Capítulo I. Introducción. de clinkerización de 1450ºC, la mayor parte de la alúmina, el óxido férrico y los compuestos secundarios se han convertido en fase líquida y los únicos sólidos presentes son el C3S, el C2S y, a menudo, un poco de CaO libre, periclasa y sulfatos alcalinos. En presencia de la fase líquida se disuelven los contornos de los granos de CaO y de C2S, facilitándose dentro de ella la difusión de los reactantes y formándose el silicato tricálcico (C3S). La cantidad de fase fundida se puede hacer variar mediante agentes fundentes o mineralizadores. Su formación a temperaturas más bajas contribuye a mejorar la nodulización del material en la zona de cocción, dando lugar a una mejora general de la marcha del horno. 5.8.. Cinética de la cocción de clínker.. Durante el proceso de formación del clínker tienen lugar reacciones entre las partículas finamente divididas de mezcla cruda. Las reacciones sólido-sólido se realizan en las superficies de los granos donde la difusión de reactivos del interior de las partículas a la superficie proceden muy lentamente. La etapa de progresión de la reacción depende de factores tales como la temperatura, el tiempo de reacción transcurrido, la velocidad de calentamiento, así como las propiedades químicas y físicas generales de los materiales de reacción. Las velocidades de las reacciones dependen en general del tamaño de las partículas, es decir de las superficies reactivas disponibles, por lo cual la finura de la mezcla cruda debe ser tal que en el proceso de cocción puedan reaccionar lo más completamente posible, incluso las partes más gruesas del mismo. La homogeneidad de una mezcla cruda es condición indispensable para obtener un clínker de composición uniforme y para conseguir una marcha regular del proceso de cocción. Los mineralizadores (por ejemplo el fluoruro cálcico, CaF2, espato flúor) pueden afectar favorablemente al proceso de cocción. El proceso final es llamado enfriamiento, en el cual el clínker pasa de la temperatura más alta a la temperatura ambiente, asimismo detiene el crecimiento de los cristales y solidifica la fase líquida para un transporte más fácil. La calidad del producto se determina por la química y la microestructura del clínker. La Figura 7 [91] es una representación de los cambios en los minerales que se producen durante los procesos de cocción y enfriamiento del clínker.. 19.
(39) Capítulo I. Introducción. Figura 7. Transformación de la harina en clínker. La línea roja muestra el perfil de temperatura. 6. Fases del clínker. El clínker de cemento Pórtland consta esencialmente de cuatro fases cristalinas: alita, belita, aluminato tricálcico y ferroaluminato [81], íntimamente asociadas entre sí. Contiene además una porosidad apropiada, cal libre (CaO sin combinar), así como periclasa (MgO) [92]. La Tabla 8, resume los datos más importantes de las fases del clínker.. 20.
(40) Capítulo I. Introducción. Tabla 8. Principales fases mineralógicas en el clínker Portland Fase Notación Composición Compuesto Fórmula Química Mineralógica Cementera Aproximada Silicato Alita C3S 45-70% 3CaOSiO2 tricálcico Silicato Belita C2S 10-35% 2CaOSiO2 dicálcico Aluminato Aluminato C3A 5-14% 3CaOAl2O3 Cálcico tricálcico Ferroaluminato Ferrita 5-15% 4CaOAl2O3Fe2O3 C4AF tetracálcico Óxido de Cal libre CaO C <2% calcio Óxido de Periclasa MgO M <5% magnesio. 6.1.. Alita.. Es el nombre que recibe el silicato tricálcico (C3S). Puede aceptar en su composición hasta un 2% de MgO y pequeñas cantidades de AI2O3, Fe2O3 y TiO2. Las cantidades de estos óxidos dependen de la composición del clínker, de la temperatura de cocción y del proceso de enfriamiento [63]. La alita presenta una morfología geométrica hexagonal y constituye la fase más importante en el clínker de cemento Pórtland [93], reacciona rápidamente con agua y es la fase que principalmente aporta al desarrollo de la resistencia temprana del cemento (generalmente en los primeros 28 días). Lo deseable es tener la mayor cantidad de C3S, aun a expensas de las otras fases. La alita se descompone por debajo de los 1275°C en C2S y CaO, siendo esta reacción lenta en su forma estable por lo que el C3S se puede presentar metaestablemente a temperatura ambiente por enfriamiento rápido [65].. 6.2.. Belita.. Es el nombre que recibe el silicato dicálcico (C2S) y la segunda fase más importante del clínker, ya que reacciona en forma similar a la alita. Puede presentarse en cuatro formas , ', y [94]. La forma no es hidráulica, la ’ da escasa resistencia mecánica, la se hidrata a una velocidad que es dependiente del tipo de estabilizador empleado y la es inerte. El silicato dicálcico β-C2S conforma principalmente esta fase. Reacciona lentamente con el agua y contribuye ligeramente a la resistencia temprana del cemento pero, con el paso del tiempo, es la fase que más aporte tiene sobre la resistencia a edades tardías del cemento [95], presenta una morfología geométrica esférica con dimensiones de 20 a 40 m [96] mostrando algunas estrías. El otro tipo de belita tiene una 21.
(41) Capítulo I. Introducción. forma irregular y muestra sólo un conjunto de estrías [81]. La alita y la belita son las fases responsables de las resistencias a la compresión que caracterizan al cemento Pórtland.. 6.3.. Alumínato tricálcico.. Conocido como Celita [97]. Dado que su formación es a partir de la fase líquida, todos los iones presentes en el líquido (en general Na y K así como Mg, S, Ti, Mn en cantidades de hasta 5%) pueden quedar atrapados en este mineral. En la producción de clínker se ha encontrado que la estructura del aluminato es ortorrómbica o cúbica ó, una combinación de ambas [81]. La fase del aluminato posee una capacidad de reacción muy alta, la cual se incrementa por la inclusión de álcalis. A fin de “frenar” la reacción de la fase aluminato al comienzo de la hidratación, es preciso añadir al cemento algún sulfato (yeso), para retardar el proceso del fraguado. Junto con la alita y la belita, la fase aluminato puede contribuir a aumentar ligeramente la resistencia del cemento a corto plazo (a causa de su elevado calor de hidratación), no obstante sus propiedades hidráulicas son escasas. 6.4.. Ferrita.. La ferrita (C4AF) no posee una composición química constante [98], forma parte de una serie de soluciones sólidas que teóricamente se extienden desde el C2A hasta el C2F; al igual que el aluminato, contiene iones extraños y es la responsable de dar el color verde grisáceo obscuro característico del clínker. La fase ferrítica reacciona muy lentamente y carece de importancia significativa directa a efectos de las propiedades del cemento. También se le conoce con el nombre brownmillerita en la química del cemento [81]. Es responsable de la reducción en la temperatura de clinkerización del cemento en el proceso de producción. 6.5.. Otras fases del clínker.. La mayor parte de los clínkeres contienen cal libre (cal no combinada), MgO libre (periclasa), y en raros casos se pueden encontrar pequeñas cantidades sulfatos alcalinos y fase vítrea. La cal libre (CaO) es el excedente de óxido de calcio que no se combina con los demás óxidos, es debida a una inadecuada preparación del crudo (demasiado grueso o inhomogéneo), a una cocción insuficiente (tal que no permite su combinación con otros óxidos), a un enfriamiento lento (que posibilita la descomposición del C3S y del C3A), o un contenido demasiado alto de cal [63]. Por lo general se utiliza como parámetro de control para inferir el grado de reacción obtenido en el proceso de clinkerizado. Industrialmente se busca que el contenido de esta fase sea menor a 2 %, porque en cantidades mayores pueden causar un aumento de volumen en el producto final al hidratarse. 22.
Figure


![Tabla 2. Composición química del cemento Pórtland [67-71].](https://thumb-us.123doks.com/thumbv2/123dok_es/7438775.394128/28.918.120.655.568.821/tabla-composición-química-del-cemento-pórtland.webp)
![Figura 4. Proceso de fabricación del cemento. Adaptado de [76]. 11 4.6. Producción de clínker en horno rotatorio](https://thumb-us.123doks.com/thumbv2/123dok_es/7438775.394128/30.918.129.785.685.1061/figura-proceso-fabricación-cemento-adaptado-producción-clínker-rotatorio.webp)
+7
Outline
Documento similar