“DEPÓSITO DE PELÍCULAS DELGADAS DE Cu2SnS3 POR EL MÉTODO SILAR PARA SU APLICACIÓN COMO ABSORBEDOR EN CELDAS SOLARES”
Texto completo
(2) Centro de Investigación en Materiales Avanzados Departamento de Estudios de Posgrado Unidad Monterrey. “DEPÓSITO DE PELÍCULAS DELGADAS DE Cu 2SnS3 POR EL MÉTODO SILAR PARA SU APLICACIÓN COMO ABSORBEDOR EN CELDAS SOLARES”. Aprobación de la Tesis.
(3) ÍNDICE GENERAL Contenido CAPÍTULO 1 INTRODUCCIÓN ............................................................................................................... 2 1.1 Energía Fotovoltaica ................................................................................................ 2 1.2 Celdas Solares ......................................................................................................... 3 1.3 Propiedades de Cu2SnS3 ......................................................................................... 5 1.4 Adsorción y reacción sucesiva de capas iónicas (SILAR) ...................................... 6 CAPÍTULO 2 ANTECEDENTES............................................................................................................ 11 2.1 Antecedentes de películas delgadas de CuS ........................................................ 11 2.2 Antecedentes de películas delgadas de SnS ........................................................ 12 2.3 Antecedente de películas delgadas de Cu2SnS3................................................... 13 2.4 Análisis crítico de literatura y aporte científico ...................................................... 15 2.5 Justificación ............................................................................................................ 16 2.6 Hipótesis ................................................................................................................. 16 2.7 Objetivos ................................................................................................................. 16 2.7.1 Objetivo General .............................................................................................. 16 2.7.2 Objetivos Específicos ...................................................................................... 16 CAPÍTULO 3 MATERIALES Y MÉTODOS........................................................................................... 19 3.1 Películas Delgadas de CdS ................................................................................... 19 3.1.1 Reactivos Químicos ......................................................................................... 19 3.1.2 Limpieza de sustratos ...................................................................................... 19 3.1.3 Depósito de películas delgadas de CdS por baño químico ............................ 19 3.2 Películas Delgadas de CuS ................................................................................... 20 3.2.1 Reactivos Químicos ......................................................................................... 20 3.2. 2 Sustratos ......................................................................................................... 20 3.2.3 Depósito de películas delgadas de CuS por SILAR ....................................... 21 3.3 Películas Delgadas de SnS.................................................................................... 21 3.3.1 Reactivos Químicos ......................................................................................... 21 3.3.2 Sustratos .......................................................................................................... 22 3.3.3 Depósito de películas delgadas de SnS por SILAR ....................................... 22 3.4 Películas Delgadas de Cu2SnS3 ............................................................................ 22.
(4) 3.4.1 Depósito de multicapas de películas delgadas de SnS-CuS ......................... 23 3.4.2 Depósito de películas alternadas ciclo x ciclo de SnS-CuS ........................... 23 3.5 Tratamiento Térmico .............................................................................................. 23 CAPÍTULO 4 DISCUSIÓN DE RESULTADOS ..................................................................................... 26 Películas delgadas de CdS 4.1 Propiedades Ópticas .............................................................................................. 26 4.2 Propiedades Estructurales ..................................................................................... 27 4.3 Propiedades Químicas ........................................................................................... 28 CAPÍTULO 5 DISCUSIÓN DE RESULTADOS ..................................................................................... 36 Compuestos Binarios 5.1 Películas delgadas de SnS .................................................................................... 36 5.1.1 Estudio del efecto del número de ciclos de depósito en etapas iniciales de crecimiento ................................................................................................................ 36 5.1.1a Propiedades Ópticas.................................................................................. 36 5.1.1b Propiedades Químicas............................................................................... 39 5.1.1c Propiedades Estructurales ......................................................................... 43 5.1.2 Estudio del efecto de la temperatura del tratamiento térmico ........................ 44 5.1.2a Propiedades Ópticas.................................................................................. 44 5.1.2b Propiedades Estructurales......................................................................... 45 5.1.2c Propiedades Químicas ............................................................................... 49 5.2 Películas delgadas de CuS .................................................................................... 53 5.2.1 Estudio del efecto del número de ciclos de depósito en etapas iniciales de crecimiento ................................................................................................................ 53 5.2.1a Propiedades Ópticas.................................................................................. 53 5.2.1b Propiedades Químicas............................................................................... 55 5.2.1c Propiedades Estructurales ......................................................................... 60 5.2.2 Estudio del efecto de la temperatura del tratamiento térmico ........................ 61 5.2.2a Propiedades Ópticas.................................................................................. 62 5.2.2b Propiedades Estructurales......................................................................... 63 5.2.2c Propiedades Químicas ............................................................................... 65 CAPÍTULO 6 DISCUSIÓN DE RESULTADOS ..................................................................................... 72 Compuestos Ternarios.
(5) 6.1 Depósito de multicapas SnS/CuS.......................................................................... 72 6.1.1 Propiedades Estructurales .............................................................................. 72 6.1.2 Propiedades Ópticas ....................................................................................... 78 6.1.3 Propiedades Químicas .................................................................................... 78 6.1.3 Propiedades Eléctricas .................................................................................... 84 6.2 Depósito de películas alternadas ciclo por ciclo de SnS y CuS............................ 85 6.2.3 Propiedades estructurales ............................................................................... 86 6.2.2 Propiedades Ópticas ....................................................................................... 88 6.2.3 Propiedades Químicas .................................................................................... 89 CAPÍTULO 7 CONCLUSIONES ............................................................................................................ 93 7.1 Películas delgadas de CuS .................................................................................... 93 7.2 Películas delgadas de SnS .................................................................................... 93 7.3 Películas delgadas de Cu2SnS3 ............................................................................. 94 CAPÍTULO 8 REFERENCIAS................................................................................................................ 96.
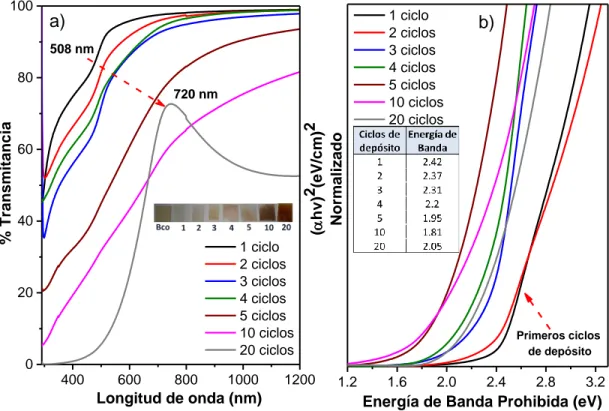
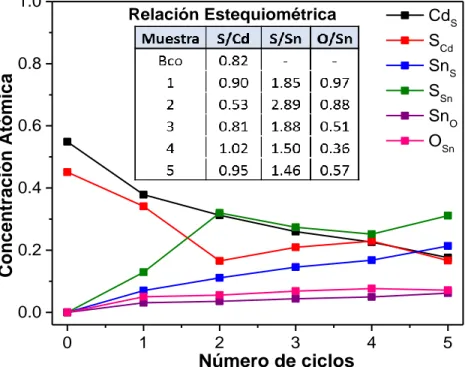
(6) ÍNDICE DE FIGURAS Figura 1.1 Mapa de irradiación solar global (W/m 2) al año [4]. ........................................ 3 Figura 1.2 Mapa de irradiación solar global (W/m2) al año. ............................................ 4 Figura 1.3 Estructura cristalina de Cu2SnS3: (a) Monoclínica y b) Cúbica [11] . ................ 6 Figura 1.4 Proceso esquematizado de las etapas en la formación de Cu2SnS3. ............ 9 Figura 3.1 Depósito por baño químico películas delgadas de CdS. ............................. 20 Figura 3.2 Depósito por SILAR de películas delgadas de CuS. .................................... 21 Figura 3.3 Depósito por SILAR de películas delgadas de SnS...................................... 22 Figura 3.4 Depósito por SILAR de estructura multicapa CdS/SnS/CuS........................ 23 Figura 3.5 Depósito por SILAR de estructura alternada SnS/CuS. ............................... 23 Figura 3.6 Tratamiento térmico de películas delgadas en N2 grado 5.0. ....................... 24 Figura 4.1 Espectros de transmitancia y valores de energía de banda prohibida para películas de CdS depositadas a diferente tiempo de depósito. ...................................... 26 Figura 4.2 Morfología superficial de películas de CdS depositadas a 1 (a), 3 (b), 6 (c) y 10 minutos (d). ................................................................................................................. 27 Figura 4.3 Topografías obtenidas de AFM de películas de CdS depositadas a 1 (a), 3 (b), 6 (c) y 10 minutos (d)................................................................................................. 28 Figura 4.4 Espectros de XPS de C1s de películas delgadas de CdS depositadas a 1, 3, 6 y 10 minutos. ................................................................................................................. 29 Figura 4.5 Espectros de XPS de Cd3d (a) y S2p (b) de películas delgadas de CdS depositadas a 1, 3, 6 y 10 minutos. ................................................................................. 30 Figura 4.6 Relación estequiométrica de películas delgadas de CdS depositadas a 1, 3, 6 y 10 minutos. ................................................................................................................. 31 Figura 4.7 a) Espectro de XPS de Si 2p y b) Relación estequiométrica Cd/Si y S/Si para películas de CdS depositadas a 1, 3, 6 y 10 minutos. .................................................... 32 Figura 4.8 Espesores determinados por XPS para películas de CdS depositadas a 1, 3, 6 y 10 minutos. ................................................................................................................. 33 Figura 5.1 Espectros de transmitancia y valores de energía de banda prohibida para películas de SnS depositadas a diferente número de ciclos. ......................................... 37 Figura 5.2 Espectros de transmitancia y valores de energía de banda prohibida para películas de SnS depositadas a diferente número de ciclos. ......................................... 38 Figura 5.3 Espectros de XPS de Cd3d y Sn3d de películas delgadas de SnS depositadas a diferente número de ciclos............................................................................................ 40 Figura 5.4 Espectros de XPS de S2p y O1s de películas delgadas de SnS depositadas a diferente número de ciclos............................................................................................ 41 Figura 5.5 Concentración atómica y relación estequiométrica obtenidas por XPS de películas delgadas de SnS depositadas a diferente número de ciclos........................... 42.
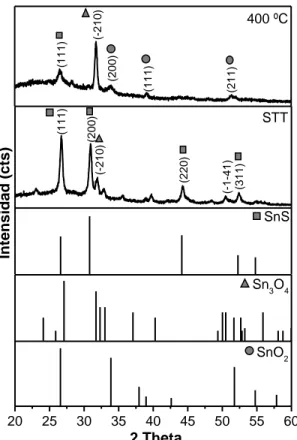
(7) Figura 5.6 Morfología de películas de SnS depositadas a distinto número de ciclos, a) 1 ciclo, b) 5 ciclos, c) 10 ciclos y d) 20 ciclos. ................................................................. 44 Figura 5.7 Espectros de transmitancia y valores de energía de banda prohibida para películas de SnS tratadas térmicamente a distinta temperatura. ................................... 45 Figura 5.8 Patrón de difracción de rayos x de películas de SnS tratadas térmicamente a distinta temperatura. ........................................................................................................ 47 Figura 5.9 Patrón de difracción de rayos x de películas de SnS tratadas térmicamente a distinta temperatura. ........................................................................................................ 48 Figura 5.10 Morfología de películas de SnS. a) Película sin y b) con tratamiento térmico con 20 ciclos de depósito................................................................................................. 49 Figura 5.11 Espectros de XPS de Cd3d y Sn3d de películas delgadas de SnS tratadas térmicamente a distinta temperatura. .............................................................................. 50 Figura 5.12 Espectros de XPS de S2p y O1s de películas delgadas de SnS tratadas térmicamente a distinta temperatura. .............................................................................. 51 Figura 5.13 Concentración atómica y relación estequiométrica obtenidas por XPS de películas delgadas de SnS tratadas térmicamente a distinta temperatura. ................... 52 Figura 5.14 Parámetro Auger para películas de SnS con 20 ciclos de depósito. ......... 53 Figura 5.15 Espectros de transmitancia y valores de energía de banda prohibida para películas de SnS depositadas a diferente número de ciclos. ......................................... 54 Figura 5.16 Espectros de transmitancia y valores de energía de banda prohibida para películas de SnS depositadas a diferente número de ciclos. ......................................... 55 Figura 5.17 Espectros de XPS de Cd3d y Cu2p de películas delgadas de CuS depositadas a diferente número de ciclos. ...................................................................... 56 Figura 5.18 Espectros de XPS para la región del Cu2p3/2 para películas de CuS con distinto número de ciclos de depósito. ............................................................................ 57 Figura 5.19 Espectros de XPS de Cu2p3/2 y S2p de películas delgadas de CuS depositadas a diferente número de ciclos. ...................................................................... 58 Figura 5.20 Concentración atómica y relación estequiométrica obtenida por XPS de películas delgadas de CuS depositadas a diferente número de ciclos. ......................... 59 Figura 5.21 Morfología de películas de CuS depositadas a distinto número de ciclos. a) 1 ciclo, b) 5 ciclos, c) 10 ciclos y d) 20 ciclos. ................................................................. 61 Figura 5.22 Espectros de transmitancia y valores de energía de banda prohibida para películas de SnS tratadas térmicamente a distinta temperatura. ................................... 62 Figura 5.23 Patrón de difracción de rayos X de películas de CuS tratadas térmicamente a distinta temperatura. ..................................................................................................... 63 Figura 5.24 Patrón de difracción de rayos X de películas de CuS tratadas térmicamente a distinta temperatura. ..................................................................................................... 65 Figura 5.25 Espectros de XPS de Cd3d y Cu2p de películas delgadas de CuS depositadas a diferente número de ciclos. ...................................................................... 66 Figura 5.26 Espectros de XPS para la región del Cu2p3/2 para películas de CuS con distinto número de ciclos de depósito. ............................................................................ 67.
(8) Figura 5.27 Pico Auger Cu LMM correspondiente para películas tratadas térmicamente. .......................................................................................................................................... 68 Figura 5.28 Espectros de XPS para la región del S2p para películas de CuS tratadas térmicamente a distinta temperatura. .............................................................................. 69 Figura 5.29 Parámetro Auger para películas de CuS con 20 ciclos de depósito tratadas térmicamente a distinta temperatura. .............................................................................. 70 Figura 6.1 Patrón de XRD de multicapas a distinta relación SnS/CuS.......................... 72 Figura 6.2 Patrón de difracción de película multicapa a distinta relación SnS/CuS con tratamiento térmico a 400 °C. .......................................................................................... 74 Figura 6.3 Patrón de difracción de película multicapa a distinta relación SnS/CuS con tratamiento térmico a 400 °C. .......................................................................................... 75 Figura 6.4 Patrón de difracción de película multicapa a distinta relación SnS/CuS con tratamiento térmico a 400 °C. .......................................................................................... 76 Figura 6.5 Espesores y potencial zeta en superficie de multicapas de SnS/CuS a distinta relación de ciclos de depósito.......................................................................................... 77 Figura 6.6 Espectros de transmitancia y coeficientes de absorción de multicapas de SnS-CuS a diferente relación en número de ciclos de depósito..................................... 84 Figura 6.7 Espectros de XPS para las regiones Cd3d, Cu2p, S2p y Sn3d para multicapas de SnS-CuS. .................................................................................................................... 79 Figura 6.8 Deconvoluciones para los espectros de XPS para las regiones Cd3d, Cu2p, S2p y Sn3d para multicapas de SnS-CuS....................................................................... 81 Figura 6.9 Concentración atómica para las multicapas de SnS-CuS............................ 82 Figura 6.10 Valores de movilidad, concentración de portadores y resistividad eléctrica multicapas de SnS-CuS tratadas térmicamente. ............................................................ 85 Figura 6.11 Figura 6.11 Patrón de difracción de películas alternadas ciclo x ciclo de SnS y CuS. ............................................................................................................................... 86 Figura 6.12 Patrón de XRD de monocapas alternadas de SnS-CuS a distinta temperatura de tratamiento térmico................................................................................. 87 Figura 6.13 Patrón de XRD de monocapas alternadas de SnS-CuS a distinta concentración de iones Cu y Sn. ..................................................................................... 88 Figura 6.14 Micrografías de monocapas alternadas de SnS-CuS a distinta concentración de iones ............................................................................................................................ 88 Figura 6.15 Espectros de transmitancia y valores de energía de banda prohibida para películas de SnS depositadas a diferente número de ciclos. ......................................... 89 Figura 6.16 Deconvoluciones para los espectros de XPS para las regiones Cd3d, Cu2p, S2p y Sn3d para películas alternadas ciclo x ciclo de SnS-CuS.................................... 90.
(9) RESUMEN En la actualidad, el alto costo y la baja eficiencia de conversión de las celdas solares, han propiciado la búsqueda de nuevos materiales fotovoltaicos con propiedades avanzadas para su utilización como capa absorbedora en dichos dispositivos. Los compuestos ternarios basados en Cu, Sn y S son materiales alternativos que cumplen con este requisito, debido a que presentan propiedades ópticas, morfológicas y eléctricas apropiadas para este fin. Además son económicos, abundantes en la naturaleza y no tóxicos, por lo que son materiales prometedores para el reemplazo de CIGS [Cu(In,Ga)Se 2] en celdas solares. En el presente trabajo se estudió la formación de películas delgadas CuS y SnS para la posterior obtención del compuesto ternario Cu2SnS3 a partir del método de adsorción y reacción sucesiva de capas iónicas (SILAR, por sus siglas en inglés). Las películas delgadas de Cu2SnS3 se obtuvieron mediante el depósito de monocapas alternadas de (SnS/CuS)n y multicapas de (SnS)n/(CuS)m. Estas dos metodologías se propusieron con la finalidad de estudiar los procesos de difusión y estabilidad química en dicho compuesto. Mediante difracción de rayos X se determinó que las multicapas sin tratamiento térmico presentan un crecimiento cristalino hexagonal correspondiente a la fase de CuS. No obstante, después de un tratamiento térmico a 400 °C, aparecen picos de difracción adicionales demostrando la presencia de la fase cúbica perteneciente a Cu2SnS3 y una segunda fase contaminante con estructura tetragonal atribuida al SnO2. Las composiciones elementales, estados de oxidación y reacciones químicas se estudiaron por espectroscopia de fotoemisión de rayos X (XPS, por sus siglas en inglés). Los resultados de XPS para las multicapas revelaron la presencia de CuS para las películas sin tratamiento térmico, mientras que para aquellas tratadas térmicamente a 400 °C en atmósfera de N2 se presenció Cu1+ y Sn4+. Además, XPS reveló la presencia de Cd en la superficie de las estructuras con monocapas alternadas, mientras que las multicapas SnS/CuS mostraron menor cantidad de Cd. Las propiedades eléctricas se determinaron a partir de mediciones de efecto Hall, encontrando que la movilidad y la resistividad de las películas se encuentran entre valores de 0.1- 0.6 cm2/Vs y 0.003-0.923 Ωcm, respectivamente. La densidad de portadores de las películas se encuentra en el orden de 10 21 cm-3. La alta densidad de portadores y baja movilidad está relacionada con defectos estructurales. Estas películas presentan un carácter semiconductor tipo p, lo cual es ideal para la utilización de este material como absorbedor en celdas solares..
(10) Capítulo 1 INTRODUCCIÓN.
(11) Capítulo 1. Introducción. CAPÍTULO 1 INTRODUCCIÓN 1.1 Energía Fotovoltaica En la actualidad, el alto consumo de energía y el rápido agotamiento de las fuentes convencionales disponibles para su generación, especialmente los combustibles fósiles pronostican un inminente estancamiento en el progreso de la humanidad. Además, el dióxido de carbono producido por la quema de combustibles está considerado como uno de los contaminantes críticos que causan el calentamiento global y el efecto invernadero. Si bien ya existen fuentes alternativas de energía, hay ventajas y desventajas en el uso de muchas de éstas. Por ejemplo, la energía nuclear es una alternativa poderosa y fuente de energía a largo plazo, sin embargo, los materiales radiactivos de las centrales nucleares son inestables, extremadamente peligrosos y la eliminación de los residuos nucleares después de la generación de energía es un problema ambiental complicado [1,2]. Es por ello que desde hace décadas se han explorado otras fuentes de energía renovables que se generen a partir de los recursos naturales como la luz solar, el viento, el agua, convirtiéndolas en fuentes de energías alternativas limpias con prospectiva para el futuro. La energía solar es una fuente de energía renovable potencial debido a que puede ser aprovechada en todo el planeta, amigable con el ambiente, benigna, permanente, limpia, además de ser el modo más accesible de proveer energía a los miles de millones de personas sin electricidad en el mundo. El Sol posee una densidad de energía promedio sobre la atmósfera terrestre de 1367 W/m2, sin embargo, después de atravesar la atmósfera este valor disminuye a 1000 W/m2 debido a distintos procesos de absorción, reflexión, difusión, etc. La insolación media de la Tierra es de aproximadamente 250 W/m 2 (6 (kW·h/m2) /día). La superficie de la Tierra recibe en 30 minutos una cantidad. 2.
(12) Capítulo 1. Introducción. de energía solar equivalente al consumo energético mundial en un año. En la figura 1.1 se muestra la distribución promedio de la energía solar que incide en la Tierra. La mayor parte de la Tierra posee niveles altos de radiación solar, sobre todo en las regiones cercanas al ecuador. Por su parte, México se encuentra dentro de la región en la cual hay más radiación solar durante todo el año. [3,4].. Figura 1. 1 Mapa de irradiación solar global (W/m 2) al año [4] .. 1.2 Celdas Solares Las celdas solares son dispositivos que producen energía eléctrica al incidir luz sobre su superficie. La fuente de luz utilizada generalmente es el sol. Una celda solar se forma mediante la unión de dos materiales semiconductores con diferentes portadores de carga: uno con alta concentración de electrones (tipo-n) y otro con alta concentración de huecos (tipo-p). Cuando se unen estos dos semiconductores n y p se produce una unión p-n, donde los electrones que se encuentran. en exceso en el semiconductor tipo n migran hacia el. semiconductor tipo p y los huecos del semiconductor tipo p hacia el semiconductor tipo n. De esta manera se establece un campo eléctrico en la interfase. La celda se completa con contactos óhmicos en las capas p y n. [5].. La figura 1.2 ilustra la operación básica de una celda solar. Los fotones son absorbidos por el semiconductor y en el proceso se generan pares electrónhueco tanto en el semiconductor tipo p como n. Los electrones y huecos difunden. 3.
(13) Capítulo 1. Introducción. a través del semiconductor a la unión p-n, en donde el campo eléctrico existente se encarga de desplazarlos a la región donde estos electrones y huecos son portadores de carga mayoritarios, la región p se carga positivamente mientras la n negativamente, dando lugar a una fuerza electromotriz y un circuito exterior acoplado a una corriente. [6].. Figura 1. 2 Esquema y diagrama de bandas de una celda solar.. Las capas semiconductoras deben ser preferentemente gruesas para absorber la mayoría de la radiación incidente y deben ser capaces de transportar los electrones y huecos a los electrodos antes de que éstos se recombinen. Un material se considera adecuado para usarse como capa absorbedora en dispositivos fotovoltaicos si cumple con las siguientes propiedades [2]: Energía de banda prohibida directa Alto coeficiente de absorción Pocos e inactivos límites de grano Buena movilidad Los avances tecnológicos más recientes están orientados a reducir los costos de fabricación de las celdas solares mediante el uso de distintos materiales, estructuras y procesos. Algunos materiales como las calcopiritas y CdTe ofrecen soluciones atractivas así como procesos de baja temperatura y aplicables a áreas grandes. Cu(In,Ga)Se2 (CIGS) ha sido anticipado como uno de los materiales más promisorios para el desarrollo de celdas solares de películas delgadas. Actualmente la eficiencia de las celdas solares basadas en CIGS han alcanzado 4.
(14) Capítulo 1. Introducción. un porcentaje de conversión energética de 20.4%. [7,8,9].. Sin embargo, la. producción masiva está limitada por la disponibilidad y abundancia de los metales raros indio y galio. Durante la última década se han investigado nuevos materiales absorbedores que sean económicos, no tóxicos y abundantes en la naturaleza. Actualmente,. el compuesto. cuaternario. Cu2ZnSnS4. (CZTS) ha sido. ampliamente estudiado como un material alternativo para celdas solares debido a su similitud en las propiedades con CIGS. Este compuesto presenta un coeficiente de absorción alto (> 104 cm-1) y una energía de banda deseable de 1.45 eV. Algunos cálculos teóricos han mostrado conversiones energéticas altas hasta de 32% utilizando espesores de hasta un par de micrómetros. Esta tecnología es más económica a las ya existentes tales como las celdas fabricadas por CdTe, silicio y CIGS. Una familia de este compuesto son los materiales obtenidos a partir de compuestos ternarios basados en cobre, estaño y azufre (CTS).. 1.3 Propiedades de Cu2SnS3 Los semiconductores ternarios basados en cobre, estaño y azufre (CTS) son candidatos potenciales para su uso como materiales absorbedores en celdas solares, ya que presentan un coeficiente de absorción alto (10 4 cm-1). En literatura,. se. pueden. encontrar. distintos. compuestos. con. diversas. estequiometrias, tales como Cu4SnS4, Cu2SnS3, Cu4Sn7S16, CuSn3.75S8 y Cu3SnS4. Los primeros dos, son los que destacan en esta lista por su baja energía de banda prohibida [10]. Aunque el estudio experimental de los compuestos ternarios CTS es ampliamente estudiado, sus propiedades fundamentales, como la estructura cristalina y la energía de banda prohibida siguen siendo objeto de debate. Existen diversas fases reportadas por varios grupos de investigación para el caso del compuesto ternario Cu2SnS3 como aquellas estructuras monoclínica, cúbica, tetragonal. y. hexagonal. respectivamente (figura 1.3). con. simetrías. Cc, F43m,. I42m. y. P63/mmc,. [11].. 5.
(15) Capítulo 1. Introducción. En contraste con el silicio, donde átomos de fósforo o boro son introducidos intencionalmente. para producir semiconductores tipo n o p,. respectivamente, el compuesto CTS se impurifica por sí mismo a través de la formación de defectos intrínsecos incluyendo vacancias (VCu, VSn, y VS), antisitios (CuSn, SnCu) e intersticios (Cui, Zni, and Sni). Algunos autores señalan que la energía de formación para los defectos aceptores es menor que para aquellos defectos aceptores, por tanto, lo convierte en un compuesto difícil de impurificar tipo n. Este material presenta un alto coeficiente de absorción >10 5cm-1, una energía de banda prohibida de 0.96-1.5 eV, densidad de 4.7 g /cm3 y una masa molar de 341.9 g /mol [12].. Figura 1. 3 Estructura cristalina de Cu2SnS3: (a) Monoclínica y b) Cúbica [11] .. 1.4 Adsorción y reacción sucesiva de capas iónicas (SILAR) Para la obtención de películas delgadas de compuestos binarios y ternarios existen diferentes métodos de depósito, tales como, evaporación térmica. [13],. sol-gel. soluciones acuosas. [14], [17].. rocío pirolítico. [15,16]. y aquellos métodos basados en. Este último tipo de técnicas se caracterizan por ser. sencillas, económicas, se pueden aplicar sobre área grande y utilizan baja temperatura.. 6.
(16) Capítulo 1. Introducción. El método basado en soluciones acuosas más utilizado para el crecimiento de películas es el depósito por baño químico. En este método, las películas son crecidas en una mezcla de reacción conteniendo simultáneamente todos los precursores necesarios para el depósito. Uno de los métodos nuevos en fase líquida para el depósito de compuestos ternarios es el método SILAR, el cual es una versión modificada del depósito por baño químico. En la técnica SILAR el crecimiento de las películas ocurre secuencialmente. Las soluciones precursoras son colocadas en distintos vasos de reacción y el sustrato es sumergido en la solución catiónica precursora y posteriormente en la solución aniónica precursora. Entre cada una de las inmersiones catiónicas y aniónicas, el sustrato es enjuagado con agua. A través de la repetición de estos ciclos, las películas delgadas son formadas capa por capa [18]. El proceso SILAR fue descrito por primera vez por Nicolau en 1985, desde entonces este ha sido utilizado comúnmente para crecer películas delgadas de materiales basados en óxidos y calcogenuros. Entre algunas de las ventajas que se encuentran al utilizar este método son: a) Es un método económico, simple y conveniente para el depósito en áreas grandes. b) La velocidad de depósito y el espesor pueden ser controlados en un rango amplio, variando el número de ciclos de inmersión. c) Se puede introducir cualquier agente. impurificante, en cualquier. proporción, simplemente adicionándolo a la solución catiónica. d) Se obtienen películas de buena calidad a temperatura ambiente y presión atmosférica. e) No se requiere niveles de alto vacío para producir películas de buena homogeneidad y calidad. f) Se pueden emplear cualquier tipo de sustrato.. 7.
(17) Capítulo 1. Introducción. Por otra parte, esta técnica también cuenta con algunas desventajas entre las que destacan su lento crecimiento y la alta probabilidad de contaminación con oxígeno debido a las condiciones de depósito en medio acuoso. Aunado a esto, se destaca la estabilidad de los sustratos (Si, CdS, ITO), ya que la mayoría son estables a pH alto convirtiendo en un inconveniente para depositar en distintos rangos de pH utilizando esta técnica. El crecimiento de una película a través de la técnica SILAR se efectúa a partir de la inmersión del sustrato en soluciones precursoras catiónicas y aniónicas, con un enjuague intermediario del sustrato. Un ciclo en el proceso SILAR está conformado por los siguientes cuatro pasos (figura 1.4). [17]:. 1) La inmersión del sustrato en la solución catiónica precursora, es decir, una solución acuosa de una sal soluble del catión del compuesto a ser crecido. Durante este paso, los cationes son adsorbidos en la superficie del sustrato. La hidrólisis de los iones metálicos mejora la adsorción. Para promover la hidrólisis e incrementar la carga negativa de las superficies oxidadas, el pH es incrementado justo por debajo del punto de pH para la precipitación. 2) El sustrato es enjuagado en agua desionizada. Debido a la presencia de cationes adsorbidos en la superficie, una doble capa es formada, los cationes adsorbidos se encuentran en la capa interior y sus contra iones en la capa externa. Durante el proceso de enjuague, los cationes excedentes, los cuales no se encuentran adsorbidos, son removidos junto con otros iones que se encuentran en la capa de difusión. 3) El sustrato es ahora sumergido en la solución precursora aniónica, es decir, una solución acuosa de la sal del anión del compuesto deseado a ser crecido. Los aniones reaccionan con los cationes adsorbidos y forman el compuesto sólido deseado. 4) El sustrato es finalmente enjuagado otra vez en agua desionizada y los iones que se encuentran en exceso en la capa de difusión son removidos.. 8.
(18) Capítulo 1. Introducción. Figura 1. 4 Proceso esquematizado de las etapas en la formación de Cu2SnS3.. 9.
(19) Capítulo 2 ANTECEDENTES.
(20) Capítulo 2. Antecedentes. CAPÍTULO 2 ANTECEDENTES En este capítulo se presentan los principales antecedentes que sirvieron de base para el planteamiento de los objetivos y desarrollo del presente proyecto.. 2.1 Antecedentes de películas delgadas de CuS En el 2000, S. Lindroos y colaboradores depositaron películas delgadas de CuS sobre películas de CdS mediante el método SILAR. Ellos utilizaron soluciones altamente diluidas como lo son Cu(CH3COO2) 0.0125M y Na2S 0.00625M, respectivamente. Los tiempos de inmersión utilizados en la etapa de adsorción y reacción fueron de 10 s, mientras que el tiempo de enjuague fue de 75 s. Estos depósitos se realizaron en una cámara con atmósfera de N 2 a temperatura ambiente y presión atmosférica. Las películas de CuS depositadas son altamente rugosas comparadas con las películas de CdS, además de ser policristalinas y no presentar un crecimiento con una orientación preferencial. Ellos determinaron la posible redisolución de la película de CdS después de 100 ciclos de depósito continuos. [19].. En el mismo año, Sartale y Lokhande depositaron películas de CuS en vidrio y Si (111) a través del método SILAR. La solución catiónica precursora fue CuSO4 0.1M, ajustada a un de pH de 10 con amoniaco, mientras que la solución aniónica precursora fue NH2CSNH2 0.1M a pH de 6. Los tiempos de inmersión en la etapa de adsorción y reacción fueron de 20s, mientras que el tiempo de enjuague fue de 30s. El total de número de ciclos fue de 25 obteniendo espesores del orden de 400 nm. Mediante difracción de rayos x presenciaron que las películas depositadas en vidrio carecen de un crecimiento cristalino, mientras que cuando son depositadas en Si (111) la fase de Cux S, donde x toma valores de 1.83-1.96, predomina cristalizando en una estructura hexagonal. La energía de banda prohibida encontrada fue de 2.36 eV. Las películas presentaron un carácter semiconductor tipo p y una resistividad de 10 2 Ωcm [20]. 11.
(21) Capítulo 2. Antecedentes. En el 2009, M. Ali Yildirim y colaboradores depositaron películas de CuS en vidrio por el método SILAR. Las soluciones precursoras utilizadas fueron CuCl2 0.1M (pH 3) y Na2S 0.05 M (pH 12). Los tiempos de inmersión en las etapas de adsorción y reacción fueron de 30s y el tiempo de enjuague fue de 50s. El número total de ciclos de depósito fue de 40, obteniendo espesores de 150 nm. Las películas se trataron térmicamente a 200, 300 y 400 ºC por 3 minutos bajo atmósfera de nitrógeno. Las películas de CuS presentaron buena homogeneidad y uniformidad, cristalizando en la fase covalita perteneciente a la estructura hexagonal del CuS. La energía de banda prohibida fue de 2.03 eV. Ellos determinaron que la fotosensibilidad temperatura del tratamiento térmico. disminuye con el incremento de la. [21].. 2.2 Antecedentes de películas delgadas de SnS En el 2008, Biswajit Ghosh y colaboradores depositaron películas de SnS en vidrio e ITO con espesores de 200 nm a través del método SILAR. Ellos utilizaron SnSO4 0.1M el cual fue disuelto en H2SO4 (pH 1.8) y Na2S 0.1M (pH 12.5). Los tiempos de inmersión en las etapas de adsorción fueron de 25s, reacción fue de 15s y el tiempo de enjuague fue de 25s. La energía de banda prohibida directa evaluada fue de 1.43 eV. Las películas presentan una fase predominante a la hergenbergita, la cual pertenece al SnS [22]. Chao Gao y colaboradores obtuvieron películas de SnS mediante la modificación del método SILAR, adicionando una cierta cantidad de NH 4Cl a la solución catiónica precursora.. Las películas presentaron una nueva estructura. cristalina designada como zinc blenda. Las películas de SnS son ligeramente ricas en Sn, además de la presencia contaminante de pequeñas cantidades de oxígeno. La conductividad de las películas en la oscuridad fue de 10-6 S/cm. Las películas policristalinas presentaron una energía de banda prohibida directa de 1.71 eV [23]. Biswajit Ghosh y colaboradores en el 2011, realizaron estructuras basadas en CdS/SnS utilizando el método SILAR. Este depósito se basó en su trabajo 12.
(22) Capítulo 2. Antecedentes. antes expuesto, solamente que en esta ocasión se realizó en películas de CdS. Las películas se sometieron a un tratamiento térmico a 250 °C por 2 h en vacío. Después de 300 ciclos el espesor de SnS fue de 525 nm. Las películas presentaron una estructura ortorrómbica. Las películas sinterizadas mostraron buena compactación y densificación [24].. 2.3 Antecedente de películas delgadas de Cu2SnS3 En el 2012, Mehdi Adelifard y colaboradores obtuvieron películas nanoestructuradas de Cu2SnS3 en sustratos de vidrio a través de la técnica de rocío pirolìtico, mediante la variación de relaciones molares de Sn/Cu. Ellos observaron que al obtener una relación estequiometrica de 1 obtenían películas cristalizadas en una fase ternaria monoclínica de Cu2SnS3. El incremento en la relación Sn/Cu provoca una disminución en los valores de energía prohibida desde 2.57 a 1.58 eV. En este caso la temperatura del sustrato utilizada fue de 285 °C. Todas las películas presentaron un carácter semiconductor tipo p y la resistividad eléctrica fue de 2.1 x 10 -4 Ωcm [25]. En 2010, P. Fernándes y colaboradores prepararon películas delgadas de Cu2SnS3 y Cu3SnS4 a partir de la técnica de erosión iónica, utilizando precursores metálicos de Sn y Cu en atmósfera de azufre. Este trabajo se basó en el estudio de la temperatura de sulfurizaciòn para observar el cambio de fases de los compuestos basados en Cu-Sn-S. Las películas tratadas térmicamente a una temperatura de 350 ºC y 400 ºC presentaron un crecimiento perteneciente a la fase de Cu2SnS3 con estructura. tetragonal (I-42m) y cúbica (F-43m),. respectivamente. El incremento en la temperatura hasta 520 ºC, provoca que el contenido de estaño en la película disminuya favoreciendo la formación de la fase de Cu3SnS4 con estructura ortorrómbica (Pmm21). Los valores de energía de banda prohibida estimados fueron de 1.35, 0.96 y 1.60 eV para los compuestos ternarios con estructura tetragonal, cúbica y ortorrómbica, respectivamente. Las películas presentaron un carácter semiconductor tipo p. Las resistividades. 13.
(23) Capítulo 2. Antecedentes. eléctricas de las películas. ternarias con estructura. tetragonal, cubica y. ortorrómbica fueron de 4.59 x 10 -2, 1.26 x 10-2 y 7.40 x 10-4 Ωcm [26]. Devendra Tiwari y colaboradores en el 2013 desarrollaron un proceso de depósito para la obtención de películas de Cu2SnS3 a partir de una solución precursora alcohólica basada en un complejo metal-tiourea por el método de recubrimiento en fase liquida directo. Estas películas fueron depositadas por dip coating y después tratadas térmicamente a 200 ºC en aire por 10 minutos. Mediante difracción de rayos x determinaron que las películas presentaron la fase tetragonal y mediante espectroscopia de fotoelectrones emitidos por rayos x confirmaron que el Cu tiene una valencia de 1+ y el Sn una valencia de 4+. Estas películas presentaron una rugosidad baja del orden de 1-2 nm. El valor de energía de banda prohibida establecido para estas películas fueron del orden de 1.12 eV. Las películas mostraron un carácter semiconductor tipo p y una conductividad de 0.5 S/cm. La concentración y movilidad de huecos fueron de 10 18 cm-3 y 1 cm2 V/s, respectivamente. Ellos utilizaron este material para incorporarlo a una celda solar estructurada con grafito/Cu2SnS3/ZnO/ITO/SLG, obteniendo una eficiencia de 2.10% con voltaje a circuito abierto, densidad de corriente de corto circuito, y factor de llenado de 0.816V, 6.14 mA/cm2, 0.42, respectivamente. Estas películas presentaron un espesor cercano a 600 nm. [27].. En el 2003, Nair y colaboradores depositaron películas de Cu-Sn-S mediante depósito por baño químico, colocando una capa de CuS sobre una capa de SnS. A través de un tratamiento térmico en atmósfera de nitrógeno a 400 °C obtuvieron la fase perteneciente a Cu4SnS4. Estas películas presentaron una energía de banda prohibida de 1eV, además de ser fotosensibles y presentar una conductividad de 1 S/cm. [28].. Posteriormente en el 2010, en conjunto con. Avellaneda, modificaron el espesor de las películas de CuS y SnS utilizado con anterioridad y la temperatura del tratamiento térmico. Las temperaturas del tratamiento térmico utilizadas fueron de 350 y 400 °C, obteniendo dos fases pertenecientes a Cu2SnS3 y Cu4SnS4. Las energías de banda prohibida para Cu2SnS3 y Cu4SnS4 fueron 0.95 y 1.2 eV, respectivamente. Estas películas 14.
(24) Capítulo 2. Antecedentes. presentaron una conductividad eléctrica de 0.5-10 S/cm y una concentración de portadores entre 1017-1018 cm-3 [12]. Por otra parte, Hao Guan y colaboradores en el 2013, depositaron películas de Cu-Sn-S utilizando la técnica SILAR en sustratos de vidrio, estudiando principalmente la influencia de la atmósfera del tratamiento térmico sobre sus propiedades estructurales. La concentración de las sales precursoras de SnCl2, CuCl2 y Na2S fueron de 0.03, 0.06 y 0.05M, respectivamente. Posteriormente a depositar 60 ciclos realizaron tratamientos térmicos en distintas atmósferas basadas en una mezcla de N2-S2 y H2S a una temperatura de 420 ºC por 1 hora. Ellos encontraron que sinterizar en una mezcla de N2-S2 favorecía la obtención de películas. con un crecimiento cristalino. con fase cúbica. perteneciente a Cu2SnS3. Mientras que para aquellas películas tratadas en atmósfera de H2S favorecían la fase ortorrómbica perteneciente a Cu4SnS4 [29].. 2.4 Análisis crítico de literatura y aporte científico En literatura. existen distintos reportes. donde señalan diferentes. composiciones, condiciones de depósito y sinterizado para la preparación de CuS, SnS y Cu2SnS3 por el método SILAR. Actualmente no existe un estudio completo sobre los mecanismos de adsorción y reacción en etapas de crecimiento iniciales de las películas cuando son crecidas por este método. Además, el crecimiento de estos compuestos sobre una película de CdS lo convierten en un tema por explorar, debido a las reacciones entre superficies, oxidación, redisolución y difusión de éstas en dichas películas. Por tanto, el aporte científico del presente trabajo se basa en la obtención de los compuestos SnS y Cu2SnS3 sobre películas delgadas de CdS mediante el método SILAR. Además de proponer un mecanismo de reacción para la formación de SnS y adicionalmente de CuS.. 15.
(25) Capítulo 2. Antecedentes. 2.5 Justificación En la actualidad, el alto costo y la baja eficiencia de conversión de las celdas solares, ha propiciado la búsqueda de nuevos materiales fotovoltaicos con propiedades avanzadas para su utilización como capa absorbente en dichos dispositivos. Los compuestos ternarios basados en Cu, Sn y S son materiales alternativos que cumplen con este requisito, debido a que presentan propiedades ópticas, morfológicas y eléctricas apropiadas para este fin, además de ser económicos, abundantes en la naturaleza y no tóxicos, por lo que son materiales prometedores para el reemplazo de CIGS [Cu(In,Ga)Se 2] en celdas solares.. 2.6 Hipótesis Se obtienen películas delgadas de Cu2SnS3 a partir de CuS y SnS con carácter semiconductor tipo p, de manera reproducible mediante el control de las condiciones de procesamiento con el método SILAR.. 2.7 Objetivos 2.7.1 Objetivo General Obtener películas delgadas de Cu2SnS3 a partir de CuS y SnS mediante el método SILAR y estudiar el efecto de las condiciones de depósito sobre las propiedades ópticas, eléctricas y estructurales de dichas películas. 2.7.2 Objetivos Específicos Determinar el potencial zeta de superficie del vidrio y de películas de CdS, CuS y SnS. Evaluar los siguientes parámetros de reacción y de tratamiento térmico, para posteriormente relacionarlos con la nucleación y crecimiento de las películas de Cu2SnS3. Temperatura, tiempo y número de ciclos de depósito. Concentración de los precursores catiónicos y aniónicos. Tipo de contraión en las soluciones precursoras 16.
(26) Capítulo 2. Antecedentes. Temperatura y atmósfera del tratamiento térmico. Determinar la estructura cristalina de las películas por Difracción de Rayos X (DRX), Microscopía de Fuerza Atómica (MFA), Microscopía Electrónica de Barrido (MEB). Determinar sus propiedades ópticas mediante Espectroscopia de UVVisible y evaluar la energía de banda prohibida. Evaluar las propiedades eléctricas como movilidad, concentración de portadores y resistividad eléctrica mediante mediciones de Efecto Hall. Estudiar el mecanismo de formación de Cu2SnS3 a través de Espectroscopia de Fotoelectrones de Rayos X (XPS).. 17.
(27) Capítulo 3 METODOLOGÍA.
(28) Capítulo 3. Metodología. CAPÍTULO 3 MATERIALES Y MÉTODOS En este capítulo se presentan de forma detallada los reactivos y materiales utilizados para la preparación de películas de CdS, SnS, CuS y Cu2SnS3 mediante depósito por baño químico y SILAR. Además, se describen brevemente las técnicas de caracterización utilizadas para determinar las propiedades ópticas, estructurales, morfológicas y eléctricas de dichas películas.. 3.1 Películas Delgadas de CdS 3.1.1 Reactivos Químicos Los reactivos químicos empleados para el depósito de las películas delgadas de CdS fueron: CdCl2 (Cloruro de cadmio, 99.99%, Sigma Aldrich), Na3C 6H5O7·2H2O (Citrato de sodio, 99.6%, Fermont), Solución reguladora (borato) pH 10 (J.T. Baker), KOH (Hidróxido de potasio, 85%, BDH), CS(NH2)2 (Tiourea, 99.0 %, Sigma Aldrich). 3.1.2 Limpieza de sustratos La limpieza de los sustratos tiene como objetivo principal remover la mayor cantidad posible de impurezas que puedan estar localizadas en el sustrato inhibiendo posteriormente la formación de una película. Se utilizaron sustratos de vidrio marca Corning de 2.5 x 7.5 cm con un espesor de 2 milímetros. La limpieza se realizó sumergiendo los sustratos en distintos solventes y sometiéndolos a vibración sónica durante 10 minutos. Los solventes que se utilizaron fueron acetona, isopropanol y agua desionizada, empleados por separado y de forma sucesiva. Finalmente, se secaron con nitrógeno y se almacenaron en un contenedor de plástico limpio y cerrado. 3.1.3 Depósito de películas delgadas de CdS por baño químico El depósito por baño químico de las películas de CdS se realizó en un vaso de precipitado de 100 mL, incorporando 9 mL de cloruro de cadmio (CdCl 2) 0.05M, 9 mL de citrato de sodio (Na 3C6H5O7) 0.5M, 3 mL de buffer pH 10, 3 mL. 19.
(29) Capítulo 3. Metodología. de hidróxido de potasio (KOH) 0.5M, 4.5 mL de tiourea (H2NCSNH2) 0.5M y 31.5 mL de agua desionizada. La mezcla de reacción se introdujo en un baño de agua a 70 ºC. Posteriormente, los sustratos se introdujeron verticalmente y pegados a la pared del vaso de precipitado. El tiempo de reacción fue de 10 minutos. Una vez concluido el tiempo de depósito se sacaron las películas del baño y se lavaron con agua desionizada para quitar el exceso de precipitado y luego se secaron en N2. Consecutivamente fue removido uno de los lados depositados de la película con HCl diluido, conservando el otro lado para realizar mediciones posteriores.. Figura 3. 1 Depósito por baño químico de películas delgadas de CdS.. 3.2 Películas Delgadas de CuS 3.2.1 Reactivos Químicos Los reactivos químicos empleados para el depósito de las películas delgadas de CuS fueron: CuSO4·5H2O (Sulfato de cobre heptahidratado, 99.0%, Merck), NH4OH al 29% (Hidróxido de amonio, J.T. Baker) y Na 2S xH2O (Sulfuro de sodio hidratado, Sigma Aldrich). 3.2. 2 Sustratos Las películas de CdS depositadas por baño químico a temperatura de 70 ºC obtenidas en 10 minutos se utilizaron como sustratos para el crecimiento de las películas de CuS.. 20.
(30) Capítulo 3. Metodología. 3.2.3 Depósito de películas delgadas de CuS por SILAR La preparación de las películas delgadas de CuS se realizó mediante la técnica de adsorción y reacción sucesiva de capas iónicas (SILAR). El depósito químico fue realizado mediante un equipo de inmersión automático que permite el control del tiempo de inmersión, secado y enjuague. Las soluciones precursoras utilizadas fueron CuSO4 0.1M llevada a un pH de 10.2 con NH4OH 29% como precursor catiónico y Na 2S 0.1M a un pH de 12 como precursor aniónico. Los tiempos de inmersión en las etapas de adsorción y reacción fueron 30 segundos, mientras que para la etapa de enjuague fueron 10 segundos. Concluido el ciclo de depósito se prosiguió a realizar la misma operación hasta obtener el espesor deseado. Posteriormente se lavaron las películas con agua desionizada y se secaron con nitrógeno para finalmente almacenarlas en un desecador.. Figura 3. 2 Depósito de películas delgadas de CuS por SILAR.. 3.3 Películas Delgadas de SnS 3.3.1 Reactivos Químicos Los reactivos químicos empleados para el depósito de las películas delgadas de SnS fueron: SnCl2·2H2O (Cloruro de estaño II dihidratado, 98.7%, Fermont) y Na2S xH2O (Sulfuro de sodio hidratado, Sigma Aldrich).. 21.
(31) Capítulo 3. Metodología. 3.3.2 Sustratos Las películas de CdS depositadas por baño químico a temperatura de 70 ºC obtenidas en 10 minutos se utilizaron como sustratos para el crecimiento de las películas de SnS. 3.3.3 Depósito de películas delgadas de SnS por SILAR La preparación de las películas delgadas de SnS se realizó mediante la técnica SILAR. El depósito químico fue realizado también utilizando el equipo de inmersión automático. Las soluciones precursoras utilizadas fueron SnCl2 0.1M con pH de 5 como precursor catiónico y Na 2S 0.1M a un pH de 12 como precursor aniónico. Los tiempos de las inmersiones de las etapas de adsorción y reacción fueron 30 segundos, mientras que para las inmersiones de enjuague fueron 10 segundos. Concluido el ciclo de depósito se prosiguió a realizar la misma operación hasta obtener el espesor deseado. Posteriormente se lavaron las películas con agua desionizada y se secaron con nitrógeno para finalmente almacenarlas en un desecador.. Figura 3. 3 Depósito de películas delgadas de SnS por SILAR.. 3.4 Películas Delgadas de Cu2SnS3 Para la obtención de un compuesto ternario se estudiaron 2 diferentes procedimientos experimentales con la intención de encontrar las condiciones óptimas de depósito.. 22.
(32) Capítulo 3. Metodología. 3.4.1 Depósito de multicapas de películas delgadas de SnS-CuS El depósito de las multicapas se realizó utilizando la metodología para el depósito de películas de SnS y CuS mediante la técnica SILAR. En la siguiente tabla se muestra la estructura formada y el número de ciclos depositados sobre películas de CdS.. Estructura. Número de ciclos. Relación SnS/CuS. SnS. CuS. 20. 40. 0.50. 40. 60. 0.66. 40. 40. 1.00. 40. 20. 2.00. Figura 3. 4 Estructura multicapa CdS/SnS/CuS.. 3.4.2 Depósito de películas alternadas ciclo x ciclo de SnS-CuS Esta metodología está basada en el depósito alternado de ciclos de SnS y CuS. En la siguiente figura se muestra el esquema de la estructura formada, donde n, representa el número de ciclos en conjunto depositados, el cual fue de 50. En este experimento se modificaron la concentración de las soluciones catiónicas precursoras, utilizando concentraciones de 0.05 y 0.01M.. Figura 3. 5 Estructura alternada de SnS/CuS.. 3.5 Tratamiento Térmico Las películas de CuS y Cu2SnS3 fueron sometidas a un tratamiento térmico con la finalidad de remover el material precursor remanente, además de promover la cristalinidad de las películas. En el caso del compuesto Cu2SnS3 el 23.
(33) Capítulo 3. Metodología. tratamiento térmico tiene como propósito el activar la difusión de las especies Cu y Sn. En la figura 3.6 se muestra el sistema construido para el acoplamiento de un horno tubular (Thermo Scientific) a un sistema de vacío. Las películas se colocaron en el portamuestra y después se realizó vacío hasta obtener una presión de 1 x 10-3 torr para evitar reacciones de oxidación en las películas. Posteriormente, se realizó el tratamiento térmico a temperatura de 200, 300 y 400 ºC en atmósfera de nitrógeno de alta pureza grado 5.0.. Figura 3. 6 Tratamiento térmico de películas delgadas en N2 grado 5.0.. 24.
(34) Capítulo 4 DISCUSIÓN DE RESULTADOS Películas delgadas de CdS.
(35) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. CAPÍTULO 4 DISCUSIÓN DE RESULTADOS Películas delgadas de CdS En este capítulo se presentan los resultados de la caracterización de películas delgadas de CdS con la finalidad de elegir la mejor película que sirva como sustrato base para crecer el material absorbedor en estudio. Los criterios utilizados para la elección de éstas consistieron en encontrar una película de CdS con un espesor pequeño el cual no interviniera con las mediciones de absorción para la estructura. CdS/absorbedor, además de presentar una relación. estequiométrica cercana a 1.. 4.1 Propiedades Ópticas Los espectros de transmitancia óptica de las películas depositadas a diferente tiempo de depósito se muestran en la figura 4.1. Los espectros de las películas. depositadas a 1, 3 y 6 minutos. son análogos al espectro. correspondiente al sustrato de vidrio (referencia). 100. (h) (eV/cm)2. 10 min 6 min 3 min 1 min. 2.0. 2.5. 2.0. 2.5. 3.0. 3.5. 4.0. Band Gap Energy (eV). 100. 3.0. 3.5. 4.0. 80. Energía de Banda Prohibida (eV). 60 2.0. 2.5. 3.0. 3.5. %T. 40. 10 min 6 min 3 min 1 min. (h)2 (eV/cm)2. Borde de absorción CdS. (h) (eV/cm)2. 60. (h)2 (eV/cm)2. %Transmitancia. 80. 4.0. Band Gap Energy (eV). 40. 20. 20 0 300. 1 min 3 min 6 min 10 min 400. 0 300. 400. 500. 600. (nm). 2.35 eV 2.0 2.5 3.0 3.5 4.0 Energía de Banda Prohibida (eV). 500. 600. 700. 800. 900. Longitud de onda (nm). Figura 4. 1 Espectros de transmitancia y valores de energía de banda prohibida para películas de CdS depositadas a diferente tiempo de depósito.. 26. 700. 800. 900.
(36) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. En cambio, el espectro de la película depositada a 10 minutos presenta un ligero borde en aproximadamente 510 nm atribuido al borde de absorción del CdS. Los valores de energía de banda prohibida se determinaron extrapolando la parte lineal de la gráfica (αhν)2 vs (hν) en el eje de abscisas (eje x). Los valores de Eg calculados fueron 4.06, 3.98, 3.97 y 2.35 eV para las películas depositadas a 1, 3, 6 y 10 minutos, respectivamente. Únicamente, el último valor coincide con el reportado en literatura para este material, mientras que los demás son atribuidos al vidrio [30,31].. 4.2 Propiedades Estructurales En la figura 4.2 se muestran las micrografías de las películas de CdS a diferente tiempo de depósito a una magnificación de 20,000X. Las imágenes obtenidas para las películas depositadas a 1 y 3 minutos carecen de buena resolución debido a que sólo se depositan pocas capas del material, por tanto, gran parte de la señal proviene del sustrato aislante. Por el contrario, las películas depositadas a 6 y 10 minutos presentan un crecimiento granular compacto, observando un depósito continuo y uniforme.. Esta última película está. compuesta de granos pequeños de aproximadamente 35 nm. Además, es posible observar que no se encontraron grietas, sólo pequeños agregados de 70 nm adheridos y dispersos por toda la película resultado de la precipitación homogénea en la solución, parte del mecanismo de formación del compuesto.. Figura 4. 2 Morfología superficial de películas de CdS depositadas a 1 (a), 3 (b), 6 (c) y 10 minutos (d).. 27.
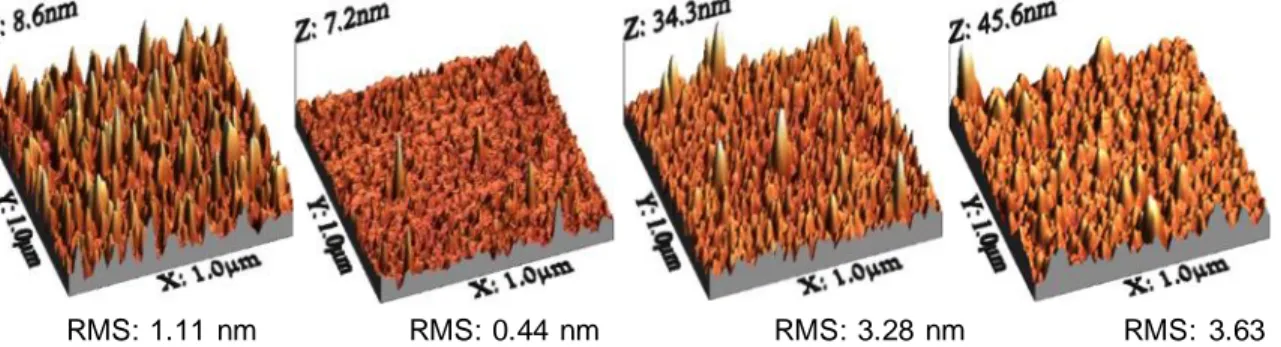
(37) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. La topografía de las películas está influenciada por la temperatura y tiempo de depósito como se puede observar en la figura 4.3. A primeros minutos de depósito las muestras presentan una topografía con muchos máximos los cuales pueden ser causados por la creación de primeros puntos de nucleación y la variación en recubrimiento en toda la superficie. No obstante, la rugosidad incrementa cuando el tiempo de depósito es de 3 y 6 minutos, observando picos máximos de hasta 34 nm, provocados por varios agregados en la película. La rugosidad aumenta hasta 3.63 nm debido al crecimiento y formación de una película homogénea y compacta. Aunque se observan aún máximos, son atribuidos a residuos superficiales de gran tamaño.. RMS: 1.11 nm nm. RMS: 0.44 nm. RMS: 3.28 nm. RMS: 3.63. Figura 4. 3 Topografías obtenidas de MFA de películas de CdS depositadas a 1 (a), 3 (b), 6 (c) y 10 minutos (d).. 4.3 Propiedades Químicas El análisis de XPS se utilizó para determinar el estado y entorno químico de los elementos constituyentes de la superficie de las películas de CdS. La calibración en la escala de energía se realizó considerando la señal proveniente del C1s (284.5 eV). Los valores de energía de enlace para C1s son mostrados en la figura 4.4, en la cual se muestra el pico principal en 284.5 eV el cual se le atribuye a los enlaces C-C y C-H, provenientes de residuos por parte del agente complejante. Por otra parte, se pueden distinguir dos picos centrados en 286.1 y 288.1 eV relacionados con los enlaces C-O y -C≡N, respectivamente. El enlace C-O es atribuido al anión citrato que proviene del agente complejante utilizado en la. 28.
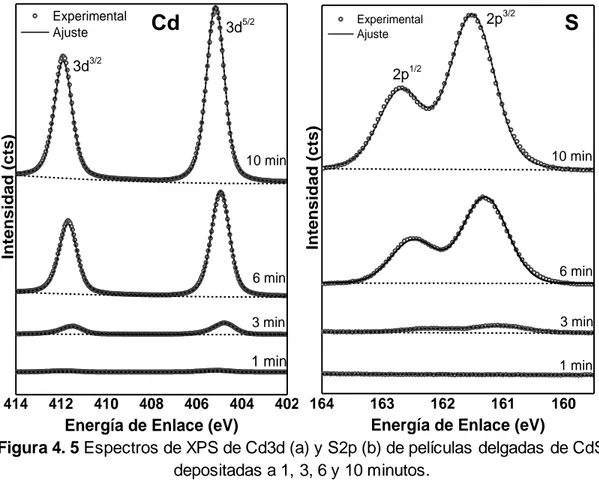
(38) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. reacción, mientras que el enlace -C≡N, pertenece al subproducto de la hidrólisis de la tiourea, la cianamida. Un pequeño pico es distinguido a energías altas para las muestras depositadas a un tiempo de 1 y 3 minutos, el cual es atribuido a la señal K2p proveniente del vidrio. Experimental Ajuste. -C=N. C-O. Intensidad (cts). K 2p. C-C. 10 min. 6 min. 3 min. 1 min 294 292 290 288 286 284 282. Energía de Enlace (eV) Figura 4. 4 Espectros de XPS de C1s de películas delgadas de CdS depositadas a 1, 3, 6 y 10 minutos.. La figura 4.5 muestra los espectros de alta resolución correspondientes a los niveles energéticos cercanos al núcleo Cd3d y S2p de las películas depositadas a diferente tiempo de depósito. Los picos centrados en 404.9 y 411.6 eV son atribuidos a los niveles Cd 3d 5/2 y Cd3d3/2 y aquellos ubicados en 161.5 y 162.7 eV son de los niveles del S2p 3/2 y S2p1/2 [32]. La intensidad de los picos del espectro muestra una diferencia entre las películas depositadas a 3 y 6 minutos. Este cambio drástico puede ser atribuido a la posible terminación de la etapa de nucleación y el comienzo de la etapa de 29.
(39) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. crecimiento. Por tanto, la señal observada a 1 y 3 minutos procede de algunos núcleos que están enlazados fuertemente al sustrato, provocando que la energía superficial en la interfase sea reducida.. Cd. 3d3/2. 410. 408. 406. Intensidad (cts). 10 min. 412. S. 2p1/2. Intensidad (cts) 414. 2p3/2. Experimental Ajuste. 3d5/2. 10 min. 6 min. 3 min. 3 min. 1 min. 1 min. 164. 1. 163. 162. 161. Binding Energy (eV). 402 164. 163. 162. 161. 160. Energía de Enlace (eV) Energía de Enlace (eV) Figura 4. 5 Espectros de XPS de Cd3d (a) y S2p (b) de películas delgadas de CdS depositadas a 1, 3, 6 y 10 minutos.. La simetría de los picos indica la formación de un sólo compuesto químico. La energía de enlace para cadmio corresponde al enlace químico con azufre y respectivamente para la energía de enlace para azufre. Para determinar la variación en la concentración atómica de las especies en función del tiempo de depósito, se utilizó la siguiente relación, la cual incluye el factor de sensibilidad (F) proveniente de datos experimentales del equipo y la intensidad de cada especie (I, área bajo la curva) en el experimento. [33].. ICd. [Cd] atómica=. 2p3/2. 2p1/2. 6 min. 404. Experimental Fit. Intensity (cps). Experimental Ajuste. ⁄F Cd ICd IS ⁄F + ⁄F Cd S. (4.1). 30. 1.
(40) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. La relación estequiométrica de las películas depositadas a 1, 3, 6 y 10 minutos se muestra en la figura 4.6, en la cual es posible apreciar que a un tiempo de 1 minuto la relación es prácticamente cero. El periodo de incubación es de alrededor 2 minutos, posteriormente el crecimiento de la película es favorecido, obteniendo relaciones estequiométricas distintas en cada tiempo de depósito, hasta obtener una relación S/Cd de 0.78. Las películas. de. CdS son utilizadas. en celdas. solares como. semiconductor tipo n, por tanto, el obtener una variación en concentración de Cd y S a través de todo el espesor de la película, puede generar dificultades con respecto al flujo de electrones a través de las interfases de la celda solar. Debido a la importancia que tiene la relación de concentraciones y el tiempo de depósito se prosiguió a determinar el espesor de las películas en función del tiempo. La tendencia en la relación estequiométrica establece que después de llegar a un tiempo límite se obtendrá una relación cercana a 1. La reacción química concluye posterior a 25 minutos, cuando se deposita polvo en la superficie de la película provocando la inhibición del continuo crecimiento. 1.0 0.9 0.8. S/Cd. 0.7 0.6 0.5 0.4 0.3 0.2 0.1 0.0 0. 2. 4. 6. 8. 10. Tiempo de depósito (min). Figura 4. 6 Relación estequiométrica de películas delgadas de CdS depositadas a 1, 3, 6 y 10 minutos.. En la figura 4.7a se muestra el espectro de XPS para la región del Si2p, en el cual se observa un pico centrado en 102.9 eV el cual es atribuido al Si 4+. 31.
(41) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. enlazado químicamente al O. Conforme transcurre el tiempo de depósito, la señal disminuye, consecuencia del aumento en espesor de la película. Para la película depositada en 10 minutos no se observa la señal para el silicio, por tanto, la película presenta un espesor mínimo de alrededor de unos 10 nm, debido a que. 10 min. 15. Cd/Si. Intensidad (cts). 6 min. 10. 3 min. b). Vidrio CdS. 0 -10 -20. 15. -30 Experimental Fit. 10 min. -50. 6 min. -60. 10. -70 -80. 3 min. 20. 15. 15. 10. 10. 5. 5. 0. 0 0. 2. 4. 6. 8. 10. Time Deposition (min). 4. 5. 6. 7 8 pH. 9 10. 1 min. 106. 105. 104. 103. 102. 101. 100. Binding Energy (eV). 5. 104. 103. 102. 101. Energía de Enlace (eV). 100. 20. 20. 15. 15. 2. 1. 0 0. 2. 4. 6. 8. Cd/Si. 0 10. Tiempo de depósito (min). Figura 4. 7 a) Espectro de XPS de Si 2p y b) Relación estequiométrica Cd/Si y S/Si para películas de CdS depositadas a 1, 3, 6 y 10 minutos.. En la figura 4.7b se muestra la relación estequiométrica considerando la concentración atómica del cadmio y azufre en relación a la concentración atómica del silicio. Es posible observar que la relación Cd/Si es mayor que S/Si, esto es consecuencia de la atracción electrostática entre el vidrio y el elemento más electropositivo. El vidrio presenta un punto isoeléctrico a un pH de 1.5, a pH por encima de éste, el potencial zeta en superficie es negativo, por tanto, casi en todo el rango de pH el vidrio está cargado negativamente, por ello, es factible que exista una preferencia por la atracción de iones Cd2+ que de S 2-. En el caso particular de la película que tiene un tiempo de depósito de 10 minutos, prevalece. 32. 10. 10. 5. 5. 0. 0 0. 2. 4. 6. Tiempo de depósito. 8. 10. S/Si. 105. 5. Cd/Si. 1 min. 106. 20. -40 Cd/Si. Si. 20. 10. S/Si. 20. a). Intensity (cps). Experimental Ajuste. Potencial de Zeta de Superficie (mV). es la profundidad de análisis para estas mediciones.. 1.
(42) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. una mayor cantidad de cadmio que de azufre, aun cuando el sustrato ya está totalmente recubierto por CdS. El potencial zeta de superficie para el CdS es negativo a pH alto, es por ello, el favorecimiento en la adsorción de iones cadmio que de azufre. En la figura 4.8 se muestra la obtención de los espesores utilizando la técnica de XPS. A través de la relación entre las intensidades del sustrato (Si2p) y la del átomo ionizado Cd o S, se puede predecir el espesor a diferente tiempo de depósito. Utilizando la ecuación siguiente se obtuvieron éstos.. I. dCdS =λCdS cos θ ln [(I CdS,∞CdS )(I SiO (I SiO ,∞) 2. 2. ]. ). (4.2). +1. Donde dCdS es el espesor de la película de CdS, λCdS es la longitud de atenuación, θ es el ángulo formado entre la normal y el haz incidente de fotones, ICdS y ISiO2 es la intensidad del pico CdS y SiO2 y ICdS∞ y ISiO2,∞ es la intensidad del pico CdS y SiO2 en el infinito. Cd S Promedio. 14 12. Espesor (nm). [34].. 10 8 6 4. CdS. 2. Vidrio. 0 0. 2. 4. 6. 8. 10. Tiempo de depósito (min). Figura 4. 8 Espesores determinados por XPS para películas de CdS depositadas a 1, 3, 6 y 10 minutos.. 33.
(43) Capítulo 4.Discusión de Resultados. Películas delgadas de CdS. La variación de los espesores considerando cualquiera de los dos elementos (Cd, S) es pequeña, por tanto, se promediaron ambos. A tiempo de 1 y 3 minutos el recubrimiento que existe es mínimo, por tanto, aún no se forma la película, mientras que el cambio significativo es perceptible cuando se tiene una duración de 6 y 10 minutos, alcanzando valores de hasta 13.87 nm. Finalmente, la película elegida para el depósito del material absorbedor fue aquella con un tiempo de depósito de 10 minutos, debido a que es ésta la que cumple con las características deseadas. Esta película homogeneidad,. presenta buena. baja rugosidad, es lo suficientemente gruesa para soportar el. recubrimiento además de no contribuir con la absorción.. 34.
(44) Capítulo 5 DISCUSIÓN DE RESULTADOS Compuestos Binarios.
Figure


Documento similar
La campaña ha consistido en la revisión del etiquetado e instrucciones de uso de todos los ter- mómetros digitales comunicados, así como de la documentación técnica adicional de
Mechanistically, HDAC6-deficient cytotoxic T lymphocytes (CTLs) showed defective in vitro cytolytic activity related to altered dynamics of lytic granules, inhibited
DS N° 012-2014-TR Registro Único de Información sobre accidentes de trabajo, incidentes peligrosos y enfermedades ocupacionales y modificación del art.110º del Reglamento de la Ley
Cedulario se inicia a mediados del siglo XVIL, por sus propias cédulas puede advertirse que no estaba totalmente conquistada la Nueva Gali- cia, ya que a fines del siglo xvn y en
No había pasado un día desde mi solemne entrada cuando, para que el recuerdo me sirviera de advertencia, alguien se encargó de decirme que sobre aquellas losas habían rodado
Abstract: This paper reviews the dialogue and controversies between the paratexts of a corpus of collections of short novels –and romances– publi- shed from 1624 to 1637:
Habiendo organizado un movimiento revolucionario en Valencia a principios de 1929 y persistido en las reuniones conspirativo-constitucionalistas desde entonces —cierto que a aquellas
Por lo tanto, en base a su perfil de eficacia y seguridad, ofatumumab debe considerarse una alternativa de tratamiento para pacientes con EMRR o EMSP con enfermedad activa