DETERMINACIÓN DE LOS PARÁMETROS FISICOQUÍMICOS ÓPTIMOS PARA LA RECUPERACIÓN DE QUERATINA DE FIBRAS DE Vicugna pacos (ALPACA) MEDIANTE EL USO DE LÍQUIDOS IÓNICOS PRÓTICOS
89
0
0
Texto completo
(2) AGRADECIMIENTO. En primer lugar quiero agradecer a Dios, por permitirme llegar a este momento tan especial en mi vida, por los triunfos y fracasos que me han enseñado a ser una mejor persona. A mis padres, por su amor y apoyo incondicional en cada etapa de mi formación. A mi novio, por sus palabras de aliento y motivación constante cada vez que sentí ganas de desistir. A mi grupo de amigos por toda su colaboración y en especial por las risas. Al CONCYTEC por darme la oportunidad de realizar este sueño. Y un agradecimiento especial a mi asesor el Dr. Badhín Gómez Valdez por su tiempo, apoyo y sabiduría, de las que siempre estaré agradecida. Gracias. 2.
(3) ÍNDICE RESUMEN ...................................................................................................................... 1 INTRODUCCIÓN .......................................................................................................... 3 HIPÓTESIS..................................................................................................................... 5 OBJETIVOS ................................................................................................................... 6 CAPÍTULO I .................................................................................................................. 7 MARCO CONCEPTUAL.............................................................................................. 7 1.. INDUSTRIA ALPAQUERA .......................................................................................... 8 1.1. Productividad ................................................................................................. 8. 1.2. Empresas en la región .................................................................................. 10. 1.3. Características químicas de la fibra de Vicugna pacos (alpaca) ................ 10. 2.. QUERATINA .......................................................................................................... 11. 3.. LÍQUIDOS IÓNICOS ................................................................................................ 12 3.1. Síntesis de líquidos iónicos .......................................................................... 13. 3.2. Clasificación de líquidos iónicos ................................................................. 13. 3.3. Propiedades de los líquidos iónicos ............................................................. 16. 3.4. Aplicaciones y perspectivas de líquidos iónicos próticos ............................ 17. CAPÍTULO II ............................................................................................................... 18 MATERIALES Y MÉTODOS .................................................................................... 18 1.. 2.. MATERIALES, REACTIVOS Y EQUIPOS.................................................................... 18 1.1. Material de partida ...................................................................................... 18. 1.2. Materiales..................................................................................................... 18. 1.3. Reactivos ...................................................................................................... 18. 1.4. Equipos ......................................................................................................... 19. METODOLOGÍA ..................................................................................................... 19 2.1. Síntesis de líquidos iónicos próticos ............................................................ 19. 2.2. Tratamiento de la fibra de Vicugna pacos (alpaca) .................................... 20. 2.3. Hidrólisis de fibra de Vicugna pacos (alpaca) ............................................ 21. 2.4. Caracterización del líquido iónico prótico .................................................. 21. 2.5. Espectroscopia infrarroja (FT-IR) ............................................................... 22.
(4) 2.6. Espectroscopia de Resonancia Magnética Nuclear (RMN) ......................... 22. 2.7. Separación de la mezcla queratina- liquido iónico prótico ......................... 22. 2.8. Cuantificación de queratina ......................................................................... 23. CAPÍTULO III ............................................................................................................. 25 RESULTADOS Y DISCUSIÓN .................................................................................. 25 1.. SÍNTESIS DE LÍQUIDOS IÓNICOS PRÓTICOS ............................................................. 25. 2.. RECOLECCIÓN Y TRATAMIENTO DE LA FIBRA DE Vicugna pacos (ALPACA) .......... 29. 3.. ENSAYOS DE DISOLUCIÓN DE FIBRAS DE Vicugna pacos (ALPACA) ...................... 30. 4.. CARACTERIZACIÓN DE LÍQUIDOS IÓNICOS PRÓTICOS ............................................ 33 4.1. Características físico químicas de líquidos iónicos próticos ....................... 33. 4.2. Espectroscopia infrarroja (FT-IR) de líquidos iónicos próticos ................. 36. 4.3. Espectroscopia de Resonancia Magnética Nuclear (RMN) de líquidos. iónicos próticos ....................................................................................................... 39 4.4. Ecotoxicidad y biodegradabilidad de líquidos iónicos próticos .................. 46. PARÁMETROS ÓPTIMOS DE DISOLUCIÓN DE FIBRAS DE Vicugna pacos (ALPACA) . 47. 5.. 5.1. Temperatura ................................................................................................. 47. 5.2. Tiempo .......................................................................................................... 49. SEPARACIÓN Y RECUPERACIÓN DE LA MEZCLA QUERATINA – LÍQUIDOS IÓNICOS. 6.. PRÓTICOS ...................................................................................................................... 6.1. 51. PORCENTAJE DE RECUPERACIÓN DE QUERATINA DE FIBRA DE Vicugna pacos. (ALPACA) ..................................................................................................................... 52 6.2 7.. DESTILACIÓN Y REUTILIZACIÓN DEL LÍQUIDO IÓNICO PRÓTICO ......................... 53 CUANTIFICACIÓN DE PROTEÍNAS TOTALES A PARTIR DE FIBRAS DE Vicugna pacos. (ALPACA) ..................................................................................................................... 54 7.1. Método de Biuret .......................................................................................... 55. 7.2. Método de Bradford ..................................................................................... 57. CONCLUSIONES ........................................................................................................ 60 RECOMENDACIONES .............................................................................................. 61 BIBLIOGRAFÍA .......................................................................................................... 62 ANEXOS ....................................................................................................................... 70. 4.
(5) RESUMEN Los líquidos iónicos próticos (PILs) son una nueva clase de disolventes que entre otras aplicaciones, permiten la disolución de polímeros naturales; en la presente tesis se han sintetizados varios PILs de base amoniacal, utilizando para esto cuatro cationes diferentes (trietanolamina, dietilamina, dietanolamina, dimetiletanolamina) y dos aniones (ácido acético y ácido fórmico), con el objetivo de disolver fibra de Vicugna pacos (alpaca), una forma de queratina, que en su porción corta y gruesa representa un desecho de la industria textil en nuestra región. El formiato dimetiletanolamina [DMEA][HCOO] ha mostrado la mayor capacidad de disolución (47.19%), con respecto a los siete PILs sintetizados en esta investigación; por lo que, se ha optimizado el proceso de disolución de queratina a partir de fibra de Vicugna pacos (alpaca), encontrando que los parámetros óptimos para la disolución de esta fibra son: 145°C por 4.5 horas. Con los cuales se ha logrado disolver 26.4 gramos de fibra de Vicugna pacos (alpaca) por litro de líquido iónico prótico. Así mismo, se han realizado estudios de caracterización de los PILs sintetizados mediante FT-IR, RMN-1H y RMN13. C que demuestran que se ha conseguido una transferencia protónica intermolecular. completa en el caso del [DMEA] [HCOO].. 1.
(6) ABSTRACT Protic ionic liquids (PILs) are a new class of solvents among others applications, allow the dissolution of natural polymers; in this thesis we have been synthesized several PILs ammoniacal base, using for this four different cations (triethanolamine, diethylamine, diethanolamine, dimethylethanolamine) and two anions (acetic acid and formic acid), with the aim of dissolving Vicugna pacos (alpaca) fiber, a form of keratin, which in its short and thick portion represents a waste of the textile industry in our region. The dimethylethanolamine formate [DMEA] [HCOO] has shown the higher dissolution capacity (47.19%), about seven PILs synthesized in this investigation; therefore, it is optimized dissolution process keratin from Vicugna pacos (alpaca), finding the optimal parameters for the dissolution of this fiber are 145 ° C for 4.5 hours. With which it has been possible to dissolve 26.4 grams of Vicugna pacos (alpaca) fiber per protic ionic liquid liter. Likewise, studies have been conducted characterization of PILs synthesized by FT-IR, 1H -NMR and. 13. C-NMR., showing that it has achieved a complete. intermolecular proton transfer in the case of [DMEA] [HCOO].. 2.
(7) INTRODUCCIÓN Uno de los principales problemas que enfrenta la sociedad en la actualidad está asociado al uso de disolventes; los cuales, se emplean en una amplia gama de tecnologías y aplicaciones desde la fabricación de medicamentos, alimentos y plásticos, hasta los procesos de extracción de minerales1. Sin embargo existen inconvenientes asociados al uso de disolventes, ya sean de carácter ambiental; tales como: las emisiones de compuestos orgánicos volátiles (COVs) y la formación de ozono troposférico, de salud; ya que al ser inhalados, podrían acumularse en el organismo y de seguridad debido a que la mayoría son inflamables y explosivos2-5. Es por ello que los investigadores se encuentran en la búsqueda de alternativas a los disolventes tradicionales que sean eficaces y amigables con el medio ambiente. Los líquidos iónicos (ILs) son sales compuestas por iones que existen en su mayoría en estado líquido a temperatura ambiente3, cuyas propiedades se pueden modificar para una aplicación específica, por la combinación adecuada de catión, anión y radical alquil6. Entre estas propiedades únicas tenemos: la no volatilidad y no inflamabilidad, solubilidad variable, alta estabilidad química y térmica, alta conductividad iónica y amplia ventana de potencial electroquímico. Es por ello que los líquidos iónicos han sido ampliamente estudiados, utilizados y reconocidos como alternativas prometedoras para diversas aplicaciones, algunas de ellas con alto potencial industrial2,3,7,8. La clasificación más utilizada para estos compuestos, está basada en su capacidad donora de protones o no donora de protones, siendo así denominados líquidos iónicos próticos y apróticos respectivamente1,9,10. Los líquidos iónicos próticos (PILs), son una clase nueva de líquidos iónicos, formados por la transferencia de protones a partir de un ácido de Bronsted a una base de Bronsted1, los cuales tienen la capacidad de promover enlaces puente de hidrógeno. El creciente interés por esta clase de líquidos iónicos se basa en su facilidad de síntesis, bajo costo de producción y su potencial reutilización al ser sometidos a procesos de destilación6,11-15. Los líquidos iónicos próticos han sido utilizados en síntesis orgánica, catálisis, tratamiento de crudo, absorción de gases, separaciones de membrana, aplicaciones farmacéuticas y biológicas, etc7,16,17.. 3.
(8) La queratina, una proteína fibrosa, está disponible en abundancia en todo el mundo como un subproducto de actividades industriales como la producción de aves de corral y también en forma de residuos de fibra corta de procesamiento de la lana en la industria textil. Esta proteína presenta una estructura tridimensional, constituida por una triple hélice de cadenas proteicas unidas por una serie de enlaces covalentes (enlaces disulfuro)18-20. La estructura compleja de la queratina; por lo general, requiere de una mezcla de disolventes, los cuales tienen diferentes funciones para romper las interacciones covalentes y no covalentes que presenta21; además cabe mencionar, que una de las más graves deficiencias con respecto a estos métodos para extraer queratina es la gran cantidad de reactivos tales como ácidos o reductores que se consumen y no se pueden reciclar22. Por ello, en esta tesis hemos realizado la determinación de los parámetros fisicoquímicos óptimos para la recuperación de queratina de fibras de Vicugna pacos (alpaca) sin valor comercial, mediante la utilización de líquidos iónicos próticos.. 4.
(9) HIPÓTESIS. Dado que el uso de disolventes comunes, como los disolventes orgánicos, es un problema ambiental, de salud y seguridad, de mucha importancia en la actualidad; es probable que, mediante el uso de líquidos iónicos próticos como alternativa a los disolventes tradicionales, se pueda determinar los parámetros fisicoquímicos necesarios para la recuperación de queratina presente en fibras de Vicugna pacos (alpaca).. 5.
(10) OBJETIVOS OBJETIVO GENERAL -. Determinar los parámetros físico químicos óptimos (temperatura, tiempo, velocidad de agitación) para la recuperación de queratina de fibra de Vicugna pacos (alpaca), mediante el uso de líquidos iónicos próticos. OBJETIVOS ESPECÍFICOS -. Sintetizar y caracterizar el líquido iónico prótico para propósitos de hidrólisis de fibras de Vicugna pacos (alpaca).. -. Evaluar la capacidad de disolución de queratina de fibra de Vicugna pacos (alpaca) mediante la utilización de líquidos iónicos próticos.. -. Optimizar el proceso de disolución de fibra de Vicugna pacos (alpaca) y el líquido iónico prótico.. -. Cuantificar la queratina obtenida en el proceso de disolución de la fibra de Vicugna pacos (alpaca).. 6.
(11) CAPÍTULO I MARCO CONCEPTUAL En el mundo, el Perú es el primer productor de Vicugna pacos (alpacas) y Vicugna vicugna (vicuñas), y el segundo en Lama glama (llamas), después de Bolivia. El aprovechamiento sostenible de estos recursos y el uso de la mejora genética de los camélidos (además de vacunos, ovinos y caprinos) es uno de los retos que tiene el país como el medio más efectivo de lucha contra la pobreza y la inseguridad alimentaria, que afecta a numerosas comunidades campesinas que viven de la cría y explotación de estas especies ganaderas23-26. La industria textil considera a la fibra de Vicugna pacos (alpaca) como una fibra especial y, las prendas que se confeccionan con ellas, están clasificadas como artículos de lujo26, 27, las características de la fibra dependerán de la localización corporal, de este modo, es más fina y larga en zonas de la espalda, dorso y flancos, siendo más grueso y corto en zonas de las extremidades y cabeza26-29. El problema principal y más serio que afecta a la cadena productiva de los camélidos en la actualidad, es el deterioro genético de Vicugna pacos (alpacas) y Lama glama (llamas), por el mal manejo del ganado y principalmente por la alarmante consanguinidad que se produce en hatos tan pequeños, que aparte de malformaciones, dan como resultado altos porcentajes de animales pintados, deficiente calidad de la fibra con mayores volúmenes de gruesa y huarizo (fibras de poco valor económico), afectando aún más los ingresos del productor25,28. Las fibras de baja calidad generan pérdidas a la industria textil, ya que deben mezclarse con otras para alcanzar un mínimo valor comercial25, ser vendidas con otros fines o simplemente desechadas26-29. Actualmente los investigadores están buscando formas de reutilizar estos recursos descartados y aquí es donde los líquidos iónicos hacen su aparición. Los líquidos iónicos han sido un tema de interés en la última década debido a sus propiedades atractivas para una variedad de aplicaciones físicas, químicas y biológicas2,4,30,31. Recientemente, han recibido el reconocimiento como materiales verdes y prometedores para posibles aplicaciones en diversos campos; ya que son, 7.
(12) típicamente no volátiles, no inflamables, presentan estabilidad química y térmica, además de una notable solubilidad22, 32. 1. Industria alpaquera El Perú posee la mayor producción de Vicugna pacos (alpaca), 87%, la importancia en el desarrollo y crianza de esta especie, radica en la actividad económica de producción de fibra (mal llamada lana), además de carne y otros subproductos. Esto debido, a la enorme capacidad de la Vicugna pacos (alpaca) y la Lama glama (llama) para adaptarse a las grandes alturas (3800-4700 m.s.n.m.); posibilitando la utilización de extensas áreas de pastos naturales que de otra forma serían desperdiciadas y de la gran habilidad del habitante andino para su domesticación y uso textil25. La fibra de Vicugna pacos (alpaca) es el pelo quela cubre; el cual, proviene de dos razas, Huacaya y Suri. Estas razas tienen aspectos diferentes y presentan los siguientes colores básicos: blancos, beige, cafés, grises y negros, los que tienen a su vez diversas tonalidades y combinaciones 1.1 Productividad Existen diversos factores que influyen en la cantidad y la calidad de la producción de fibra en camélidos sudamericanos, estos se clasifican en factores medioambientales externos y factores genéticos o internos. Los factores externos que modifican la respuesta productiva en Vicugna pacos (alpacas) son la alimentación26, 33, la locación geográfica o lugar de pastoreo34 y, en el caso del peso de vellón, es particularmente relevante considerar la frecuencia, año de esquila25, 26,35 y la precipitación pluvial36. La altitud no ejerce influencia ni sobre la cantidad ni la calidad de fibra26, 37. Entre los factores internos que afectan el diámetro de fibra y peso de vellón resaltan el sexo, la edad, la raza, sanidad, estado fisiológico, condición corporal y color de vellón38-40. El Instituto Nacional de Defensa de la Competencia y de la Protección de la Propiedad Intelectual (INDECOPI), aprueba mediante resolución las Normas Técnicas Peruanas (NTP) para la categorización en vellón y la clasificación de la fibra de Vicugna pacos (alpaca); de acuerdo a lo cual, se tienen 6 categorías de fibras, tal como se aprecia en la Tabla 1. 8.
(13) Tabla 1 Clasificación de la fibra de Vicugna pacos (alpaca) MICRONAJEa. LONGITUDb. Alpaca baby. ≤23.0. ≥65. Alpaca fleece. 23.1-26.5. ≥70. Alpaca médium flecce. 26.6-29.0. ≥70. Alpaca huarizo. 29.1-31.5. ≥70. Alpaca gruesa. >31.5. ≥70. -. 20-50. CATEGORÍA. Alpaca corta a. en µm, b en mm. Fuente: PNTP 231.301. Del total anual de producción de la fibra de Vicugna pacos (alpaca); en el Perú, 6.4 millones de kilogramos., más del 50% corresponde a calidades inferiores (huarizo y gruesas), 35% a flecce y 8% a baby alpaca (calidades superiores) y el resto son fibras cortas y mermas (paja, tierra, otros desperdicios, etc.)25. En la Figura 1, podemos observar, la forma de clasificación de la fibra de Vicugna pacos (alpaca); dicha clasificación es realizada principalmente por los criadores de dicho camélido, para luego proceder a la venta de la misma.. Figura 1: Clasificación de fibra de Vicugna pacos (alpaca). 9.
(14) 1.2 Empresas en la región En este contexto, la industria textil de fibra de camélidos ha logrado edificar importantes. empresas,. altamente. especializadas. y tecnificadas. en. el. procesamiento y exportación de productos derivados de la fibra de los camélidos, generalmente ha estado desligada de la producción pecuaria, lo que no permitió una sana articulación productiva para generar mejores ingresos en la cadena de valor25. Esta industria se encuentra localizada principalmente nuestra ciudad y ha alcanzado un nivel tecnológico de punta y por ello está considerada como la mejor de Sudamérica y una de las mejores a nivel mundial, contrariamente a lo que pasa en el nivel de la producción animal, el conglomerado textil de la ciudad está constituido por: GRUPO INCA, MICHELL & CIA, SARFATTY y PROMPEX. En general, tanto en Perú como en Bolivia, se fabrican productos terminados con diseños y modelos propios, orientados a mercados de alta moda, aprovechando las excelentes características de las fibras especiales de camélidos andinos, tanto para el mercado nacional como internacional26. Las industrias de fibra de camélidos andinos, en Bolivia y Perú, mayoritariamente comercializan la fibra para exportación en materia prima semi procesada (tops, hilados, telas; hasta en un 70%) lo que ocasiona una gran debilidad en la determinación del precio, que generalmente se establece en los lugares de compra. 1.3 Características químicas de la fibra de Vicugna pacos (alpaca) El pelo es una proteína compuesta de varios aminoácidos. La queratina del pelo es un polímetro natural que presenta una composición química elemental: 50% de carbono, 16% de nitrógeno, 3.7% de azufre, 7% de hidrógeno y 23.5% de oxígeno. La fibra de Vicugna pacos (alpaca) se diferencia por tener un mayor contenido de azufre, 4.19%41. En la Tabla 2, se muestra la composición de la fibra de Vicugna pacos (alpaca); en ella, podemos apreciar que se caracteriza por un alto contenido de fibra (75-82%).. 10.
(15) Tabla 2 Composición de la fibra de Vicugna pacos (alpaca)27 Vicugna pacos COMPOSICIÓN (ALPACA) Fibra (%). 75-82. Suciedad y material vegetal (%). 3-10. Agua (%). 12. Sudor (%). 1. Grasa (%). 1-3. El porcentaje de fibra (Tabla 2), varía de acuerdo a la raza del animal así tenemos que en Vicugna pacos (alpaca) Huacaya color el porcentaje oscila entre 85-95%, mientras que en la Vicugna pacos (alpaca) Huacaya 68-88% y en la raza Suri 75-90%42. 2. Queratina De acuerdo a su composición la queratina es una proteína fibrosa simple; ya que, en su estructura solo se observan α-aminoácidos; así mismo, de acuerdo a la función biológica que desempeña se halla en el grupo de las proteínas estructurales. La queratina se encuentra en el pelo, las uñas, las plumas, el algodón y la lana. Su estructura molecular está constituida por cadenas paralelas de α-hélices, enrolladas hacia la derecha formando fibras muy fuertes, la mayoría de las queratinas poseen grandes cantidades de cisteína43.. Figura 2: Estructura de una de las formas de queratina. 11.
(16) 3. Líquidos iónicos Hace cien años, el químico alemán Walden hizo un descubrimiento sorprendente: una sal pura (nitrato de etilamonio, EAN), la cual era líquida a temperatura ambiente. Hasta entonces, nunca se sospechó que los iones podrían formar un líquido a temperatura ambiente; a menos que, se diluyeran en un disolvente molecular 1,44. EAN fue sorprendentemente similar al agua en muchos aspectos, ya era claro, incoloro, inodoro, con una densidad de tipo sólido (1.21g/mL) y poseía una viscosidad razonablemente alta. Sin embargo, la clave del hallazgo de Walden fue la conductividad eléctrica, una propiedad intrínseca a todos líquidos que contienen iones móviles1,45. La conductividad de EAN era consistente con una composición de (casi) puramente aniones y cationes. Esta conclusión se basó en estudios anteriores a Walden, en los que se propone una relación entre la viscosidad, conductividad molar y la densidad de electrolitos acuosos. Por estas razones, Walden es ampliamente acreditado con la concepción del campo de sales líquidas, a pesar de los informes de trabajados anteriores en la creación de materiales similares, con puntos de fusión justo por encima de la temperatura ambiente1,10. La ciencia de sales líquidas o "líquidos iónicos" (IL) ha progresado a pasos agigantados desde los días de Walden. En particular, las última tres décadas se han caracterizado por un crecimiento exponencial en publicaciones, con descubrimientos que abarcan toda la química46,47, tal es así ha superado sustancialmente sus raíces en la electroquímica y síntesis orgánica. Hoy en día, la investigación en IL es verdaderamente un área interdisciplinaria, con químicos, físicos, biólogos, ingenieros, y simuladores que los utilizan para hacer frente a importantes problemas científicos. Esto ha sido impulsado por el movimiento químico verde y la relativa facilidad con la que estos disolventes pueden integrarse en los sistemas existentes13,48-50. Los IL son sales con un punto de fusión bajo (por debajo de 100°C) 3. En el artículo original de Walden en EAN, se describió a los materiales como "sales libres de agua... que se funden a temperaturas relativamente bajas, sobre 100°C". Esta definición se reafirmó y codificó en un taller de la OTAN en Creta en 20001.. 12.
(17) Esta definición es importante ya que el campo es relativamente joven; el término "líquidos iónicos" fue acuñado originalmente en referencia a las escorias de silicato con puntos de fusión mayor a 1000K y materiales similares se han descrito en la literatura con nombres incluyendo "sales fundidas", "electrolito líquido puro", "sal líquida", "ionóforo" o "sal fundida a temperatura ambiente"1,13,51. 3.1 Síntesis de líquidos iónicos Los LI existen como líquidos a temperatura ambiente debido a su estructura química. El anión y catión se eligen precisamente para desestabilizar la fase sólida del cristal. Por lo tanto, si bien no existen reglas fijas a hacer un IL; en general, esto se puede lograr con una variedad de estructuras de iones mediante el equilibrio de las interacciones ión-ión y la simetría. 3.2 Clasificación de líquidos iónicos Los IL, como disolventes en general, se suelen clasificar en función de estructura química; sin embargo, esta clasificación resulta difícil debido a la similitud con otros compuestos, dependiendo de si el anión, catión, o un grupo funcional se considera más importante1. Los dos tipos más comunes son los prótico y apróticos, basados en la división bien establecida entre donador (próticos) y aceptor (apróticos) de protones1,45. a. Líquidos Iónicos Próticos (PIL) Se forman mediante la transferencia de un protón de un ácido de Bronsted a una base de Bronsted, de acuerdo con el Esquema 1. Esto conduce a características distintivas entre PIL y AIL, todos los PIL tienen un protón disponible para el enlace de hidrógeno, presión de vapor generalmente no despreciable, y algunos son medios destilables, donde su punto de ebullición se produce a una temperatura inferior a la descomposición45. Esto significa que PILs son generalmente más simples y más baratos de preparar en comparación con otras clases IL ya que no hay subproductos. 13.
(18) 𝐵 + 𝐴𝐻 → 𝐻𝐵+ + 𝐴− Esquema 1: Formación de PIL a travez de la transferencia protónica de ácido Bronsted (A) a una base Bronsted (B). El proceso de transferencia de protones se puede mejorar mediante el uso de ácidos y/o bases más fuertes, por lo tanto, lleva a una mayor fuerza de conducción para la transferencia de protones. Los valores de pKa de los ácidos y las bases pueden ser considerados como una indicación de con qué fuerza se transferirá un protón desde el ácido a la base, aunque debe tenerse en cuenta que el pKa que por lo general se considera para soluciones acuosas y puede no ser apropiado para los prospectos no acuosos45. Los cationes más utilizados en PILs están representados en la Figura 3, estos incluyen iones de amonio primario, secundario o terciaria, iones imidazol mono o di sustituidos, caprolactama, y los iones de guanidinio45.. R2 R1. NH. R1. R3. N. NH. R1 N. NH. R2 O NH. N NH2. N Figura 3: Cationes representativos usados en PIL. No se han representado la amplia gama de iones heterocíclicos que contienen nitrógeno en el anillo. El imidazol y otros anillos heterocíclicos pueden contener sustituyentes en cualquiera de los carbonos en el anillo, siempre y cuando el nitrógeno que contiene la carga positiva retenga un protón. Una gran variedad de aniones se han acoplado con estos cationes, los usados comúnmente se muestran en la Figura 445.. 14.
(19) O CF3CF2. F3 C. R. O. O O F3 C. S O. O. O. O. S. N. O. O N. S. O. N. O HO. O. O. CF3CHF2. O. O CF3. S. S. O. O. Figura 4: Aniones representativos usados en PIL. Estos aniones pueden ser ácidos orgánicos como carboxilatos, inorgánicos tal como el nitrato o sulfato de hidrógeno, fluorados tales como bis- (trifluorometanosulfonil) imida (TFSI), ácido trifluoroacético (TFA), y bis. (perfluoroethylsulfonyl). imida. (BETI),. tetrafluoroborato,. o. hexafluorofosfato) 45. b. Líquidos Iónicos Apróticos (AIL) Los AIL no comparten una característica estructural común al igual que los PIL, estos pueden abarcar una amplia gama de estructuras de aniones y cationes químicos, algunos de los cuales tienen la capacidad de formar enlaces puentes de hidrógeno, mientras que otros no1,2,7,52. La síntesis de AIL es generalmente más cara y complicada que la de los PIL, implicando a menudo reacciones múltiples. Esto es porque los iones se forman a partir de enlaces covalentes entre dos grupos funcionales. En la mayoría de casos, esto conduce a un disolvente que es más térmicamente y electroquímicamente estable que el correspondiente PIL1,13,14,53,54. c. Otras subclases de líquidos iónicos Varias otras subclases IL son reportados en la literatura, en base a las distintas características estructurales, por ejemplo, un centro quiral (IL quiral), un átomo/grupo paramagnético (IL magnético), un ión divalente (IL divalente), un ión polimérico o polimerizable (IL poliméricos), un resto de fluorocarbono (IL fluorado) 1.. 15.
(20) 3.3 Propiedades de los líquidos iónicos a. Pureza Las impurezas, tales como agua, halogenuros, sales orgánicas que no han reaccionado y los compuestos orgánicos, fácilmente se acumulan en los IL. Los usuarios deben ser conscientes de las impurezas que son de esperar, ya que pueden influir en las propiedades disolventes y/o interferir con el biocatalizador15,48,55. b. Polaridad Los IL son considerados generalmente como altamente polares, en razón de su naturaleza iónica, pero la realidad es mucho más accidentada. La polaridad del disolvente, que no debe confundirse con carácter hidrófilo, es un concepto complejo, y es muy poco probable que se defina una escala universal15,48,55. c. Propiedades disolventes y miscibilidad Muchos compuestos son suficientemente solubles en IL para llevar a cabo reacciones. Con respecto a sus propiedades disolventes estas son muy diferentes de líquidos moleculares atómicos, diatómicos o apróticos, pero se ha llegado a la conclusión, que se asemejan a los líquidos polares próticos, tales como ACN, N-metilpirrolidona, o metanol5,15,48,56-58. d. Estabilidad y viscosidad Son considerados altamente estables. Los IL dialquilimidazolio utilizados comúnmente son de hecho, termoestables hasta 300 ° C. Su viscosidad es alta comparada con disolventes moleculares y aumenta con la longitud de cadena, entre otros factores. En consecuencia, la difusión está destinada a ser lenta55. e. Líquidos iónicos: Aspectos verdes Una importante fuerza impulsora detrás del desarrollo IL es el deseo de procedimientos más ecológicos. Se ha propuesto el uso de líquidos iónicos como alternativas ambientalmente amigables para disolventes orgánicos volátiles3, 56,57. 16.
(21) 3.4 Aplicaciones y perspectivas de líquidos iónicos próticos Los PIL tienen aplicaciones en la cromatografía, en síntesis orgánica, en electroquímica, y como explosivos, así como aplicaciones adicionales en las que tener un protón disponible es esencial, como muchos usos biológicos y como medios conductores de protones5,47,53,57,58. Una aplicación potencialmente muy útil de líquidos iónicos apróticos polares, sería el uso de estos como un medio para la conversión de compuestos, tales como proteínas y carbohidratos, que son escasamente solubles en medios orgánicos comunes55. Hay un gran número de combinaciones de ácido-base potenciales que se puede utilizar para preparar nuevos PIL. Como una nueva clase de disolventes los PIL tienen una amplia gama de propiedades, aunque comparten en común que son solventes altamente polares, capaz de formar enlaces puente de hidrógeno45.. 17.
(22) CAPÍTULO II MATERIALES Y MÉTODOS 1. Materiales, reactivos y equipos La investigación propuesta es de tipo descriptiva, prospectiva y aplicativa. Así mismo de nivel explicativo. A continuación, se presentan los materiales, equipos y reactivos, utilizados en su realización: 1.1 Material de partida Para los ensayos de hidrolisis de fibra de Vicugna pacos (alpaca), se recolectará material de desecho de las empresas presentes en la cuidad, tales como MICHELL & CIA S.A. e INCALPACA.TPX S.A. 1.2 Materiales -. Sistema de reflujo. -. Termómetro. -. Plancha de calentamiento. -. Soportes y pinzas. -. Material de vidrio: Balón de tres bocas, adaptadores, buretas, vasos de precipitado, pipetas, probetas, entre otros.. 1.3 Reactivos -. Dietanolamina, 99.0%, Merck. -. Trietanolamina, 99.0%, Merck. -. Dietilamina, 99.5%, Sigma. -. N,N- dimetiletanolamina, 9.5% P.A Sigma Aldrich. -. Ácido fórmico, 98.0-100.0% P.A Loba-Chemie. -. Ácido acético glacial, 100.0%, Merck. -. Ácido fosfórico 88% Merck. -. Ioduro de potasio, Merck. -. Sulfato de cobre, Merck. -. Metanol PA, Merck 18.
(23) -. Tartrato de sodio y potasio, Merck. -. Azul de Comassie G-250. -. Etanol absoluto, Merck. 1.4 Equipos -. Centrifuga Thermo IEC Centra CL2. -. Equipo EASYPURE II. -. Viscosímetro Brookfield. -. Potenciómetro Orion 525-A. -. Conductímetro Orion 162. -. Balanza analítica Pioner Ohaus. 2. Metodología. En la ejecución de la presente investigación se decidió, dividir el trabajo en ocho etapas fundamentales, las cuales son detalladas a continuación: 2.1 Síntesis de líquidos iónicos próticos Para la síntesis de líquidos iónicos próticos, se utilizó un balón de tres bocas, equipado con: un termómetro, una bureta y la tercera boca será clausurada para evitar contaminaciones. Se colocó dentro del balón la amina, utilizada según sea el caso, en el volumen correspondiente a 0.1mol, que para la dietanolamina es 12mL, a la cual se le agregará el volumen correspondiente de ácido, utilizado según sea el caso; por ejemplo, para el ácido acético es 6mL. Mantener la mezcla en agitación constante por espacio de 1 hora32. Este procedimiento es el mismo para los ocho líquidos iónicos próticos que se utilizarán en esta investigación. Cabe mencionar que, los ácidos y bases utilizados para la síntesis se utilizaron sin purificación adicional. La reacción esperada en la síntesis de líquidos iónicos próticos se muestra en el Esquema 2.. 19.
(24) N HO. HO +. HO. O. O. NH O. Dimetilatenolamonio formiato Esquema 2: Reacción esperada en la síntesis de líquido iónico prótico (formiato de dimetiletanolamonio). N,N-dimetiletanolamina. Ac. fórmico. Una vez que la reacción se llevó a cabo, se procedió a un proceso de calentamiento del producto, a una temperatura de 160°C, en condiciones de agitación constante por un periodo de 2 horas, asegurando de esta forma el término de la reacción (ver Figura 5). Para eliminar el exceso de alguno de los reactivos, se realizó a un calentamiento adicional por un lapso de 1 hora, a una temperatura de 200°C.. Figura 5. Síntesis de líquidos iónicos próticos, 2 h agitación constante. 2.2 Tratamiento de la fibra de Vicugna pacos (alpaca) Lavar la fibra de Vicugna pacos (alpaca) las veces necesarias para eliminar todas las impurezas presentes en la misma, principalmente grasa, paja, excremento, tierra, entre otros; este lavado se realizará con detergente neutro. Una vez que se consiga una muestra limpia, se homogenizará la misma, para lo cual se procederá a cortar la fibra de Vicugna pacos (alpaca) en pequeñas porciones. 20.
(25) Una vez que se tienen pequeñas porciones de fibra, se realizará la eliminación de toda el agua presente en la misma, para lo cual se utilizará una estufa a 50 ° C durante 18 horas. 2.3 Hidrólisis de fibra de Vicugna pacos (alpaca) La hidrólisis de la fibra de Vicugna pacos (alpaca), previamente limpia y seca, se realizará en un matraz de fondo redondo de dos bocas, equipado con un condensador de reflujo, añadiendo pequeñas porciones de fibra de Vicugna pacos (alpaca) hasta que la fibra adicionada no pueda ser vista, el procedimiento se realiza en agitación constante a una temperatura determinada; que en el caso de esta investigación varía en un rango de 95 a 155°C. El tiempo necesario para la hidrolisis de cada porción de fibra deberá ser anotado, así mismo, se deberá mantener un control constante en la variación de la coloración del líquido iónico prótico utilizado en cada ensayo de disolución hasta encontrar las condiciones óptimas del proceso. 2.4 Caracterización del líquido iónico prótico Para caracterizar los líquidos iónicos próticos sintetizados se realizarán mediciones de pH, conductividad, viscosidad y densidad. a. pH En el caso de la medida de pH, primero realizar la verificación operacional del potenciómetro de trabajo, utilizando para ello los buffers pH 4, 7 y 10. Colocar las muestras a ser analizadas en tubos de 50 mL y realizar la lectura correspondiente, teniendo cuidado de que el electrodo se encuentre correctamente sumergido dentro de la solución (posición vertical) y anotar la lectura respectiva. b. Conductividad Para realizar la medida de conductividad, se verifica el equipo utilizando para ello la solución patrón de 1413 µS/cm. Una vez realizado este procedimiento, proceder sumergiendo el electrodo de forma que el bulbo se halle correctamente sumergido y anotar la lectura correspondiente. 21.
(26) c. Viscosidad Para la medida de viscosidad, nivelar la burbuja del equipo, configurar la velocidad adecuada, insertar la aguja correspondiente (2, 3, 4, 5, etc.), ingresar la aguja a la muestra en forma oblicua para evitar la formación de burbujas en la muestra y así, no obstaculizar la lectura, posicionar la aguja en forma vertical y colocarla en el nivel correspondiente y anotar la lectura. d. Densidad Para la medida de densidad, utilizar un picnómetro de 24. 373 mL, colocar el líquido iónico prótico y calentar a 25 C; una vez que se llegue a esta temperatura, pesar el picnómetro y anotar la lectura. Realizar los cálculos necesarios para obtener el valor de densidad correspondiente. 2.5 Espectroscopia infrarroja (FT-IR) Los espectros infrarrojos fueron llevados a cabo con un espectrofotómetro FTIR Nicolet 8700, cuyo rango de fiabilidad es en la región del infrarrojo mediano (4000 - 400cm-1), resolución de 4cm-1, en cada corrida se realizaron un total de 75 barridas utilizando un detector DTGS. Las muestras líquidas o semilíquidas fueron preparadas en forma de película sobre ventanas de ioduro de cesio. 2.6 Espectroscopia de Resonancia Magnética Nuclear (RMN) Los espectros de RMN-1H y RMN-13C fueron tomados en un espectrómetro de 300 MHz. Los desplazamientos químicos se presentan en ppm en la escala de δ, y la constante de acoplamiento está dada en Hz., las corridas de RMN se llevaron a cabo para todos los líquidos iónicos próticos sintetizados. Los solventes utilizados fueron cloroformo deuterado y dimetilsulfóxido. 2.7 Separación de la mezcla queratina- liquido iónico prótico Con el fin de obtener queratina regenerada la mezcla queratina – líquidos iónicos próticos, se lavó tres veces con metanol y sometida a centrifugación a 22.
(27) 6000 rpm por 5 minutos luego de cada lavado y se recolectó el precipitado en placas Petri. Una vez realizado el procedimiento anterior las muestras fueron llevadas a la estufa a 50 °C durante 1 hora. 2.8 Cuantificación de queratina Realizar un espectro de absorción a cada una de las muestras de disolución, para todas las temperaturas de trabajo, para lo cual se midió 2mL de muestra, esta se colocó en tubos eppendorf y fue centrifugada (Thermo IEC Centra CL2) por 10 minutos a 5000 rpm. Se tomó el sobrenadante y se realizó un barrido en el Espectrofotómetro Cary 60 UV-vis. En este trabajo de investigación se utilizarán dos técnicas colorimétricas para cuantificar proteínas totales, ya que no se cuenta con una metodología específica para queratina. Estos son el método de Biuret y el método de Bradford. -. Preparación de reactivos. a. Reactivo de Biuret Para la preparación de 200 mL del reactivo de Biuret, disolver 0.3 g de CuSO4 y 1.2 g de tartrato de Na y K en 100 mL de agua destilada. Posteriormente añadir 60 mL de NaOH al 10% y 5 mL de IK (0.4 g en 10 mL), finalmente llevar a volumen con agua destilada. La solución final que tiene un color celeste intenso y translúcido se guardó en un frasco plastificado. b. Reactivo de Bradford Para la preparación de 200 mL del reactivo de Bradford, pesar 20 mg del reactivo azul Comassie G-250, adicionar 20 mL de H3PO4 al 88% y 10 mL de etanol absoluto. Llevar a volumen, filtrar y guardar en frasco ámbar en oscuridad, la solución tiene una coloración inicial marrón tenue. -. Preparación de las curvas de calibración. 23.
(28) Para la elaboración de las curvas de calibración, preparar soluciones madre de 5000 y 500 ppm con albúmina de suero bovino (BSA). Luego calcular el volumen de las alícuotas necesarias para obtener concentraciones de 100, 250, 500, 750 y 1000 ppm en el caso del método de Biuret y 25, 50, 75, 100 y 150 ppm para el método de Bradford. Realizar este procedimiento se realizó por triplicado. Adicionar a cada fiola 1 mL del reactivo correspondiente, observar el cambio de coloración (en el caso del método de Biuret, dejar reaccionar durante 30 minutos) y realizar la lectura de absorbancia a 545 nm para el método de Biuret y a 595 nm para el método de Bradford. -. Lectura de muestras Para la lectura de las muestras tomar 400 µL, adicionar 1 mL del reactivo. de Biuret y llevar a 3 mL. En el caso del método de Bradford tomar 20 µL, adicionar 1 mL del reactivo de Bradford recientemente preparado y llevar a 2 mL. Proceder a la lectura de absorbancia en las longitudes de onda mencionadas anteriormente.. 24.
(29) CAPÍTULO III RESULTADOS Y DISCUSIÓN Se procedió a sintetizar los Líquidos Iónicos Próticos (PILs), propuestos en nuestra investigación, mediante neutralización ácido - base según el procedimiento descrito en los artículos de referencia, como se detalla a continuación: 1. Síntesis de líquidos iónicos próticos La síntesis de líquidos iónicos próticos procedió a través de la neutralización ácido – base, que consiste en la transferencia de un protón desde un ácido de Brönsted hasta una base del mismo tipo1,6,8,31,45,59-64 (Esquema 3), ocasionando la cesión de al menos un protón, el cual es capaz de promover puentes de hidrógeno6,17,62,65-67.. 𝐵 + 𝐴𝐻 ⇌ 𝐻𝐵+ + 𝐴− Esquema 3: Formación de líquidos iónicos próticos a travez de la transferencia protónica de ácido Bronsted (A) a una base Bronsted (B). Se sintetizaron ocho líquidos iónicos próticos (Tabla 3) por el método de neutralización; la base fue colocada inicialmente en un balón de tres bocas equipado con: un embudo de goteo, termómetro y la tercera boca fue clausurada para evitar contaminación. Se añadió gota a gota una cantidad equimolar del ácido, sobre el recipiente que contenía la base, la mezcla se mantuvo en agitación constante durante una hora. En la Tabla 3, se halla resumida la información de los nombres químicos, las estructuras químicas esperadas, el estado físico a temperatura ambiente de cada uno de los líquidos iónicos próticos respectivamente y finalmente la coloración de la sal resultante. Tres de los líquidos iónicos próticos, presentaron estado sólido a temperatura ambiente, estos fueron: formiato de trietanolamonio ([TEOA][HCOO]), acetato de trietanolamonio ([TEOA][CH3COO]) y acetato de dietilamonio ([DEA][CH3COO]), todos los líquidos iónicos próticos restantes presentaron estado líquido a temperatura ambiente. La coloración que presentaron, fue variada desde un color blanco para el [TEOA][HCOO], hasta un color caramelo oscuro en el caso de [TEOA][CH3COO].. 25.
(30) Tabla 3 Nombre, estructura, estado y apariencia de líquidos iónicos sintetizados PILs. Estructura. Abreviatura. Estado. Apariencia. [TEOA][HCOO]. Sólido. Cristales blancos. [DEOA][HCOO]. Líquido. [DEA][HCOO]. Líquido. HO. Formiato de trietanolamonio. NH HO O. O. OH. OH. HO N H2. Formiato de dietanolamonio. O. O. N H2. Formiato dietilamonio. O. Cristales amarillo pálido. Color caramelo. O. Color. Formiato de. NH. [DMEA][HCOO]. HO. dimetiletanolamina. O. Líquido. O. ligeramente amarillento. HO. Acetato de trietanolamonio. NH HO O. [TEOA][CH3COO]. Sólido. [DEOA][CH3COO]. Líquido. [DEA][CH3COO]. Sólido. [DMEA][CH3COO]. Líquido. Cristales caramelo oscuro. OH. O. OH. HO N H2. Acetato de. O. dietanolamonio. O. N H2. Acetato de dietilamonio. O. Color caramelo claro. Color caramelo claro. O. Acetato de. NH HO. dimetiletanolamina O. O. Color amarillo pálido. Fuente: Elaboración propia. 26.
(31) Adicionalmente, la temperatura fue controlada mediante un baño de hielo, debido a que la reacción de neutralización presentó exotermicidad68,69 en todos los casos (aproximadamente de 60°C a más), como se puede apreciar en la Figura 6.. Figura 6: Incremento de la temperatura al entrar en contacto el ácido y la amina, en la síntesis de PIL, alrededor de 60°C. El producto obtenido fue sometido a un calentamiento adicional por lapso de 1 hora, a una temperatura de 200°C, con el fin de eliminar el posible exceso de alguno de los reactivos (ver Figura 7). Una vez culminada la síntesis de líquidos iónicos próticos se evalúo sus principales características, particularmente en lo respecta a la transferencia de protones como se detalla a continuación.. Figura 7. Síntesis de líquidos iónicos próticos, 2 h agitación constante. Debido a que la síntesis de líquidos iónicos próticos se basa en un método de neutralización ácido-base62,70, que conduce a la transferencia de protones desde el ácido 27.
(32) a la base. Cuando se presenta un equilibro, fundamentalmente en una transferencia protónica, la base retorna el protón al ácido y viceversa17, siendo considerado una transferencia incompleta del protón. Para evitar este tipo de equilibrio, la literatura nos indica que se debe seleccionar el par ácido-base con una diferencia de pKa mayor a 4 17,45. . En la Tabla 4, podemos observar el ΔpKa de los ocho líquidos iónicos próticos. sintetizados en nuestra investigación, el que presentó una diferencia de pKa mayor fue el [DEA][HCOO], por lo tanto, de acuerdo a lo referido líneas arriba, debiera presentar una transferencia completa del protón. Por el contrario, el [TEOA] [CH3COO] presentó la menor diferencia de pKa, por lo que la transferencia protónica fue incompleta. Tabla 4 Diferencia de pKa de los líquidos iónicos próticos sintetizados PILs SINTETIZADOS ΔpKac [TEOA][HCOO]. 4.009. [DEA][HCOO]. 7.049. [DEOA][HCOO]. 5.129. [DMEA][HCOO]. 5.509. [TEOA[CH3COO]. 3.004. [DEA][CH3COO]. 6.044. [DEOA][CH3COO]. 4.129. [DMEA][CH3COO]. 4.504. C. los valores de pKa fueron tomados de tablas de constantes. Con respecto a las características organolépticas de los líquidos iónicos próticos sintetizados, como se observa en la Tabla 3, podemos destacar que tanto la coloración como el estado físico que presentaron fue muy variable; por ejemplo, se obtuvo cristales blanquecinos en el caso del [TEOA][HCOO] y un líquido espeso, ligeramente amarillento cuando nos referimos al [DMEA][HCOO].. 28.
(33) En la mayoría de los casos, los artículos científicos en lo que refiere a líquidos iónicos próticos, no realizan informe de las características organolépticas para sus productos sintetizados. Sin embargo; tenemos que, el producto de la síntesis del acetato de etilamonio es un líquido espeso, incoloro y transparente; mientras que el acetato de propilamonio es un líquido espeso, transparente o ligeramente amarillo62, en el caso del nitrato de N-butil-(N-hidroxietil) amonio y el trifluoro acetato de N-butil-(N-hidroxietil) amonio la mezcla de reacción cambió de incoloro a un líquido amarillento y viscoso71. En nuestro caso cinco productos de síntesis presentan características muy similares; es decir, son líquidos, tienden a ser más espesos que los reactivos iniciales y presentan coloraciones amarillentas. De acuerdo al trabajo realizado por investigadores australianos, el producto final de la síntesis de [DMEA][HCOO] es un líquido incoloro31, pudiendo tener una ligera variación por efecto de impurezas; nuestro producto de síntesis para el mismo líquido iónico prótico, presentó una ligera coloración “amarillo pálido”, lo que puede ser explicado por una potencial presencia de impurezas en alguno de los reactivos, estando en concordancia con el grupo de investigación australiano. 2. Recolección y tratamiento de la fibra de Vicugna pacos (alpaca) La fibra de Vicugna pacos (alpaca) que fue utilizada en el presente proyecto se adquirió de la empresa distribuidora Pitata SAC, Arequipa, Perú. La muestra correspondía a la categoría de fibra corta de acuerdo a la clasificación dada por el Instituto Nacional de Defensa de la Competencia y de la Protección de la Propiedad Intelectual (INDECOPI), raza Huacaya color blanco. Para obtener una fibra sin impurezas, se sometió a un tratamiento de lavado en forma reiterada con detergente neutro, para así eliminar los contaminantes presentes en la misma (grasa, paja, tierra, excremento, etc.). Una vez limpia la muestra, se cortó en pequeños segmentos de fibra y se secó en estufa a 50 °C durante 18 horas (ver Figura 8).. 29.
(34) Figura 8. Fibra corta de Vicugna pacos (alpaca) Raza huacaya lavada y secada en estufa a 50° C por 18 h. 3. Ensayos de disolución de fibras de Vicugna pacos (alpaca) Se llevaron a cabo pruebas preliminares de disolución de la fibra de Vicugna pacos (alpaca) con el sistema que se presenta en la Figura 9, se utilizó 5mL de líquido iónico prótico sintetizado y 10mg de fibra, la mezcla fue sometida a dos temperaturas, por un periodo máximo de 7 horas a condición de agitación constante.. Figura 9. Disolución de fibra corta de vicugna pacos (alpaca) Raza huacaya (lavada y secada en estufa por 18 h) en [DEOA][HCOO].. Los resultados de las pruebas de disolución realizadas se presentan en la Tabla 5, donde se muestra la temperatura de disolución (se tomaron dos temperaturas, 115 y 30.
(35) 140°C), tiempo de disolución y solubilidad de la fibra de Vicugna pacos (alpaca). Para el caso de [TEOA][HCOO], [DEA][HCOO], [TEOA][CH3COO] y [DEA][CH3COO] no se presentó actividad de disolución de la fibra de Vicugna pacos (alpaca), a pesar de haber sido sometidos hasta el tiempo límite de disolución. Los líquidos iónicos próticos que presentaron actividad de disolución fueron en orden de mayor a menor solubilidad fueron [DMEA][HCOO] >[DEOA][HCOO] > [DEOA][CH3COO], [DMEA][CH3COO] con valores de 10 > 5 > 4 = 4, respectivamente. Los líquidos iónicos próticos [DMEA][HCOO] y [DEOA][HCOO] presentaron un tiempo de disolución de la fibra de Vicugna pacos (alpaca) de 3 horas. Tabla 5 Pruebas de disolución para todos los líquidos iónicos próticos sintetizados Tiempoa. Solubilidadb. Solubilidadc. [TEOA][HCOO]. >7. -. -. [DEA][HCOO]. >7. -. -. [DEOA][HCOO]. 3. 5. 5. [DMEA][HCOO]. 3. 10. 10. [TEOA][CH3COO]. >7. -. -. [DEA][CH3COO]. >7. -. -. [DEOA][CH3COO]. 5. 4. 4. [DMEA][CH3COO]. 5. 4. PILs. a. b. 4 c. (horas), (mg fibra/mL líquidos iónicos próticos) a 115°C, (mg fibra/mL líquidos iónicos próticos) a 140°C. Sin embargo; estas pruebas preliminares muestran que la solubilidad puede realizarse a menor tiempo (3 horas) que lo reportado en la bibliografía31. En la Figura 10, se puede apreciar la disolución completa de la fibra de Vicugna pacos (alpaca) utilizando [DMEA][HCOO], ya que a simple vista no se observó restos del soluto. Así mismo, la cantidad de fibra hidrolizada en nuestra investigación es menor que la reportada en trabajos similares, que tienen como materia prima la queratina de la plumas (150mg/g)31; así como, los que utilizan como disolventes líquidos iónicos apróticos para extraer queratina a partir de plumas de pavo32, probablemente debido la diferencia de composición en los tipos de materias primas utilizadas para cada investigación.. 31.
(36) Figura 10 . Queratina disuelta en [DMEA][HCOO], 3 horas de agitación, 140°C.. A 115°C, ninguna de las muestras presentó capacidad de disolución, cuando incrementamos la temperatura a 140°C, pudimos observar que cuatro de los líquidos iónicos próticos presentaron capacidad de disolución de la fibra de Vicugna pacos (alpaca). La combinación del incremento de temperatura y la agitación aumentan el superficie activa de los polímeros y de esta forma pueden ser accesibles al solvente perdiendo los puentes de hidrógeno y probablemente la ruptura de puentes disulfuro. Por efecto de las pruebas preliminares, la investigación continuó con los dos líquidos iónicos próticos que presentaron la mayor solubilidad, estos fueron: formiato de dimetiletanolamina [DMEA][HCOO] y formiato de dietanolamina [DEOA][HCOO]. Por lo que, se procedió a la síntesis de estos líquidos iónicos próticos a mayor escala, manteniendo la relación equimolar, el producto obtenido se muestra en la Figura 11.. Figura 11: [DMEA][HCOO] y [DEOA][HCOO] sintetizados a mayor escala. 32.
(37) 4. Caracterización de líquidos iónicos próticos La característica más resaltante de los líquidos iónicos próticos es su ionicidad así tenemos que, idealmente la transferencia de protones es completa del ácido a la base, de manera que las únicas especies individuales presentes son el catión y el anión resultante. En realidad, existe la probabilidad de que la transferencia de protones sea incompleta, lo que resultará en la presencia de especies de ácidos y bases neutras45. Hasta el momento no existe ningún método "estándar" para la determinación de la ionicidad de los líquidos iónicos próticos, ni una clasificación en lo que debería considerarse “líquidos iónicos próticos puros”. Por ello se han utilizado diferentes técnicas para proporcionar información sobre la ionicidad de estos, incluyendo RMN, cambios en las propiedades térmicas en función de la estequiometría, la espectroscopia de IR y la conductividad iónica en la forma de un diagrama de Walden45,72-76. Estas técnicas generalmente dan una medida cualitativa de la naturaleza iónica de los líquidos iónicos próticos. Así mismo, se han reportado que varias propiedades fisicoquímicas de líquidos iónicos próticos se correlacionan con la ΔpKa45,66,72,73; es decir que, a mayor sea esta diferencia el líquido iónico prótico será considerado ideal. 4.1 Características físico químicas de líquidos iónicos próticos Los parámetros físico químicos analizados fueron pH, densidad, viscosidad y conductividad para los líquidos iónicos próticos seleccionados anteriormente; para lo cual, se utilizó en el caso de la medida de pH el Potenciómetro Orion 525-A, que cuenta con un rango de medición de 0 a 14 y una resolución de 0.001. Para la medida de conductividad se utilizó el Conductímetro Orion 162, con un rango de medición de 0 a 199µS/cm, resolución de 0.1µS/cm; ambos equipos fueron previamente verificados para su correcto funcionamiento. Para la medida de viscosidad se utilizó el Viscosímetro Brookfield DV2T a 120 rpm, aguja número 4. En el caso de la determinación de densidad la lectura se realizó en la balanza analítica Pioner Ohaus a 25°C utilizando un picnómetro con un volumen de 24.373mL, tal como se muestra en la Figura 12.. 33.
(38) Figura 12: Instrumentos de medición utilizados en la lectura de pH, conductividad, viscosidad y densidad para [DMEA][HCOO] y [DEOA][HCOO]. Los resultados de las pruebas de caracterización fisicoquímica se muestran en la Tabla 6, se realizaron lecturas por triplicado de todos los parámetros. Tabla.6 Características fisicoquímicas de líquidos iónicos próticos Parámetros. [DMEA][HCOO]. [DEOA][HCOO]. pH. 7.603 ± 0.006. 7.203 ± 0.006. Conductividada. 4.847 ± 0.006. 1.353 ± 0.008. Densidadb. 1.095 ± 0.000. 1.092 ± 0.000. Viscosidadc. 110.0 ± 0.034. 158.3 ± 0.053. a. (µS/cm), b(g/mL), c(cP). En cuanto a la densidad en relación al ΔpKa, podemos observar en nuestra investigación que en el caso de [DEOA][HCOO] el ΔpKa = 5.129, y para [DMEA][HCOO] ΔpKa = 5.509, aunque ambos contienen el mismo anión pero diferente catión, el volumen molecular del [DEOA][HCOO] es mayor que el del [DMEA][HCOO], el ΔpKa parece seguir el sentido contrario del volumen molecular, esto se halla en concordancia con observaciones realizadas para líquidos iónicos próticos que mantienen el mismo anión pero diferentes cationes77, el autor (Chhotaray, et al. 2014) nos manifiesta que cuando esto se presenta la densidad va en sentido contrario del ΔpKa, esto mismo podemos observar al comparar la densidad con respecto de la ΔpKa.. 34.
(39) Así mismo, los líquidos iónicos próticos estudiados tienen densidades que guardan relación con los valores reportados para el formiato de etilamonio con un valor de 1.039g/mL, propionato de etilamonio con 1.018g/mL, formiato de etanolamina 1.184g/mL, acetato de etanolamina con 1.176g/mL45, formiato de dimetiletilendiamina con 1.030g/mL12. La densidad de los compuestos depende del tipo de aniones y cationes, tamaño y forma de los iones y las interacciones ión – ión. Generalmente, un mayor tamaño de aniones conduce a una mayor densidad y un volumen más grande del catión orgánico conduce a una menor densidad16,71,78,79. La longitud de la cadena del radical alquilo también tiene un efecto en las propiedades de los líquidos iónicos próticos, de acuerdo con investigaciones previas11,12,77,80, la densidad y la velocidad del sonido disminuyen; mientras que, la viscosidad aumenta al incrementarse la longitud de la cadena alquilo en el lado catiónico. Lo que guarda relación en nuestra investigación, ya que en el caso del [DEOA][HCOO] al tener un radical alquilo más complejo, en el lado catiónico, presenta mayor viscosidad que el [DMEA][HCOO]. La conductividad de los líquidos iónicos próticos parece ser que se rige por su movilidad iónica y tiene un comportamiento similar a la viscosidad81-84. Los iones más pequeños con pocas interacciones inter iónicas muestran altos valores de conductividad y viceversa. Por ejemplo, en un estudio realizado en el trifluoro acetato de N-butil-(N-hidroxietil) y el nitrato de N-butil-(N-hidroxietil) amonio la conductividad del trifluoro acetato muestra una disminución más significativa que el nitrato, debido a la menor movilidad y la desigualdad en el tamaño del anión71. Esta relación guarda concordancia con los valores obtenidos en esta investigación; tal es así que, el [DMEA][HCOO] al tener como catión a la dimetiletanolamina, un ión de menor volumen molecular que la dietanolamina, presenta un valor mayor de conductividad (4.847 µS/cm). El radical hidroxilo presente en la cadena lateral catiónica tiene un efecto pronunciado sobre todas las propiedades experimentales, debido al potencial puente de hidrógeno que pudiera encontrarse adicionalmente, además de las interacciones de Coulomb y Van der Waals45,77.. 35.
(40) 4.2 Espectroscopia infrarroja (FT-IR) de líquidos iónicos próticos Todos los líquidos iónicos próticos fueron enviados para su análisis mediante FT-IR, en el Laboratorio de Materiales del Instituto Mexicano del Petróleo, con la colaboración de la Dra. Natalya Likanova Victoronova. Los líquidos iónicos próticos de mejor desempeño, se analizarán a continuación los cuales son: [DMEA] [HCOO] y [DEOA] [HCOO]. Para el [DMEA] [HCOO], es necesario observar en el espectro de FT-IR las señales correspondientes a los grupos funcionales principales, como es el carboxilo (suma del grupo carbonilo y grupo hidroxilo), la identificación de la amina cuaternaria, el grupo hidroxilo del etanol, como los grupos metilo. En la Figura 13, podemos observar que el pico que se halla marcado en la elipse de color rojo, con el número 1, presenta una longitud de onda entre 1020 – 1220 cm-1, según tablas esta vibración corresponde a la interacción entre un átomo de carbono y un nitrógeno, que pueden ser aminas primarias, secundarias, terciarias o cuaternarias, normalmente esta vibración suele indicarse como una interacción sp3-sp3 entre el carbono y nitrógeno. Con la presencia del pico entre las longitudes de onda 3200 – 3500 cm-1, podríamos concluir en forma contundente que nos hallamos en presencia de una amina cuaternaria, pero en nuestro espectro, aunque tenemos la señal en la elipse 5 que corresponde a la vibración entre un enlace nitrógeno – hidrógeno, esta se halla solapada por la señal del grupo hidroxilo (elipse 4), con una banda intensa y ancha entre las longitudes de 2400 – 3300 cm-1, probablemente debido a un enmascaramiento por efecto esteárico de los sustituyentes de la amina. Para el grupo carbonilo se presenta en la elipse 2, en el rango de longitud de onda entre 1550 – 1650 cm-1, con una banda en 1613 cm-1, confirmando la presencia del anión formiato. Los grupos metilo estarán caracterizados por las vibraciones carbono – hidrógeno, esta señal la podemos encontrar en la elipse 3, con un rango en la longitud de onda entre 2800 – 3000 cm-1, estas señales encontradas en el espectro de FT-IR, nos confirman los grupos funcionales esperados para nuestro líquido iónico prótico71,77,85.. 36.
(41) 4. O-H. 1. C-N. 3. C-H. 5. 2. C=O. N-H. Figura 13: Espectro FT-IR de [DMEA] [HCOO]. Para el caso del [DEOA][HCOO], se debería esperar las señales correspondientes a los grupos funcionales como el carboxilo (suma de las funciones carbonilo e hidroxilo), la identificación de la amina cuaternaria, el grupo hidroxilo del etanol, y una fuerte señal acoplada de los hidrógenos enlazados al nitrógeno. El espectro para el [DEOA][HCOO] se muestra en la Figura 14, en ella podemos hallar con la elipse 1, la señal correspondiente a la vibración del enlace carbono nitrógeno, característico para sistemas sp3-sp3, el cual presenta un pico muy característico en 1339 cm-1, en este caso la elipse 5, nos muestra claramente la presencia de enlaces nitrógeno hidrogeno a una longitud de onda entre 3200 – 3500 cm-1, con un pico en 3479 cm-1, lo que nos indica en forma contundente la presencia de este tipo de enlace, debido a la estructura, los dos hidrógenos que se hallan unidos al nitrógeno, pueden estar generando esta característica señal. El grupo carbonilo, en la Figura 14 se halla claramente representado por una banda intensa en la longitud de onda de 1598 cm-1 (elipse 2), con la presencia de la banda ancha entre 2400 – 3300 cm-1, correspondiente al grupo hidroxilo (elipse 4), podemos concluir la existencia del anión. Adicionalmente, los enlaces carbono hidrógeno vibran en la región 2600 – 3000 cm-1,. 37.
(42) correspondientes a los grupos CH2 propios del etanol como se aprecia en la elipse 3.. 4. O-H. 3. C-H. 5. 1. C-N. 2. N-H. C=O. Figura 14: Espectro FT-IR de [DEOA] [HCOO]. Las señales obtenidas para los espectros FT-IR, están en concordancia con las reportadas en la literatura, tal es el caso de la banda en el rango de 3500 – 3200cm-1, muestra el estiramiento del enlace N-H17,60,68,86,O-H17,60,68,77; mientras que la banda alrededor de 1600 cm-1 confirma la presencia del carbonilo 17,60,68,86. Para el caso del estiramiento del enlace C-N la banda característica se encuentra entre 1220 – 1020cm-1. 60,71. , lo cual también se halla reflejado en nuestro. espectros. En el anexo 1, depositamos la información de los espectros de FT-IR para los demás líquidos iónicos próticos sintetizados en el presente trabajo de investigación. En todos ellos encontramos las mismas características descritas líneas arriba para los dos líquidos iónicos próticos de mejor desempeño en la disolución de la fibra de Vicugna pacos (alpaca), lo que nos hace suponer que, al presentar todos los grupos funcionales esperados, son los líquidos iónicos próticos que esperábamos sintetizar.. 38.
(43) 4.3 Espectroscopia de Resonancia Magnética Nuclear (RMN) de líquidos iónicos próticos Todos los líquidos iónicos próticos fueron enviados para su análisis mediante RMN-1H y RMN-13C, al Laboratorio de Materiales del Instituto Mexicano del Petróleo, con la colaboración de la Dra. Natalya Likanova Victoronova. Los líquidos iónicos próticos de mejor desempeño, se analizarán a continuación los cuales son: [DMEA][HCOO] y [DEOA][HCOO]. El espectro de RMN-1H del [DMEA] [HCOO], teóricamente deberíamos esperar una señal singlete que integres a 6 debido a los grupos metilo, un singlete que integra a uno, debido al hidrógeno que protona al nitrógeno, un singlete que integra a uno, correspondiente al protón unido al grupo carboxilo, un triplete y un cuarteto que integren a dos protones cada uno, correspondientes al CH2 de la cadena alifática del alcohol y una última señal singlete que integra a uno, correspondiente al hidrógeno del grupo hidroxilo. En la Figura 15, se muestra el espectro, con las señales en: 2.771(S), 3.069(T), 3.880(Q), 8.534(S) y 9.270(S), aparentemente solo poseemos 5 señales, pero revisando la literatura, podemos notar que el protón del hidroxilo y el protón de la amina cuaternaria se han solapado por lo que la señal de 9.270 a pesar de ser un singlete es un poco más ancha de lo normal. En la cual observamos que se ha producido la transferencia completa de protones en todo el líquido iónico prótico sintetizado, por la ausencia de la señal correspondiente al protón del hidroxilo del grupo carboxílico, también sabemos que ΔpKa es mayor que 417,45 como condición previa para la transferencia de protones completa85. En la Figura 16, se presenta el RMN-13C, deberiamos esperar cuatro señales correspondientes a los tipos de carbono presentes en nuestra estructura, y esto es corroborado en forma positiva en: 43.47: 56.49: 60.05: 169.25, claramente se observa lo esperado, es más con la presencia de la señal en 169.25 queda confirmada la presencia del formiato.. 39.
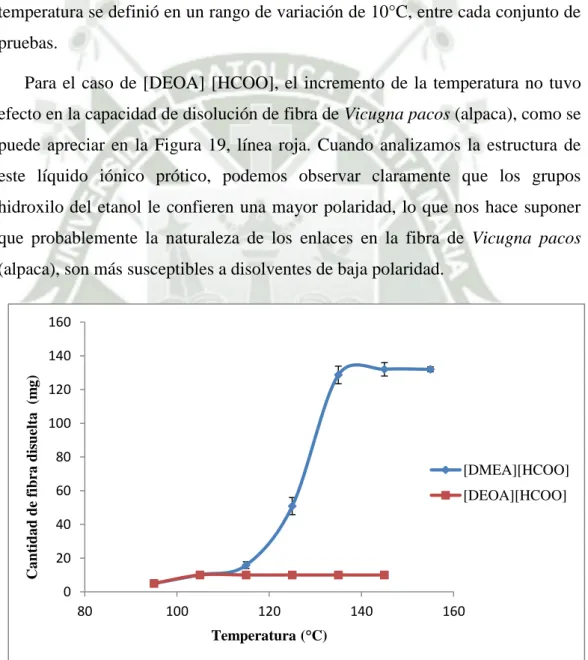
(44) 1. 2CH3 2. CH2. 3. CH2. 4. HCOO. 5. -. +. NH y OH. Figura 15: Espectro RMN-1H de [DMEA] [HCOO]. 40.
(45) 1. 2CH3. 2. CH2 3. CH2. 4. HCOO. 13. Figura 16: Espectro RMN-. -. C de [DMEA] [HCOO] 41.
Figure




+7
Documento similar



![Figura 11: [DMEA][HCOO] y [DEOA][HCOO] sintetizados a mayor escala](https://thumb-us.123doks.com/thumbv2/123dok_es/7177932.420784/36.892.118.844.17.512/figura-dmea-hcoo-deoa-hcoo-sintetizados-mayor-escala.webp)
![Figura 14: Espectro FT-IR de [DEOA] [HCOO]](https://thumb-us.123doks.com/thumbv2/123dok_es/7177932.420784/42.892.139.774.182.806/figura-espectro-ft-ir-de-deoa-hcoo.webp)