EVALUACIÓN DE LA ACTIVIDAD CITOTÓXICA DE LOS EXTRACTOS ETANÓLICOS DE LAS PLANTAS Annona muricata, Annona cherimola y Physalis peruviana EN LA LINEA CÉLULAR MCF-7 DE
ADENOCARCINOMA DE SENO
DANIELA ARDILA DURANGO
Trabajo de grado presentado como requisito para optar al título de
MICROBIOLOGA INDUSTRIAL
PONTIFICIA UNIVERSIDAD JAVERIANA FACULTAD DE CIENCIAS
DEPARTAMENTO DE MICROBIOLOGIA INDUSTRIAL BOGOTÁ, D.C.
EVALUACIÓN DE LA ACTIVIDAD CITOTÓXICA DE LOS EXTRACTOS DE LAS PLANTAS Annona muricata, Annona cherimola y Physalis peruviana EN LA LINEA CÉLULAR MCF-7 DE
ADENOCARCINOMA DE SENO
DANIELA ARDILA DURANGO
PONTIFICIA UNIVERSIDAD JAVERIANA FACULTAD DE CIENCIAS
DEPARTAMENTO DE MICROBIOLOGIA INDUSTRIAL BOGOTÁ, D.C.
JUNIO, 2014 ______________________
DRA. CONCEPCION PUERTA BULA DECANA ACADEMICA FACULTAD DE CIENCIAS
_____________________
DRA. JANETH DEL CARMEN ARIAS PALACIOS DIRECTORA CARRERAS DE MICROBIOLOGIA
EVALUACIÓN DE LA ACTIVIDAD CITOTÓXICA DE LOS EXTRACTOS ETANÓLICOS DE LAS PLANTAS Annona muricata, Annona cherimola y Physalis peruviana EN LA LINEA CÉLULAR MCF-7 DE
ADENOCARCINOMA DE SENO
DANIELA ARDILA DURANGO
_____________________________ DIRECTOR
RICARDO VERA BRAVO. PhD DOCENTE DEPARTAMENTO DE QUÍMICA GRUPO DE INVESTIGACIÓN FITOQUÍMICA
UNIVERSIDAD JAVERIANA
_______________________________ CODIRECTORA
GINA MARCELA MENDEZ. PhD, MSc
DOCENTE UNIVERSIDAD DE CIENCIAS APLICADAS Y AMBIENTALES (UDCA)- GRUPO DE INVESTIGACIÓN
PRONAUDCA Y GIBGA
__________________________ CODIRECTOR
JORGE ELIECER ROBLES CAMARGO, PhD. MSc DOCENTE DEPARTAMENTO DE QUÍMICA GRUPO DE INVESTIGACIÓN FITOQUÍMICA
UNIVERSIDAD JAVERIANA
__________________________ EVALUADOR/JURADO
JHON JAIRO SUTACHAN RUBIO, PhD. MSc. DOCENTE DEPARTAMENTO DE NUTRICIÓN Y BIOQUÍMICA-LINEA DE INVESTIGACIÓN DE CANALES
IONICOS
PONTIFICIA UNIVERSIDAD JAVERIANA FACULTAD DE CIENCIAS
DEPARTAMENTO DE MICROBIOLOGIA INDUSTRIAL BOGOTÁ, D.C.
NOTA DE ADVERTENCIA
Artículo 23 de la resolución N°13 de julio de 1946
AGRADECIMIENTOS
A mi familia y especialmente a mi madre y a mi hermana por creer en mí, apoyarme durante todo este duro proceso, y hacer lo posible por ayudarme a cumplir mis metas, porque sin sus esfuerzos esto no hubiera sido posible.
A mi director de tesis el profesor Ricardo Vera, por aceptarme en el grupo de investigación fitoquímica, por llevar un seguimiento continuo, por su paciencia y acompañamiento a lo largo de este proyecto y por creer en mis habilidades y siempre darme fuerza para seguir adelante.
A la profesora Gina Méndez profesora de la Universidad de Ciencias aplicadas y ambientales, por brindarme su conocimiento y guiarme en el aprendizaje respecto a las células, cultivos celulares y todos sus afines, para poder realizar esa parte experimental exitosamente.
Al profesor Jorge Robles por su acompañamiento, por sus enseñanzas y aporte en el conocimiento en el campo de la fitoquímica.
Agradezco de igual forma a todos los integrantes del grupo de investigación en fitoquímica por guiarme y brindarme ayuda cuando lo requerí, para llevar a cabo un experimento.
Tabla de contenido
RESUMEN ... 10
1. INTRODUCCIÓN ... 1
2. JUSTIFICACION Y PLANTEAMIENTO DEL PROBLEMA ... 3
2.1. Pregunta de investigación ... 3
2.2. Planteamiento del problema y justificación ... 3
3. MARCO TEORICO-REFERENTES CONCEPTUALES ... 4
3.1. Productos naturales bioactivos y metabolitos secundarios ... 4
3.2. Descripción, Clasificación y distribución geográfica del género Annona y Physalis ... 4
3.2.1. Genero Annona ... 4
3.2.2. Genero Physalis ... 8
3.3. Uso y antecedentes fitoquímicos del género Annona y Physalis ... 9
3.3.1. Género Annona ... 9
3.3.2. Género Physalis ... 9
3.4. División celular y el origen del cáncer ... 9
3.5. Anatomía del seno y cáncer de seno ... 9
3.6. Incidencia y mortalidad. ... 10
3.7. Tratamientos para el cáncer ... 12
3.8. Clasificación de medicamentos quimioterapéuticos. ... 12
3.8.1. Agentes alquilantes ... 12
3.8.2. Antimetabolitos ... 12
3.8.3. Antibióticos contra el cáncer ... 12
3.8.4. Inhibidores de la topoisomerasa ... 13
3.8.5. Inhibidores de la mitosis ... 13
3.8.6. Terapia hormonal ... 13
3.8.7. Otros medicamentos quimioterapéuticos ... 13
3.8.8. Terapias dirigidas... 13
3.8.9. Agentes de diferenciación ... 13
3.8.10. Inmunoterapia ... 14
4. OBJETIVOS ... 15
4.1. Objetivo general ... 15
5. METODOLOGIA ... 16
5.1. Diseño de la investigación ... 16
5.2. Recolección y clasificación del material vegetal ... 16
5.3. Obtención de extractos ... 16
5.4. Pruebas químicas preliminares ... 17
5.5. Cultivo y tratamiento de las células ... 20
5.6. Evaluación de la actividad citotóxica de los extractos ... 21
5.7. Análisis estadístico ... 21
6. RESULTADOS Y DISCUSIÓN ... 22
6.1. Extracción ... 22
6.2. Identificación cualitativa de metabolitos secundarios. ... 22
6.3. Cultivo celular ... 27
6.4. Ensayo citotóxico... 28
7. CONCLUSIONES Y RECOMENDACIONES ... 38
8. BIBLIOGRAFÍA ... 39
INDICE DE FIGURAS
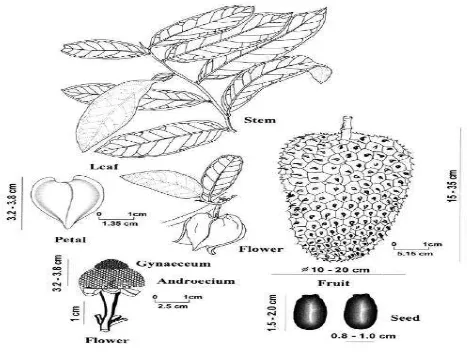
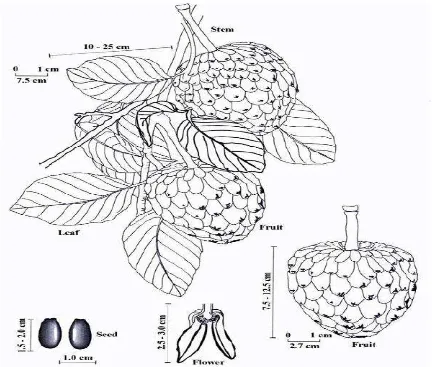
FIGURA 1. PARTES Y CARACTERÍSTICAS DE LA PLANTA ANNONA CHERIMOLA. IMAGEN TOMADA DE (PINTO, 2005).. 6 FIGURA 2. PARTES Y CARACTERÍSTICAS DE LA PLANTA ANNONA CHERIMOLA. IMAGEN TOMADA DE PINTO, 2005. ... 7
FIGURA 3. INCIDENCIA Y MORTALIDAD SEGÚN EL TIPO DE CÁNCER, ESTANDARIZADA POR EDADES DE HOMBRES Y MUJERES. IMAGEN TOMADA DE OMS (2012). GLOBOCAN.IARC.FR. ... 10
FIGURA 4. INCIDENCIA Y MORTALIDAD DE CÁNCER DE SENO EN EL MUNDO. IMAGEN TOMADA DE OMS (2012). GLOBOCAN.IARC.FR... 11 FIGURA 5. REACCIÓN DE LA PRUEBA DE SHINODA. IMAGEN TOMADA DE
HTTP://UPLOAD.WIKIMEDIA.ORG/WIKIPEDIA/COMMONS/9/90/SHINODA_TEST.PNG ... 18
FIGURA 6. REACCIÓN DE LA PRUEBA DE CLORURO FÉRRICO. IMAGEN TOMADA DE HTTP://LH5.GGPHT.COM ... 18 FIGURA 7. REACCIÓN DE LA PRUEBA DE ANTRONA. IMAGEN TOMADA DE HTTP://INTRANET.TDMU.EDU.UA ... 18 FIGURA 8. REACCIÓN DE LA PRUEBA DE DRAGENDORFF. IMAGEN TOMADA DE
HTTP://ES.SCRIBD.COM/DOC/38898384/LA-REACCION-DE-VITALI ... 19
FIGURA 9. REACCIÓN DE LA PRUEBA DE LIERBERMAN-BURCHARD. IMAGEN TOMADA DE
HTTP://UPLOAD.WIKIMEDIA.ORG ... 19
FIGURA 10. REACCIÓN DE LA PRUEBA DE BALJET. IMAGEN TOMADA DE HTTP://INTRANET.TDMU.EDU.UA ... 20 FIGURA 11. REACCIÓN QUÍMICA DE LA PRUEBA DE HIDROXAMATO FÉRRICO. IMAGEN TOMADA DE
HTTP://1.BP.BLOGSPOT.COM ... 20
FIGURA 12. RESULTADOS DE PRUEBAS QUÍMICAS PRELIMINARES PARA EL EXTRACTO DE SEMILLAS DE ANNONA MURICATA [A] EXTRACTOS REFERENTES, [B] PRUEBAS PARA EXTRACTOS ETANÓLICOS: (1) PRUEBA DE SHINODA, (2) PRUEBA DE FECL3, (3) PRUEBA DE ANTRONA, (4) PRUEBA DE DRAGENDORFF Y (5) PRUEBA DE LA ESPUMA. [C] PRUEBAS PARA FRACCIONES EN ÉTER DE PETRÓLEO: (1) PRUEBA DE HIDROXAMATO FÉRRICO, (2) PRUEBA DE BALJET, (3) PRUEBA DE SALKOWSKI Y (4) PRUEBA DE LIERBERMANN-BURCHARD. ... 24
FIGURA 14. RESULTADOS DE PRUEBAS QUÍMICAS PRELIMINARES PARA EL EXTRACTO DE SEMILLAS DE ANNONA CHERIMOLA. [A] EXTRACTOS REFERENTES, [B] PRUEBAS PARA EXTRACTOS ETANÓLICOS: (1) PRUEBA DE SHINODA, (2) PRUEBA DE FECL3, (3) PRUEBA DE ANTRONA, (4) PRUEBA DE DRAGENDORFF Y (5) PRUEBA DE LA ESPUMA. [C] PRUEBAS PARA FRACCIONES EN ÉTER DE PETRÓLEO: (1) PRUEBA DE HIDROXAMATO FÉRRICO, (2) PRUEBA DE BALJET, (3) PRUEBA DE SALKOWSKI Y (4) PRUEBA DE LIERBERMANN-BURCHARD. ... 26 FIGURA 15. RESULTADOS DE PRUEBAS QUÍMICAS PRELIMINARES PARA EL EXTRACTO HOJAS Y TALLOS DE P.
PERUVIANA. [A] EXTRACTOS REFERENTES, [B] PRUEBAS PARA EXTRACTOS ETANÓLICOS: (1) PRUEBA DE SHINODA, (2) PRUEBA DE FECL3, (3) PRUEBA DE ANTRONA, (4) PRUEBA DE DRAGENDORFF Y (5) PRUEBA DE LA ESPUMA. [C] PRUEBAS PARA FRACCIONES EN ÉTER DE PETRÓLEO: (1) PRUEBA DE HIDROXAMATO FÉRRICO, (2) PRUEBA DE BALJET, (3) PRUEBA DE SALKOWSKI Y (4) PRUEBA DE LIERBERMANN-BURCHARD. ... 27 FIGURA 16. FOTOGRAFÍA ENSAYO DE MTT DE CRISTALES DE FORMAZAN SIN DILUIR ... 29 FIGURA 17. GRÁFICO COMPARACIÓN DEL EFECTO CITOTÓXICO DE LOS EXTRACTOS DE A. MURICATA (GES), A.
CHERIMOLA (CEH Y CES) Y PHYSALIS PERUVIANA (UHT) EN LA LÍNEA CELULAR MCF-7. [A] GRÁFICO DE DISPERSIÓN Y [B] GRÁFICO BARRAS EN 3D. ... 30
FIGURA 18. GRÁFICO COMPARACIÓN DEL EFECTO CITOTÓXICO DE LOS EXTRACTOS DE A. MURICATA (GES), A. CHERIMOLA (CEH Y CES) Y PHYSALIS PERUVIANA (UHT) EN LA LÍNEA CELULAR HEK-293... 31
FIGURA 19. GRAFICAS EFECTO CITOTÓXICO DEL EXTRACTO DE SEMILLA DE ANNONA MURICATA EN LAS LÍNEAS CÉLULARES MCF-7 Y HEK-293. ... 33
FIGURA 20. GRÁFICO EFECTO CITOTÓXICO DEL EXTRACTO DE HOJAS DE ANNONA CHERIMOLA EN LAS LÍNEAS
CÉLULARES MCF-7 Y HEK-293. ... 34
FIGURA 21. GRÁFICO EFECTO CITOTÓXICO DEL EXTRACTO DE SEMILLAS DE ANNONA CHERIMOLA EN LAS LÍNEAS CÉLULARES MCF-7 Y HEK-293. ... 35
FIGURA 22. GRÁFICO EFECTO CITOTÓXICO DEL EXTRACTO DE HOJAS Y TALLOS DE PHYSALIS PERUVIANA EN LAS LÍNEAS CÉLULARES MCF-7 Y HEK-293. ... 37
FIGURA 23. GRÁFICO DE RESIDUALES PARA PRUEBA DE HOMOGENEIDAD. ... ¡ERROR!MARCADOR NO DEFINIDO. FIGURA 24. GRÁFICO DE QQPLOT PARA PRUEBA DE NORMALIDAD Y PRUEBA DE SHAPIRO-WILK. ... ¡ERROR!
MARCADOR NO DEFINIDO.
INDICE DE TABLAS
TABLA 1. CLASIFICACIÓN TAXONÓMICA DE LA ESPECIE ANNONA MURICATA Y ANNONA CHERIMOLA ... 5
TABLA 2. CLASIFICACIÓN TAXONÓMICA DE LA ESPECIE PHYSALIS PERUVIANA. ... 8
TABLA 3. PESOS DEL MATERIAL SECO-MACERADO Y CANTIDAD DE SOLVENTE UTILIZADO. ... 17
TABLA 4. PESO DE 10 ML DE EXTRACTOS TOTALES CONCENTRADOS. ... 17
TABLA 5. PESOS Y RENDIMIENTO DE LOS EXTRACTOS. ... 22
RESUMEN
1
1. INTRODUCCIÓN
La organización mundial de la salud (OMS) ha clasificado al cáncer como el responsable del 63% de muertes en todo el mundo (Sawadogo W et al. 2012), por ende su relevancia en la búsqueda de nuevos medicamentos con actividad anticancerígena.
El cáncer causa alrededor de 3,2 millones de muertes al año, por lo que el índice de mortalidad según la sociedad americana de cáncer constituye el 2% al 3% de las muertes anuales registradas a nivel mundial (Unnati S, et al. 2013). Dentro de los cánceres con mayor importancia se encuentra el cáncer de seno, puesto que es el más común entre las mujeres a nivel mundial (OMS 2013) y la primera causa de muerte en el mundo y la tercera en Colombia (Liga colombiana contra el cáncer, 2013).
El cáncer de seno exhibe una notable heterogeneidad, debido a la alteración en los receptores hormonales (estrógeno, progesterona), el receptor del factor de crecimiento epidérmico humano (HER2/neu), tamaño del tumor, grado y estado ganglionar; por lo tanto, se plantean diferentes necesidades de tratamiento y esto lleva a la búsqueda de nuevos fármacos para el tratamiento y control de esta enfermedad (Carvalho A, et al.2012).
Las sustancias derivadas de plantas han sido durante siglos el pilar de la medicina tradicional antes de la llegada de la medicina alopática (Dhanamani et al. 2011). La búsqueda de organismos y microorganismos con actividad antitumoral se inicio en la década de los 50’s, en los cuales se encontraron principalmente flavonoides con características anticancerosas (Cragg and Newman, 2005) y desde entonces se ha incrementado el uso de productos naturales en los tratamientos de cáncer.
Según Cragg y Newman (2000), más del 50 % de los fármacos en ensayos clínicos para la actividad contra el cáncer fueron aislados de fuentes naturales o se relacionan con ellas. Se puede incluir los alcaloides de la Vinca, vinblastina y vincristina, aislados a partir de Catharanthus roseus (Apocynaceae), los derivados semisintéticos de epipodofilotoxina, aislados de las especies del género Podophyllum (Berberidaceae), así como los taxanos aislado de especies del género Taxus (Taxaceae), los derivados semi sintéticos de camptotecina, irinotecan y topotecan, aislado de Camptotheca acuminata (Nyssaceae), entre otros (De Mesquita M, et.al., 2009).
2
Adicionalmente, otra planta con alto potencial como antineoplásico es Physalis peruviana, la cual contiene compuestos bioactivos que exhiben efectos anti-inflamatorios, antimicrobianos, antifúngicos y antitumorales, en los cuales se incluyen los withanolidos (Fang, S et al. 2012)
3
2. JUSTIFICACION Y PLANTEAMIENTO DEL PROBLEMA
2.1. Pregunta de investigación
¿Los extractos etanólicos de las plantas Annona muricata, Annona cherimola y Physalis peruviana, poseen actividad citotóxica frente a células MCF-7 de adenocarcinoma de seno?
2.2. Planteamiento del problema y justificación
El cáncer de seno es un gran problema de salud en Colombia, el cual tiene un alto impacto psicológico, social y económico en la comunidad. Su detección es primordial para saber el tipo de tratamiento que se va a suministrar al paciente, puesto que según el avance del cáncer se puede realizar quimioterapia, radioterapia, hormonoterapia, cirugía o terapias dirigidas (Cragg and Newman, 2005).
La falta de control en la proliferación celular, la diferenciación y la muerte celular programada, son las principales características del cáncer, por las cuales su tratamiento es de mayor dificultad, puesto que existe una alta frecuencia de resistencia a los medicamentos, hay baja especificidad y los tratamientos se vuelven tóxicos para las células no tumorales, lo cual afecta la salud del paciente (De Mesquita, 2009), esto ocasiona la disminución de la calidad de vida del paciente, además tiene efectos psicológicos, sociales y económicos, por ende son factores que se deben combatir para poder contrarrestar la morbilidad y la mortalidad del cáncer de seno.
En Colombia la respuesta social en relación con actividades de detección temprana para el cáncer de seno muestra serias dificultades en el acceso a un diagnóstico definitivo a partir de una prueba de tamización sospechosa, así como dificultades en el acceso y la oportunidad de la atención (INC, 2012).
Adicionalmente, estos tratamientos son muy costosos, por lo que se vuelve poco asequible para la población de países en vía de desarrollo como es el caso de Colombia, por lo cual se plantea la necesidad de buscar un tratamiento adyuvante fitoquímico preventivo y post detección, el cual sea menos costoso, eficiente y especifico, y se obtenga a partir de productos naturales, no genere un efecto negativo y brinde mayor esperanza con calidad de vida a los pacientes.
De igual forma aprovechando que Colombia es un país mega diverso y rico en flora, el cual ha sido poco estudiado como potencial medicinal, se busca a partir de una investigación en plantas promisorias, extractos crudos totales que presenten actividad citotóxica frente a células cancerosas de seno y no presenten una actividad citotóxica frente a células sanas.
4
3. MARCO TEORICO-REFERENTES CONCEPTUALES
3.1. Productos naturales bioactivos y metabolitos secundarios
Hay cerca de 500.000 especies de plantas que crecen en la tierra, y se estima que al menos 5.000 compuestos químicos diferentes de metabolitos secundarios están presentes en una sola especie de planta (Tringali C, 2001).
Desde la antigüedad los productos naturales han sido fuente importante de medicamentos, y actualmente cerca de la mitad de los fármacos útiles son derivados de estos, esto debido a la quimio diversidad de la naturaleza. Sin embargo, el problema radica en la identificación de los compuestos bioactivos presentes en los productos naturales (Tringali C, 2001).
Los compuestos bioactivos naturales están constituidos por una alta variedad de estructuras con múltiples funcionalidades, las cuales proporcionan un conjunto de moléculas potenciales para la producción de productos farmacéuticos (Gil JG, et al. 2013), por ende surge la importancia de evaluar su efecto citotóxico como extracto crudo, para posteriormente realizar una búsqueda mas especifica hasta llegar a la molécula o compuesto de interés.
Estos compuestos naturales de las plantas se dividen en metabolitos primarios y metabolitos secundarios. Los metabolitos primarios son aquellos que son esenciales para las necesidades metabólicas de las plantas, en los cuales encontramos los azucares, aminoácidos, ácidos grasos y ácidos nucleicos, y otros compuesto que esenciales para el crecimiento y desarrollo de la planta, es decir son los vitales (Gil JG, et al. 2013). Por otra parte se encuentran los metabolitos secundarios, los cuales son productos de rutas bioquímicas secundarias que les permite sintetizar productos químicos, a menudo en respuesta a los estímulos ambientales específicos. Estos metabolitos secundarios pueden ser exclusivos de especies o géneros específicos y no desempeñan ningún papel en las necesidades metabólicas primarias de las plantas. Estos metabolitos secundarios le proporcionan la planta su capacidad general para sobrevivir y superar los desafíos locales, lo que les permite interactuar con su medio ambiente (Kennedy DO y Wightman EL, 2011).
Debido a la amplia gama de funciones que los metabolitos secundarios de las plantas tienen en las células vegetales, estos compuestos son de especial interés para los investigadores que centran sus estudios sobre su bioactividad para aplicaciones útiles. Sobre la base de sus orígenes biosintéticos, los metabolitos secundarios de plantas se pueden dividir en 5 grupos: Policétidos, terpenos, compuestos fenólicos, glicósidos y alcaloides (Gil et al. 2013).
3.2. Descripción, Clasificación y distribución geográfica del género Annona y Physalis
3.2.1. Genero Annona
5
contiene 119 géneros y más de 2000 especies; por otra parte Popenoe describe que la familia Annonacea contiene 40 a 50 géneros y más de 500 especies (Pinto, 2005); por ende este dato aun es ambiguo.
Después de la llegada de los españoles en el continente americano, la especie Annona se distribuyó en todo el trópico. Arboles de este género son comunes en los trópicos y subtrópicos, se encuentran en las indias occidentales, el norte y sur de América, las tierras bajas de África, islas del pacifico y el sudeste asiático (Badrie N et al. 2010). Un número limitado de especies produce frutos comestibles, los cuales se encuentran silvestres y otros han sido domesticados. (Pinto, 2005).
El género corresponde a arbustos o arboles pequeños con estatura de 5 a 11 m, esto depende de factores como la especie, el clima, el suelo y el manejo del cultivo. Su corteza y tallo posee un color gris-café, una textura áspera y ondulada. Son caducifolios, es decir, en ciertas épocas los arboles se encuentran desprovistos de hojas (Pinto, 2005). Poseen abundantes raíces finas laterales y una raíz principal que generalmente no se pronuncia, cuando el árbol se encuentra en estado adulto la raíz puede alcanzar una profundidad de 1,5 a 1,8m, todo depende de las características del suelo (Pinto, 2005).
Las flores son hermafroditas, se encuentran solitarias o en fascículos con 2 a 4 flores, con tres sépalos de color verde y seis pétalos dispuestos en dos verticilos. El verticilo externo tiene tres pétalos de color amarillo-verdoso y el interno tiene tres pétalos amarillentos. Posee varios estambres conglomerados y dispuestas en espiral por debajo y alrededor de la parte superior, formando una cúpula de numerosos carpelos unidos, que tienen un ovulo cada uno. Después de la fertilización, los carpelos unidos formaran un sincarpo o fruta compuesta (Pinto, 2005).
[image:16.612.81.549.542.652.2]Las especies a estudiar son de especial interés por su comercio y la reciente investigación en la producción de fármacos encontrados a partir de extractos de hojas y semillas de los frutos comúnmente conocidas en Colombia como guanábana (Annona muricata) y chirimoya (Annona cherimola) pertenecientes a la familia Annonaceae (tabla 1).
Tabla 1. Clasificación taxonómica de la especie Annona muricata y Annona cherimola
Filo Clase Orden Familia Genero Especie
Angiospermophyta Magnoliophyta
Magnoliopsida magnoliales Annonaceae Annona Annona muricata
Angiospermophyta Magnoliophyta
6 3.2.1.1. Annona muricata
Conocido comúnmente en Colombia como guanábana, es un árbol delgado de altura baja que llega a medir entre 4 a 8 m de altura, de hoja perenne. En Suramérica se domestico como planta de jardín. Los tallos son redondos, ásperos y no pubescentes, poseen un color café oscuro. Las hojas tienen peciolos cortos y son ovaladas a cilíndrica con un largo de 14 a 16 cm y un ancho de 5 a 7 cm (Pinto, 2005).
[image:17.612.94.561.289.642.2]El árbol de Annona muricata produce frutas de forma oblonga, elíptica o en forma de corazón, las cuales poseen un color verde, esta fruta es la comúnmente llamada en Colombia como guanábana. La corteza de la fruta posee en su madurez numerosas prolongaciones puntiagudas, parecidas a “espinas”. La fruta puede contener de 127 a 170 semillas, repartidos por toda la pulpa, y su tamaño varia de 1 a 2 cm de longitud con un peso de 0,33 a 0,59 g, poseen un color negro que con el tiempo se torna café oscuro (Fig. 1) (Pinto, 2005).
7 3.2.1.2. Annona cherimola
Conocida comúnmente en Colombia como chirimoya, es una árbol pequeño de hoja caduca, que rara vez alcanza más de 15 m. posee hojas simples y alternas, con una forma ovada-lanceoladas elípticas, con una longitud de 10 a 25 cm. Su aspecto brillante es debido a las glabras en la superficie ventral y dorsal (Pinto, 2005). La floración comienza cuando el árbol tiene una edad de 3 a 4 años, la flor emerge de las axilas de las hojas y posee un pedúnculo corto de 2,4 cm, la floración depende del ambiente (Pinto, 2005).
[image:18.612.96.528.316.683.2]La fruta es normalmente en forma de corazón, cónica, ovalada o algunas veces de forma irregular debido a la polinización irregular. El fruto puede medir de 7,5 a 12,5 cm de largo y tener un peso de 200 a 700g. La superficie de la fruta depende de la variedad, pero la comúnmente conocida y trabajada posee una superficie suave y fina, con un color verde-amarillo dependiendo de su estado de madurez. Adicionalmente la fruta puede contener de 21 a 41 semillas, con una longitud de 1,5 a 2,0 cm y un ancho de 1,0 cm (Fig. 2) (Pinto, 2005).
8 3.2.2. Genero Physalis
Comprende entre 75 y 90 especies, es una de los géneros más grandes de la familia Solanaceae. Se encuentran en las zonas cálidas ya sea como cultivo o en forma de maleza. Es un género característico debido a cáliz que se desarrollo durante el periodo de fructificación, rodeando la baya/fruto completamente, debido a esta importante característica Physalis es el género más fácil de reconocer dentro de la familia de las Solanaceae (Dostert, 2011).
Las especies de Physalis son anuales o perennes, con flores solitarias y exiliares de color amarillo con un centro negro difuso. La corola es normalmente indivisa, campanulada, frecuentemente presenta puntos oscuros en la base (Dostert, 2011).
La especie de mayor relevancia en Colombia debido a su comercio y consumo es la especie Physalis peruviana, en la cual Colombia ocupa el primer puesto en exportación (Mazorra et al. 2006). Su clasificación botánica o taxonómica se observa en la tabla 2.
Tabla 2. Clasificación taxonómica de la especie Physalis peruviana.
Filo Clase Orden Familia Genero Especie
Magnoliophyta Magnoliopsida Solanales solanaceae Physalis Physalis peruviana
3.2.2.1. Physalis peruviana
Es originaria de los Andes del norte de Suramérica y actualmente es cultivada en todos los Andes Suramericanos. P. peruviana está hoy documentada en varios países, como por ejemplo, Perú, Colombia, Ecuador, Chile, Venezuela, Hungría, India, Australia, China, Macronesia y Sudáfrica (Dostert, 2011).
Es una hierba perenne, mide aproximadamente desde 45 a 9 cm de alto, posee un tallo erecto poco ramificado, cilíndrico y densamente pubescente. La raíz principal alcanza una profundidad de 50 a 80 cm. La mayoría de las raíces son fibrosas y se desarrollan a una profundidad de 10 a 15 cm (Dostert, 2011). El peciolo tiene una longitud aproximada de 2 a 6 cm, y la lamina foliar es anchamente aovada, con una longitud de 0,9 a 13,5 cm y un ancho de 1,4 a 10 cm. Las hojas son alternas, densamente pubescentes, con base sub-cordadas, enteras o con pocos dientes inconspicuos, y cortamente apiculadas (Dostert, 2011). El pedículo floral es de 10 a 13mm de largo; el cáliz es anchamente campanulado, en floración mide de 15 a 18 cm de largo y pubescente en la cara exterior, en fructificación es acrescente, de color verde a beige, ovoide, con 5 a 10 nervios sobresaliente y algo rojizos con 8-10 cm de largo y 3 mm de ancho, laxamente pubescente en la cara exterior (Dostert, 2011).
9
filamentos y anteras son (azul-) púrpuras y las anteras de 2.5—3 mm de largo. El ovario es verde con un anillo o disco en base, estilo púrpura con estigma claviforme. Las bayas maduras son amarillas a anaranjadas, 1—2 cm de longitud y 1-1.5 cm ancho (diámetro) y pesan 4—10 gr. Los frutos contienen 100—200(—300) semillas amarillas, de 1,25—2,5 mm de diámetro (Dostert, 2011).
3.3. Uso y antecedentes fitoquímicos del género Annona y Physalis 3.3.1. Género Annona
Se han obtenido compuestos bioactivos encontrados en las raíces, hojas, cortezas, semillas y frutas, principalmente compuestos como las acetogeninas, flavonoides y alcaloides. Teniendo en cuenta su efecto citotóxico, se ha descrito como potencial agente anti-cancerígeno. También se ha descrito que su uso como cardiotónico, insecticida, antiparasitario, anticonvulsivos y actividad de tipo ansiolítico (Carballo et al. 2010, Ferreira et al. 2013).
Adicionalmente en la Annona cherimola se han identificado compuestos que promueven la salud, como cherimoline, cherinonaine, kauranes, ligananos, amidas, purinas, amida lactamicos, esteroides, ρ-quinona, benzenoides y poliaminas (Barreca et al. 2011)
3.3.2. Género Physalis
Las bayas han demostrado proporcionar beneficios para la salud debido a su alto contenido de antioxidantes, vitaminas, minerales y fribras (Radam, 2011).
Se han reportado compuestos bioactivos presentes en Physalis peruviana tales como los withanolidos y compuestos fenólicos, los cuales tienen propiedades antioxidantes, anti-inflamatoria, antihepatotoxica, anti-hepatoma, y aportan alto contenido de vitaminas (Radam, 2011).
3.4. División celular y el origen del cáncer
Las células crecen y se multiplican a través de un proceso que se conoce como división celular, el cual es controlado en el núcleo de cada célula, puesto que da la información correspondiente sobre donde deben crecer y como deben funcionar correctamente. Cuando las células se replican, forman dos células hijas idénticas, ciertas proteínas hacen parte de esta división celular y algunas de ellas dan la información a la célula de cuando dividirse o no dividirse o son responsables de que el ADN se copie con precisión (Cragg and Newman, 2005).
Los genes que promueven el crecimiento y la división celular se denominan oncogenes, y aquellos encargado de desacelerar la división celular o responsables de hacer que las celular mueran en el momento indicado se denominan genes supresores de tumores. El cáncer generalmente es causado por mutaciones en el ADN, las cuales pueden activar los oncogenes y/o desactivar los genes supresores de tumores (Tan et al. 2005, cáncer 2014)
3.5. Anatomía del seno y cáncer de seno
10
El cáncer se genera cuando las células se dividen sin control y demasiado rápido, formando una masa de tejido anormal llamado tumor, lo cual es debido a una anormalidad genética (Cragg and Newman, 2005). El cáncer de seno es la proliferación descontrolada de las células mamarias, estas células cancerosas pueden invadir el tejido sano circundante dándose paso a los ganglios linfáticos, por ende podrán tener acceso a todo el cuerpo y generar una metástasis invadiendo los demás órganos.
3.6. Incidencia y mortalidad.
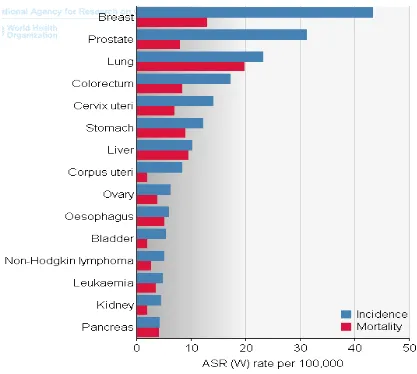
[image:21.612.85.502.239.613.2]El cáncer de seno es el segundo cáncer más común en el mundo (figura 3), y el mas frecuente entre las mujeres con un estimado de 1,67 millones de nuevos de cáncer diagnosticados en el 2012, lo cual corresponde al 25% de todos los canceres (OMS, 2012).
Figura 3. Incidencia y mortalidad según el tipo de cáncer, estandarizada por edades de hombres y mujeres. Imagen tomada de OMS (2012). Globocan.iarc.fr.
11
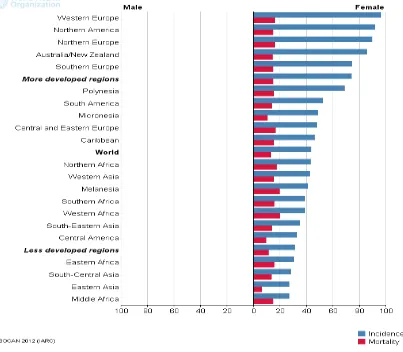
[image:22.612.110.513.149.501.2]segunda muerte por cáncer en los países desarrollados (198.000 muertes, 15,4%) después del cáncer de pulmón (figura 4) (OMS, 2012).
Figura 4. Incidencia y mortalidad de cáncer de seno en el mundo. Imagen tomada de OMS (2012). Globocan.iarc.fr.
Anualmente se diagnostican cerca de 1.38 millones de casos de cáncer de seno y ocurren 458 mil muertes (Baena A, et al. 2011). La incidencia de morbilidad y mortalidad aumenta drásticamente en países en desarrollo, como lo es Colombia y esto es debido al sistema de salud, puesto que los tratamientos llegan a las mujeres 6 meses e incluso 1 año después de su diagnostico por lo cual esto repercute en un problema mayor en la salud de la mujer, mientras que las mujeres que tienen una atención privada recibe un tratamiento luego de confirmar el diagnostico de la enfermedad.
12 3.7. Tratamientos para el cáncer
Los tratamientos difieren según los estadios del cáncer (breast cáncer, 2013). Los tratamientos existentes son: Cirugía, quimioterapia, radioterapia, terapia dirigida, inmunoterapia, la hipertermia, trasplante de células madre, terapia fotodinámica, laser, donación de sangre del producto y transfusión, terapia molecular dirigida (American Cáncer Society, 2013).
3.8. Clasificación de medicamentos quimioterapéuticos.
Los medicamentos quimioterapéuticos se dividen en carios grupos basándose en su mecanismo de acción, estructura química y su relación con otros medicamentos. Es importante conocer el mecanismo de acción de un medicamente, puesto que dependiendo de este factor se puede predecir sus efectos secundarios (American Cáncer Society, 2013).
Se clasifican en:
3.8.1. Agentes alquilantes
Dañan directamente el ADN evitando la reproducción de las células tumorales. Estos agentes no son específicos de la fase, es decir pueden actuar en todas las fases del ciclo celular. Se utilizan para tratar la leucemia, linfomas, la enfermedad de Hodgkin, melanoma múltiple y el sarcoma, al igual que canceres de pulmón, seno y de ovarios (American Cáncer Society, 2013).
Estos medicamentos al actuar directamente en el ADN celular, pueden causar daños a largo plazo en la medula ósea, teniendo como riego padecer de leucemia luego de 5 a 10 años de tratamiento (American Cáncer Society, 2013).
Los tipos de alquilantes son:
• Mostazas nitrogenadas • Nitroso ureas
• Alquil sulfonatos • Triazinas
• Etilenimas
• Algunos medicamentos con platino (American Cáncer Society, 2013).
3.8.2. Antimetabolitos
Se encargan de sustituís elementos fundamentales del ADN y el ARN, causando un daño en las células en la fase S. se utilizan normalmente para tratar leucemias, canceres de seno, ovario y tracto intestinal, etc (American Cáncer Society, 2013).
3.8.3. Antibióticos contra el cáncer
13
• No antraciclinas: actúan de igual manera que las antraciclinas. Se encuentran antibióticos como actinomicina D, Bleomicina y la mitocina-C (American Cáncer Society, 2013).
3.8.4. Inhibidores de la topoisomerasa
Estos medicamentos interfieren con las enzimas llamadas topoisomeras, las cuales están encargadas de mantener la estructura terciaria del ADN, siendo la encargada del enrollamiento o desenrrollamiento, durante la síntesis, replicación, condensación y descondensación del ADN (American Cáncer Society, 2013).
Los tratamientos inhibidores de la topoisomerasa II pueden causar leucemia secundaria después de un tratamiento de 2 a 3 años (American Cáncer Society, 2013).
3.8.5. Inhibidores de la mitosis
Generalmente son alcaloides de origen vegetal y otros compuestos derivados de productos naturales. Actúan deteniendo la mitosis o evitando que las enzimas implicadas en este proceso sinteticen las proteínas necesarias para la reproducción celular (American Cáncer Society, 2013). Estos medicamentos ejercen su acción durante la fase M del ciclo celular, pero pueden causar daño en todas las fases. A largo plazo puede causar daño en los nervios periféricos (American Cáncer Society, 2013).
Dentro de este grupo se encuentran los taxenos, epotilones, los alcaloides de la vinca y la estramustina (American Cáncer Society, 2013).
3.8.6. Terapia hormonal
Se utilizan hormonas sexuales o medicamentos que actúan inhibiendo la producción de hormonas o cambian la acción de las hormonas implicadas en el desarrollo de las células cancerígenas, es decir, esta terapia evita que la célula tumoral use la hormona necesaria para su crecimiento y su reproducción, o evita que el cuerpo produzca esta hormona (American Cáncer Society, 2013).
3.8.7. Otros medicamentos quimioterapéuticos
En este grupo se encuentran aquello que tienen un mecanismo de acción diferente y no se pueden clasificar en ninguna categoría. Dentro de este grupo se encuentran la L-asparaginasa (enzima) y el bortezomib (inhibidor de la proteosoma) (American Cáncer Society, 2013).
3.8.8. Terapias dirigidas
Son tratamientos que se desarrollaron a partir del funcionamiento interno de las células tumorales, es decir, se han creado nuevos medicamentos más específicos utilizando genes mutados o células que sobre expresen un gen de interés (American Cáncer Society, 2013).
3.8.9. Agentes de diferenciación
14 3.8.10. Inmunoterapia
15 4. OBJETIVOS 4.1. Objetivo general
Evaluar el potencial de actividad citotóxica de diferentes extractos crudos frente a células cancerosas MCF-7 de seno, obtenidos a partir de las plantas Annona cherimola (chirimoya), Annona muricata (guanabana)y Physalis peruviana (uchuva).
4.2. Objetivos específicos
4.2.1 Obtener extractos polares de las plantas seleccionadas.
16
5. METODOLOGIA 5.1. Diseño de la investigación
Finalidad : Analítico
Secuencia temporal: longitudinal
Control de asignación de los factores de estudio: experimental Direccionalidad contexto tiempo: prospectivo
Niveles del factor de diseño
a) Extracto etanólico de hojas de Annona cherimola b) Extracto etanólico de semillas de Annona cherimola c) Extracto etanólico de semillas de Annona muricata d) Extracto etanólico de hojas y tallos de Physalis peruviana
Variable respuesta
Porcentaje (%) de viabilidad celular
Unidad de muestreo
Células/ mL de medio RPMI
Población de estudio y muestra
La población de estudio corresponde a 7x103 células/ 100μL correspondientes a las líneas celulares MCF-7 y HEK-293, adquiridas de la ATCC
Variables de estudio
a) Variable independiente: concentraciones de los extractos
b) Variable dependiente: porcentaje (%) de viabilidad celular
5.2. Recolección y clasificación del material vegetal
Se realizó la recolección de las plantas respetando las directrices de la Organización mundial de la salud sobre buenas prácticas agrícolas y de recolección (BPAR) de plantas medicinales (OMS, 2003). Una planta completa de cada especie de Annona cherimola, Annona muricata y Physalis peruviana se recolectaron en la finca “La reina del Caribe” ubicada en Urabá, Antioquia. Se procedió a separar la estructura de interés. Todo el material fue conservado en cadena de frio durante el transporte de tal forma que no se contamirá o se marchitaran.
5.3. Obtención de extractos
El material vegetal utilizado correspondiente a hojas y semillas de Annona cherimola, las semillas de Annona muricata y las hojas y tallos de Physalis peruviana, se secaron a temperatura ambiente sin exposición directa a la luz solar durante 4 días.
17
utilizar según lo reportado en la literatura (tabla 3). Una vez macerado el material vegetal se realizo una extracción con etanol durante 4 días.
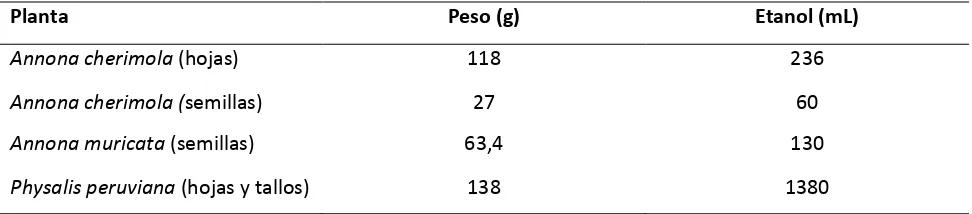
Tabla 3. Pesos del material seco-macerado y cantidad de solvente utilizado.
Planta Peso (g) Etanol (mL)
Annona cherimola (hojas) 118 236
Annona cherimola (semillas) 27 60
Annona muricata (semillas) 63,4 130
Physalis peruviana (hojas y tallos) 138 1380
[image:28.612.64.550.132.239.2]Los extractos etanólicos fueron filtrados y centrifugados a 7000 rpm por 20 minutos y se recupero el sobrenadante. Posteriormente los extractos filtrados y centrifugados fueron concentrados por rotaevaporación con vacio a una temperatura de 45°C, dejando un volumen de 80 mL aproximadamente para cada uno, y posteriormente se concentraron en una campana de vacío obteniéndose los pesos totales de los extractos a evaluar (tabla 4).
Tabla 4. Peso de 10 mL de extractos totales concentrados.
Planta Peso (g)
Annona cherimola (hojas) 0,9879
Annona cherimola (semillas) 0,6629
Annona muricata (semillas) 1,016
Physalis peruviana (hojas y tallos) 1,8461
5.4. Pruebas químicas preliminares
Se realizaron pruebas fitoquímicas preliminares o las comúnmente llamadas “marcha fitoquímica” con el fin de caracterizar los metabolitos secundarios contenidos en los diferentes extractos. Es una detección rápida colorimétrica, es decir, se produce una reacción química que altera rápidamente la estructura molecular del compuesto.
Como los extractos son etanólicos, se realizaron pruebas rápidas para detectar flavonoides, fenoles, saponinas, glicósidos y alcaloides utilizando el método descrito por Wall. Todos los extractos fueron diluidos en etanol y se pasaron 5 mL de extracto diluido a un tubo de hemolisis para cada prueba. Adicionalmente se realizo un fraccionamiento en éter de petróleo de cada muestra con el fin de detectar esteroides, esteroles, terpenos y sesquiterpenlactonas.
18
[image:29.612.147.503.132.209.2]• Prueba de Shinoda: esta prueba determina los fenoles y flavonoides presentes en los extractos a través de la formación de un compuesto de color naranja-rojizo (Fig. 5). Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adiciono 1 cm de Mg y 4 gotas de HCl 2N.
Figura 5. Reacción de la prueba de Shinoda. Imagen tomada de http://upload.wikimedia.org/wikipedia/commons/9/90/Shinoda_test.png
• Prueba de cloruro férrico FeCl3: esta prueba determina los flavonoides y fenoles presentes
[image:29.612.203.443.321.413.2]en los extractos a través de la formación de un compuesto de color verde fuerte o verde oliva (Fig. 6). Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adicionaron 4 gotas de FeCl3 al 1%.
Figura 6. Reacción de la prueba de cloruro férrico. Imagen tomada de http://lh5.ggpht.com
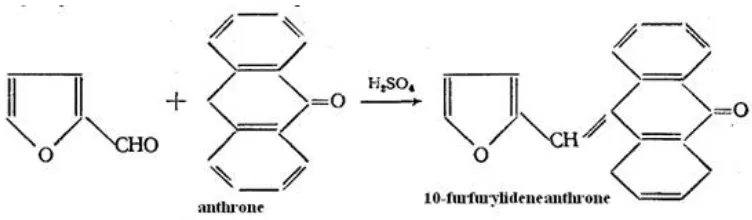
[image:29.612.138.514.525.635.2]• prueba de antrona: esta prueba determina los glucósidos de flavonoides o de terpenos presentes en los extractos a través de la formación de un anillo verde en la interfase (Fig. 7). Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adiciono 1 mL de antrona diluido en H2SO4 concentrado.
Figura 7. Reacción de la prueba de Antrona. Imagen tomada de http://intranet.tdmu.edu.ua
19
[image:30.612.121.557.105.233.2]ensayo se tomo un tubo de hemolisis con el extracto y se le adicionaron 4 gotas de HCl y 4 gotas del reactivo de Dragendorff (yoduro de bismuto).
Figura 8. Reacción de la prueba de Dragendorff. Imagen tomada de http://es.scribd.com/doc/38898384/La-reaccion-de-Vitali
• Prueba de la espuma: esta prueba se realiza para determinar las saponinas presentes en los extractos a través de la formación de una espuma constante durante 15 min o más. Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adicionó 1 mL de agua y se agito fuerte.
Las pruebas para las fracciones de éter de petróleo con cloroformo fueron las siguientes:
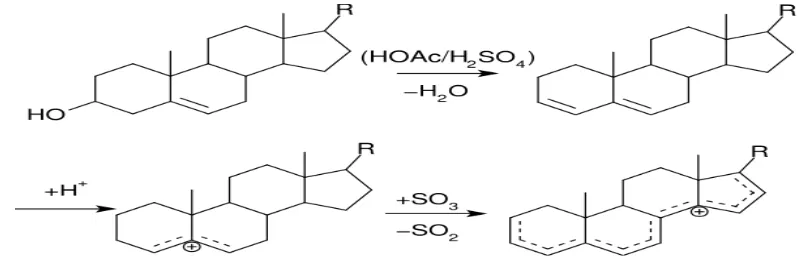
• Prueba de Liebermann-Burchard: esta prueba se realiza para determinar esteroides y esteroles presentes en los extracto a través de la formación de coloraciones rosa, violeta, azul o verde (Fig. 9). Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adicionaron 4 gotas de del reactivo de Lierberman-Burchard (Anhídrido acético con acido sulfúrico).
Figura 9. Reacción de la prueba de Lierberman-Burchard. Imagen tomada de http://upload.wikimedia.org
• Prueba de Salkowski: esta prueba se realiza para determinar terpenos presentes en los extracto a través de la formación de un complejo de coloración amarillo-rojiza. Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adicionaron 4 gotas acido sulfúrico (H2SO4). Su reacción es similar a la prueba de Lieberman-Burchard. • Prueba de Baljet: esta prueba se realiza para determinar terpenos y esteroles presentes
[image:30.612.122.521.452.582.2]20
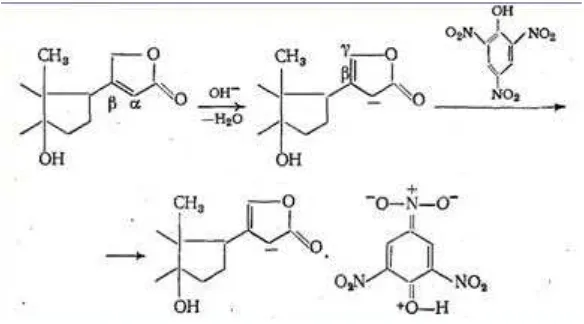
[image:31.612.179.471.101.263.2]Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adicionaron la solución A (acido pícrico) y la solución B (NaOH).
Figura 10. Reacción de la prueba de Baljet. Imagen tomada de http://intranet.tdmu.edu.ua
• Prueba de Hidroxamato férrico: esta prueba se realiza para determinar
sequiterpenlactonas presentes en los extracto a través de la formación de un complejo de coloración café o violeta (Fig. 11). Para realizar este ensayo se tomo un tubo de hemolisis con el extracto y se le adicionaron 2 gotas de MeOH 2N de Clorhidrato de hidroxilamina, 2 gotas de MeOH 2N de KOH, HCl 0,5 N y FeCl3, y se llevo a baño maría hasta observar cambio o dilución de compuestos.
Figura 11. Reacción química de la prueba de hidroxamato férrico. Imagen tomada de http://1.bp.blogspot.com
5.5. Cultivo y tratamiento de las células
La línea celular MCF-7 de adenocarcinoma de seno y la línea celular HEK-293 fueron adquiridas en la ATCC. Las células fueron criopreservadas en el laboratorio de Biología Celular de la Universidad de ciencias aplicada y ambientales (UDCA) en nitrógeno líquido luego de ser enfriadas y congeladas gradualmente a -20 y -86°C.
[image:31.612.120.486.400.482.2]21
5.6. Evaluación de la actividad citotóxica de los extractos
22
6. RESULTADOS Y DISCUSIÓN
La ciencia ha reconocido desde la antigüedad el valor y la utilidad de los compuesto bioactivos naturales y actualmente el interés por encontrar productos naturales con potencial medicinal ha resurgido.
Realizando experimentos en líneas celulares y en animales se ha demostrado el efecto anticancerígeno de productos naturales para inducir apoptosis y diferenciación celular, mejora el sistema inmune, inhibición de angiogénesis y revertir la resistencia a múltiples fármacos
6.1. Extracción
[image:33.612.81.525.455.555.2]Después de pulverizar el material vegetal, se procedió a pesar y se obtuvo 118 g, 27 g, 63,4 g y 138 g peso seco de semillas de A. muricata, semillas de A. cherimola, hojas de A. cherimola y hojas y tallos de P. peruviana respectivamente. Posterior a la extracción en etanol y a la rotaevaporación se obtuvo un volumen final de 80 mL de cada extracto, a partir de los cuales se tomaron 10 mL del extracto y se secaron utilizando la campana de vacío y se obtuvo un peso de 1,016 g, 0,6629 g, 0,9879 g y 1,8461 g de semillas de A. muricata, semillas de A. cherimola, hojas de A. cherimola y hojas y tallos de P. peruviana respectivamente, y se hizo una relación para hallar la cantidad en 80 mL del extracto, y a partir de este se obtuvo el rendimiento en porcentaje (%) de los extractos etanólicos (tabla 5), obteniendo que el extracto con mejor rendimiento es el extracto de semillas de A. cherimola con un valor de 19,6%, seguido de un 12,5% de rendimiento de las hojas de A. cherimola y el menor valor corresponde al extracto de semillas de A. muricata con un rendimiento del 6,8%.
Tabla 5. Pesos y rendimiento de los extractos.
Planta partes Peso seco (g) Peso total (g) Rendimiento (%)
Annona muricata Semillas 118 8,128 6,8
Annona cherimola Semillas 27 5,3032 19,6
Annona cherimola Hojas 63,4 7,9032 12,5
Physalis peruviana Hojas y tallos 138 14,7680 10,7
6.2. Identificación cualitativa de metabolitos secundarios.
23
Tabla 6. Metabolitos identificados cualitativamente presentes en los extractos etanólicos y fracciones de éter de petróleo.
*característica de la reacción es débil.
Se puede observar que el extracto de semillas de Annona muricata presenta metabolitos secundarios tales como fenoles, taninos, alcaloides, terpenos y esteroles puesto que dio positivo para las pruebas de cloruro férrico, Dragendorff, Baljet (Fig. 12), lo cual es coherente con el estudio realizado por Arroyo et al (2005) en el cual encontraron una gran cantidad de flavonoides, taninos, alcaloides y terpenos, encontrando en los extractos con terpenos una actividad citotóxica.
Metabolitos secundarios Prueba reveladora Característica de reacción positiva Resultado obtenido Extractos evaluados A. muricata A. cherimolia (hojas) A. cherimolia (semillas) P. peruviana Flavonoides y fenoles Prueba de Shinoda Coloración naranja-rojizo (formación de gas) (-) (-) (+)* (-) Fenoles y taninos Prueba de FeCl3 Coloración verde oscura (+) (+) (+) (+) Glicósidos de flavonoides Prueba de Antrona Anillo verde en la interfase
(-) (+)* (+) (+)
Alcaloides Prueba de Dragendorf
Precipitado naranja ladrillo
(+) (+) (+) (-)
Saponinas Prueba de la espuma Espumas estable durante 15 min (-) (-) (-) (+) Esteroides y esteroles Prueba de Lierbermann -Buchard Coloraciones rosa, violeta, azul o verde
(-) (-) (-) (-)
Terpenos Prueba de
Salkowski Coloración amarillo-rojiza (-) (-) (-) (-) Terpenos y esteroles Prueba de Baljet Coloración amarilla (+) (+) (+) (+) Sequiterpenla ctonas Prueba de hidroxamato férrico Coloración café o violeta
24
Figura 12. Resultados de pruebas químicas preliminares para el extracto de semillas de Annona muricata [A] extractos referentes, [B] pruebas para extractos etanólicos: (1) prueba de Shinoda, (2) prueba de FeCl3, (3) prueba de antrona, (4) prueba de Dragendorff y (5) prueba de la espuma. [C] pruebas para fracciones en éter de petróleo: (1) prueba de
hidroxamato férrico, (2) prueba de Baljet, (3) prueba de Salkowski y (4) prueba de Lierbermann-Burchard.
El extracto de hojas de Annona cherimola presenta metabolitos secundarios tales como fenoles, taninos, glicósidos de flavonoides y alcaloides, puesto que dio positivo para las pruebas de Cloruro férrico, antrona y Dragendorff (Fig. 13)
1 2 3 4 5
1 2 3 4
A
B
25
Figura 13. Resultados de pruebas químicas preliminares para el extracto de hojas de Annona cherimola. [A] extractos referentes, [B] pruebas para extractos etanólicos: (1) prueba de Shinoda, (2) prueba de FeCl3, (3) prueba de antrona, (4) prueba de Dragendorff y (5) prueba de la espuma. [C] pruebas para fracciones en éter de
petróleo: (1) prueba de hidroxamato férrico, (2) prueba de Baljet, (3) prueba de Salkowski y (4) prueba de Lierbermann-Burchard.
El extracto de semillas de Annona cherimola difirió en el resultado a las metabolitos encontrados en las hojas de esta planta, puesto que presenta flavonoides, fenoles, taninos, glicósidos de flavonoides, alcaloides y terpenos, observando de este modo que dio positivo para un mayor número de pruebas, las cuales fueron la prueba de Shinoda, cloruro férrico, antrona, Dragendorrf y Baljet (Fig. 14).
A
B
C
1 2 3 4 5
26
Figura 14. Resultados de pruebas químicas preliminares para el extracto de semillas de Annona cherimola. [A] extractos referentes, [B] pruebas para extractos etanólicos: (1) prueba de Shinoda, (2) prueba de FeCl3, (3) prueba de antrona, (4) prueba de Dragendorff y (5) prueba de la espuma. [C] pruebas para fracciones en éter de petróleo: (1) prueba de hidroxamato férrico, (2) prueba de Baljet, (3) prueba de Salkowski y (4) prueba de Lierbermann-Burchard.
El extracto de hojas y tallos de Physalis peruviana presenta metabolitos secundarios como fenoles, taninos, glicósidos de flavonoides o de terpenos, saponinas y terpenos y esteroles, dando respectivamente positivo para las pruebas de cloruro ferrico, antrona, espuma y Baljet (Fig. 15).
1 2 3 4 5
1 2 3 4
C
27
Figura 15. Resultados de pruebas químicas preliminares para el extracto hojas y tallos de P. peruviana. [A] extractos referentes, [B] pruebas para extractos etanólicos: (1) prueba de Shinoda, (2) prueba de FeCl3, (3) prueba de antrona,
(4) prueba de Dragendorff y (5) prueba de la espuma. [C] pruebas para fracciones en éter de petróleo: (1) prueba de hidroxamato férrico, (2) prueba de Baljet, (3) prueba de Salkowski y (4) prueba de Lierbermann-Burchard.
El valor medicinal de estas plantas radica en sus constituyentes fitoquímicos bioactivos, los cuales producen acciones fisiológicas definidas en el cuerpo humano. Se ha descrito que flavonoides, fenoles, taninos, esteroles, terpenos y saponinas naturales forman la base de los medicamentos.
Se le ha otorgado a las saponina un efecto como limpiador de la sangre, los taninos ayudan a la cicatrización de las heridas (Wahua and Sam, 2013). Adicionalmente poseen diversos mecanismos
de acción, por ende estas plantas tienen un alto potencial como fuente de nuevos fármacos. 6.3. Cultivo celular
El cultivo celular se ha convertido en una de las principales técnicas en investigación, y se asocia a la extracción de células, tejidos u órganos de un animal o una planta, para su posterior adaptación a un ambiente artificial propicio para su desarrollo y proliferación (Arrora, 2013). Para el crecimiento óptimo de las células fue necesario tener los requisitos básicos como temperatura a 37°C, 5% CO2, pH y sustrato.
1 2 3 4
1 2 3 4 5
C
28
Se observo una diferenciación en el crecimiento de las líneas celulares MCF-7 y HEK-293 debido al medio utilizado, puesto que el medio DMEM suplementado con 1% de estreptomicina/penicilina, 10% suero fetal bovino, 1% de L-glutamina y 4,5g/L de glucosa se observo un crecimiento lento y un alto índice de muerte celular, mientras que el medio RPMI-1640 suplementado con 1% de estreptomicina/penicilina, 10% suero fetal bovino, 1% de L-glutamina sin glucosa se observo una fácil adaptación y rápida proliferación. Lo cual fue referenciado en diversos estudios, en los cuales se discute sobre los componentes de cada medio y la inducción o inhibición de enzimas según las cantidades y disponibilidad de un sustrato (Diawpanich et al. 2008, Wu et al. 2009). El medio DMEM y RPMI 1640 son los medios comúnmente utilizados para el cultivo de diferentes tipos de células. Sin embargo, existen diferencias significativas en su composición, lo cual podría afectar la proliferación, viabilidad y diferenciación celular. (Wu et al. 2009)
El medio DMEM utilizado tiene una concentración de 4,5g/L de glucosa, la cual puede afectar las células adherentes, por ende este puede ser el factor de baja proliferación y viabilidad celular, puesto que altas concentraciones de glucosa alteran las funciones celulares e inducen apoptosis (Li et al. 2007) mientras que el RPMI-1640 utilizado no contiene glucosa, por ende la adaptación de las células adherentes fue mejor, por lo cual se decidió trabajar con el medio RPMI-1640
6.4. Ensayo citotóxico
Para la evaluación de productos naturales con actividad biológica es necesario implementar ensayos que utilicen un programa de cribado a gran escala, por lo cual se realizó el ensayo de MTT en microcultivo para evaluar el efecto citotóxico, el cual se fundamenta en la reducción metabólica de la sal de tetrazolio a formazan realizada por las células viables. Esta técnica permite evaluar la variable tratamiento-efecto por medio del análisis de regresión lineal.
Los extractos obtenidos a partir de las plantas Annona muricata, Annona cherimola, y Physalis peruviana se probaron frente a la línea célular tumoral MCF-7 de cáncer y la línea celular sana humana embrionaria de riñón HEK-293. Con el fin de evaluar el efecto citotóxico selectivo sobre las células tumorales.
29
Figura 16. Fotografía ensayo de MTT de cristales de formazan sin diluir en las líneas celulares MCF-7 y HEK293
30
[image:41.612.89.537.138.573.2]En los extractos de semillas de Annona muricata se obtuvo unIC50= 9 μg/mL, en los extractos de semillas de Annona cherimola se obtuvo un IC50= 11μg/mL, mientras que para el extracto de hojas se encontró un IC50= 34 μg/mLy en el de hojas y tallos de Physalis peruviana se encontró un IC50=8 μg/mL.
Figura 17. Gráfico comparación del efecto citotóxico de los extractos de A. muricata (GES), A. cherimola (CEH y CES) y Physalis peruviana (UHT) en la línea celular MCF-7. [A] Gráfico de dispersión y [B] Gráfico barras en 3D.
Adicionalmente, se observó que los extractos con mayor efecto citotóxico fueron los de hojas y tallos de Physalis peruviana, semillas de Annona muricata y de Annona cherimola, obteniendo en los extractos un porcentaje de viabilidad entre 4% y 0% a unas concentraciones de 100 µg/mL y 200 µg/mL. 0 10 20 30 40 50 60 70 80 90 100
-5 5 15 25 35 45 55 65 75 85 95 105 115 125 135 145 155 165 175 185 195 205
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
UHT CEH CES GES UHT CEH CES GES 0 50 100
2 10 25 50 75 100 200
V ia b ilid ad c e lu la r %
31
A partir de una concentración de 75 µg/mL en todos los extractos, se observa que la viabilidad celular disminuyo en un 90% aproximadamente, con excepción al extracto de hojas de Annona cherimola que a esta concentración tiene un porcentaje del citotoxicidad del 25%(Fig. 17), indicando que todos los extractos evaluados tiene un efecto citotóxico sobre las células cancerosas MCF-7 a concentraciones medias.
[image:42.612.87.529.191.661.2]Se valuaron estos mismos extractos en iguales concentraciones frente a las células no cancerosas HEK293, con el fin de determinar la selectividad de los extractos (Fig.18).
Figura 18. Gráfico comparación del efecto citotóxico de los extractos de A. muricata (GES), A. cherimola (CEH y CES) y Physalis peruviana (UHT) en la línea celular HEK-293.
0 20 40 60 80 100
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180 190 200 210
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
UHT CEH CES GES UHT CEH CES GES 0 50 100
2 10 25 50 75 100 200
V ia b ilid ad c e lu la r %
32
Se observa que los extractos presentan bajo efecto citotóxico en las células no cancerosas HEK293, es decir, los porcentajes de viabilidad no son menores al 50% en la concentración más alta, correspondiente a 200 μg/mL.
La figura 19 presenta el comportamiento del efecto citotóxico para el extracto de semillas de Annona muricata (GES) frente a las células MCF-7 de cáncer de seno y las células control HEK293. Se observó a partir de la concentración de 2 µg/mL un efecto citotóxico con un porcentaje de viabilidad del 70,3%, y fue disminuyendo dependiendo de la concentración, de tal forma que en una concentración de 25 µg/mL se obtuvo un porcentaje de viabilidad del 5,7% y a la mayor concentración de 200 µg/mL se alcanza el mayor efecto citotóxico con un porcentaje de viabilidad del 0,5% (Fig. 19), con un IC50 9 µg/mL. Adicionalmente, se evidencia un efecto selectivo sobre las células tumorales, puesto que el porcentaje de viabilidad de la línea celular HEK293 no disminuye al 50% a una concentración de 200 µg/mL. Sin embargo, este fue el extracto con mayor actividad citotóxica sobre esta línea celular. Las concentraciones de 75 µg/mL, 100 µg/mL y 200 µg/mL no tienen una mayor variabilidad, los porcentajes de viabilidad son muy próximos.
100
90,0 86,6
81,0 82,5
75,9
55,0 100
70,3
47,9
5,7 2,9 3,5
0,7 0,5
0 10 20 30 40 50 60 70 80 90 100 110
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180 190 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
33
Figura 19. Graficas efecto citotóxico del extracto de semilla de Annona muricata en las líneas célulares MCF-7 y HEK-293.
A una concentración de 25 µg/mL para el extracto de GES, se contempla un tratamiento favorable, debido a que se observa un efecto citotóxico frente a las celular MCF-7 con una viabilidad menor al 10% y un efecto selectivo frente a las células HEK293 con una viabilidad mayor al 90%.
El resultado obtenido en este estudio fue mejor que el realizado en un extracto de hojas por Nur et al. (2012) en el cual encontraron un IC50= 17,19 μg/mL para las celulas T47D de cáncer de seno. Este efecto citotóxico puede ser debido a las acetogeninas presentes en las semillas y en las hojas de la Annona muricata, debido a que se ha reporta su actividad citotóxica contra células cancerosas pancreáticas, de próstata, de pulmón y de hepatoma (Ragasa et al. 2012). Las acetogeninas son metabolitos secundarios considerados como el grupo más potente de inhibidores del complejo I mitocondrial afectando la cadena respiratoria mitocondrial, esta acción agota el ATP e induciendo la apoptosis celular, por ende muestran un efecto antiproliferativo sobre las líneas celulares cancerosas (Schlie et al. 2009), lo que posiciona a este extracto revelante para el desarrollo de nuevos fármacos antineoplásicos.
El extracto de hojas de Annona cherimola (CEH) no mostro un efecto citotóxico representativo entre las concentraciones de 2 μg/mL hasta 50 μg/mL, con porcentajes de viabilidad muy cercarnos, entre 74,6% y 40,8%. Un mejor efecto de citotoxicidad se alcanza en la concentración de 200 μg/mL, el cual muestra un 0,9% de viabilidad celular, con un IC50=34 μg/mL. Adicionalmente. Se evidencia un efecto citotóxico selectivo, teniendo en cuenta que el porcentaje de viabilidad de las células HEK-293 disminuye aproximadamente un 15% para una concentración de 200 μg/mL (Fig. 20).
Un estudio realizado por Elhawary et al. (2013) muestra que el extracto etanólico de hojas de A. cherimola presento valores de IC50=3,43 μg/mL, por ende el valor obtenido sobrepasa este valor IC50, esto puede ser debido a que el extracto no se encuentra totalmente purificado.
0,0 10,0 20,0 30,0 40,0 50,0 60,0 70,0 80,0 90,0 100,0
2 10 25 50 75 100 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
34
Figura 20. Gráfico efecto citotóxico del extracto de hojas de Annona cherimola en las líneas célulares MCF-7 y HEK-293.
A una concentración de 75 µg/mL para el extracto de CEH, se contempla un tratamiento propicio, debido a que se observa un efecto citotóxico frente a las celular MCF-7 con un porcentaje de viabilidad menor al 25% y un efecto selectivo frente a las células HEK293 con una viabilidad mayor al 85%.
En comparación al extracto de hojas de Annona cherimola, el extracto de semillas (CES) de esta especie manifiesta una mayor actividad. A una concentración de 2 μg/mL el porcentaje de viabilidad fue del 59,5%, lo cual indicia que a esta concentración presenta una actividad citotóxica del 40% con un IC50=11 μg/mL y las diferencias son pequeñas hasta una concentración de 10 μg/mL. Se observo que a concentraciones mayores de 25 μg/mL tiene un porcentaje de
100
92,6
87,4
82,5 84,5 86,1
74,6 68,8
54,2
40,8
26,2 24,6
0,9 0 10 20 30 40 50 60 70 80 90 100 110
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180 190 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
HEK293 MCF-7 0,0 10,0 20,0 30,0 40,0 50,0 60,0 70,0 80,0 90,0 100,0
2 10 25 50 75 100 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
35
citotoxicidad del 96%, y mantiene una viabilidad celular inferior al 5% hasta la concentración de 200 μg/mL (Fig. 21).
Los resultados concuerdan con el estudio realizado por Quispe et al. (2009) en los cuales se encontró un IC50=9,4 µg/mL para línea celular MCF-7.
[image:46.612.88.523.207.653.2]En la línea celular HEK-293 se observa baja actividad citotóxica, presentando porcentajes de viabilidad desde 93,9% hasta 72,3% para las concentraciones desde 2 hasta 200 μg/mL, lo cual indica que tiene un porcentaje de citotoxicidad del 20% en las células sanas (Fig. 21).
Figura 21. Gráfico efecto citotóxico del extracto de semillas de Annona cherimola en las líneas célulares MCF-7 y HEK-293.
92,0 93,9 93,0
75,2 73,9 72,9 72,3
100
59,5 52,7
4,0 3,6 1,4 1,0 1,0
0 10 20 30 40 50 60 70 80 90 100 110
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180 190 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
HEK293 MCF-7 0,0 10,0 20,0 30,0 40,0 50,0 60,0 70,0 80,0 90,0 100,0
2 10 25 50 75 100 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
36
A una concentración de 25 µg/mL para el extracto de CES, se contempla un tratamiento favorable, debido a que se observa un efecto citotóxico frente a las células MCF-7 con un porcentaje de viabilidad menor al 10% y un efecto selectivo frente a las células HEK293 con una viabilidad mayor al 93%.
De igual forma los extractos de Annona cherimola poseen acetogeninas, puesto que estos metabolitos son comúnes en la familia Annonanceae.y los resultados alcanzados corresponderian a este tipo de moleculas y solo dependerian de la cantidad producida por cada especie.
El extracto de Physalis peruviana (UHT) mostro un mayor efecto citotoxico a una menor concentracion en comparacion con los demas extractos, esto se ve reflejado en el valor de IC50= 8 µg/mL. En las concentraciones de 2 μg/mL y 10 μg/mL presentó un porcentaje de viabilidad del 40%, esto puede corresponder probablemente a un error humano con respecto a la preparación de la muestra/tratamiento en la concentración de 2 μg/mL. Se obtuvo un 0% de viabilidad en las concentraciones de 100 y 200 μg/mL. Mientras que para los ensayos con la línea celular HEK293 a concentraciones de 100 y 200 μg/mL, presento un porcentaje de viabilidad del 70%.
Zavala et al (2006) reportaron un efecto toxico en la línea celular colo-205 con un IC50=1,93 µg/mL y la liena celular K562 con un IC50= 2 µg/mL. Los resultados varian de acuardo con la linea celular utilizada.
37
Figura 22. Gráfico efecto citotóxico del extracto de hojas y tallos de Physalis peruviana en las líneas célulares MCF-7 y HEK-293.
El efecto citotóxico de este extracto se puede deber a que Physalis peruviana posee un conjunto de compuestos fitoquímicos bioactivos, dentro de los cuales se encuentran los withanolidos, los cuales pertenecen a un grupo de lactonas. Diversos estudios han demostrado importantes propiedades farmacológicas, tales como insecticida, hepaprotector, inmunomodulador, antibacterial, anti-inflamatorio y actividad citotóxica para estos compuesto (Ramadan, 2011).
Debido a que la vincristina se evaluó a una concentración (120nM), no se puede realizar una comparación directa en la cual se muestra viabilidad sobre concentración con los resultados obtenidos en los extractos de las plantas, pero si se puede evaluar el posible uso de estos extractos para el control de las células cancerosas.
100 100,0 100,0 100,0
71,7 71,2
100
40,6 41,2
16,9
8,1
2,8 0,0 0,0
0 10 20 30 40 50 60 70 80 90 100 110
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180 190 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)
HEK293 MCF-7 0,0 10,0 20,0 30,0 40,0 50,0 60,0 70,0 80,0 90,0 100,0
2 10 25 50 75 100 200
V ia b ilid ad c e lu la r %
Concentración (μg/mL)