1
VALIDACION LINGÜÍSTICA Y PSICOMÉTRICA
(ADAPTACION CULTURAL) DEL CUESTIONARIO
DERMATOLOGICO DE CALIDAD DE VIDA EN NIÑOS, EN
2
VALIDACION LINGÜÍSTICA Y PSICOMÉTRICA
(ADAPTACION CULTURAL) DEL
CUESTIONARIO DERMATOLOGICO DE
CALIDAD DE VIDA EN NIÑOS, EN PACIENTES
CON DERMATITIS ATÓPICA
Clara Patricia Ordoñez R. MD. MSc
Tesis presentada a la Facultad de Medicina Como requisito parcial para optar al Grado de
Maestría en Epidemiología Clínica Pontificia Universidad Javeriana
3
TUTORES
Alvaro Ruiz Morales MD MSc Profesor titular
Departamento de Epidemiología Clínica y Bioestadística Facultad de Medicina-Pontificia Universidad Javeriana
Fabian Gil MSc Bioestadístico
4
TABLA DE CONTENIDOS
CAPITULO 1:
INTRODUCCION………16
CAPITULO 2:
JUSTIFICACION Y MARCO TEORICO………18
2.1. Definición, epidemiología y cuadro clínico de la Dermatitis Atópica 2.2. Calidad de Vida en Dermatitis Atópica
2.3. Definición de Calidad de Vida Relacionada con la Salud e Instrumentos para evaluarla
2.4. Cuestionario Dermatológico para evaluar Calidad de Vida en niños 2.5. Adaptación cultural de las escalas
CAPITULO 3:
OBJETIVOS: GENERAL YESPECIFICOS……… 33
CAPITULO 4:
METODOLOGIA……… 35
4.1. Tipo de estudio
4.2. Población de referencia 4.3. Muestra y tamaño de muestra
4.4. Criterios para seleccionar la población de estudio 4.4.1. Criterios de inclusión
5 4.6. Enumeración y definición de las variables del estudio
4.7. Descripción de la metodología y análisis estadístico para la validación lingüística y psicométrica
4.7.1. Descripción de la metodología 4.7.2. Descripción de la escala
4.7.3. Validación Lingüística……… 40 4.7.3.1. Traducción – Retro-traducción
4.7.3.2. Revisión aspectos conceptuales 4.7.3.3. Prueba piloto
4.7.3.4. Revisión aspectos clínicos 4.7.3.5. Correcciones y versión final 4.7.4. Plan de análisis de los resultados
4.7.4.1. Estadísticas descriptivas
4.7.5. Validación Psicométrica……… 43 4.7.5.1. Validez de Apariencia y Contenido
4.7.5.2. Validez de Constructo 4.7.5.3. Consistencia Interna 4.7.5.4. Validez Discriminativa 4.7.5.5. Validez Convergente 4.7.5.6. Confiabilidad
4.7.5.7. Sensibilidad al cambio 4.7.6. Utilidad de la escala
CAPITULO 5:
RESULTADOS………50
6 5.2. Descripción de la muestra y los puntajes de la escala
5.2.1. Clasificación clínica de acuerdo con el sexo y la edad 5.2.2. Puntaje de la escala
5.2.2.1. Según sexo y edad 5.3. Validez de apariencia y Contenido 5.4. Estimación de la validez de constructo 5.5. Estimación de la consistencia interna 5.6. Estimación de la validez discriminativa 5.7. Estimación de la validez convergente 5.8. Estimación de la Confiabilidad Test-retest 5.9. Estimación de la sensibilidad al cambio 5.10. Utilidad de la escala
CAPITULO 6:
DISCUSION Y CONCLUSIONES……… 67
CAPITULO 7:
FORTALEZAS Y LIMITACIONES……… 76
CAPITULO 8:
REFERENCIAS……… 79
CAPITULO 9:
7
INDICE DE TABLAS
Tabla 1. Criterios para el diagnóstico de la Dermatitis Atópica en estudios epidemiológicos.
Tabla 2. Cuestionarios para evaluar la Calidad de Vida en pacientes con Dermatitis Atópica.
Tabla 3. Variables, definición y nivel de medición.
Tabla 4. Aspectos demográficos de los pacientes con Dermatitis Atópica.
Tabla 5. Clasificación clínica de la Dermatitis Atópica (escala TIS) según el sexo. Tabla 6. Clasificación de la Dermatitis Atópica (escala TIS) según la edad.
Tabla 7. Distribución porcentual de las respuestas del CDQLI en niños con Dermatitis Atópica.
Tabla 8. Distribución del puntaje del CDLQI según la edad.
Tabla 9. Valores Propios y Cargas Factoriales (Método de Factores Principales). Tabla No. 10 Valores de Unicidad (Método de Factores Principales).
Tabla No.11Valores Propios (Método de Factores Componentes Principales) Tabla No. 12 Cargas Factoriales (Método de Factores Componentes Principales) Tabla No. 13 Cargas Factoriales y Unicidad (Método de Factores Componentes Principales) después de la rotación Varimax.
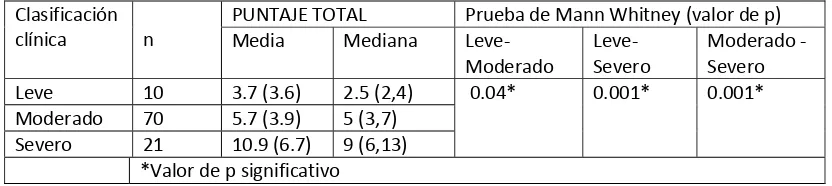
Tabla 14. Comparación del puntaje de la escala CDQLI de acuerdo con la severidad clínica de la Dermatitis Atópica.
8
INDICE DE FIGURAS
Figura 1. Distribución del puntaje de la escala CDQLI según el sexo de los pacientes con Dermatitis Atópica
Figura 2. Distribución del puntaje de la escala CDQLI según la edad de los pacientes con Dermatitis Atópica
Figura 3. Valores propios para la selección de Factores
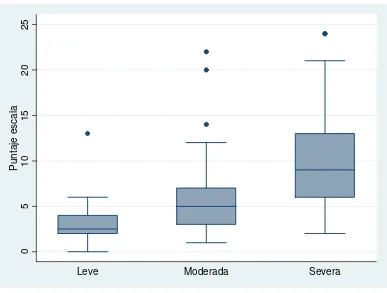
Figura 4. Puntajes del CDLQI según la clasificación clínica de la Dermatitis Atópica
Figura 5. Coeficiente de correlación concordancia de Lin
9
RESUMEN
Objetivo
Realizar la Validación Lingüística y Psicométrica (Adaptación Cultural) de la Escala Dermatológica para Evaluar Calidad de Vida en niños (CDLQI) en pacientes
con Dermatitis Atópica.
Diseño
Estudio de Validación de escalas, prospectivo.
Población
Pacientes con Dermatitis Atópica que asistieron a consulta ambulatoria de Dermatología Pediátrica, en consultorios particulares de atención de Medicina pre- pagada en Bogotá, Colombia, seleccionados secuencialmente hasta obtener el tamaño de muestra.
Procedimiento
1. Validación Lingüística: Se realizó la traducción-retro-traducción por traductores bilingües, en consenso con el autor original; se evaluó la equivalencia conceptual y semántica, se hizo una prueba piloto para evaluar comprensión y se obtuvo una versión definitiva.
2. Validación Psicométrica
10 factorial), la validez discriminativa (entre los diferentes grupos de la enfermedad con la prueba de Kruskal-Wallis) y la validez convergente comparando los puntajes del CDLQI con los de la escala clínica TIS mediante el coeficiente de correlación de Spearman.
2.2. Evaluación de la confiabilidad: pruebas de consistencia interna (alfa de Cronbach), el test-retest (coeficiente de correlación concordancia de Lin) y correlación de puntajes del CDLQI entre padres e hijos (coeficiente de correlación de Spearman).
2.3. Sensibilidad al cambio: Evaluamos el tamaño del efecto y el cambio clínicamente importante para lo cual se compararon los puntajes del CDLQI de los niños que mejoraron y los que no, al mes de tratamiento, mediante la prueba de Mann-Whitney para muestras independientes.
Resultados
11 significativamente más bajos que los de los niños que permanecieron igual o empeoraron (p<0.001).
Conclusiones
La Validación Lingüística y Psicométrica (Adaptación Cultural) de la escala CDLQI permitió desarrollar una versión en español colombiano del CDLQI con una equivalencia conceptual y semántica comparables a las de la versión original; demostró su utilidad, con una buena confiabilidad, estabilidad y capacidad de respuesta al cambio, permitió diferenciar los grupos clínicos de pacientes con Dermatitis Atópica, tiene una validez estimada aceptable en cuanto al contenido y al constructo; evalúa el concepto global de bienestar sin discriminar los diferentes aspectos del mismo.
Este estudio permitió evaluar el impacto que la Dermatitis Atópica tiene en los niños y sus familias, en este grupo de pacientes; los aspectos que más influyen en la Calidad de Vida de los niños son los relacionados con los síntomas como prurito y alteraciones del sueño, así como los sentimientos generados por la enfermedad y las molestias ocasionadas por el tratamiento.
12
ABSTRACT
Objective: To evaluate the Linguistic and Psychometric properties of the Children’s Dermatology Quality of Life Index (CDLQI) in order to do the Cultural Adaptation process to test the Quality of Life issue in Atopic Dermatitis patients.
Design: Scale validation and prospective study
Patients:
Patients with Atopic Dermatitis attending Pediatric Dermatology outpatient care in private offices of prepaid Medicine in Bogota-Colombia, selected sequentially until reaching the sample size.
Procedure
1. Linguistic Validation: We performed the translation and back translation by bilingual translators, in consensus with the original author; we assessed their conceptual and semantic equivalence, and performed a pilot testing to assess comprehension and the final version was obtained.
2. Psychometric Validation:
2.1. Validity: To assess the face validity (experts), construct validity (factor analysis), discriminant validity (among different disease groups with the Kruskal-Wallis test) and convergent validity comparing CDLQI scores with TIS( Three Item Score) clinical scores using Spearman rank coefficient.
13 comparing the scores of children who improved and those who remained stable, after a month of treatment, with the Mann-Whitney test for independent samples.
Results
We included 101 children, aged 4-16 years, of whom 44 completed the questionnaire 48 hours after baseline and 47 attended the 1 month follow-up. Factor analysis revealed a unidimensional structure with a Cronbach alpha=0.80. The correlation concordance coefficient of Lin in the test-retest was 0.87 (95% CI 0.79-0.94); the correlation of CDLQI scores between parents and children was r=0.70 (p<0.001). The correlation between scores CDLQI and the TIS was r = 0.50 (p <0.001). The CDLQI scores were significantly different in the clinical disease groups (p <0.001). The effect size was 0.88 and the CDLQI scores of children who improved the lesions of Atopic Dermatitis were significantly lower than those of children who remained unchanged or worsened (p <0.001).
Conclusions
The Linguistic and Psychometric Validation (Cultural Adaptation) of the CDLQI scale allowed us to develop a Colombian version with a conceptual and semantic equivalence comparable to those of the original; the scale proved to be useful, with good reliability, stability and responsiveness; it allowed to differentiate clinical groups of patients with Atopic Dermatitis; with an acceptable estimated validity in terms of content and construct. The scale assesses the overall concept of well-being without discriminating it’s different aspects.
14 families in this group of patients; the aspects that influence the most the Quality of Life of Children are related to symptoms such as itching and sleep disturbance, as well as the feelings generated by the disease and the discomfort caused by treatment.
15
AGRADECIMIENTOS
Al Dr. Alvaro Ruiz M porque como todo un Maestro tuvo la infinita paciencia de lanzarme múltiples salvavidas para avanzar y llegar al puerto.
A Fabian Gil por su amabilidad y paciencia para escuchar cada una de mis ideas y, por su colaboración en el análisis estadístico.
A Nicolás porque su amor y compañía fueron el estímulo para iniciar y terminar la Maestría.
A las doctoras Mariela Tavera y Ana María Salazar dermatólogas pediatras y amigas, por su participación en la evaluación de los pacientes en este estudio.
Al Dr Andrew Finlay por permitirme la utilización de la escala y por sus valiosos comentarios al revisar la retro-traducción de la misma.
A los pacientes y sus padres por participar y porque fueron el estímulo para desarrollar este estudio.
Al Dr. Ricardo Sánchez por sus aportes para el diseño de este estudio.
A la Dra. Claudia Jaramillo quien compartió conmigo sus conocimientos durante toda la Maestría.
Al grupo de profesores de la Maestría porque nos permiten tener una visión completa de la Epidemiología Clínica.
16
CAPITULO 1: INTRODUCCION
La Dermatitis Atópica es una enfermedad crónica recidivante caracterizada por prurito intenso, piel seca e inflamación. Alrededor del 70% de los casos son diagnosticados antes de los 5 años de edad (1). La prevalencia de la enfermedad ha aumentado en los últimos años y varía entre el 0.73% en Tanzania y el 23% en Noruega; en Colombia Dennis y col. reportaron una prevalencia de 3.9%, y el estudio ISAAC fase III encontró una prevalencia 14.65% en niños de 6-7 años y de 12.28% en los de 13 a 14 años (2,3). La prevalencia ha aumentado en los países más desarrollados y es mayor en los estratos socio-económicos más altos (1).
Es una enfermedad que produce un fuerte impacto en la Calidad de Vida de los pacientes. El prurito es el síntoma más importante de la enfermedad y se ha asociado con alteración en el patrón del sueño hasta en un 60% de los pacientes, lo que produce cansancio físico y mental en el paciente y la familia, con disminución de la concentración y del rendimiento escolar; así el mayor efecto se aprecia en las áreas relacionadas con los aspectos físicos, emocionales y sociales (4).
La evaluación de la Calidad de Vida en los niños con diferentes patologías crónicas, empezó en los años 80 (5). El Cuestionario Dermatológico de Calidad de Vida en niños (CDLQI) es el cuestionario más utilizado en niños con enfermedades dermatológicas; fue validado en 1995 por Susan Lewis-Jones y Andrew Finlay en Inglaterra. Es un cuestionario específico de dermatología y consta de 10 preguntas que evalúan la
17 Calidad de Vida teniendo en cuenta los síntomas, los sentimientos, las actividades, las relaciones sociales, el sueño y el tratamiento. Está diseñado para ser aplicado entre los 4 y 16 años, es auto-administrado y puede ser contestado por los pacientes con o sin ayuda de los padres (6).
Las opiniones acerca del estado de salud personal varían de cultura a cultura, por lo que la utilización de un instrumento en un contexto cultural diferente del original en el que fue desarrollado no puede llevarse a cabo mediante la traducción del mismo. Es necesario realizar su adaptación cultural, que comprende dos fases: la Validación Lingüística, que incluye la traducción-retro-traducción y la evaluación de los aspectos conceptuales, semánticos y operativos y, la Validación Psicométrica que incluye la evaluación de la validez, la confiabilidad, y la sensibilidad al cambio del instrumento (7).
18
CAPITULO 2
JUSTIFICACION Y MARCO TEORICO
JUSTIFICACION
Los estudios demuestran que la Dermatitis Atópica tiene un gran impacto en la Calidad de Vida de los pacientes y de su grupo familiar. Esto, sumado al aumento progresivo de la prevalencia de la enfermedad, a los costos del tratamiento y al desconocimiento de los aspectos que influyen en la Calidad de Vida en los niños con Dermatitis Atópica en Colombia, fue la motivación para diseñar este estudio.
Como no existe ningún cuestionario desarrollado o adaptado para evaluar la Calidad de Vida en niños con enfermedades dermatológicas en nuestro medio, se decidió realizar la adaptación del Cuestionario Dermatológico de Calidad de Vida en Niños (CDLQI) por ser el instrumento más utilizado en estudios clínicos y en diferentes países, para evaluar el desenlace de Calidad de Vida en niños enfermedades dermatológicas.
19
MARCO TEORICO
2.1. Definición, epidemiología, cuadro clínico de la Dermatitis Atópica
2.1.1. Definición de la Dermatitis Atópica
La Dermatitis Atópica es una enfermedad difícil de definir por su localización y morfología variables, el curso intermitente y la falta de pruebas diagnósticas que sirvan de referencia. En 1990, un grupo liderado por H. Williams en Inglaterra, propuso los criterios que se muestran en la Tabla No. 1. Estos criterios han sido validados en población hospitalaria y ambulatoria en niños en edad escolar; cuando se comparan con el diagnóstico hecho por dermatólogos, tienen una sensibilidad del 80% y una especificidad del 97%. Son fáciles de utilizar en un amplio rango de edad y en diferentes grupos étnicos y han sido utilizados en diversos estudios epidemiológicos (8).
Tabla No.1 Criterios para el diagnóstico de la Dermatitis Atópica en estudios epidemiológicos (8).
Debe tener:
Una enfermedad cutánea pruriginosa (o reporte de los padres de rascado) en los últimos 12 meses
Adicionalmente 3 o más de los siguientes:
-Historia de lesiones en pliegues(ante-cubitales, poplíteos, tobillos, cuello o peri- ocular)
-Historia personal de asma o rinitis (o historia de atopia en un familiar de primer grado si el niño es menor de 4 años)
-Xerosis en el último año
-Inicio antes de los 2 años (no se utiliza en menores de 4 años)
20
2.1.2. Epidemiología
La prevalencia de Dermatitis Atópica en países desarrollados varía entre 5 y 20%; esta prevalencia es variable, siendo mayor del 20% en el norte de Europa y Australasia y menos frecuente en países en desarrollo. Predomina en la infancia, por lo que la prevalencia en mayores de 20 años es alrededor del 2%(9).
Es mucho más común en clase socioeconómica alta y en familias pequeñas, esto último probablemente por una menor exposición a ciertos patógenos virales y bacterianos. Hay evidencia que sugiere que la prevalencia ha aumentado de 2 a 3 veces en los últimos 30 años; las causas de este incremento no son claras pero se postula que un aumento de la susceptibilidad a la sensibilización por factores ambientales asociado con el estilo de vida occidental sería una explicación más plausible que el aumento de alérgenos específicos o un súbito aumento en el número de individuos genéticamente susceptibles (10,11).
En un estudio con 1760 niños en Inglaterra se encontró que la severidad de la enfermedad se distribuye así: leve en 84% de los casos, moderada en 14% y severa en 2% (12).
21 La Dermatitis Atópica es una enfermedad costosa; los estudios económicos realizados en Holanda, Inglaterra, Estados Unidos, Alemania y Australia demuestran que los costos asociados con la enfermedad varían de acuerdo con el país, entre U$71 dólares en Holanda hasta U$2559 dólares en Alemania por paciente por año; estas diferencias son debidas a diferencias en las poblaciones estudiadas y a los costos de los componentes incluidos (14). En Colombia no tenemos estudios económicos pero el costo de los medicamentos, de las consultas y de la ropa adecuada es alto, lo que influiría en el cálculo del costo total de la enfermedad.
Hasta 45% de los casos de Dermatitis Atópica inician en los seis primeros meses de vida, 60% durante el primer año y el 85% antes de los 5 años de edad; es la primera manifestación de la diátesis atópica que incluye el asma y la rinitis (15). Alrededor de 1/3 de los niños entre 5 y 7 años con Dermatitis Atópica tienen asma o rinitis, aunque la edad de inicio es diferente; los niños con dermatitis atópica severa pueden desarrollar asma. El asma y la rinitis se asocian con un peor pronóstico para la evolución de la Dermatitis Atópica, así como el inicio temprano y una enfermedad severa (16). En Colombia el estudio ISAAC fase III reporta una prevalencia de dermatitis atópica, asma y rinitis de 14.6%, 10.3% y 30.7% en escolares y de 12.2%, 8.5% y 36.5% en adolescentes. (17)
2.1.3. Cuadro clinico
22 enfermedad y de los factores agravantes. Son características constantes la xerodermia o piel seca, el prurito, la tendencia a las recidivas y el curso crónico (16).
La xerodermia está presente en 73-98% de los casos, a menudo es generalizada, se relaciona con una alteración en la función del estrato córneo y una disminución en la producción de los lípidos de superficie (ceramidas). El otro síntoma es el prurito, que induce lesiones secundarias como excoriaciones y liquenificación.
Las manifestaciones clínicas varían con la edad así (16):
Fase en lactantes (0-2 años) empieza desde el tercer mes de vida son frecuentes las lesiones simétricas, con máculas eritematosas que forman vesículas y costras. Se inicia en cara y cuero cabelludo, luego en tronco y manos. El prurito aparece después del tercer mes.
Fase en preescolares y escolares (2-12 años): varían las lesiones y la localización; el prurito induce engrosamiento de la piel o liquenificación, las lesiones aparecen en sitios de extensión y de flexión en el 88% de los casos, puede haber compromiso de las manos, las plantas y distrofia ungueal.
Fase en adolescentes (12-18 años) la principal característica clínica es el eczema de los pliegues y la liquenificación en muñecas, cuello, párpados y tobillos; en los casos generalizados afecta el tronco y cuero cabelludo.
23 que se registran en una escala visual análoga. En la práctica clínica se utiliza el TIS (puntaje de severidad con 3 ítem) que evalúa la presencia de eritema, edema/pápulas y excoriaciones (máximo puntaje 9); este puntaje tiene una buena correlación con el SCORAD y una gran concordancia inter-observador (18,19).
2.2. Calidad de Vida en Dermatitis Atópica
La Dermatitis Atópica es una enfermedad de niños, por lo que la familia, especialmente los padres, son afectados por: el tiempo que requieren los tratamientos, los cambios en las dietas y en las actividades familiares.
La Dermatitis Atópica afecta la conducta y las emociones de los niños; el síntoma más frecuente es la alteración del sueño asociado con el prurito, lo que hace que se despierten varias veces en la noche; esto produce cansancio, irritabilidad y dificultad para levantarse. En adolescentes hay datos limitados en un período crítico para el desarrollo de la auto-identidad y la autoestima; se ha reportado mayor ansiedad, dificultades interpersonales y timidez asociadas con la enfermedad (20).
Coincidiendo con el impacto en los niños, las madres tienen: dificultades para asistir al trabajo, estrés y cambios en el estilo de vida, especialmente relacionados con las actividades al aire libre, en el hogar y en las vacaciones. La severidad de la enfermedad está asociada con un mayor impacto en la familia (21).
24 un desenlace importante en la práctica clínica, la investigación y en la evaluación del tratamiento. Las actividades que con mayor frecuencia se alteran son las actividades diarias, escolares, sociales y recreativas en 60% de los encuestados y 80% experimentaron alteraciones en el sueño (22).
En el 2006 Beattie y col compararon la Calidad de Vida en niños con enfermedades cutáneas con otras enfermedades crónicas de la infancia como fibrosis quística y encontraron que las enfermedades crónicas de la piel como el eccema, la urticaria y la psoriasis, aunque no acortan la vida, causan mayor alteración en la vida diaria y esto es percibido en forma diferente por los padres y los niños (23).
25
2.3. Definición de Calidad de Vida Relacionada con la salud e Instrumentos
para evaluarla
El desarrollo del estudio de la Calidad de Vida y de la calidad de vida relacionada con la salud (CVRS) surgió de la necesidad de nuevos indicadores clínicos, como parte del proceso de aumento de la expectativa de vida, mayor prevalencia de enfermedades crónicas y degenerativas; al mayor conocimiento de los pacientes sobre sus enfermedades y a los cambios en la percepción sobre salud y enfermedad, lo que derivó en una participación del paciente en la toma de decisiones relativas a su enfermedad. En la década de los 80 el concepto se introduce como variable en la práctica e investigación clínica(25).
En la evaluación de la Calidad de Vida se han considerado diferentes definiciones: algunos autores la expresan como bienestar, que es la percepción general del paciente sobre su estado de salud o sobre su enfermedad, sin discriminar los diferentes aspectos que lo determinan; mientras otros fragmentan el concepto en dimensiones como: función física, síntomas, bienestar psicológico, social, función cognitiva, actividades, constructos personales y satisfacción (26). La CVRS está centrada en el concepto de discapacidad (corresponde a los síntomas de las enfermedades) y la actividad (habilidad del individuo de funcionar en los aspectos físicos, emocionales y sociales) (27).
26 De acuerdo con el interés de investigación, los instrumentos pueden ser discriminativos o evaluativos; las propiedades psicométricas varían en cada caso: los cuestionarios discriminativos requieren altos niveles de confiabilidad para distinguir entre las personas con o sin enfermedad o con diferentes niveles, en tanto que los evaluativos deben ser sensibles al cambio y tener la habilidad de detectar los cambios importantes(29) .
En los niños el interés por el estudio de la Calidad de Vida empezó en los años 80; los primeros estudios enfatizaron dos aspectos: los niños después de un estrés o de lesiones traumáticas pueden adaptarse a su situación y, su punto de vista acerca de su alteración es muy importante (5-30). En el 2006 Ravens y col evalúan las escalas genéricas de Calidad de Vida en niños y adolescentes, resaltan la importancia de tener en cuenta, para el análisis o desarrollo de una escala, las fases del desarrollo de los niños (para lograr una adecuada correspondencia entre las mismas), así como la evaluación simultánea entre los padres y los niños y las diferencias interculturales para lograr una evaluación adecuada de este aspecto en los niños (31).
Inicialmente las escalas para medir la Calidad de Vida en niños fueron diseñadas para ser contestadas por los padres, pero al evaluar la concordancia entre los datos que suministran los padres y los hijos, se encontró que hay diferencias en algunos dominios evaluados, aunque cuantificar estos aspectos ha sido difícil por la heterogeneidad en las medidas.
27 niños. Otro aspecto es que los padres tienen experiencias que modifican la percepción de la Calidad de Vida en niños.
Actualmente se acepta que hay circunstancias en las cuales los padres deben contestar las escalas y es cuando los niños son muy jóvenes o están demasiado enfermos para responder. Así mismo es importante obtener datos directamente de los niños, evaluar y analizar los puntajes suministrados por padres e hijos, obtener información de otras personas que estén involucrados en el cuidado de los niños, para mejorar la exactitud de los resultados obtenidos en la evaluación de la Calidad de Vida en niños (5).
Los instrumentos para evaluar la Calidad de Vida pueden ser generales o específicos (32):
-Las pruebas generales se han utilizado en diversas enfermedades y en la evaluación de programas, para la asignación de recursos.
- Los instrumentos específicos para evaluar la calidad de vida en el paciente con Dermatitis Atópica son más útiles, pero hasta el momento no hay medidas específicas para niños en edad escolar.
28
Tabla No. 2. Cuestionarios para evaluar la Calidad de Vida en pacientes con Dermatitis Atópica (22).
1. Específico de Especialidad
Children’s Dermatology Life Quality Index (CDLQI) para niños 4-16 años 2. Específico de Enfermedad (Dermatitis Atópica)
Infant’s Dermatitis Quality of Life measure (IDQOL) para niños 0-4 años 3. Escalas para evaluar calidad de vida en padres de niños con dermatitis atópica - The Dermatitis Family Impact Questionnaire (DFI) mide el impacto en la vida
familiar
- Parent’s Index of Quality of Life in Atopic Dermatitis(PIQoL-AD) para padres de niños con eccema entre los 0-8 años
- Childhood Atopic Dermatitis Impact Scores (CADIS) para evaluar la calidad de vida en padres y niños con dermatitis atópica hasta los 6 años.
McKenna y col en el 2008 resaltan la poca atención que se le dado al impacto de la Dermatitis Atópica en la Calidad de Vida de los niños y sus padres, a pesar de sus características; enfatiza la necesidad de evaluar cuidadosamente este desenlace y su medición, para aprender sobre el mismo y para juzgar en forma objetiva si las intervenciones son aceptables para el paciente, así como seguras y efectivas (34).
2.4. El Cuestionario Dermatológico para evaluar Calidad de Vida en niños
(CDLQI)
29 deportes, escuela, sueño, tratamiento) y se seleccionaron 10 preguntas para evaluar los aspectos identificados; se diseñó el cuestionario y se hizo un piloto con 40 niños modificando algunos aspectos para mejorar la claridad del mismo(6).
Es el cuestionario específico de especialidad más utilizado en estudios clínicos y, ha sido validado en varios idiomas y comparado con otras escalas específicas de Calidad de Vida en Dermatitis Atópica.
En su validación inicial se aplicó a 233 niños con edades entre 4 y 16 años, se compararon los resultados con 47 niños sanos; para la evaluación del test-retest 46 niños con enfermedades dermatológicas estables completaron el formulario al 4 día de la evaluación inicial. Los puntajes de los niños sanos fueron más bajos que los de los niños con enfermedades dermatológicas y, de estos los niños con eczema tuvieron los puntajes más altos; el coeficiente de correlación de Spearman para el test-retest fue 0.86.
No se realizó el análisis factorial y hasta la fecha no se ha realizado (comunicación personal Dr A. Finlay); otras características psicométricas han sido evaluadas y ha demostrado una buena confiabilidad y sensibilidad al cambio (35,36).
30 (pregunta 10). El marco temporal hace referencia a la última semana y, cada pregunta tiene 4 posibles opciones: nada, sólo un poco, mucho y muchísimo (37).
El máximo puntaje es 30, los puntajes mayores indican mayor compromiso en la Calidad de Vida. El cuestionario puede ser auto-administrado y contestado por el paciente con o sin ayuda de sus padres; su administración requiere unos cinco minutos.
El CDLQI ha sido utilizado como medida de desenlace en estudios clínicos (con ciclosporina, metilpredinisolona y pimecrolimus) y de respuesta psicológica en niños con Dermatitis Atópica y sus familias después de diversas intervenciones (38,39,40,41,42).
2.5.Adaptación cultural de las escalas
Herdman y col en 1998 proponen un modelo más amplio que la simple traducción de la escala para la selección y aplicación de las escalas en diferentes culturas. Este modelo está basado en que el concepto de Calidad de Vida varía transculturalmente y que por lo tanto estas diferencias deben explorarse. Sugieren estudiar seis tipos de equivalencia: conceptual, semántica, operacional, de los ítem, de medición y funcional (43).
31 en diferentes países, por lo que que un instrumento no debe ser utilizado sin una adecuada adaptación cultural (44).
Guyatt G en el 2007 propone que para realizar la adaptación cultural de una escala es importante tener en cuenta dos aspectos: la evaluación lingüística que evalúa aspectos de equivalencia entre el instrumento original y la versión obtenida y la evaluación psicométrica (7). Diferentes grupos han estandarizado los pasos que deben seguirse para la validación lingüística de las escalas, que varían si la escala se traduce desde el idioma original o si ya existe una versión en el idioma en que se quiere aplicar (45). De igual manera los criterios para la validación psicométrica han sido continuamente evaluados. A continuación se revisan las definiciones de los aspectos que serán considerados en este estudio.
Lorn y col. en 1996 y posteriormente Terwee y col. en el 2007 definieron y revisaron algunos de los aspectos que se consideran importantes para evaluar las escalas de Calidad de Vida (46,29):
Confiabilidad: es el grado en el cual el instrumento está libre de error aleatorio; se examina mediante la consistencia interna que mide la correlación entre los ítem y la reproducibilidad que es la estabilidad en el tiempo (test-retest) o la comparación de los puntajes de la evaluación independiente por dos evaluadores del fenómeno en una medición puntual.
32
Sensibilidad al cambio (capacidad de respuesta): es la capacidad del instrumento para detectar cambios clínicamente importantes en el tiempo, aún si estos cambios son pequeños; a veces es considerado un aspecto que contribuye a la validez de constructo (validez longitudinal); se recomienda evaluarlo comparando los puntajes de un grupo que cambia con el que permanece estable; este cambio en los puntajes se expresa con el tamaño del efecto.
33
CAPITULO 3
PREGUNTA DE INVESTIGACION
¿Son válidos y confiables los resultados del Cuestionario Dermatológico de Calidad de Vida en Niños (CDLQI) en los pacientes con Dermatitis Atópica que asisten a consulta ambulatoria de Dermatología Pediátrica en Bogotá, Colombia?
OBJETIVOS:
3.1. Objetivo General
Realizar la Validación Lingüística y Psicométrica (adaptación cultural) del Cuestionario Dermatológico (CDQLI) para evaluar Calidad de Vida en niños, en pacientes con Dermatitis Atópica que asisten a consulta ambulatoria de dermatología en Bogotá-Colombia
3.2. Objetivos Específicos
3.2.1. Validación Lingüística
3.2.1.1. Realizar la traducción- retro-traducción de la escala
3.2.1.2. Evaluar los aspectos conceptuales, semánticos y operativos
3.2.2. Validación Psicométrica
34 3.2.2.4. Evaluar la validez discriminativa: comparar los puntajes de la
escala en pacientes con dermatitis atópica leve, moderada y severa 3.2.2.5. Estimar la validez convergente: comparar los puntajes de la
escala de Calidad de Vida con el puntaje clínico 3.2.2.6. Estimar la confiabilidad de la escala
3.2.2.6.1. Estabilidad: test-retest
3.2.2.6.2. Consistencia interna u homogeneidad: alfa de Cronbach 3.2.2.6.3. Concordancia entre observadores (padres e hijos) 3.2.2.7. Evaluar la sensibilidad al cambio
3.2.2.7.1. Tamaño del efecto: comparar los puntajes de la escala al inicio y al mes de tratamiento
3.2.2.7.2. Capacidad para detectar cambios clínicamente importantes: comparar los puntajes de los pacientes que mejoran y los que permanecen estables o empeoran después del tratamiento
3.2.3. Determinación de la utilidad de la escala
3.2.3.1. Tiempo requerido para la aplicación de la escala 3.2.3.2. Condiciones de aplicación
35
CAPITULO 4
METODOLOGÍA
4.1. Tipo de estudio: Estudio de Validación de escalas, prospectivo.
4.2. Población: Pacientes con dermatitis atópica que asistieron a consulta ambulatoria de dermatología pediátrica en Bogotá; los pacientes tenían acceso a Medicina pre-pagada y pertenecían a estratos socio-económicos 4, 5 y 6.
4.3. Muestray tamaño de muestra
Se obtuvo una muestra por conveniencia, reclutada en forma consecutiva hasta completar el tamaño de muestra calculado, de la consulta ambulatoria de Dermatología Pediátrica de 3 dermatólogas pediatras en Bogotá, Colombia desde mayo de 2008 a junio de 2009.
36
4.4. Criterios para seleccionar la población de estudio
4.4.1. Criterios de Inclusión
Diagnóstico clínico de Dermatitis Atópica según los criterios de Williams y col. (8) Edad entre 4 y16 años
Lengua madre el español-colombiano
4.4.2. Criterios de Exclusión
Trastorno psiquiátrico que limite el proceso de aplicación del formulario Incapacidad física que le impida entender o contestar el formulario. Otras enfermedades dermatológicas concomitantes
Enfermedades infecciosas agudas en las últimas 2 semanas Negativa a participar en el estudio
4.5. Consideraciones éticas
Este estudio cumple los criterios del Ministerio de Salud según la resolución 008430 de 1993 para ser clasificada como una investigación sin riesgo (consiste en la aplicación de un cuestionario) y en el artículo 16 (parágrafo 1) además está descrito que en ocasiones el Comité de Ética en Investigación de la Institución podrá dispensar al investigador de la obtención del mismo (48).
37 Se solicitó y obtuvo el consentimiento del autor de la escala Dr Andrew Finlay.
Se solicitó y obtuvo el consentimiento del Comité de Ética de la Facultad de Medicina de la Pontificia Universidad Javeriana.
4.6. Enumeración y definición de las variables del estudio
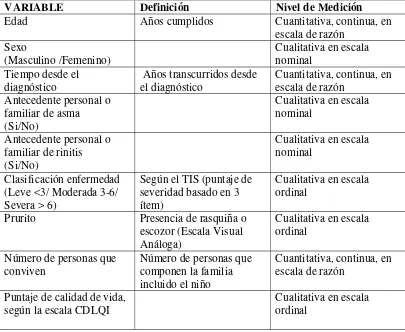
[image:37.612.115.520.313.645.2]Las variables del estudio se describen en la Tabla No. 3, así como su definición y nivel de medición.
Tabla No. 3 Variables, definición y nivel de medición
VARIABLE Definición Nivel de Medición
Edad
Años cumplidos Cuantitativa, continua, en escala de razón Sexo
(Masculino /Femenino)
Cualitativa en escala
nominal Tiempo desde el
diagnóstico Años transcurridos desde el diagnóstico Cuantitativa, continua, en escala de razón Antecedente personal o
familiar de asma (Si/No)
Cualitativa en escala nominal
Antecedente personal o familiar de rinitis (Si/No)
Cualitativa en escala nominal
Clasificación enfermedad (Leve <3/ Moderada 3-6/ Severa > 6)
Según el TIS (puntaje de severidad basado en 3 ítem)
Cualitativa en escala ordinal
Prurito Presencia de rasquiña o escozor (Escala Visual Análoga)
Cualitativa en escala ordinal
Número de personas que
conviven Número de personas que componen la familia incluido el niño
Cuantitativa, continua, en escala de razón
Puntaje de calidad de vida, según la escala CDLQI
Cualitativa en escala ordinal
38
4.7. Descripción de la metodología y análisis estadístico para la
validación lingüística y psicométrica
4.7.1. Descripción de la metodología
La definición operativa de Dermatitis Atópica para este estudio fue: una enfermedad cutánea pruriginosa en el último año con tres o más de los siguientes criterios: inicio antes de los dos años, historia personal o familiar de asma y rinitis, lesiones eccematosas de predominio en los pliegues y xerosis (8).
Para la clasificación clínica de la enfermedad se utilizó el puntaje de severidad de tres ítem (TIS) que evalúa la intensidad del eritema, del edema y las excoriaciones de 0 a 3, en la lesión más representativa. El máximo puntaje es nueve; de acuerdo con el puntaje la enfermedad se clasifica en leve (menor de 3), moderada (3-6) y severa (mayor de 6)(18).
39 La escala fue completada por los niños con o sin ayuda de los padres, pero siempre se insistió en registrar el concepto del niño; cuando los niños no necesitaban ayuda de los padres para completar el formulario, el mismo fue contestado en forma simultánea e independiente por el niño y el padre o la madre. Todos los pacientes incluidos en el estudio fueron citados a control al mes para realizar una nueva evaluación clínica y completar la escala visual de prurito y el formulario CDQLI.
4.7.2. Descripción de la escala
Se utilizó el Cuestionario Dermatológico para Evaluar Calidad de Vida en niños (CDQLI), que fue desarrollado por Susan Lewis-Jones y Andrew Finlay en 1995 y fue validado en español en España; al revisar el cuestionario final se observó que algunos ítem podrían no ser entendidos por los pacientes en Colombia, no había un consenso sobre cómo utilizar un instrumento en el mismo lenguaje para su uso en diferentes países y el autor recomendaba seguir los pasos de traducción y retro-traducción, por lo que se decidió en este estudio seguir las recomendaciones del consenso del ISPOR y del Instituto MAPI para la traducción y adaptación cultural de escalas (45,50).
40 En la última semana ¿cuánto has evitado la natación u otros deportes a causa de tu problema de la piel?
Muchísimo __ Mucho___ Solo un poco____ Nada____
El cuestionario puede ser auto-administrado y contestado por el paciente con o sin ayuda de sus padres. La calificación del mismo según los autores se realiza así (37): -si una pregunta no se contesta se anota cero y se suman todos los puntajes
-si dos o más preguntas no se contestan no se suman los puntajes
-si la pregunta 7a y 7b se contestan simultáneamente se tiene en cuenta el mayor puntaje de las dos.
El máximo puntaje es de 30, los mayores puntajes indican un mayor compromiso en la Calidad de Vida. El tiempo de administración varía entre dos y cinco minutos (6,37).
4.7.3. Validación Lingüística
La validación lingüística comprendió los siguientes pasos, según las recomendaciones del Instituto MAPI y del consenso del ISPOR (45,50):
4.7.3.1. Traducción-Retro traducción
41 revisada por el autor de la escala (A. Finlay), las correcciones del autor fueron discutidas con los traductores, se le enviaron al autor y se obtuvo una traducción definitiva por consenso.
4.7.3.2. Definición conceptual (equivalencia conceptual)
Para evaluar que la versión traducida tuviera los mismos conceptos que la versión original se solicitó a cuatro dermatólogos que revisaran e identificaran los ítem que podían ser potencialmente problemáticos.
4.7.3.3. Prueba piloto para evaluar comprensión
Se evaluó que el lenguaje fuera claro, que la redacción fuera adecuada, y que hubiera comprensión de las preguntas y de la escala de respuestas incluidas en el cuestionario. Se realizó en una muestra de diez niños sanos y en diez adultos, cuya lengua madre era el español colombiano, que vivían en Colombia; con características similares en cuanto a edad, sexo y nivel socioeconómico de los pacientes en los que se aplicaría la escala. Se realizó una entrevista en profundidad, evaluando la comprensión, qué entendían por cada ítem y se revisaron los ítem que presentaban dificultades.
4.7.3.4. Revisión clínica
42
4.7.3.5. Correcciones y versión final del instrumento
Se revisaron los errores de ortografía, gramaticales y de tipografía. El instrumento definitivo se evalúo en diez pacientes con Dermatitis Atópica y en sus padres, para determinar la utilidad de la escala; se registró el tiempo requerido para contestarlo y calificarlo y, las condiciones de su aplicación.
4.7.4. Plan de Análisis
Se recopilaran los datos en una base de datos en Microsoft Access 2007 y para el análisis estadístico se utilizó el programa STATA 10.
4.7.4.1. Análisis Descriptivo
43 Para la comparación entre los grupos se utilizaron medidas no paramétricas por la naturaleza ordinal del puntaje de la escala; la prueba de Mann-Whitney para muestras independientes y la prueba de rangos con signo de Wilcoxon para muestras pareadas.
4.7.5. Validación Psicométrica
Se consideraron los siguientes aspectos: evaluar la validez (de apariencia, de contenido, de constructo, discriminativa y concurrente), la confiabilidad y la sensibilidad al cambio.
4.7.5.1. Validez de apariencia y de contenido
Se solicitó a cinco médicos dermatólogos con entrenamiento en dermatología pediátrica que emitieran su concepto escrito respecto a si el instrumento en su apariencia correspondía a lo que se pretendía medir y si todos los aspectos pertinentes al constructo sobre calidad de vida en Dermatitis Atópica en niños estaban incluidos en el mismo, teniendo en cuenta la cantidad y contenido de las preguntas (validez de contenido) (32,51).
4.7.5.2. Validez de constructo
44 factores principales los factores son generados de la varianza común y no de la varianza total y utiliza el coeficiente de correlación múltiple al cuadrado como indicador de la comunalidad (la varianza que los ítem y los factores comparten) mientras que en el método de factores componentes principales se asume que esta es 1.0. Para mejorar la interpretación de los factores se realizó rotación ortogonal tipo Varimax (que asume independencia entre los factores). Los pasos fueron los siguientes (52):
• Paso 1. Elaboración de la base de datos, estadística descriptiva de las variables
(ítem)
• Paso 2. Establecer si cumplía los supuestos para la realización del análisis
factorial:
- Verificar la matriz de correlación
-Establecer si el determinante es diferente de 0
- Realizar el test de Kaiser-Meyer-Olkin que es un indicador de la fortaleza de la correlación entre los ítems y el coeficiente de correlación parcial. Su valor fluctúa entre 0 y 1 y entre más cercano este a 1, mayor indicación tendrá el análisis factorial.
- Prueba de esfericidad de Bartlett para descartar que la matriz de correlación sea una matriz de identidad, es decir que no hay relación entre los ítem. Es una prueba de ji cuadrado que tiene en cuenta el tamaño de la muestra, el número de ítem en la matriz y el determinante de la matriz de correlación
• Paso 3. Extracción de los factores, se obtuvo el número de factores que pudieran
45
• Paso 4: Se utilizó la rotación ortogonal tipo varimax, basado en el principio de
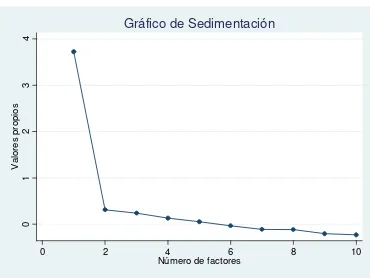
independencia de los factores entre sí. Al realizar la rotación se seleccionó los ítems de cada factor, tomando los que tienen una carga mayor de 0.4, si hay ítem que tengan cargas similares en dos o más factores se recomienda realizar un análisis de consistencia mediante el alfa de Cronbach . A partir de la matriz de factores rotados se conservaron los factores de acuerdo con los criterios: valores propios o eigenvalues >1, porcentaje de varianza extraída equivalente al 50% del total de la varianza y análisis del gráfico de sedimentación (screen plot) en busca de los puntos donde la pendiente cambiaba en forma significativa.
• Paso 5. Verificar la nominación de los factores de acuerdo con los ítem que
tienen mayor peso y que identifique el contenido.
4.7.5.3. Consistencia interna u homogeneidad
Se realizó en la totalidad de la muestra el alfa de Cronbach que permite detectar los ítem que contribuyen a la confiabilidad del instrumento; el valor de este coeficiente aumenta con el número de ítem y debe tener un grado moderado a alto de homogeneidad (0.7-0.9) (53). Adicionalmente se evalúo el cambio en el alfa de Cronbach al retirar cada ítem y en los factores detectados.
4.7.5.4. Validez discriminativa
46 Se realizó una prueba de Kruskal-Wallis para evaluar las diferencias entre los puntajes del CDQLI en los pacientes con dermatitis atópica leve, moderada y severa; al encontrar diferencia en al menos una de las parejas se decidió realizar la prueba de Mann-Whitney.
4.7.5.5. Validez convergente
Se comparó el resultado del puntaje del cuestionario CDLQI con el puntaje clínico de los pacientes mediante el coeficiente de correlación de Spearman; dado que no existe otra escala validada en nuestro medio para evaluar la Calidad de Vida en niños con Dermatitis Atópica, ni hay un patrón de oro en la evaluación de la Calidad deVida.
4.7.5.6. Confiabilidad o reproducibilidad
A todos los pacientes incluidos en el estudio se les solicitó completar nuevamente el formulario 48 horas después de la visita inicial, se escogió este tiempo porque el instrumento está diseñado para evaluar cambios en la semana previa, se espera que en este tiempo no haya cambios clínicos en la enfermedad y se evita el sesgo producido por recuerdo. Se midió la concordancia entre los dos valores obtenidos por cada sujeto mediante el coeficiente de correlación concordancia de Lin, esperando un valor mayor de 0.7 (54,55).
47 en cero; en la gráfica la línea interrumpida indica perfecta concordancia y la línea continua la exactitud (56).
Los resultados se observaron mediante el gráfico de los límites de concordancia, si las dos mediciones generan los mismos valores, los datos deben estar alrededor de cero y para determinar si las diferencias son sistemáticas o son debidas al azar se calculan los limites de concordancia y se espera que el 95% de las diferencias entre las dos mediciones se encuentren dentro de 1,96 desviaciones estándar (57).
Para evaluar la correlación entre observadores de un mismo fenómeno se solicitó a un grupo de padres y niños que contestaran simultáneamente la escala CDLQI y se compararon los resultados mediante el coeficiente de correlación y concordancia de Lin y el coeficiente de correlación de Spearman.
4.7.5.7. Sensibilidad al cambio de la escala
48 En este estudio la sensibilidad al cambio fue evaluada mediante la capacidad de la escala para detectar cambios en general y para detectar cambios clínicamente importantes (59).
La capacidad de la escala de detectar cambios en general, se evaluó mediante el cálculo del tamaño del efecto que provee información directa de la magnitud del cambio, expresado en términos de alguna medida de variabilidad. Se propone que valores de: 0.20, 0.50, 0.80 representan un tamaño del efecto pequeño, moderado y grande (58). Hay dos formas de calcularlo:
La primera es calculando el tamaño del efecto estandarizado que es la diferencia entre las medias del puntaje basal y el puntaje al control, dividido por la desviación estándar del puntaje basal; así una medida que al inicio tiene una gran variabilidad tendrá un tamaño del efecto pequeño.
La segunda es calculando la respuesta media estandarizada que se obtiene al dividir el promedio del cambio en los puntajes por su desviación estándar; es un estimativo del cambio en la medición que tiene en cuenta la variabilidad de los puntajes entre los pacientes.
La capacidad de la escala para detectar cambios clínicamente importantes, para lo cual se compararon los puntajes de la escala CDLQI los pacientes que mejoraron con los que permanecieron igual o empeoraron después de un mes de tratamiento, mediante una prueba de Mann-Whitney para muestras independientes.
49 visual análoga de prurito se preguntó ¿En comparación con visita anterior que tanto ha cambiado el prurito (rasquiña o escozor) que le produce su enfermedad de piel?) y se solicitó que completaran nuevamente la escala CDLQI.
Se compararon los puntajes obtenidos en la escala CDQLI, los puntajes del TIS y los de la EVA de prurito en pacientes con Dermatitis Atópica al inicio y al mes de tratamiento, mediante una prueba de rangos con signos de Wilcoxon para muestras pareadas.
50
CAPITULO 5
RESULTADOS
5.1. Validación Lingüística
El proceso de validación del CDLQI se realizó de Febrero a Mayo del 2008, siguiendo las normas propuestas, y permitió lograr la equivalencia conceptual y semántica de la versión final con la escala original. Durante la evaluación conceptual hubo acuerdo en que los conceptos evaluados en la versión final eran los mismos que medía la escala original y sólo se identificó las diferentes maneras con que las personas se refieren al prurito en nuestro medio por lo que se decidió utilizar la que con mayor frecuencia utilizan los pacientes.
5.2. Descripción de la muestra y los puntajes de la escala
51
Tabla No. 4 Aspectos demográficos de los pacientes con Dermatitis Atópica
VARIABLE Medición
Edad
Media 8.5(3.2)
IC95% 7.842‐9.178
Sexo
Masculino
Femenino
39(39%)
62 (61%)
Tiempo desde el diagnóstico
(años)
Media 4.2(3.8)
IC95% 3.47 ‐ 4.99
Antecedente personal o
familiar de asma
Si
No
Sin respuesta
43(43%)
54 (53%)
4 (4%)
Antecedente personal o
familiar de rinitis
Si
No
Sin respuesta
68 (67%)
32 (32%)
1 (1%)
Clasificación de la
enfermedad (TIS)
Leve <3
Moderada 3‐6
Severa > 6
10(10%)
70 (69%)
21 (21%)
Prurito Media 7.0(2.4) IC 95% 6.54‐7.49
Mediana 8
Número de personas que
forman la familia
Media 4(1.35) IC95% CI 3.34‐4.23
Mediana 4(3,5)
5.2.1. Clasificación clínica de acuerdo con el sexo y la edad
52
Tabla No.5 Clasificación clínica de la Dermatitis Atópica (escala TIS) según el sexo
Clasificación clínica Niños Niñas
Leve 3 (8%) 7 (11%)
Moderada 28 (71%) 42 (68%)
Severa 8 (21%) 13 (21%)
[image:52.612.115.491.260.341.2]
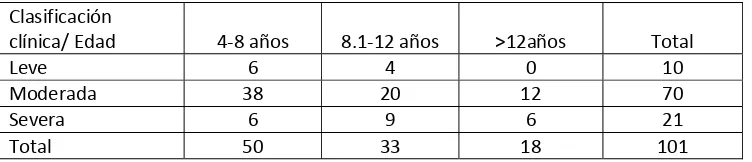
Tabla No.6 Clasificación de la Dermatitis Atópica (escala TIS) según la edad
Clasificación
clínica/ Edad
4‐8 años
8.1‐12 años
>12años
Total
Leve 6 4 0 10
Moderada 38 20 12 70
Severa 6 9 6 21
Total 50 33 18 101
5.2.2. Puntaje de la escala
53
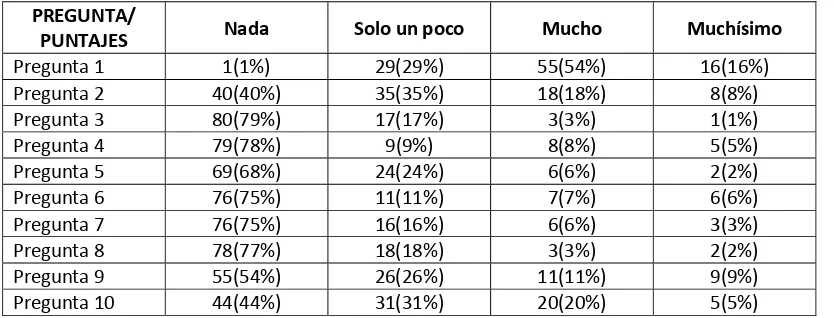
Tabla No. 7 Distribución porcentual de las respuestas del CDQLI en niños con Dermatitis Atópica
PREGUNTA/
PUNTAJES Nada Solo un poco Mucho Muchísimo
Pregunta 1 1(1%) 29(29%) 55(54%) 16(16%)
Pregunta 2 40(40%) 35(35%) 18(18%) 8(8%)
Pregunta 3 80(79%) 17(17%) 3(3%) 1(1%)
Pregunta 4 79(78%) 9(9%) 8(8%) 5(5%) Pregunta 5 69(68%) 24(24%) 6(6%) 2(2%)
Pregunta 6 76(75%) 11(11%) 7(7%) 6(6%)
Pregunta 7 76(75%) 16(16%) 6(6%) 3(3%)
Pregunta 8 78(77%) 18(18%) 3(3%) 2(2%) Pregunta 9 55(54%) 26(26%) 11(11%) 9(9%)
Pregunta 10 44(44%) 31(31%) 20(20%) 5(5%)
Para evaluar de acuerdo con el sexo y la edad los ítem que presentaban mayor frecuencia de respuestas se sumaron los porcentajes de las opciones de repuesta que indicaban algún grado de compromiso (solo un poco, mucho y muchísimo). En las niñas y los niños se observó que las preguntas relacionadas con prurito (100%vs 97%), sentimientos (65%vs 54%), sueño (44%vs 49%) y tratamiento (50%vs 64%) mostraban mayor porcentaje de compromiso; en las niñas se observó un mayor porcentaje en la pregunta relacionada con las preguntas sobre la enfermedad (27% vs 13%). Esta frecuencia de respuestas en los tres grupos de edad categorizada, mostró que en los mayores de 12 años la mayoría de las preguntas presentaban algún efecto de la enfermedad que fue mayor del 40%( Anexos 1 y 2).
5.2.2.1. Según sexo y edad
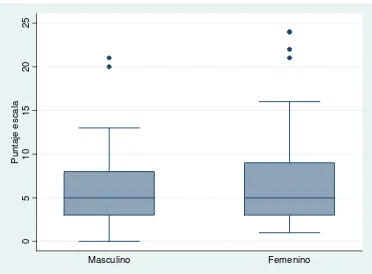
54
Figura No. 1 Distribución del puntaje de la escala CDQLI según el sexo de los pacientes con Dermatitis Atópica
0
5
10
15
20
25
P
u
nt
aj
e
e
s
c
a
la
Masculino Femenino
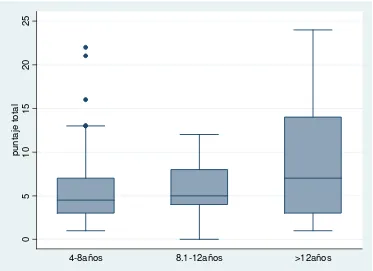
En la Tabla No. 8 se describen los puntajes de acuerdo con los grupos de edad; no se observó diferencia en el puntaje entre los grupos de edad (X2 3.84 p=0.14). En la Figura No.2 se observa la distribución de los mismos.
Tabla No. 8 Distribución del puntaje del CDLQI según la edad
Edad(años) n Mediana(rango) Media(DE)
4.0 – 8.0 50 4,5 (3,7) 5.8 (4.8) 8.1 – 12.0 33 5 (4,8) 6.15 (2.8)
[image:54.612.203.436.551.607.2]55
Figura No.2 Distribución del puntaje de la escala CDQLI según la edad de los pacientes con Dermatitis Atópica
0
5
10
15
20
25
pu
nt
aj
e t
o
ta
l
4-8años 8.1-12años >12años
5.3.Validez de validez de apariencia y de contenido
Hubo acuerdo en el grupo de dermatólogos en que el instrumento en su apariencia correspondía a lo que se pretendía medir y que los aspectos pertinentes al constructo sobre Calidad de Vida en Dermatitis Atópica en niños estaban incluidos en el mismo, teniendo en cuenta la cantidad y el contenido de las preguntas (validez de contenido).
5.4. Estimación de la validez de constructo
56 esfericidad de Barlett ( X2 347.56, p <0.001), el determinante de la matriz fue diferente de 0 (0.025) y la prueba de Kaiser Meyer Olkin que es una medida de homogeneidad de las variables que mide la adecuación de los datos para un análisis factorial fue de 0.86, lo que es considerado muy bueno para efectuar el análisis factorial. Al cumplirse los supuestos se realizó el análisis factorial.
5.4.2. Extracción de los factores: Se hizo un análisis factorial exploratorio, mediante dos procedimientos de análisis de factores comunes (Factores Principales y Factores Componentes Principales) para determinar la estructura de dominios de la escala.
57
Figura 3. Valores propios para la selección de Factores
0
1
2
3
4
Val
o
re
s p
ro
p
io
s
0 2 4 6 8 10
Número de factores
Gráfico de Sedimentación
Tabla No.9 Valores Propios y Cargas Factoriales (Método de Factores Principales)
Factor Valor propio Porcentaje de la Varianza
Porcentaje Acumulado
1 3.720 0.983 0.983
2 0.312 0.082 1.066
3 0.242 0.108 1.130
4 0.133 0.035 1.165
5 0.053 0.014 1.179
6 -0.030 -0.008 1.171
7 -0.107 -0.028 1.143
8 -0.113 -0.030 1.113
9 -0.201 -0.053 1.059
[image:57.612.156.486.462.628.2]58
Tabla No.10 Valores de Unicidad (Método de Factores Principales)
Item Unicidad
Prurito 0.761 Sentimientos 0.583
Relación amigos 0.345
Cambio de ropa 0.496
Juegos 0.298 Deportes 0.775 Actividades diarias 0.349
Preguntas 0.604
Alteración sueño 0.563
Problemas tratamiento 0.759
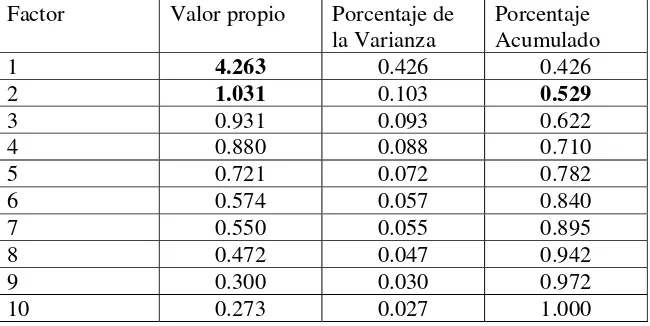
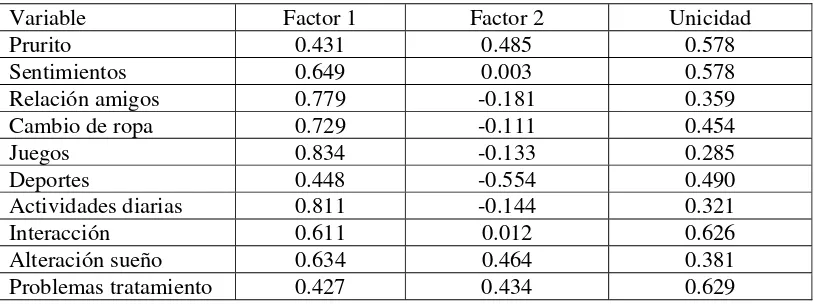
Con el procedimiento de Factores Componentes Principales se encontró que dos factores explicaban el 53% de la varianza (Tabla No. 11 y 12). Las cargas factoriales luego de la rotación ortogonal (Varimax) sugieren que el Factor 1 agrupa aspectos relacionados con sentimientos, cambio de ropa, efecto sobre los juegos, efecto sobre las actividades deportivas, actividades diarias y de interrelación personal, el Factor 2 agrupa los síntomas (prurito y alteración del sueño) y los problemas con el tratamiento(Tabla No. 13).
Tabla No.11 Valores Propios (Método de Factores Componentes Principales)
Factor Valor propio Porcentaje de la Varianza
Porcentaje Acumulado
1 4.263 0.426 0.426
2 1.031 0.103 0.529
3 0.931 0.093 0.622
4 0.880 0.088 0.710
5 0.721 0.072 0.782
6 0.574 0.057 0.840
7 0.550 0.055 0.895
8 0.472 0.047 0.942
9 0.300 0.030 0.972
[image:58.612.116.441.481.644.2]59
Tabla No. 12 Cargas Factoriales (Método de Factores Componentes Principales)
Variable Factor 1 Factor 2 Unicidad
Prurito 0.431 0.485 0.578
Sentimientos 0.649 0.003 0.578
Relación amigos 0.779 -0.181 0.359
Cambio de ropa 0.729 -0.111 0.454
Juegos 0.834 -0.133 0.285
Deportes 0.448 -0.554 0.490
Actividades diarias 0.811 -0.144 0.321
Interacción 0.611 0.012 0.626
Alteración sueño 0.634 0.464 0.381
Problemas tratamiento 0.427 0.434 0.629
Tabla No.13 Cargas Factoriales y Unicidad (Método de Factores Componentes Principales) después de la rotación Varimax
Variable Factor 1 Factor 2 Unicidad
Prurito 0.110 0.640 0.578
Sentimientos 0.549 0.346 0.578
Relación amigos 0.757 0.258 0.359
Cambio de ropa 0.678 0.290 0.454
Juegos 0.778 0.327 0.285
Deportes 0.674 0.233 0.490
Actividades diarias 0.765 0.305 0.321
Interacción 0.512 0.333 0.626
Alteración sueño 0.293 0.729 0.381
Problemas tratamiento 0.133 0.594 0.629
5.5. Estimación de la consistencia interna de la escala y de los factores
identificados
[image:59.612.115.524.331.481.2]60
5.6. Estimación de la validez discriminativa
[image:60.612.112.528.404.497.2]Se comparó el puntaje obtenido con el CDLQI en cada uno de los grupos clínicos en los que fueron clasificados los pacientes (leve, moderado, severo). Se realizó una prueba de Kruskal-Wallis, se encontró que la mediana de los puntajes era diferente en por lo menos una de las parejas (X2 18.36 p<0.001). Posteriormente se compararon de forma pareada los diferentes grupos, encontrando diferencias estadísticamente significativas entre todos ellos; los resultados se presentan en la Tabla No.14. En la Figura No.4 se aprecia la distribución de los puntajes de acuerdo con la severidad clínica de la enfermedad.
Tabla No. 14 Comparación del puntaje de la escala CDQLI de acuerdo con la severidad clínica de la Dermatitis Atópica
Clasificación
clínica
n
PUNTAJE TOTAL Prueba de Mann Whitney (valor de p)
Media Mediana Leve‐
Moderado
Leve‐
Severo
Moderado ‐
Severo
Leve 10 3.7 (3.6) 2.5 (2,4) 0.04* 0.001* 0.001*
Moderado 70 5.7 (3.9) 5 (3,7)
Severo 21 10.9 (6.7) 9 (6,13)
61
Figura No. 4. Puntajes del CDLQI según la clasificación clínica de la Dermatitis Atópica
0
5
10
15
20
25
P
u
nt
a
je e
s
c
a
la
Leve Moderada Severa
5.7. Estimación de la validez convergente:
62
5.8. Estimación de la confiabilidad o reproducibilidad:
46 pacientes contestaron el formulario a las 48 horas de la primera evaluación; dos pacientes fueron excluidos del análisis porque los datos estaban incompletos; la distribución en cuanto a severidad de la enfermedad de los pacientes fue leve (7%), moderada (70%) y severa (23%), similar a la distribución de la muestra en general.
El resultado del coeficiente de correlación y concordancia de Lin fue de 0.87 (IC95% 0.79-0.94) p <0.001, c_b=0.97; la media de la diferencia entre las mediciones fue de 0.86 (SD 2.27) y los limites de concordancia 95% están entre -3.60 y 5.32.
[image:62.612.124.511.485.685.2]
En la Figura No. 5 se observa la distribución de los puntajes en las dos mediciones; la línea interrumpida indica una perfecta concordancia y la línea continua indica la exactitud de los resultados y mide la precisión.
63 En la Figura No. 6 se observa la distribución de las diferencias alrededor de la media de la diferencia de los puntajes (0.86) medidos al inicio y a las 48 horas. Cada punto representa la diferencia del puntaje del CDLQI entre las dos mediciones, los niños que tuvieron el mismo valor están cerca del cero y la mayoría de las diferencias se encuentran dentro de los límites de concordancia; así mismo estas diferencias no presentan un patrón de distribución específico, lo que hace pensar que las mismas son debidas al azar.
Figura No.6 Diferencias de las mediciones de los puntajes del CDLQI y límites de concordancia en el test-retest (Gráfico de Blant-Altman)
64
5.9. Estimación de la sensibilidad al cambio de la escala
Esta estimación se realizó en 47 pacientes de la muestra total que asistieron al control al mes de la consulta inicial (uno fue excluido porque no se completó la evaluación clínica en el control). Todos los pacientes que fueron incluidos en el estudio fueron citados al control, a los no asistentes se les llamó y la causa más frecuente de no asistencia fue que el niño estaba mejor, otra causa fue viaje; se observó una mayor tendencia a volver al control cuando había recidiva de la enfermedad. Todos los que asistieron al control fueron incluidos en el análisis.
De acuerdo con la severidad de la enfermedad los pacientes que volvieron a control eran leves (6%), moderados (77%), severo (17%), lo cual fue similar a lo observado en el grupo total.
65
Tabla No.15 Clasificación clínica (TIS), prurito y puntaje de la escala CDLQI al inicio y al control
Variables/ Estadísticas Media (DE) Mediana (rango) Prueba del signo de Wilcoxon TIS Inicial control 4.8 (1.7) 2.2 (1.7) 4(4,6) 2(1,3) p<0.001* Prurito(EVA) inicial control 7 (2.3) 3 (2.6) 7 (5,9) 3 (0,5) p<0.001* CDLQI inicial
control 7.6 (5.7) 2.5 (3.1) 5.5(4,9) 1(1,4) p<0.001* *estadísticamente significativo
Adicionalmente para evaluar los cambios clínicos en los pacientes con Dermatitis Atópica después del tratamiento, se realizó a una prueba de homogeneidad (Stuart-Maxwell); en siete pacientes desaparecieron las lesiones y hubo tendencia a la mejoría, (p<0.001).
5.9.1. Tamaño del efecto
El puntaje basal promedio de la escala es los niños fue de 7.6 (DE 5.7) y el puntaje al control fue de 2.5 (DE 3.1), el tamaño del efecto fue= 5.0/5.7=0.88 y la Respuesta media estandarizada fue=5.0/5.6=0.89, de acuerdo con lo propuesto, este es un tamaño de efecto grande.
66 De los 47 niños que asistieron al control, 70% presentaron mejoría clínica con el tratamiento; con la prueba de Mann-Whitney se observó que no había diferencia entre los puntajes de la escala CDLQI en la visita inicial entre los niños que mejoraron y los que permanecieron igual o empeoraron (p=0.7) mientras que en el control si hubo diferencia en los puntajes (p<0.001).
5.10. Determinación de la utilidad de la escala
67
CAPITULO 6
DISCUSION Y CONCLUSIONES
El cuestionario CDLQI es el más utilizado para evaluar la Calidad de Vida en niños con enfermedades dermatológicas crónicas y recidivantes, como la Dermatitis Atópica y aunque en su desarrollo inicial se puede detectar algunas omisiones, por su amplio uso para evaluar el desenlace de Calidad de Vida en niños, en diferentes países y en estudios clínicos, se decidió realizar la Validación Lingüística y Psicométrica de este instrumento (adaptación cultural).
Una de las ventajas que ofrece la adaptación de un cuestionario existente frente al desarrollo de un nuevo instrumento es la de proporcionar un instrumento apto para la realización de estudios multicéntricos internacionales y es el primer paso para evaluar la Calidad de Vida en niños en una de las enfermedades dermatológicas más frecuentes y con una prevalencia que va en aumento en nuestro país. Adicionalmente, dado que es el más utilizado, tenerlo validado permite que los resultados sean fácilmente comparables con otros estudios.