TEMA 5: Reacciones de transferencia de electrones
1. Concepto de oxidación y reducción.
Desde un punto de vista electrónico se define:
A. Oxidación: Aquel proceso por el que una especie química pierde electrones.
Fe – 2e- Fe2+
B. Reducción: Aquel proceso por el que una especie química gana electrones.
Fe3+ + 1e- Fe2+
De acuerdo con el principio de conservación de la carga, cuando una especie se oxida (pierde electrones) debe haber otra que se reduzca (gane esos electrones) por lo tanto, siempre que se produzca una oxidación, habrá una reducción.
A la sustancia que provoca la oxidación se le denomina oxidante, esta sustancia es la encargada de aceptar los electrones de la sustancia a la que se enfrenta (a la que oxida), por lo que podemos afirmar que el oxidante se reduce. Por otro lado, el reductor es aquella especie química que pierde electrones, que serán absorbidos por el oxidante, por lo que el reductor terminará oxidado. Por ejemplo:
Fe + Cu2+ Fe2+ + Cu Reductor oxidante
(se oxida –2e-) (se reduce +2e-)
Un reductor se define como fuerte cuando tiene una gran tendencia a desprenderse de electrones y se entiende como débil, cuando esa tendencia es baja. De forma análoga, un oxidante puede ser fuerte o débil según su alta o baja tendencia a aceptar electrones. El carácter oxidante o reductor de una sustancia es relativo ya que depende de la sustancia a la que se enfrente. Por lo que es bastante común que una sustancia pueda actuar como ocidante en unos procesos y como reductor en otros.
1.2. Números de oxidación.
El número de oxidación se define como la carga que un átomo tendría si los electrones de cada uno de los enlaces que forma perteneciesen exclusivamente al átomo más electronegativo. Existen reglas sencillas que permiten hacer una rápida asignación de los números de oxidación.
- Los átomos neutros libres no tienen carga y los átomos de moléculas homonucleares tampoco (por los enlaces apolares). Cualquier elemento, cuando no está combinado con átomos de otro elemento tiene un número de oxidación igual a 0.
- La suma de los átomos de un compuesto debe de ser nula, y en le caso de iones debe de ser igual a la carga.
- Los metales siempre tienen número de oxidación positivo, los alcalinos +1 y los alcalino térreos +2.
- El hidrógeno siempre se combina con número de oxidación +1, excepto en los hidruros metálicos que lo hace con -1
- El oxígeno presenta casi siempre estado de oxidación +2, excepto en los peróxidos, donde su número de oxidación es +1.
Una reacción química es redox si en el curso de la misma alguno de los átomos cambia de número de oxidación, un aumento es oxidación y un descenso reducción. Por ejemplo:
En este proceso observamos las siguientes variaciones en los números de oxidación:
Mn Mn proceso de oxidación ( pérdida de 5 electrones) +2 +7
Pb Pb proceso de reducción (ganancia de 2 electrones) +4 +2
2. Reacciones redox
2.1. Ajuste de reacciones redox mediante el método ión-electrón.
Supongamos la siguiente reacción redox:
K2Cr2O7 + K2SO3 + HCl Cr2 (SO4)3 + KCl + H2O
En medio ácido:
1- Se calculan los números de oxidación y se escriben los iones de las especies que se reducen u oxidan.
Reducción ( + 3e-)
K2Cr2O7 + K2SO3 + HCl Cr2 (SO4)3 + KCl + H2O +1 +6 -2 +1 +4 –2 +1 -1 +3 +6 –2 +1 –1 +1 –2
Oxidación ( -2 e-)
Semirreacción de reducción: Cr2O7 = Cr3+
Semirreacción de oxidación: SO3= SO4=
2- Se escriben por separado las semirreacciones y se ajusta, añadiendo agua donde sea necesario (para ajustar el oxígeno) y los protones (para ajustar hidrógeno) necesarios para contrarrestar al otro lado.
Semirreacción de reducción: Cr2O7 = + 14 H+ 2Cr3+ + 7H2O
Semirreacción de oxidación: SO3= + H2O SO4= + 2 H+
3- Se ajustan las cargas eléctricas añadiendo electrones.
Semirreacción de reducción: Cr2O7 = + 14 H+ + 6e- 2Cr3+ + 7H2O
Semirreacción de oxidación: SO3= + H2O SO4= + 2 H+ + 2e
-4- Se multiplican para igualar los electrones cedidos en cada caso y se suman:
Semirreacción de reducción: Cr2O7 = + 14 H+ + 6e- 2Cr3+ + 7H2O
Semirreacción de oxidación: 3 x (SO3= + H2O SO4= + 2 H+ + 2e-)
Cr2O7 = + 14 H+ + 6e- + 3SO3= + 3H2O 2Cr3+ + 7H2O + 3SO4= + 6 H+ + 6e-
Cr2O7 = + 8 H+ + 3SO3= 2Cr3+ + 4H2O + 3SO4=
5- Se identifica el resultado con cada especie química y se ajusta la reacción final.
En medio básico:
1- Se comienza como en las ácidas, pero a la hora de ajustar añadimos OH- para igualar al agua que haya y los protones necesarios para contrarrestar.
2- El procedimiento sigue como antes.
2.2. Estequiometría en reacciones redox. Equivalente Redox.
Un a vez ajustada la reacción tenemos la información suficiente para poder realizar cálculos estequiométricos.
2.2.1. Equivalente redox.
Se denomina equivalente redox de una sustancia a la cantidad de esa sustancia que está implicada en el intercambio de un mol de electrones. A la masa resultante se le denomina peso equivalente y se calcula:
Por ejemplo: el ion NO3- actúa como oxidante en medio ácido, pudiendo reducirse a NO2 o NO dependiendo de los casos:
NO3- + 2H+ 1e- NO2 + H2O
NO3- + 4H+ 3e- NO + 2H2O
Si tenemos al oxidante o al reductor en disolución, la concentración de esta se puede expresar utilizando el concepto de Normalidad, que se define como el nº de equivalentes presentes por cada litro de disolución:
Se ha observado que las reacciones redox transcurren equivalente a equivalente, es decir que por cada equivalente de oxidante reacciona un equivalente de reductor. Este concepto teórico es la base de las valoraciones redox, que son procesos experimentales que permiten conocer la concentración de una disolución problema a partir de una disolución patrón de concentración conocida gracias al proceso redox que se produce al ponerse ambas en contacto. El punto de equivalencia se obtiene cuando el nº de equivalentes del oxidante coincide con el nº de equivalentes del reductor. Para poner de manifiesto este punto usaremos un indicador redox, que será una sustancia que presenta distinto color en su forma oxidada y en su forma reducida. El procedimiento experimental es similar al descrito en el tema de acidos y base.
En el punto de equivalencia se cumple:
nº de equivalentes del oxidante = nº de equivalentes del reductor
3. Celdas electroquímicas.
Son dispositivos que permiten obtener una corriente eléctrica a partir de una reacción redox. Una celda electroquímica bastante común es la llamada pila Daniell. Se basa en la siguiente exeriencia: al poner en contacto una barra de cinc con una disolución de sulfato de cobre (color azul) se observa que la disolución va perdiendo color poco a poco y el la barra de cinc se va recubriendo de residuos de cobre. La explicación es el siguiente proceso redox:
CuSO4 + Zn ZnSO4 + Cu
Oxidación: Zn - 2e- Zn2+
Reducción: Cu2+ + 2e- Cu
Zn(s) + Cu2+(ac) Zn2+ (ac) + Cu(s)
Para lograr que los electrones pasen por un hilo conductor externo, Daniell separó físicamente las dos semirreacciones mediante el siguiente dispositivo:
Así la celda electroquímica constaba de :
Dos electrodos:
1. Ánodo (-): electrodo donde tiene lugar la oxidación Zn(s) - 2e- Zn2+(ac)
2. Cátodo (+): electrodo donde tiene lugar la reducción Cu2+ (ac) + 2e- Cu(s)
Los dos electrodos se encuentran sumergidos en disoluciones propias (sulfatos de cobre y de zinc)
La separación de los dos electrodos se puede realizar mediante un tabique poroso o un puente salino, que permitan la movilidad iónica, cerrando así el circuito. Al conectar un voltímetro en el hilo conductor se observaba una ddp.
3.1. Representación de las celdas electroquímicas.
Las celdas o pilas se representan mediante el siguiente diagrama:
Se escribe a la izquierda el proceso del ánodo y a la derecha el proceso ocurrido en el cátodo, separados por un doble barra vertical que representa al puente salino. Por ejemplo:
(-) Zn(s) Zn2+(ac) Cu2+ (ac) Cu(s) (+)
3.2. Potencial de una pila.
El potencial de una pila es la diferencia de potencial existente entre los electrodos de la celda.
Si la reacción global de la pila se obtiene mediante la suma de las semireacciones del ánodo y del cátodo, el potencial de la pila se podría conocer mediante la suma algebraica de los potenciales de cada electrodo. Sin embargo es imposible conocer el potencial de un electrodo aislado. Para solucionar este problema, se puede tomar un electrodo de referencia al que se le asigna arbitrariamente un valor cero. Este electrodo de referencia es un electrodo de hidrógeno en condiciones estándar (1 atm, 1 M). El proceso que tiene lugar es el siguiente:
H+(ac) (1M) + 2e- H2(g) (1atm) Eº = 0,00 V Eº es el potencial estándar o normal de reducción
A continuación construiremos una pila con este electrodo ( de hidrógeno) y otro cualquiera, por ejemplo, el de Cu, y medimos la diferencia de potencial generada en la celda. Esta diferencia será asignada al electrodo de Cu denominándose potencial estándar o normal de reducción del cobre:
Eº( Cu2+/Cu) = 0,34 V Eº( Zn2+/Zn) = -0,76 V
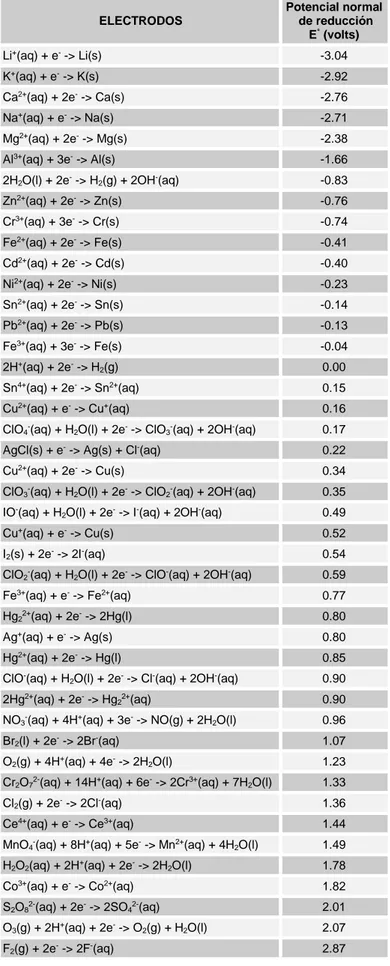
Si a continuación efectuamos esto con otros electrodos, asignaremos los potenciales normales de reducción a cada uno de ellos, recogidos en la tabla. En esta tabla los potenciales hacen referencia a los procesos de reducción, si queremos el potencial de oxidación invertiremos el proceso y cambiaremos de signo al potencial.
Cuanto mayor sea el valor del potencial de reducción, mayor será la tendencia de la especie a reducirse
Gº = - nFEº n =nº moles de electrones
F= carga por mol de electrones (96500 C)
A partir de la tabla podremos conocer el potencial normal de una pila constituida por dos electrodos, para ellos tendremos en cuenta:
1º Aquella sustancia que presente mayor potencial, actuará de cátodo
2º En el otro electrodo tendrá el papel de ánodo, donde se llevará a cabo la oxidación, teniendo que invertir el proceso y cambiar el signo del potencial asociado al electrodo 3º El potencial de la pila resultará sumando los dos potenciales
Eº( Cu2+/Cu) = 0,34 V cátodo, reducción, al ser mayor Eº Eº( Zn2+/Zn) = -0,76 V ánodo, oxidación
Cátodo: Cu2+ (ac) + 2e- Cu(s) ; E1º = 0,34 V
Ánodo:
Zn(s) - 2e- Zn2+(ac); E2º( Cu2+/Cu) = 0,76 V
TABLA DE POTENCIALES NORMALES DE REDUCCIÓN
ELECTRODOS
Potencial normal de reducción
E° (volts)
Li+(aq) + e- -> Li(s) -3.04
K+(aq) + e- -> K(s) -2.92
Ca2+(aq) + 2e- -> Ca(s) -2.76
Na+(aq) + e- -> Na(s) -2.71
Mg2+(aq) + 2e- -> Mg(s) -2.38
Al3+(aq) + 3e- -> Al(s) -1.66
2H2O(l) + 2e- -> H2(g) + 2OH-(aq) -0.83
Zn2+(aq) + 2e- -> Zn(s) -0.76
Cr3+(aq) + 3e- -> Cr(s) -0.74
Fe2+(aq) + 2e- -> Fe(s) -0.41
Cd2+(aq) + 2e- -> Cd(s) -0.40
Ni2+(aq) + 2e- -> Ni(s) -0.23
Sn2+(aq) + 2e- -> Sn(s) -0.14
Pb2+(aq) + 2e- -> Pb(s) -0.13
Fe3+(aq) + 3e- -> Fe(s) -0.04
2H+(aq) + 2e- -> H
2(g) 0.00
Sn4+(aq) + 2e- -> Sn2+(aq) 0.15
Cu2+(aq) + e- -> Cu+(aq) 0.16
ClO4-(aq) + H2O(l) + 2e- -> ClO3-(aq) + 2OH-(aq) 0.17
AgCl(s) + e- -> Ag(s) + Cl-(aq) 0.22
Cu2+(aq) + 2e- -> Cu(s) 0.34
ClO3-(aq) + H2O(l) + 2e- -> ClO2-(aq) + 2OH-(aq) 0.35
IO-(aq) + H
2O(l) + 2e- -> I-(aq) + 2OH-(aq) 0.49
Cu+(aq) + e- -> Cu(s) 0.52
I2(s) + 2e- -> 2I-(aq) 0.54
ClO2-(aq) + H2O(l) + 2e- -> ClO-(aq) + 2OH-(aq) 0.59
Fe3+(aq) + e- -> Fe2+(aq) 0.77
Hg22+(aq) + 2e- -> 2Hg(l) 0.80
Ag+(aq) + e- -> Ag(s) 0.80
Hg2+(aq) + 2e- -> Hg(l) 0.85
ClO-(aq) + H
2O(l) + 2e- -> Cl-(aq) + 2OH-(aq) 0.90
2Hg2+(aq) + 2e- -> Hg
22+(aq) 0.90
NO3-(aq) + 4H+(aq) + 3e- -> NO(g) + 2H2O(l) 0.96
Br2(l) + 2e- -> 2Br-(aq) 1.07
O2(g) + 4H+(aq) + 4e- -> 2H2O(l) 1.23
Cr2O72-(aq) + 14H+(aq) + 6e- -> 2Cr3+(aq) + 7H2O(l) 1.33
Cl2(g) + 2e- -> 2Cl-(aq) 1.36
Ce4+(aq) + e- -> Ce3+(aq) 1.44
MnO4-(aq) + 8H+(aq) + 5e- -> Mn2+(aq) + 4H2O(l) 1.49
H2O2(aq) + 2H+(aq) + 2e- -> 2H2O(l) 1.78
Co3+(aq) + e- -> Co2+(aq) 1.82
S2O82-(aq) + 2e- -> 2SO42-(aq) 2.01
O3(g) + 2H+(aq) + 2e- -> O2(g) + H2O(l) 2.07
3.3 Ecuación de Nerst
Cuando no se trabaja en condiciones estándar, el potencial de una pila se calcula aplicando la ecuación de Nerst:
Por ejemplo:
Cuando una pila se agota, se alcanza el equilibrio, el potencial de la pila se hace nulo y el cociente de reacción se convierte en la constante de equilibrio:
4. Electrolisis.
Es el proceso por el cual se ocasionan reacciones químicas a partir de energía eléctrica. El recipiente donde tiene lugar la electrolisis recibe el nombre de cuba electrolítica. En la cuba se introducen los reactivos en disolución o fundidos y a continuación se les somete a una intensidad de corriente por parte de dos electrodos, forzando así la reacciones químicas en el cátodo y en el ánodo.
No debemos confundir una pila con una cuba electrolítica, las principales diferencias son las siguientes:
Pila Electrolisis
Produce energía eléctrica a partir de reacciones químicas
Produce reacciones químicas a partir de energía eléctrica
Reacción espontánea Reacción no espontánea
Ánodo: oxidación, polo negativo Cátodo: reducción, polo positivo
Ánodo: oxidación, polo positivo Cátodo: reducción, polo negativo
Veamos algunos ejemplos:
A. Electrolisis de sales fundidas: introducimos en la cuba NaCl fundido:
Reducción : cátodo (-) : 2 Na+(l) + 2 e- 2 Na (s) Eº1 = - 2,71 V
Oxidación : ánodo: (+) : 2 Cl- (l) - 2 e- Cl
2 (g) Eº2 = - 1,36 V
El signo (-) de Eº indica que el proceso no es espontáneo y que habrá que aportar al menos 4,07 V para que se produzca.
B. Electrolisis del agua: se le añade un poco de H2SO4 para mejorar su conductividad
Reducción : cátodo (-) : 4 H+(ac) + 4 e- 2 H
2 (g) Eº1 = 0,00 V
Oxidación : ánodo: (+) : 2 H2O(l) - 4 e- 4 H+(ac) + O2 (g) Eº2 = - 1,23 V
2 H2O(l) 2 H2(g) + O2 (g) Eº = -1,23 V
C. Electrolisis de NaCl en disolución:
Ahora tenemos dos especies que pueden reducirse, Na+ y el H2O, sin embargo, al ser mayor el potencial de reducción de agua (-0,83 V) que el del sodio (-2,71 V), se reducirá el agua:
Reducción : cátodo (-) : 2 H2O(l) + 2 e- H2 (g) + 2 OH- Eº1 = - 0,83 V
Oxidación : ánodo: (+) : 2 Cl- (l) - 2 e- Cl
2 (g) Eº2 = - 1,36 V
2 H2O(l) + 2 Cl- (l) H2(g) + Cl2 (g) + 2 OH- Eº = -2,19 V
4.1. Leyes de Faraday
Las leyes de Faraday relacionan la energía electrica administrada con la masa acumulada en los electrodos
1ª Ley: La cantidad de una sustancia producida durante una electrólisis es directamente
proporcional a la intensidad (I) y al tiempo (t) que circula la misma, es decir, a la cantidad de carga eléctrica (Q) que circula por el electrolito.
2ª Ley: Cuando por un electrodo pasa un mol de electrones, se deposita o se libera un
equivalente de la sustancia. La carga correspondiente a un mol de electrones se calcula fácilmente:
1 mol de electrones: 6,022·1023 e- carga del e- = 1,6·10-19 C
carga de 1 mol de e- = 6,022·1023 x 1,6·10-19 = 96485 C
Aunque generalmente vamos a usar el valor de 96500 C, que recibe el nombre de Faraday (F):
1F=96500 C
Cuanto mayor sea el tiempo que pase la corriente eléctrica sobre la disolución, mayor será la carga puesta en juego: